网络首发时间: 2016-11-04 15:00
稀有金属 2017,41(10),1105-1111 DOI:10.13373/j.cnki.cjrm.xy16050037
表面活性剂辅助合成正极材料LiNi0.5Co0.2Mn0.3O2的性能
吴天涯 张正富 王梓 孙冬 郭文凯 徐顺涛
昆明理工大学材料科学与工程学院
摘 要:
在表面活性剂、超声振动和机械搅拌的协同作用下, 采用共沉淀法制备镍钴锰复合氢氧化物前驱体 (Ni0.5Co0.2Mn0.3 (OH) 2) , 最后将制备得到的纳米片前驱体与碳酸锂 (Li2CO3) 采用高温固相法烧结合成三元层状正极材料 (LiNi0.5Co0.2Mn0.3O2) 。对于实验制得的前驱体和正极材料使用X射线衍射 (XRD) 、扫描电镜 (SEM) 、透射电镜 (TEM) 、电感耦合等离子体发射光谱仪 (ICP-OES) 以及电池测试仪对前驱体和正极材料进行表征和电化学性能的检测, 以探究表面活性剂对正极材料LiNi0.5Co0.2Mn0.3O2和其前驱体的影响。实验结果表明:使用两种表面活性剂油胺 (OA) 和聚乙烯吡咯烷酮-K30 (PVP-K30) 所制备出的前驱体为近正六边形的纳米片, 纳米片尺寸为400 nm左右。所制备出的正极材料在室温下, 2.84.5 V, 1C充放电条件下, 其初始放电容量分别达到151.699和157.093 mAh・g-1, 经过50次循环后容量保持率分别达到88.22%和99.04%。这样也表明所制备出的正极材料LiNi0.5Co0.2Mn0.3O2具有良好的电化学性能。
关键词:
锂离子电池;正极材料;表面活性剂;纳米片;
中图分类号: TM912
作者简介:吴天涯 (1991-) , 男, 湖北武穴人, 硕士, 研究方向:锂离子电池正极材料, E-mail:657823151@qq.com;;张正富, 教授, 电话:15911515534, E-mail:zhang-zhengfu@163.com;
收稿日期:2016-05-25
基金:国家自然科学基金项目 (U1202272) 资助;
Properties of Cathode Materials LiNi0.5Co0.2Mn0.3O2 in Li-Ion Batteries Assisted by Surfactants
Wu Tianya Zhang Zhengfu Wang Zi Sun Dong Guo Wenkai Xu Shuntao
School of Materials Science and Engineering, Kunming University of Science and Technology
Abstract:
The cathode material precursor ( Ni (0. 5) Co (0. 2) Mn (0. 3) ( OH) 2) was synthesised by using co-precipitation method assisted by surfactants, supersonic vibration and stirring. Then the ternary layered cathodematerial ( LiNi0.5Co0.2Mn0.3O2) was prepared by calcining the mixture of nanoplates precursor and lithium carbonate ( Li2Co3) . The cathode material and its precursor were analyzed by Xray diffractometry ( XRD) , transmission electron microscope ( TEM) , scanning electron microscope ( SEM) , inductively coupled plasma optical emission spectrometry ( ICP-OES) and electrochemical tests. The results showed that the precursor exhibited a regular hexagon nanoplates with average size of 400 nm; the prepared cathode material which was assisted by OA and PVP-K30 had excellent electrochemical properties, and the initial discharge capacities were 151. 699 and 157. 093 mAh・g-1, respectively, when they were charged and discharged at 1C within 2. 0 ~ 4. 5 V. The specific capacity retention rate was 88. 22% and 99. 04% respectively after 50 cycles.
Keyword:
lithium-ion battery; cathode materials; surfactants; nanoplates;
Received: 2016-05-25
在人们的现代化生活中可充电的锂离子电池 (lithium-ion batteries) 扮演着越来越重要的角色, 特别是在便携式3C电子设备、电动车辆 (EVs) 和大规模的储能设备上的应用[1,2,3]。这是因为锂离子电池具有显著的优点:体积小、能量高、质量轻、功率高、污染小和寿命长等[4,5,6]。为了进一步推广锂离子电池的商业化, 急需研究出高效的合成高性能的锂离子电池正极材料方法。在众多正极材料中, 富镍层状正极材料由于其较高的能量密度, 也就是在高电压下 (4.5 V以上) 拥有高的放电比容量 (>200 m Ah・g-1) , 而成为了各国科研工作者的研究热点, 然而它自身固有的较差的循环性能阻碍了其商业化应用[7,8,9,10,11]。
近年来, 各国科学界都在为改善高镍层状正极材料的电化学性能做努力, 例如表面改性[12,13]、掺杂、包覆[14]等等。本文研究的也是一种尝试优化改善正极材料电化学性能的方法:以油胺 (OA) 和聚乙烯吡咯烷酮-K30 (PVP-K30) 作为表面活性剂, 在制备前驱体的共沉淀反应中抑制复合氢氧化物的成核过程, 再将合成所得到的前驱体采用高温固相法合成得到正极材料Li Ni0.5Co0.2Mn0.3O2, 并且探究其电化学性能。新型环境友好的锂离子正极材料的研究对于促进国家经济发展、环境保护和为人们创造美好的生活都有重要的意义。因此研究和发展Li Ni0.5Co0.2Mn0.3O2正极材料具有很重要的现实意义和应用价值。
1 实验
1.1 前驱体的合成
将一定量的表面活性剂倒入20 ml无水乙醇中, 完全溶解后再将其倒入已盛有300 ml蒸馏水的500 ml反应釜中作为底液, 滴加氨水调节底液p H值至11.3。按物质的量比Ni∶Co∶Mn=5∶2∶3的比例, 用蒸馏水配制Ni SO4, Mn SO4, Co SO4混合盐溶液作为金属盐溶液, 溶液中金属离子总浓度为2 mol・L-1;再称量能沉淀以上金属阳离子且过量0.5%的物质的量的氢氧化钠, 并与氨水混合 (其中氨碱物质的量比为1∶1) , 加入蒸馏水使氢氧化钠溶液的浓度为4 mol・L-1, 作为碱溶液。在氮气的保护下, 以超声波的空化作用和机械搅拌的分散作用辅助, 使用蠕动泵将盐溶液和碱溶液分别缓慢滴入底液中, 并控制整个反应过程中体系的p H值为11.3, 温度为60℃, 以沉淀硫酸盐溶液中的镍钴锰离子。得到的沉淀物经过洗涤和干燥即为镍钴锰复合氢氧化物前驱体 (Ni0.5Co0.2Mn0.3 (OH) 2) 。
1.2 正极材料的合成
将得到的镍钴锰复合氢氧化物与碳酸锂按物质的量1∶1.1的比例行星球磨混合, 再将得到的混合物放入管式炉中, 在室温下以8℃・min-1的升温速率升温至500℃, 保温360 min;再以8℃・min-1的升温速率升温至850℃, 保温720 min, 最后随炉冷却至室温, 即制得层状镍钴锰氧化物正极材料 (Li Ni0.5Co0.2Mn0.3O2) 。
1.3 实验电池的组装
将充分研磨的Li Ni0.5Co0.2Mn0.3O2正极材料, 导电剂乙炔黑和粘结剂聚偏氟乙烯 (PVDF) 按质量比8∶1∶1的比例混合, 再加入适量溶剂N-甲基吡咯烷酮 (NMP) , 以调整粘度。将混合均匀、粘度适宜的浆料涂布到铝箔上, 然后在120℃真空下干燥整晚, 使用专用模具冲切, 得到直径为14 mm的电极片。在充满氩气的手套箱内, 水和氧气的含量都小于0.1×10-6, 将所得的电极片作为正极, 锂片作为负极, 微孔聚丙烯膜作为隔膜, 以1 mol・L-1Li PF6为电解液锂盐, 以碳酸乙烯脂 (EC) 、碳酸二乙酯 (DEC) 和碳酸甲乙酯 (EMC) 为电解液溶剂, 其中各种有机溶剂的体积比为1∶1∶1, 组装成CR2025扣式电池。
2 结果与讨论
2.1 前驱体结构和形貌的分析
在实验中合成锂离子电池正极材料前驱体―――过渡族金属镍钴锰复合氢氧化物是基于以下反应:
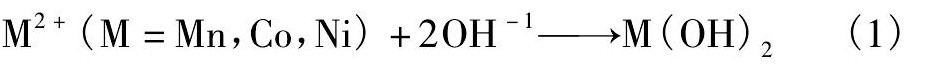
由图1衍射峰可见, 合成所得的前驱体均为六方晶系β-Ni (OH) 2, 且物相单一无杂峰, 这就表明了Co2+, Mn2+离子都进入了β-Ni (OH) 的结构中, 3种过渡金属离子已经是原子水平上的混合, 区别在于使用OA作为表面活性剂的前驱体结晶更好。
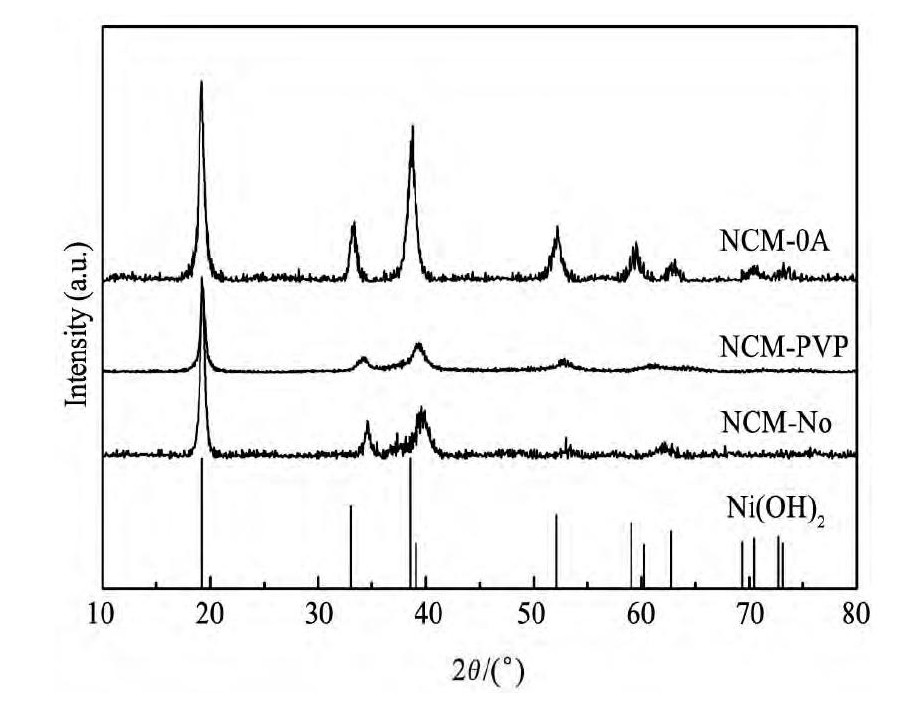
图1 前驱体Ni0.5Co0.2Mn0.3 (OH) 2的X射线衍射 (XRD) 图谱Fig.1X-ray diffraction (XRD) patterns of Ni0.5Co0.2Mn0.3 (OH) 2powdersNCM-OA:oleylamine, NCM-PVP:polyvinylpyrrolidone-K30, NCM-No:without surfactant
添加表面活性剂制备所得的前驱体Ni0.5Co0.2Mn0.3 (OH) 2粉末, 在透射电镜 (transmission electron microscopy, TEM) 下得到图2。图2中 (b, f) 为高倍率下的透射电镜图 (HRTEM) , 都可以看到很明显的晶格条纹, 说明其都具有较高的结晶度。从图2 (c, d, g, h) 可以看出复合氢氧化物为很规则的近正六边形纳米片状, 由图2 (d) 可以看出添加PVP合成的纳米片的直径在600 nm左右;由图2 (h) 可以看出添加OA合成的纳米片的直径在240nm左右。由图2 (e) 的衍射花样可以再次可以看出其为密排六方结构。对比图2 (a) , 虽然是在完全相同的工艺步骤和环境条件下, 不同之处仅在未加入表面活性剂, 但其形貌却差别很大, 虽然也为纳米级层状的, 但是却没有形成具体的规则形状, 说明以上两种表面活性剂对镍钴锰复合氢氧化物有较好的控形作用。使用OA作为表面活性剂的控形机制是:OA吸附在前驱体的{100}晶面上, 从而导致了晶体沿[111]方向上快速增长, 最终诱导生成近正六边形纳米片颗粒[15]。PVP的控形机制虽不见报道, 但是对同一物质的控形, 得到同一形状, 可见其机制应该是一致的。
2.2 正极材料的分析
在烧结成正极材料之前, 为了确定前驱体中化学成分, 而做了电感耦合等离子发射光谱的检测, 结果显示:使用OA和PVP作为表面活性剂的和未使用表面活性剂的前躯体里所含镍、钴、锰3种元素的物质的量比依次为:5∶2.125∶2.982, 5∶2.980∶3.455和5∶2.074∶3.020。由检测结果可以看出使用OA作为表面活性剂的和未使用表面活性剂的前躯体里镍、钴、锰三种元素的物质的量比的结果在误差要求的范围之内, 如果掺锂比例一定, 就说明最终烧结产物为Li Ni0.5Co0.2Mn0.3O2粉末。而使用PVP作为表面活性剂所合成的前驱体检测出的结果显示锰的含量偏高, 掺锂烧结后可能会有其他杂质产生。
由图3衍射峰可以看出无论是否添加表面活性剂所制备出的正极材料都属于六方晶系R3m空间群, 具有典型α-Na Fe O2层状结构。使用OA作为表面活性剂的和未使用表面活性剂合成的前驱体掺锂烧结出来的正极材料没有杂峰, 且峰形尖锐, 说明产物结晶较好, 且纯度较高。而使用PVP作为表面活性剂合成的前驱体掺锂烧结出来的正极料可以看出在21°~25°之间有很多细小的杂峰, 在25°之后也有零星的杂峰分布。经过jade软件分析, 这些杂峰为Li2Mn O3, 这些杂峰的产生也与电感耦合等离子发射光谱的检测结果相吻合。据文献[16]报道, (006/102) 以及 (108/110) 峰的分离的程度反应了所得材料的结构特性, 如果这两对峰完全分离, 则表明所得到的正极材料具有完整的层状结构。在图3中可以明显的看出所制备材料的分峰, 即所制备的正极材料具有显著的层状结构, 且经过前驱体和正极材料的衍射图谱可以看出表面活性剂对材料的相结构没有明显的影响。

图2 前驱体Ni0.5Co0.2Mn0.3 (OH) 2的TEM图Fig.2 TEM images of Ni0.5Co0.2Mn0.3 (OH) 2powder
(a) Without surfactant; (b, c) With 2 g PVP; (d) With 4 g PVP, (e~h) With 2 g OA
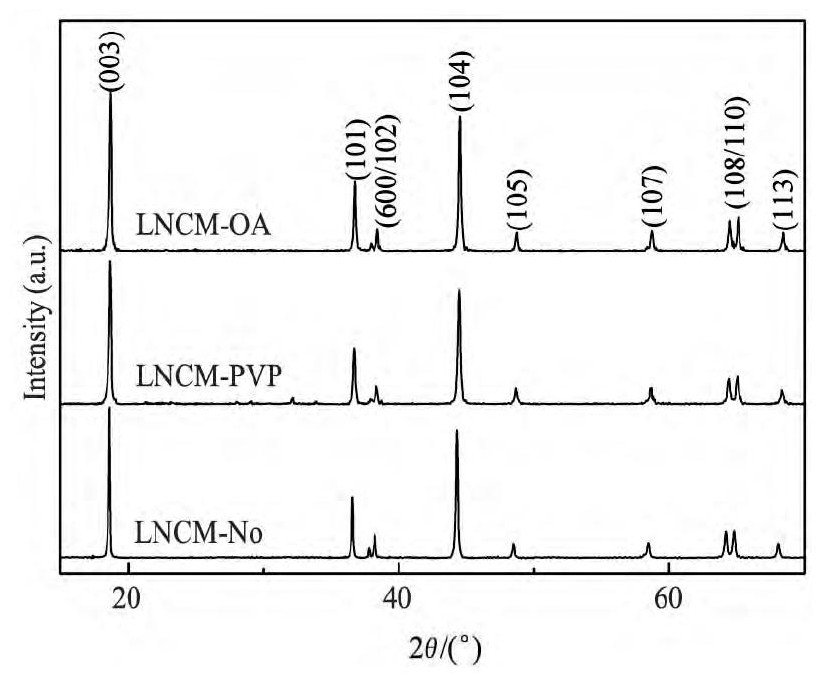
图3 正极材料Li Ni0.5Co0.2Mn0.3O2的XRD图谱Fig.3 XRD patterns of Li Ni0.5Co0.2Mn0.3O2powders LNCM-OA:oleylamine, LNCM-PVP:polyvinylpyrrolidoneK30, LNCM-No:without surfactant
经过MDI Jade 6.0软件的计算, 得到如表1中的常数。I003/I104的比值R被认为能反映材料的阳离子的混排程度[17], R<1.2是阳离子混排严重影响材料的电化学性能;R>1.2时, 阳离子混排程度较小, 其层状结构更稳定, 电化学性能更优越。由表1可以看出添加PVP的正极材料R值最大, 为1.25749, 而添加OA的最小, 为1.17434; (I006+I102) /I101值常被用来判断密排六方结构的有序性, 该值代表六方晶体的有序性, 一般在0.5左右为最佳[18], 所得的正极材料都在0.5附近, 差距较小。此外晶胞常数c与a的比值也能说明其是否是层状结构的标准, 当c/a>4.9时, 说明所制备的材料为层状结构良好, 且比值越大, 层状结构越明显, 越有利于锂离子在层状之间脱嵌。所得结果可以看出, 所有的正极料的c/a值均大于4.96。综上所述, 所合成得到的正极材料均为密排六方结构, 且为层状结构, 除了添加OA作为表面活性剂的正极材料阳离子混排度较高, 其他两种都较小。
图4为不同放大倍率下正极材料的SEM (scanning electron microscopy, SEM) 图。从图4中可以看出, 使用表面活性剂所制备出来的Li Ni0.5Co0.2Mn0.3O2的正极材料颗粒呈现出统一的块状, 大小均一。添加OA作为表面活性剂制备出的正极材料的颗粒尺寸在0.2~0.5μm左右;而添加PVP的颗粒尺寸稍大一些, 在0.7μm左右, 且颗粒团聚现象比添加OA的严重。而未添加表面活性剂的正极材料无论是颗粒大小还是团聚程度都要劣于添加表面活性剂的正极材料:颗粒尺寸更大, 团聚更严重。造成这种情况的原因应该是表面活性剂都为有机物, 且均匀地分布在前驱体中, 在掺锂烧结成正极材料时, 这些有机物有效地阻止了晶粒的长大和团聚。从它们颗粒之间形成孔隙通道和颗粒分散度来分析:3种正极材料都能看到明显的颗粒之间的孔隙通道, 这些通道可以增加正极材料与电解液的接触面积, 缩短Li+的扩散路径, 从而减少极化, 改善电化学性能。但是在通道半径更大, 分散度更高的条件下, 又会在增加了正极材料与电解液的接触面积的同时也加剧了正极材料与电解液之间的副反应的发生, 从而影响正极材料的电化学的性能。由图4 (c~e) 和相同放大倍率下的图4 (f~h) 对比可以看出:相较于使用PVP作为表面活性剂的正极材料使用OA的正极材料分散度更高, 也有更多更大的通道, 致使副反应的增多, 这就是导致使用OA作为表面活性剂合成的正极材料的电池性能不如使用PVP的原因。
图5 (a) 为电池在2.8~4.5 V, 1C放电倍率和室温条件下所做的电池循环检测得到的充放电曲线。由曲线可以看出, 添加OA, PVP和未使用表面活性剂制备出的正极材料的第一次放电比容量分别为151.699, 157.093和154.174 m Ah・g-1, 首次库伦效率分别为77.63%, 41.56%和76.89%。可以看出添加PVP的正极材料比容量高, 但却首次库伦效率差, 而添加OA做表面活性剂和未使用表面活性剂的正极材料首次放电比容量和首次库伦效率相差较小。影响库伦效率的因素很多:电解质的分解, 电极界面的钝化, 电极活性材料的结构、形态和导电性等。而使用PVP的正极材料之所以首次库伦效率那么差, 是因为前期前驱体内的锰元素过多, 在掺锂烧结后产生了Li2Mn O3的杂峰, 致使所制备的正极材料有类似于富锂锰基正极材料 (x Li2Mn O3・ (1-x) Li MO2 (M=Ni, Co, Mn) ) 结构的特性, 同时也就具备了它的电学性能特性。
表1 不同表面活性剂合成的正极材料的晶体常数Table 1 Lattice structural parameters of cathode materials with different surfactants 下载原图
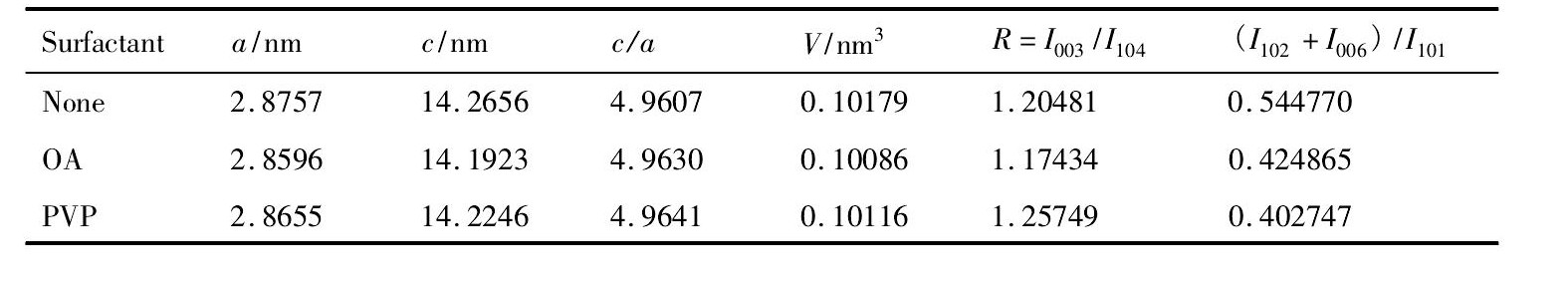
表1 不同表面活性剂合成的正极材料的晶体常数Table 1 Lattice structural parameters of cathode materials with different surfactants

图4 正极材料Li Ni0.5Co0.2Mn0.3O2的SEM图Fig.4 SEM images of Li Ni0.5Co0.2Mn0.3O2powder
(a, b) Without surfactant; (c~e) With 2 g OA; (f~h) With 2 g PVP
图5 (b) 为3种正极材料分别组装成的电池在2.8~4.5 V、室温条件下, 分别在1C, 2C, 5C和10C的放电倍率下的循环性能曲线。由图形的走势可以看出:添加PVP做表面活性剂合成的正极材料的比容量保持率比较好, 而添加OA的和未使用表面活性剂的衰减相差较小, 除了在10C的放电倍率下, 添加OA的比容量相对小很多。同时可以看出同一倍率下, 添加PVP的正极材料经过前期的活化, 比容量都会呈现出波浪形, 且略有上升, 而添加OA的和未使用表面活性剂的都是缓慢下降。添加OA作为表面活性剂合成的正极材料在1C的放电倍率下的首次放电比容量为151.699 m Ah・g-1, 循环50次后容量保持率为88.22%;同样的添加PVP的在1C的放电倍率下的首次放电比容量为157.093 m Ah・g-1, 循环50次后容量衰减微弱。PVP的正极材料循环性能表现的更加优异可以通过其掺杂有Li2Mn O3来解释, 因为Li2Mn O3能够保持Li Ni0.5Co0.2Mn0.3O2层状结构的稳定, 使正极材料在循环过程中结构更加稳定, 不易崩塌[19]。而添加OA作为表面活性剂合成的正极材料的电化学性能相对较差, 可以通过其R<1.2阳离子混排严重和c值太小影响锂离子从层状氧化物脱出来说明, 此外OA合成出来的正极材料颗粒分散度过高, 孔隙通道半径过大, 在电池循环过程中副反应加剧, 从而循环性能和倍率性能都不如PVP的。总体来说, 他们基本上都具有较好的循环性能, 而添加PVP的更加优异。
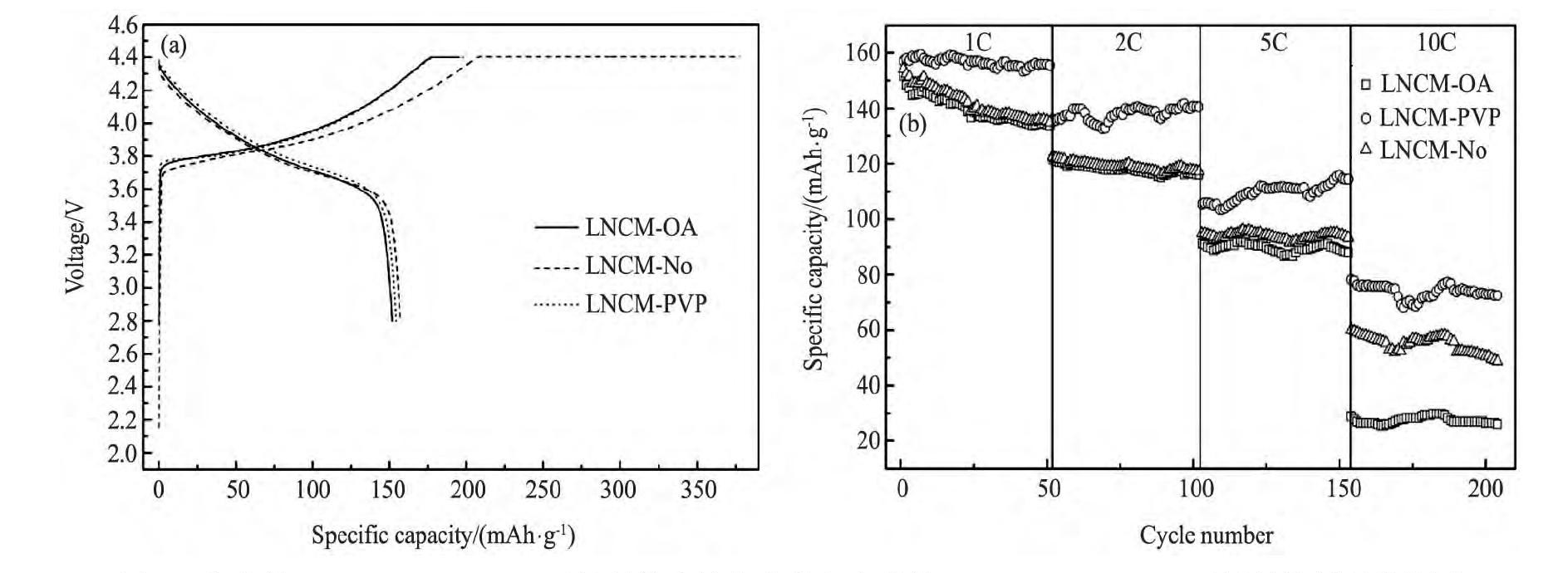
图5 合成的Li Ni0.5Co0.2Mn0.3O2正极料的充放电曲线和合成的Li Ni0.5Co0.2Mn0.3O2正极料的循环性能图Fig.5 Charge-discharge curves of Li Ni0.5Co0.2Mn0.3O2samples (a) and cycling performance of Li Ni0.5Co0.2Mn0.3O2samples (b)
3 结论
首先使用OA和PVP作为表面活性剂能制备出形貌优异的正六边形纳米片状正极材料前驱体Ni0.5Co0.2Mn0.3 (OH) 2, 且所得纳米片的粒度分布较均匀, 尺寸为400 nm左右。其次表面活性剂对材料的相结构影响微小, 但有很好的控形作用。再次由添加PVP作为表面活性剂制备出的正极材料组装成的电池的所检测得到的结果:在1C的放电倍率下的首次放电比容量为157.093 m Ah・g-1;然后在1C, 2C, 5C和10C的放电倍率下各循环50次后容量保持率依次为:99.04%, 103.32%, 108.58%和92.72%, 可以看出PVP作为表面活性剂能明显的改善制备出的正极材料循环性能。
参考文献
[1] Dunn Bruce, Kamath Haresh, Tarascon Jean-Marie.Electrical energy storage for the grid:a battery of choices[J].Science, 2011, 334 (6058) :928.
[2] Goodenough John B, Kim Youngsik.Challenges for rechargeable Li batteries[J].Chem.Mater, 2010, 22 (3) :587.
[3] Uchaker E, Cao G.Mesocrystals as electrode materials for lithium-ion batteries[J].Nano Today, 2014, 9 (4) :499.
[4] Marom Rotem, Amalraj S Francis, Leifer Nicole, Jacob David, Aurbach Doron.A review of advanced and practical lithium battery materials[J].Journal of Materials Chemistry, 2011, 21 (27) :9938.
[5] Thackeray Michael M, Wolverton Christopher, Isaacs Eric D.Electrical energy storage for transportation―approaching the limits of, and going beyond lithium-ion batteries[J].Energy&Environmental Science, 2012, 5 (7) :7854.
[6] Yin Y P, Zhuang W D, Wang Z, Lu H Q, Lu S G.Electrochemical characteristics of Li-rich cathode material Li1.2Mn0.54Ni0.13Co0.13O2with different manganese raw materials[J].Chinese Journal of Rare Metals, 2015, 39 (10) :891. (尹艳萍, 庄卫东, 王忠, 卢华权, 卢世刚.不同锰源对富锂正极材料Li1.2[Mn0.54Ni0.13Co0.13]O2性能的影响[J].稀有金属, 2015, 39 (10) :891) .
[7] Zheng J, Kan W H, Manthiram A.Role of Mn content on the electrochemical properties of nickel-rich layered Li[Ni0.8-xCo0.1Mn0.1+x]O2 (0≤x≤0.08) cathodes for lithium-ion batteries[J].ACS Appl.Mater.Interfaces, 2015, 7 (2) :770.
[8] Lee M J, Noh M, Park M H, Jo M, Kim H, Nam H, Cho J.The role of nanoscale-range vanadium treatment in Li[Ni0.8Co0.15Al0.05]O2cathode materials for Li-ion batteries at elevated temperatures[J].Journal of Materials Chemistry A, 2015, 3 (6) :421.
[9] Bi Y, Yang W, Du R, Zhou J, Liu M, Liu Y, Wang D.Correlation of oxygen non-stoichiometry to the instabilities and electrochemical performance of Li[Ni0.8Co0.1Mn0.1]O2utilized in lithium ion battery[J].Power Sources, 2015, 283 (9) :211.
[10] Wu F, Tian J, Su Y, Wang J, Zhang C, Bao L, He T, Li J, Chen S.Effect of Ni2+content on lithium/nickel disorder for Ni-rich cathode materials[J].Acs Applied Materials&Interfaces, 2015, 7 (14) :7702.
[11] Kim H, Kim M G, Jeong H Y, Nam H, Cho J.A new coating method for alleviating surface degradation of Li[Ni0.6Co0.2Mn0.2]O2cathode material:nanoscale surface treatment of primary particles[J].Nano Lett., 2015, 15 (3) :2111.
[12] Wang K X, Li X H, Chen J S.Surface and interface engineering of electrode materials for lithium-ion batteries[J].Advanced Materials, 2015, 27 (3) :527.
[13] Wu F, Tian J, Su Y, Guan Y, Jin Y, Wang Z, He T, Bao L, Chen S.Lithium-active molybdenum trioxide coated Li[Ni0.5Co0.2Mn0.3]O2cathode material with enhanced electrochemical properties for lithium-ion batteries[J].Power Sources, 2014, 269 (4) :747.
[14] Kong J Z, Ren C, Tai G A.Ultrathin Zn O coating for improved electrochemical performance of Li Ni0.5Co0.3Mn0.3O2cathode material[J].Journal of Power Sources, 2014, 266 (266) :433.
[15] Yan M F, Liu Z R.Progress in rare earth thermochemical treatment[J].Heat Treatment of Metals, 2003, 28 (3) :1.
[16] Tian J, Su Y F, Wu F, Xu S Y, Chen F, Chen R J, Li Q, Li J H, Sun F C, Chen S.High-rate and cyclingstable nickel-rich cathode materials with enhanced Li+diffusion pathway[J].ACS Applied Materials&Interfaces, 2015, 8 (1) :582.
[17] Wang Z, Lu H Q, Yin Y P, Zhuang W D, Lu S G.Synthesis and properties of Li-rich cathode material Li1.2Ni0.13Co0.13Mn0.54O2in Li-ion batteries[J].Chinese Journal of Rare Metals, 2016, 40 (1) :38. (王忠, 卢华权, 尹艳萍, 庄卫东, 卢世刚.锂离子电池富锂正极材料Li1.2Ni0.13Co0.13Mn0.54O2的合成及性能[J].稀有金属, 2016, 40 (1) :38.)
[18] Kim J H, Park C W, Sun Y K.Synthesis and electrochemical behavior of Li[Li0.1Ni0.35-x/2CoxMn0.55-x/2]O2cathode materials[J].Solid State Ionics, 2003, 164 (164) :43.
[19] Vu An, Qin Y, Lin C K, Abouimrane Ali, Burrell Anthony K, Bloom Samuel, Bass Dean, Bloom Ira Effect of composition on the voltage fade phenomenon in lithium-manganese-rich x Li Mn O3 (1-x) Li NiaMnbCocO2:a combinatorialsynthesis approach[J].Journal of Power Sources, 2015, 294:711.