文章编号:1004-0609(2008)04-0660-06
锂离子电池橄榄石结构正极材料LiMnPO4的合成与性能
王志兴,李向群,常晓燕,郭华军,彭文杰,李新海,陈启元
(中南大学 冶金科学与工程学院,长沙 410083)
摘 要:采用固相反应法合成掺碳锂离子电池正极材料LiMnPO4。利用XRD、SEM和充放电测试表征LiMnPO4的结构、形貌与充放电性能,并研究LiMnPO4电极的交流阻抗和锂离子的扩散行为。研究表明:适当提高合成温度与延长反应时间有利于促进晶体结构的完整,提高材料的放电平台和放电容量,改善电极反应表面电荷传递和材料中的锂离子扩散特性。在600 ℃烧结时间为24 h的条件下可合成出一次颗粒大小为0.1~0.3 μm的纯相LiMnPO4, 样品容量达到95 mA?h/g,充电态下锂离子的扩散速度为5.65×10-13 cm2/s。
关键词:LiMnPO4;锂离子电池;橄榄石;正极材料
中图分类号:TM 912.2 文献标识码:A
Synthesis and characterization of olivine type positive material LiMnPO4 for lithium ion batteries
WANG Zhi-xing, LI Xiang-qun, CHANG Xiao-yan, GUO Hua-jun, PENG Wen-jie, LI Xin-hai, CHEN Qi-yuan
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: Carbon-containing LiMnPO4 was synthesized by solid-state reaction. The structure, surface morphology and charge-discharge performance of LiMnPO4 were characterized by X-ray diffractometry, scanning electron microscopy and electrochemical measurement respectively. The AC impedance and diffusion coefficient of lithium ion for LiMnPO4 were also studied. The results show that proper increase of temperature and sintering time improve the crystal structure, increase the discharge voltage plateau and capacity, and enhance the transfer of surface electrons and lithium ion diffusion. Good samples with pure phase and primary particle size of 0.1~0.3 μm can be prepared at 600 ℃ for 24 h. These samples possess capacity of 95 mA?h/g and lithium ion diffusion coefficient of 5.65×10-13 cm2/s.
Key words: LiMnPO4; lithium ion batteries; olivine; cathode materials
在锂离子电池正极材料中,层状LiCoO2已经获得商业使用。然而,钴资源的稀少和高昂的价格导致锂离子电池生产成本高,限制其使用范围。1997年,PADHI等[1]首次发现具有橄榄石结构的LiFePO4能够可逆充放电,继而引发对这类材料的研究[2-10]。LiFePO4的理论容量约为170 mA?h/g,然而其相对于Li+/Li的电极电势仅为3.4 V。研究者进行理论计算发现,LiMnPO4相对于Li+/Li的电极电势为4.1 V[11],位于现有电解液体系的稳定电化学窗口,这种材料具有潜在的高能密度的优点。另外,合成LiMnPO4成本低、对环境友好。然而,合成能够可逆充放电的LiMnPO4非常困难。YAMADA等[12]采用第一原理对电子能级进行计算得出,电子在LiFePO4中发生跃迁的能隙为0.3 eV,有半导体特征,而LiMnPO4为2 eV,电子导电性极差,属绝缘体。LI等[13]对可充放电的LiMnPO4进行了报道,通过掺入导电碳黑获得了较高容量的LiMnPO4材料。TARASCON[14]通过一步低温(373 K)法合成LiMnPO4纯相,但可逆容量仅70 mA?h/g。本文作者对LiMnPO4的合成与掺杂进行深入研究,并获得可逆容量超过90 mA?h/g的掺碳锂离子正极材料LiMnPO4[15-16]。
为了合成具有较高容量的LiMnPO4,本文作者通过掺碳并结合球磨混料的方法,用固相反应法合成了LiMnPO4纯相,并对影响LiMnPO4电化学性能的因素进行系统研究,为固相合成LiMnPO4奠定基础。
1 实验
按组成LiMnPO4的化学计量比称取Li2CO3 (99.9%,新余市赣丰锂业有限公司)、MnCO3(分析纯,广东台山化工厂)、NH4H2PO4(99.5%,河南焦作市化工三厂),并与适量的碳黑(电池级,广东省化工进出口公司)混合,碳在产物中的理论质量比含量为10%(采用德国Eltar公司CS800红外碳硫检测仪测得最终样品中碳的实际含量为8.59%)。将反应物进行球磨(ND6-2L行星式球磨机,南京南大天尊电子有限公司),在N2气氛下300 ℃预烧3 h,得到中间产物。将其取出进行第二次球磨,在N2气氛下于一定温度进行烧结,冷却至室温,得到产物。
采用X射线衍射仪(Rigaku公司,日本)对合成的材料进行物相分析,以Cu Kα耙作为辐射源,电压40 kV,电流50 mA,步宽0.02?,扫描速度2 (?)/min,衍射角的扫描范围为10?~90?。用JEOL公司生产的JSM-5600LV型扫描电子显微镜对材料的表面形貌进行观察。
通过2025型扣式电池测试材料的电化学性 能。LiMnPO4、乙炔黑(电池级,广东省化工进出口公司)和PVDF(聚偏二氟乙烯,电池级,法国阿托化学)按质量比8?1?1混合并研磨均匀后,加入适量有机溶剂NMP(N-甲基吡咯烷酮,99.9%,南京京龙化工厂),研磨成均匀糊状物后,涂于铝箔上,在120 ℃下真空干燥12 h,制作成正极片。以金属锂片作为负极,Celgard2400微孔聚丙烯膜(Celgard Inc. USA)为隔膜,以溶于体积比1?1?1的EC(碳酸乙烯酯)/DMC(1, 2-二甲基碳酸酯)/EMC(碳酸甲乙酯)混合溶剂的1 mol/L LiPF6为电解液(三菱化学),组装成2025型扣式电池,在BTS-51二次电池性能检测仪(深圳新威尔多电子设备有限公司)上测试样品的充放电性能。充放电电流为0.1C,充放电电压为2.75~4.5 V,测试温度为(25±2) ℃。
 交流阻抗测试采用三电极体系,辅助电极和参比电极均为金属锂片,测试仪器为美国CHI660电化学工作站。过电势为5 mV,测量频率范围0.01 Hz~ 100 kHz。
交流阻抗测试采用三电极体系,辅助电极和参比电极均为金属锂片,测试仪器为美国CHI660电化学工作站。过电势为5 mV,测量频率范围0.01 Hz~ 100 kHz。
采用恒电位阶跃法测定LiMnPO4电极中的锂离子扩散系数,测定体系采用三电极。电极在某种荷电状态下稳定至电位每小时变化不超过1 mV时,认为电极电位达到准平衡状态,此时施加一阶跃幅度为200 mV的电位,在此阶跃电位下,由于液相中的扩散系数远大于固相中的扩散系数,电极反应受固相中锂离子扩散控制,此时测得的扩散系数为锂离子在LiMnPO4晶格中的扩散系数。扩散系数的计算公式参见文献[17]。
2 结果与讨论
2.1 LiMnPO4的物理特性
图1所示为不同温度合成LiMnPO4的XRD谱。由图中可以看出,合成的LiMnPO4均具有明显的衍射峰。对照标准图谱(卡片号PDF33-0804)可以看出,样品为橄榄石结构LiMnPO4,空间点群属Pnmb。其中,650 ℃合成的样品其晶格常数为a=0.609 77 nm,b= 1.049 94 nm,c=0.475 13 nm,与标准LiMnPO4相符合。300 ℃合成的样品衍射峰最弱,随着温度的升高,衍射峰变尖锐,强度明显增大,650 ℃合成的LiMnPO4样品衍射峰最强。说明升高温度在很大程度上促进晶粒的长大,有利于晶体结构更完整。
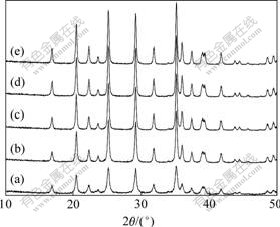
图1 不同条件下合成LiMnPO4的XRD谱
Fig.1 XRD patterns of LiMnPO4 synthesized under different conditions: (a) 300 ℃, 3 h; (b) 500 ℃, 24 h; (c) 550 ℃, 24 h; (d) 600 ℃, 24 h; (e) 650 ℃, 24 h
图2所示为600 ℃时烧结不同时间合成样品的XRD谱。从图中可以看出,合成的样品均为LiMnPO4纯相。其中,600 ℃烧结2 h合成样品的衍射峰强度明显低于其它几个样品,说明一定温度下,适当延长烧结时间有助于形成较完整的晶型结构。烧结12、24和48 h的样品晶型结构均比较完整,随着烧结时间的延长,衍射峰只轻微升高。表明烧结时间达到一定程度以后,晶粒的生长变得缓慢。
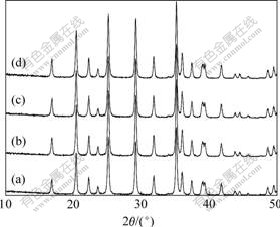
图2 600 ℃烧结不同时间合成LiMnPO4的XRD谱
Fig.2 XRD patterns of LiMnPO4 synthesized at 600 ℃ for different sintering times: (a) 2 h; (b) 12 h; (c) 24 h; (d) 48 h
图3所示为不同温度下合成LiMnPO4的SEM像。从图中可以看出,300 ℃合成的样品由分散均匀的单一小颗粒组成,颗粒间无明显结聚现象。随着合成温度的升高,样品颗粒越来越圆润,粒度有增大趋势,且团聚现象越来越明显,表明温度的升高有助于样品晶粒的完整。

图3 不同温度合成LiMnPO4的SEM像
Fig.3 SEM micrographs of LiMnPO4 synthesized at different temperatures: (a) 300 ℃; (b) 500 ℃; (c) 550 ℃; (d) 650 ℃
图4所示为600 ℃烧结不同时间合成LiMnPO4的SEM像。由图可见,各个样品的形貌差别很小,一次颗粒大小为0.1~0.3 μm。随着烧结时间的延长,样品颗粒呈现轻微的增大趋势,且小颗粒间的结合变得紧密。说明烧结时间能从一定程度上促进颗粒的生长,晶型更完整。

图4 600 ℃烧结不同时间合成LiMnPO4的SEM像
Fig.4 SEM micrographs of LiMnPO4 synthesized at 600 ℃ for different sintering times: (a) 2 h; (b) 12 h; (c) 24 h; (d) 48 h
2.2 LiMnPO4的充放电性能



对不同温度下合成的样品进行充放电测试,其结果如图5所示。由图可以看出,较低温度下合成的样品充放电性能较差。其中300 ℃合成的样品仅为37 mA?h/g,500 ℃合成的样品只有55 mA?h/g,其原因是合成温度太低,样品晶体形成不完整,锂离子扩散通道未完全形成,造成锂离子扩散难以进行。而较高温度下合成的样品均具有较好的电化学活性,容量较高。550、600和650 ℃合成样品的放电容量分别为95、93和88 mA?h/g。其原因可能是晶粒形成比较完整。从电位的高低来看,650 ℃合成的样品具有最接近4 V的平台,说明晶体生长完整,从一定程度上减小了电化学极化。
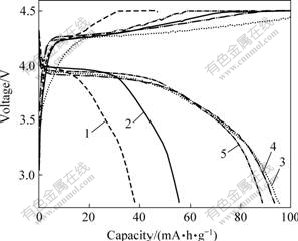
图5 不同条件下合成LiMnPO4的充放电曲线
Fig.5 Charge-discharge curves of LiMnPO4 synthesized at different temperatures: 1―300 ℃, 3 h; 2―500 ℃, 24 h; 3―550 ℃, 24 h; 4―600 ℃, 24 h; 5―650 ℃, 24 h
图6所示为600 ℃烧结不同时间合成产物的充放电曲线。从图中可以看出,样品均有着较高的放电容量。烧结2、12、24和48 h合成样品的容量分别为71、78、93和88 mA?h/g,可见随着烧结时间的延长,容量呈现上升趋势。从图中还可以看出,随着时间的延长,放电平台也同样呈现上升趋势。结合XRD和SEM分析可知,随着烧结时间的延长,晶型趋于完整,在一定程度上减小了充放电过程中电化学反应极化,使得充放电更容易进行,容量上升。
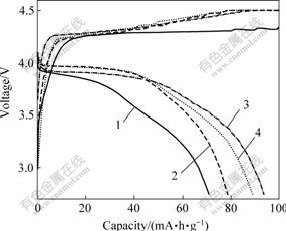
图6 600 ℃烧结不同时间合成LiMnPO4充放电曲线
Fig.6 Charge-discharge curves of LiMnPO4 synthesized at 600 ℃ for different sintering times: 1―2 h; 2―12 h; 3―24 h; 4―48 h
图7所示为不同温度下合成的样品的循环性能。从图中可以看出,550和600 ℃得到的样品的首次放电容量虽然达到95 mA?h/g,但循环衰减较大,30次后容量损失约为36.8%。而300和500 ℃合成的样品容量较低,衰减也较大,500 ℃合成样品在30次循环后容量容量损失为25.5%,300 ℃合成样品容量损失约为30%。而650 ℃合成的样品,首次放电容量约为 85 mA?h/g,随着循环的进行,容量不断上升,最高容量超过100 mA?h/g,到25周期后放电容量呈平稳趋势,维持在100 mA?h/g。可见,650 ℃合成的样品具有优良的循环性能和高的可逆容量。结合XRD谱和SEM分析可知,650 ℃合成的样品晶型完整,粒度 小,且分布很均匀,晶粒细小降低了锂离子的扩散距离。可见适当提高温度能够改善材料的循环性能。
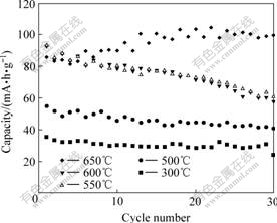
图7 不同温度合成LiMnPO4的循环性能
Fig.7 Cycling performances of LiMnPO4 synthesized at different temperatures
图8所示为不同烧结时间合成产物的循环性能比较图。从图中可以看出,烧结2 h和12 h的样品循环性能较好,循环30次后容量几乎不变。而烧结24 h和48 h合成的样品循环性能较差,随着循环的进行,放电容量下降很快,循环30次后其容量分别下降37.6%和36.8%。可见,烧结时间的延长虽然有利于LiMnPO4样品容量的发挥,但是过长的烧结时间会严重影响材料的循环性能。本实验条件下,烧结12 h合成的样品其循环性能最好。
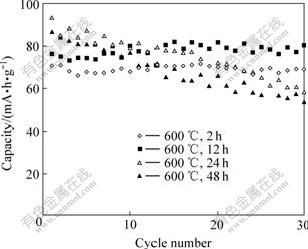
图8 600 ℃烧结不同时间合成LiMnPO4的循环性能
Fig.8 Cycling performances of LiMnPO4 synthesized at 600 ℃ for different sintering times
2.3 LiMnPO4的交流阻抗谱
图9所示为烧结温度对合成材料的电极阻抗的影响(电极为充电态)。从图中可以看出,曲线由高频区的半圆和低频区的直线组成。比较不同温度合成的材料的电化学反应阻抗发现,随着温度的升高,电化学反应阻抗呈现下降趋势,但温度升高到650 ℃时阻抗有所上升。表明较高温合成的样品具有较大的表面电荷传递速度,从而有利于提高材料的倍率性能。
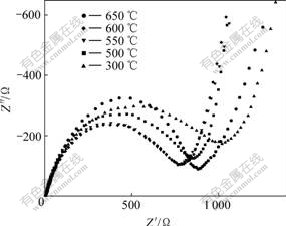
图9 不同温度合成LiMnPO4的交流阻抗图谱(充电态)
Fig.9 Impedance spectrum of LiMnPO4 synthesized at different temperatures (charged)
2.4 Li+在LiMnPO4晶格中的扩散
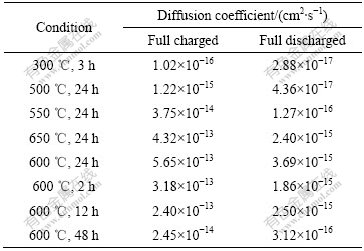
为了深入研究LiMnPO4的动力学特征,对合成的材料进行了扩散系数测定,结果如表1所列。从表1可以看出,材料在不同的状态下锂离子的扩散系数存在很大的差别,充电态的扩散系数最大,而放电态的扩散系数最小。对比充电态不同温度合成材料中的锂离子扩散系数发现,300 ℃合成的材料具有最小的锂离子扩散系数,其充电态扩散系数仅为1.02×10-16 cm2/s,600、650 ℃合成的材料中锂离子扩散系数提高约3个数量级。这些结果表明,如果合成温度太低,晶型不完整,锂离子扩散通道形成不完全,会导致锂离子在材料中的扩散速度缓慢。对比充电态在600 ℃烧结不同时间合成样品的扩散系数发现,烧结2、12、24 h合成的样品锂离子扩散系数均在同一个数量级,而烧结48 h合成的样品中锂离子扩散系数降低一个数量级。表明烧结时间过长,对锂离子的扩散不利。
表1 锂离子在LiMnPO4中的扩散系数
Table 1 Diffusion coefficient of Li+ ion for LiMnPO4
3 结论
1) 适当地提高合成温度与延长反应时间有利于促进晶体结构的完整,提高材料的放电平台和放电容量,改善电极反应表面电荷传递和材料中的锂离子扩散特性。
2) 在600 ℃烧结24 h的条件下可合成出一次颗粒大小为0.1~0.3 μm的纯相LiMnPO4, 样品容量达到95 mA?h/g,充电态下锂离子的扩散速度为5.65×10-13 cm2/s。
REFERENCES
[1] PADHI A K, NAJUNDASWAMY K S, GOODENOUGH J B. Phospho-olivines as positive-electrode materials for rechargeable lithium batteries[J]. J Electrochem Soc, 1997, 144(4): 1188-1194.
[2] ZHU B Q, LI X H, WANG Z X, GUO H J. Novel synthesis of LiFePO4 by aqueous precipitation and carbothermal reduction[J].Materials Chemistry and Physics, 2006, 98(2/3): 373-376.
[3] PADHI A K, NAJUNDASWAMY K S, MASQUELIER C, OKADA S, GOODENOUGH J B. Effect of structure on the Fe3+/Fe2+ redox couple in iron phosphates[J]. J Electrochem Soc, 1997, 144(5): 1609-1613.
[4] AMINE K, YASUDA H, YAMACHI M. Olivine LiCoPO4 as 4.8 V electrode material for lithium batteries[J]. Electrochem Solid-State Lett, 2000, 3(4): 178-179.
[5] YANG J, XU J. Synthesis and characterization of carbon-coated lithium transition metal phosphates LiMPO4 (M=Fe, Mn, Co, Ni) prepared via a nonaqueous sol-gel route[J]. J Electrochem Soc, 2006, 153(4): A716-723.
[6] ZHANG S S, ALLEN J L, XU K, JOW T R. Optimization of reaction condition for solid-state synthesis of LiFepO4-C composite cathodes[J]. J Power Sources, 2005, 147: 234-240.
[7] 王晓琼, 李新海, 王志兴, 郭华军, 彭文杰, 刘凤举. 锂离子电池正极材料LiFe0.9Ni0.1PO4的合成与性能[J]. 中国有色金属学报, 2006,16(4): 739-745.
WANG Xiao-qiong, LI Xin-hai, WANG Zhi-xing, GUO Hua-jun, PENG Wen-jie, LI Feng-ju. Synthesis and performance of LiFe0.9Ni0.1PO4 as cathode material in lithium-ion battery[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(4): 739-745.
[8] CHUNG S C, BLOKING J T, CHIANG Y M. Electronically conductive phospho-olivines as lithium storage electrodes[J]. Nature Materials, 2002, 1(2): 123-128.
[9] PROSINI P P, LISI M, ZANE D, PASQUALI M. Determination of the chemical diffusion coefficient of lithium in LiFePO4[J]. Solid State Ionics, 2002, 148(1/2): 45-51.
[10] HUANG H, YIN S C, NAZAR L F. Approaching theoretical capacity of LiFePO4 at room temperature at high rates[J]. Electrochem Solid-State Lett, 2001, 4(10): A170-172.
[11] WAKIHARA M, YAMAMOFO O. Lithium ion batteries[M]. Tokyo: Kodansha Ltd., 1998.
[12] YAMADA A, HOSOYA M, CHUNG S C, KUDO Y, HINOKUMA K, KUANG Y L, NISHI Y. Olivine-type cathodes achievements and problems[J]. J Power Sources, 2003, 119: 232.
[13] LI G H, AZUMA H, TOHDA M. LiMnPO4 as the cathode for lithium batteries[J]. Electrochemical and Solid-State Letters, 2002, 5(6): A135-A137.
[14] DELACOURT C, POIZOT P, MORCRETTE M, TARASCON J M, MASQUELIER C. One step low-temperature route for the preparation of electrochemically active LiMnPO4 powders[J]. Chem Mater, 2004, 16(1): 93.
[15] 常晓燕, 王志兴, 李新海, 匡 琼, 彭文杰, 郭华军, 张云河. 锂离子电池正极材料LiMnPO4的合成与性能[J]. 物理化学学报, 2004, 20(10): 1249-1252.
CHANG Xiao-yan, WANG Zhi-xing, LI Xing-hai, KUANG Qiong, PENG Wen-jie, GUO Hua-jun, ZHANG Yun-he. Synthesis and performance of LiMnPO4 used as cathode material for lithium ion batteries[J]. Acta Phys-Chim Sin, 2004, 20(10): 1249-1254.
[16] CHANG X Y, WANG Z X, LI X H, ZHANG L, GUO H J, PENG W J. Synthesis and performance of LiMn0.7Fe0.3PO4 cathode material for lithium ion batteries[J]. Materials Research Bulletin, 2005, 40(9): 1513-1520.
[17] WANG Z X, LI X H, CHEN Q Y, PENG W J, GUO H J. Study on diffusion of hydrogen in AB5 non-stoichiometric hydrogen absorbing alloys[J]. Journal of Rare Earths, 2003, 21(6): 657-759.
基金项目:国家重点基础研究发展计划资助项目(2007CB613607)
收稿日期:2007-07-23;修订日期:2007-12-18
通讯作者:王志兴,教授,博士;电话:0731-8836633;E-mail: zxwang@mail.csu.edu.cn
(编辑 龙怀中)