文章编号:1004-0609(2008)12-2166-06
铁基合金粉末氧化行为
刘东华,刘 咏,黄伯云,张宁一,方京华,刘 锋
(中南大学 粉末冶金国家重点实验室,长沙 410083)
摘 要:采用质量变化、氧含量测定、XRD、SEM和能谱分析研究铁基合金粉末500 ℃氧化行为及氧化机理。结果表明,氧化质量增量、氧含量随时间变化明显,前期呈线性关系,后期则呈抛物线关系;前期由于氧化时间较短,铁基合金粉末颗粒与氧反应不明显,后期氧与颗粒表面反应,生成Fe、Cr和Ti的氧化物,并形成致密的氧化膜;铁基粉末形成(Fe, Cr)2O3相,随着氧化时间的延长,形成的(Fe, Cr)2O3相衍射峰强度增强。
关键词:铁基粉末;氧化行为;氧化机理
中图分类号:TG 156.98 文献标识码: A
High temperature oxidation behavior of iron-based metal powder
LIU Dong-hua, LIU Yong, HUANG Bai-yun, ZHANG Ning-yi, FANG Jing-hua, LIU Feng
(State Key Laboratory of Powder Metallurgy, Central South University, Changsha 410083, China)
Abstract: The oxidation behavior of an iron-based metal powder at 500 ℃ was investigated by mass gain and oxygen content measurements, X-ray diffraction, scanning electron microscope and energy spectrum analysis. The results show that the change of mass gain and oxygen content increase obviously with the time increasing; their relationship is linear at the former stage and parabolic at the later stage. The reaction between iron-based powder and oxygen at the initial stage was very slow. After a certain period, oxygen clearly reacted with the surface of the particles, and the formed oxide scale became thick and compact, which consisted of oxides of Fe, Ti and Cr, (Fe, Cr)2O3 was detected by XRD, the intensity of its diffraction peaks became stronger with time.
Key words: iron-based powder; oxidation behavior; oxidation mechanism
传统的高温合金一般采用析出相的沉淀硬化做为其主要的强化手段[1?2],但析出相在高温下易聚集长大或重新固溶于基体中,失去了强化作用,限制了高温合金的使用温度。Y2O3、Al2O3和ThO2等氧化物具有很好的热稳定性和化学稳定性,其强化效果可以维持到接近合金的熔点温度,氧化物弥散强化(ODS)高温合金就是采用这些纳米(<50 nm=氧化物质点对基体进行强化[3],使合金在高温下具有高强度的一类合金。近几年,氧化物弥散强化铁素体钢(ODS钢)作为核聚变反应堆用材料正在被美国、日本及欧洲等国家开发和研究[4?5]。氧化物弥散强化铁素体钢作为结构材料越来越广泛地应用在快速增值反应堆和核聚变壳用材 料[6?7]。这是由于氧化物弥散强化铁素体钢具有高温抗蠕变性能[8?9]、抗放射稳定性[10]、聚变能量体系中低的活化性能[6]等优良特性。
目前,ODS铁素体钢粉末的制备主要是通过对预合金粉中添加Y2O3,进行机械合金化[11?12]。但这种方式存在杂质元素含量不可控制,可重复性差等问题,很难大规模生产。作者拟直接对含Y的预合金粉末进行氧化,从而促使粉末能够满足预定的成分要求,然后再通过大变形的方式,使氧弥散分布于合金内部。因此本文作者主要研究气雾化铁基合金粉末在空气中的氧化行为,通过质量增加、氧含量的测定、X射线衍射(XRD)、扫描电镜(SEM)和能谱分析粉末的氧化过程和氧化机理。
1 实验
实验中用雾化铁基合金粉末的名义成分为Fe-12Cr-2.5W-0.4Ti-0.3Y-0.3O (质量分数,%),铁基合金粉末的制备主要采用惰性气体雾化方法。将所有合金原料在雾化过程中直接熔化,然后采用氩气雾化。通过雾化参数的控制获得要求的粉末粒度。熔化温度为1 650 ℃,雾化压力3.5 MPa,金属熔液流量6.0 kg/min,雾化介质,氩气,纯度大于99.995%。为了减小成分误差,对Ti、Y等易挥发性元素,待温度升高至接近雾化温度时再加入,溶解均匀后立即进行雾化。原料雾化粉末的成分如表1所列。
表1 原始粉末化学成分
Table 1 Composition of original powder (mass fraction, %)

对原始雾化粉末进行粒度分析,其粒度分布如图1所示。可见,粉末的中位径为53.58 μm,粒径范围为20~200 μm。粉末颗粒的比表面积由实验测得为0.02 m2/g。

图1 原始雾化粉末粒度的累积分布
Fig.1 Particle size cumulative distribution of atomized powder
为研究其氧化行为,将质量为15 g的雾化粉末装入规格为100 mL的刚玉坩埚中,粉末尽量分散开,使氧化较为充分,在箱式电阻炉中500 ℃高温加热自然氧化,氧化时间分别为:1、2、4、8 和16 h,氧化后粉末在氮/氧分析仪(美国LECO的TC?436)上测定氧含量。氧化后样品自然冷却后利用电子天平(感应量1×10?2 g) 称其质量。采用D8?Advance型全自动X射线衍射仪进行物相分析,采用JM?6360LV扫描电子显微镜观察试样的显微组织形貌,同时用EDAX对部分区域进行成分分析。
2 实验结果
2.1 氧化动力学
图2所示为500 ℃氧化后粉末的氧含量及由氧化导致的粉末总质量随时间的变化和单位表面质量增量的平方与时间的关系。由图2(a)可知,随着氧化时间的延长,氧不断与粉末颗粒反应,与粉末颗粒的表层发生氧化反应,粉末氧含量变化明显;粉末的氧化质量增量随时间变化近似地呈抛物线趋势上升,氧化前期氧化质量增量明显,抛物线斜率较大,氧化后期质量变化缓慢,抛物线斜率较氧化前期平缓。
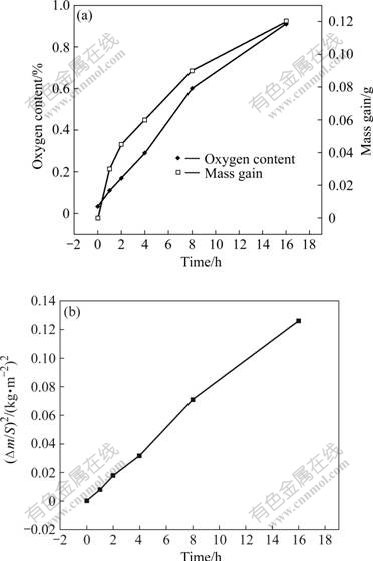
图2 氧化后粉末总质量增加及氧含量和单位表面质量增量的平方随时间的变化
Fig.2 Relationships between iron-based alloy powder and oxidation time: (a) Oxygen content and mass gain of whole powder caused by oxidation; (b) Square of unit area mass gain
由图2(b)可知,铁基合金粉末在500 ℃氧化时,单位表面质量增量的平方与时间呈线性关系。因此,其恒温氧化动力学行为符合抛物线规律,可以用以下公式表示:

2.2 粉末物相分析
氧化不同时间粉末的相成分如图3所示。不同氧化时间所得的物相组成有所不同。粉末500 ℃氧化4 h后,出现了新的衍射峰,根据粉末所含元素,参照XRD谱分析,暂判定粉末形成新的物相为Ti2O3;粉末氧化8 h时,又有新的衍射峰出现,为铬和铁的氧化物;粉末氧化16 h表层出现铬、铁的氧化物衍射峰强度更高。氧化16 h粉末颗粒最终产生Fe、Cr和Ti的氧化物,随着氧化时间的延长,氧化物相(Fe, Cr)2O3的衍射峰也逐渐增强。这与上述氧含量分析中的结果,随氧化时间的延长氧含量不断增加是相对应的。根据初始粉末元素分析可知,能够参与氧化反应的还有Y和W元素,而在相成分分析的结果中并未出现其氧化物相。

图3 不同氧化时间氧化后粉末的XRD谱
Fig.3 XRD patterns of powder for different oxidating times
2.3 粉末氧化后的显微组织
图4所示为铁基合金粉末500 ℃氧化1、2和4 h的显微形貌。在500 ℃氧化1 h和2 h的粉末颗粒(图4(a)和4(b)),氧与粉末颗粒表层发生反应十分缓慢,在颗粒周围没有发现明显的氧化层。由能谱分析可知,在颗粒内部及周围氧含量基本一致且很低。随着氧化时间延长到4 h,对颗粒的边缘和内部进行成分分析,颗粒边部的氧含量比氧化2 h明显增加,结合粉末颗粒的形貌(图4(c))分析,说明颗粒表层的氧化层已经形成,只是在形貌像中还不能观察到。

图4 氧化不同时间后铁基粉末的显微形貌
Fig.4 Morphologies of iron-based powder for different oxidating times: (a) 1 h; (b) 2 h; (c) 4 h
图5和图6分别为500 ℃氧化8 h和16 h的显微组织和成分分析。从图5中可以明显地观察到细小颗粒周围有氧化层形成。氧化8 h粉末的氧化层并没有出现在所有的粉末颗粒中,细小的粉末颗粒表面能较高,在500 ℃下,与氧的结合能力比粗大的粉末颗粒强,形成了氧化层,而粗大的粉末颗粒在8 h的时间内不能充分地与氧结合形成可观察的氧化层,这与相成分分析的结果是一致的。因此氧化层不是连续的,发生了破碎,具有显著的脆性。氧化16 h粉末样品的氧化层更为明显,观察到几乎所有的颗粒都有很明显的氧化层出现。随着氧化层的出现,能谱分析发现颗粒表层的氧含量也明显增加,表面氧化层的成分主要为Fe、Cr和Ti等元素。随着氧化时间的增加,衍射峰越来越强,表明了参与氧化反应的更多是Fe、Cr和Ti。Y元素比Fe和Cr更加活泼,但在X射线谱上并不能观察到Y2O3,这是由于Y的含量太少,其氧化物的量也低于X射线相分析的检测限。

图5 铁基粉末氧化8 h后的形貌及成分分析
Fig.5 Morphology (a) and element analysis (b), (c) of iron-based powder for 8 h oxidating
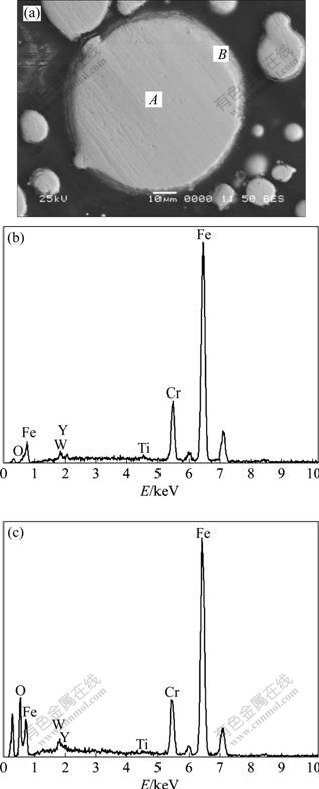
图6 铁基粉末氧化16 h后的形貌及成分分析
Fig.6 Morphology (a) and element analysis (b), (c) of oxidated iron-based powder for 16 h
3 分析与讨论
粉末的氧化方式与金属和合金有相似之处,在高温下,氧与粉末颗粒接触后,与颗粒表面的原子发生反应,形成氧化膜。本实验研究的铁基合金粉末颗粒尺寸较小,表面能高,位于表面的原子占较大的体积分数。当氧含量不高即氧化不充分时,表面能较高的细小粉末颗粒首先与氧反应,在其颗粒表面形成氧化膜;随着氧化时间延长,氧原子在颗粒表面化学吸附形成初始氧化层,由于电子热激发或隧道效应机制电子脱离金属原子的束缚成为自由电子,这些电子跟初始氧化层上的氧分子结合成为带负电的氧离子,而金属原子由于失去电子带正电荷,通过这个内建的电场吸引带负电的氧离子从而使金属原子氧 化[13]。Fe、Cr和Ti等金属原子在500 ℃的氧化温度和16 h的氧化时间都达到充分氧化的条件,能够在粉末颗粒的表面形成致密的氧化膜[14]。
随着氧化时间的增加,粉末质量变化显著,初始氧化速率大于后阶段的氧化速率。铁基粉末在500 ℃氧化时,氧化质量增量和氧含量的变化随时间变化明显,且随氧化时间的延长质量增量值变化越来越小。在没有足够的氧化时间下,氧化初期,氧原子与粉末颗粒表面的原子反应不充分且反应缓慢,所测得含氧量与氧化质量增量值随时间的变化规律不同,氧含量的变化很大,但氧化质量增量值较小。氧化4 h后,粉末表面氧化膜形成并不断增厚,氧原子不断与粉末颗粒表面的原子结合,形成致密的氧化膜。在500 ℃氧化16 h内氧含量随氧化时间的变化趋势与氧化质量增量一致。
根据热力学手册[15]计算,在300~700 ℃,Y、Ti、Cr、Fe和W的化学反应生成自由能曲线如图7所示。从图中可以看出,在计算的温度范围内各个反应的自由能均为负值,说明在热力学上这些反应都可能发生。但比较可知,钇元素氧化反应的负值最大,随之依次为Ti、Cr、Fe和W。这说明在500 ℃时,Y的氧化反应优先进行,随后依次为Ti、Cr、Fe和W的氧化反应。氧化时间较短时,氧只与活泼的稀土元素Y反应,由于粉末中Y的含量不高,故在反应刚刚开始时可能就已经完全消耗,氧还没有来得及与粉末颗粒中的其他元素发生反应,氧化质量增量变化不明显。500 ℃氧化时间为4 h,粉末颗粒的氧化是以Ti元素的氧化作为优先反应的,表层氧化膜分析表明以Ti2O3为主,这与物相分析的判定结果是一致的。到了氧化后期,虽然Fe元素氧化生成吉布斯自由能值比Cr元素氧化物生成吉布斯自由能高,但由于金属粉末中的Fe元素的浓度明显大于Cr元素的浓度,在氧化时间达到8 h时,同时生成了Fe和Cr的氧化物。氧化质量增量变化明显,氧与粉末颗粒表层元素反应,粉末氧化质量增量值随氧化时间的延长而增长,这与所得到的氧化质量增量曲线相对应。在500 ℃下W元素氧化生成吉布斯自由能值比Fe元素氧化物生成吉布斯自由能高,在本实验中的铁基合金粉末中基体Fe优先发生氧化反应,由显微形貌的能谱分析和相成分分析结果可知,在氧化16 h后,W元素仍未参与氧化反应。
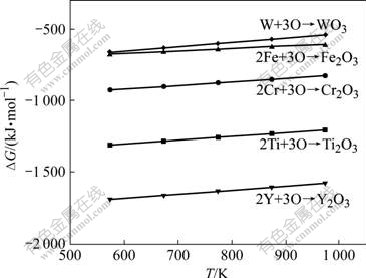
图7 不同氧化反应的自由能随温度的变化
Fig.7 Plot of ?G of different oxidation reaction vs temperature
4 结 论
1) 铁基合金粉末在500 ℃氧化时,前期氧化时间较短,氧化质量增量及氧含量的变化随氧化时间呈线性变化,但在粉末颗粒表面未能观察到氧化膜的形成;后期铁基合金粉末颗粒表层生成的Fe、Cr和Ti的氧化物混合组成的致密氧化膜,随氧化时间的延长氧化质量增量及氧含量的变化缓慢。
2) 铁基合金粉末500 ℃氧化符合动力学方程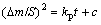 ,氧化16 h以内,氧化机制受表面反应控制。
,氧化16 h以内,氧化机制受表面反应控制。
REFERENCES
[1] 陈国胜, 周乐澄, 伍伯华, 奚壮行, 史新民, 张赫童. 铁基高温合金GH2871成分对组织和性能的影响[J]. 特殊钢, 1994, 15(6): 63?69.
CHEN Guo-sheng, ZHOU Le-cheng, WU Bo-hua, XI Zhuang-xing, SHI Xin-min, ZHANG He-tong. Influence of composition on structure and properties of iron-based superalloys GH2871[J]. Special Steel, 1994, 15(6): 63?69.
[2] 郝红元, 曹士锐, 郝 曜. 新型(A+F)双相铁基堆焊合金热处理工艺探讨[J]. 热加工工艺, 2006, 35(3): 8?10.
HAO Hong-yuan, CAO Shi-rui, HAO Yao. Heat treatment technology for two-phase iron-based high temperature alloy[J]. Hot Working Technology, 2006, 35(3): 8?10.
[3] CAPDEVILA C, BHADESHIA H K. Manufacturing and microstructural evolution of mechanically alloyed oxide dispersion strengthened superalloys[J]. Advanced Engineering Materials, 2001, 3(9): 647?656.
[4] KLUEH R L, SHINGLEDECKER J P, SWINDEMAN R W, HOELZER D T. Oxide dispersion-strengthened steels: A comparison of some commercial and experimental alloys[J]. Journal of Nuclear Materials, 2005, 341(2/3): 103?114.
[5] KLUEH R L, MAZIASZ P J, KIM I S, HEATHERLY L, HOELZER D T, HASHIMOTO N, KENIK E A, MIYAHARA K. Tensile and creep properties of an oxide dispersion-strengthened ferritic steel[J]. Journal of Nuclear Materials, 2002, (307/311): 773?777.
[6] MUKHOPADHAYAY D K, FROES F H, GELLES D S, Development of oxide dispersion strengthened ferritic steels for fusion[J]. Journal of Nuclear Materials, 1998, 258/263(2): 1209?1215.
[7] SCHAUBLIN R, RAMAR A, BALUC N, CASTRO V, MONGE M A, LEGUEY T, SCHMID N, BONJOUR C. Microstructural development under irradiation in European ODS ferritic/martensitic steels[J]. Journal of Nuclear Materials, 2006, 351(1/3): 247?260.
[8] CHEN J, JUNG P, POUCHON M A, REBAC T, HOFFELNER W. Irradiation creep and precipitation in a ferritic ODS steel under helium implantation[J]. Journal of Nuclear Materials, 2008, 373(1/3): 22?27.
[9] OHTSUKA S, UKAI S, SAKASEGAWA H, FUJIWARA M, KAITO, NARITA T. Nano-mesoscopic structural characterization of 9Cr-ODS martensitic steel for improving creep strength[J]. Journal of Nuclear Materials, 2007, 367/370(1): 160?165.
[10] OHTA J, OHMURA T, KAKO K, TOKIWAI M, SUZUKI T, Hardness of 12Cr-8Mo ferritic steels irradiated by Ni ions [J]. Journal of Nuclear Materials, 1995, 225: 187?191.
[11] RAMAR A, OKSIUTA Z, BALUC N, SCH?UBLIN R. Effect of mechanical alloying on the mechanical and microstructural properties of ODS EUROFER 97[J]. Fusion Engineering and Design, 2007, 82(15/24): 2543?2549.
[12] SAKASEGAWA H, OHTSUKA S, UKAI S, TANIGAWA H, FUJIWARA M, OGIWARA H, KOHYAMA A. Particle size effects in mechanically alloyed 9Cr ODS steel powder[J]. Journal of Nuclear Materials, 2007, 367/370(1): 185?190.
[13] SHAFRANOVSKY E A, PETROV Y I. Aerosol Fe nanoparticles with the passivating oxide shell[J]. Journal of Nanoparticle Research, 2004, 6: 71?90.
[14] OHTSUKA S, UKAI S, FUJIWARA M, KAITO T, NARITA T. Nano-structure control in ODS martensitic steels by means of selecting titanium and oxygen contents[J]. Journal of Physics and Chemistry of Solids, 2005, 66(1/2): 571?575.
[15] 梁英教, 车荫昌, 刘晓霞, 李乃军. 无机物热力学数据手册[M]. 沈阳: 东北大学出版社, 1993: 457?476.
LIANG Ying-jiao, CHE Yin-chang, LIU Xiao-xia, LI Nai-jun. Data manual of inorganic thermodynamics[M]. Shenyang: Northeastern University Press, 1993: 457?476.
基金项目:国家自然科学基金资助项目(50634060);国家自然科学基金创新群体资助项目(50721003)
收稿日期:2008-03-18;修订日期:2008-08-25
通讯作者:刘 咏,教授,博士;电话:0731-8830406;E-mail: yonliu@mail.csu.edu.cn
(编辑 陈爱华)