DOI: 10.11817/j.ysxb.1004.0609.2020-39188
��̼�������⾫�����ұ����������Ҫ����Ԫ�ص���Ϊ����
�� ��1, 2��������1, 2�������1, 2���� ��1, 2����־��1, 2
( 1. �����ɻ��Ƽ��ɷ�����˾������ 100081��
2. �����о���Ժ �Ƚ��������̼����Ϲ����ص�ʵ���ң����� 100081)
ժ Ҫ���������⾫�����ұ������������̼�۵ķ�������һ�������⾫�����ұ����������Ҫ����SiO2��MgO��Al2O3��CaO�ĺ���������ѧ������������SiO2��MgO��Al2O3��CaO���п�����̼������Ӧ��������̬���ʱ�ȥ���������о�������������⾫�����ұ�������м���̼�ۿ������Խ�������Si��Mg��Al��Ca�ĺ���������Si���ѳ���Լ�ﵽ100%��Mg���ѳ���Լ�ﵽ99.7%��Al���ѳ���Լ�ﵽ78.44%��Ca���ѳ������ԼΪ9.8%������ƷλΪ48%�ĵ�Ʒλ�⾫��Ϊԭ�ϣ��������ұ�����̣��õ��Ľ������Ʒ���⺬���ﵽ92%��S��������0.69%����Ҫ����Ԫ��SiO2��������0.0021%��Cu����С��0.005%��P����С��0.005%��Mg��������0.001%��Al��������0.64%��Ca����Ϊ0.51%��
�ؼ��ʣ��⾫��̼�����ұ��������Ԫ�أ��������Ʒ
���±�ţ�1004-0609(2020)-02-0438-09���� ��ͼ����ţ�TF841.2���� ���ױ�־�룺A
���������Ȼ��������й�ҵ��������ʯ���ڴ�ͳ��ұ�������У����⾫���������չ����ͷų��Ķ�������Ի���Σ��������ұ�����̳������ո��ӣ�����յ��ʽϵ�[1]��Ϊ�˽����Щ���⣬��ұ����������˺ܶ���¹��գ����������ֱ���ԭ[2]��ʯ���������շ�[3-4]���Ȼ�����[5]��ˮ����������[6]��ʪ���ֽ�[7-9]������ұ��[10]�ȣ�������Щ���ն�û�еõ����ģӦ�á�
�����о���Ժ��2008�꿪ʼ�����⾫����շֽ�Ĺ�������[11-14]������Ҫ˼·�ǽ��⾫���������¯�ڼ���ʹ��ֽ⣬һ��ֱ�ӵõ�������ۺ�������ֲ�Ʒ�����ô˹��վ������̶̡��������ŵ㡣ʵ���о�����������⾫����1748 K��ѹ��1~100 Pa��Χ֮��ʵ����ȫ�ֽ��ǿ��еģ��ڴ������£��⾫����������ֽ�[15-16]�����ô˹��յõ��˺ܺõIJ�Ʒ������һ���Ĺ�ҵӦ��ǰ����
�о�����[17]���⾫���е�SiO2��CaO��MgO��Al2O3����շֽ�����к��ѱ�ȥ���������⾫���м���̼���ܼ���شٽ���շֽⷴӦ���У��ҵõ��Ľ������Ʒ�е�Si��Ca��Mg��Al������Ԫ�صĺ������Խ��ͣ����Ǵ˹����п��ܷ����ķ�Ӧ����Ԫ�ص�����ֲ������������ˣ�����ͨ�����⾫����շֽ�����е�����Ԫ�ؿ��ܵ���Ϊ��������ѧ������������ʵ�������֤���õ�Ӱ���⾫��ֽ��������Ҫ����Ԫ��Si��Ca��Mg��Al����Ĺ��ɣ�Ϊ�⾫�����ұ�������������ṩ����ָ����
1 �⾫���������
���о���ʹ�õ��⾫��ԭ��Ϊij��ҵ��������ƷλΪ48%�ĵ�Ʒλ�⾫������Ҫ�ɷ����1���С�
�ɱ�1�п��Կ����������⾫�����ƷλԼΪ48.32%�����ڽϵ�Ʒλ�⾫����Ҫ����ΪSiO2��FeS2��Al2O3��CaO��MgO�������������ͼ1��ʾ��
��1 �⾫����Ҫ�ɷ����
Table 1 Chemical composition of molybdenite concentrates (mass fraction, %)

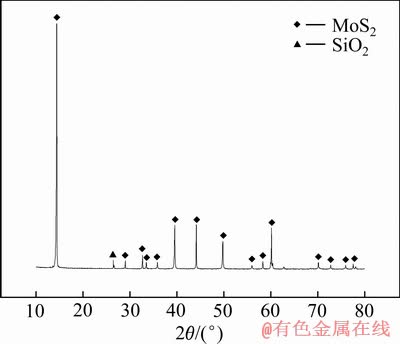
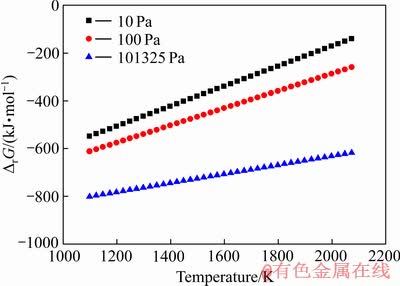
ͼ1 �⾫�����XRD��
Fig. 1 XRD pattern of molybdenite concentrates
��ͼ1���Կ������⾫����Ҫ����ΪMoS2����������SiO2����ϻ�ѧ�ɷַ�����֪���⾫����MoS2�������Դﵽ80.5%����Ҫ�����У�SiO2������ߣ��ɴﵽ7.0%��Al2O3����Ϊ3.02%��CaOΪ0.35%��MgOΪ0.18%����ˣ����ĵ��о�����Ϊ��Ҫ����SiO2��MgO��Al2O3��CaO�����ұ�������е���Ϊ��
2 ���̼�Ȼ�ԭȥ������Ԫ�ص�����ѧ����
�����⾫���е�����SiO2��CaO��MgO��Al2O3��������շֽ������ֱ��ȥ�����������⾫���м���������ԭ��̼�ķ�����ʹSiO2��CaO��MgO��Al2O3��̼������Ӧ���Դﵽȥ�����߽�������Si��Ca��Mg��Al������Ŀ�ġ����ڸ���Ӧ����������½��У�����Ӧ����������д�����������ҷ�Ӧǰ�����Ħ�����������仯���˷�Ӧ�������������Ӱ�죬��ˣ����о��ж�������ֵ�ƽ���ѹ�����ص��о�����ij��Ӧ���������ֵ�ƽ���ѹ�ܺʹﵽѹ��Ҫ��ֵ(��ն�)ʱ���˷�Ӧ��˳������[18-19]��
2.1 SiO2��C�ķ�Ӧ
���⾫���м�������̼�ۺ������ұ�������£��⾫���е�SiO2������̼������Ӧ������ܷ����ķ�Ӧ���2����[20]��
SiO2�Ļ�ԭ���̽�Ϊ���ӣ���������Ľ���Ҳ������ͬ����������ķ�Ӧʽ��һ�µġ���ͬѹ���£�SiO2����ԭ�ķ�Ӧ������˹������������ѧ�¶�(T)�Ĺ�ϵ���2���С�
���о���SiO2�Ļ�ԭ��Ӧ��1~100 Pa�½��У���˷ֱ��SiO2�Ļ�ԭ��Ӧ�ļ���˹�������ڱ�����ѹ��100 Pa��10 Pa��1 Pa�½��м��㣬�����ͼ2��ʾ��
�ڱ�����ѹ(101325 Pa)�£����о����¶ȷ�Χ�ڣ���Ӧ(1)��(2)��(3)��(5)��(6)��(7)����������У�����ѹ�����ͣ��������з�Ӧ(1)~(9)����������С����з�Ӧ(3)�������У���Ӧ(1)��(2)Ҳ�������У�����Ӧ(7)Ҳ�ɽ��У��ҷ�Ӧ(7)�ɿ�����Ӧ(2)�ͷ�Ӧ(3)����ϣ����߷�Ӧ(2)�ͷ�Ӧ(4)����ϣ���Ӧ(8)Ҳ�ɽ��У��ҷ�Ӧ(8)�ɿ�����Ӧ(1)�ͷ�Ӧ(3)����ϣ������������������ĵķ�Ӧ�ͽϸ��ӡ���Ӧ(5)�ļ���˹���������о����¶ȷ�Χ�ں�Ϊ�����䷢���Ŀ�����Ҳ�ܴ�Ӧ(5)�ͷ�Ӧ(7)Ϊ�������෴Ӧ���ڵ�ѹ�����£�����������SiO��ܿ챻���ߣ���̼��SiO���������Ҳ��������˷�Ӧ(5)�ͷ�Ӧ(7)���ܽ��е��Ȼ��С�����������SiO���壬�����¶ȵĽ��ͣ������绯��Ӧ(��Ӧ(6))������������ԭ��Ӧ���ɵ�Si�ڽϸߵ��¶��£�Ҳ�ɻӷ������������ʽ�����ߣ����������¶ȵĽ��ͣ���һ�������¯���²������ᡣ�������⾫���е�SiO2�ɱ���ԭΪSiO���屻ȥ�������߱���ԭΪSi����������̬��ʽȥ����
��2 ���������SiO2��C�ķ�Ӧ
Table 2 Possible reaction of SiO2 and C under vacuum condition
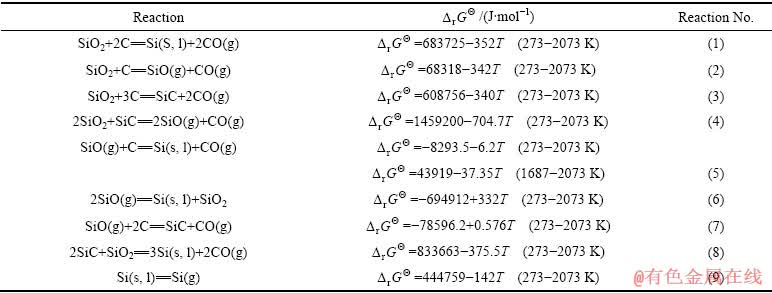
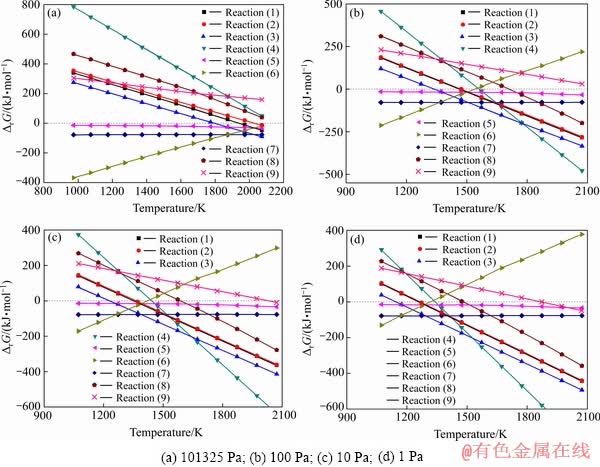
ͼ2 ��ͬѹ���¶���������ܷ����ķ�Ӧ�ļ���˹������
Fig. 2 Gibbs free energy of possible reactions of SiO2 vs temperature under different pressures
2.2 CaO��C�ķ�Ӧ
���⾫���м���̼֮������������£����е�CaO������̼�����ķ�Ӧ����[21]��
1.5S2(g)+2CaO=2CaS+SO2(g)
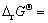 -168733+56T (273-2073 K) (10)
-168733+56T (273-2073 K) (10)
CaO+C=Ca(g)+CO(g)
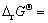 692204-291T (273-2073 K) (11)
692204-291T (273-2073 K) (11)
2CaS+C=2Ca(g)+CS2(g)
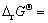 1405312-398T (273-2073 K) (12)
1405312-398T (273-2073 K) (12)
CaS+C=Ca(g)+CS(g)
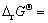 922350-285T (273-2073 K) (13)
922350-285T (273-2073 K) (13)
CaO���ܷ����ķ�Ӧ��ƽ��ѹ�����¶ȵĹ�ϵ��ͼ3��ʾ����ͼ3���Կ��������⾫���м���̼֮������ѹ��Ϊ1~100 Paʱ��CaO����C������Ӧ����Ca������CO���ڴ������£��⾫��ֽ�õ���S2Ҳ������CaO������Ӧ����CaS����CaS�ֽ���ѡ��ڴ���̼������£����¶ȸ�����ѹ������ʱ��CaS�ɱ���ԭΪCa������CS���塣������⾫���м���̼�����е�CaO������Ca������ʽȥ��������ת��ΪCaS��Ȼ���ڸ��ߵ��¶��Լ����͵�ѹ���£��ٲ��ַֽ����ԭΪCa������ȥ����
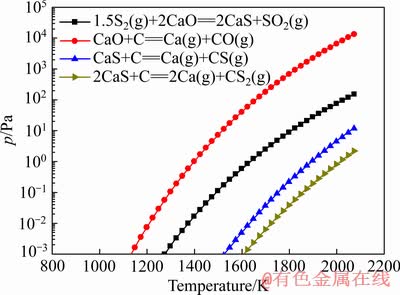
ͼ3 �����ƿ��ܷ�����Ӧ��ƽ��ѹ�����¶ȵĹ�ϵ
Fig. 3 Equilibrium pressures of possible reactions of CaO vs temperature
���⾫���У���Ҫ����ΪMoS2��������ֻ����CaO��C�ķ�Ӧ����CaO���ڵ�����£�MoS2����C��CaO������Ӧ���䷴Ӧ��ʼ���¶�Ҳ�ϵ͡������߽��жԱȣ������ͼ4��ʾ��
��ͼ4�п��Կ�������ѹ��Ϊ1~100 Paʱ��MoS2����C��CaO������Ӧ���¶����Ե���CaOֱ�ӱ�̼��ԭ���¶ȣ���ˣ��⾫���е�CaO��������̼���ڵ��������MoS2������Ӧ������CaS��Mo��CO����������CaS�ڽϸ��¶�1873 K(1600 ������)Ҳ����̼������Ӧ������Ca������CS��
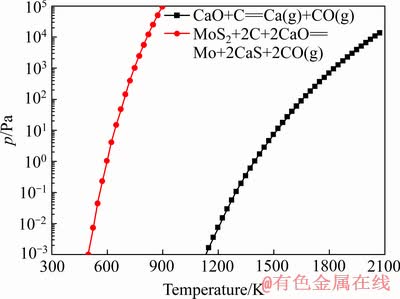
ͼ4 �����ƿ��ܷ�����Ӧ��ƽ��ѹ�����¶ȵĹ�ϵ
Fig. 4 Equilibrium pressures of possible reactions of CaO vs temperature
��������������֪������CaO���ڵ�����£�̼������ԭMoS2��CaO�ɴٽ�MoS2�Ļ�ԭ��������CaO�п��ܱ�ֱ̼�ӻ�ԭ��������CaS���ٱ�̼��ԭ����������CaS��̼��ԭ���¶Ƚϸߣ�����⾫���е�CaO���ܱ�ֱ̼�ӻ�ԭȥ����������CaS��
2.3 MgO��C�ķ�Ӧ
�⾫���е�Mg��Ҫ��MgO��ʽ���ڣ������⾫��Ʒλ�IJ�ͬ������MgO����Ҳ��ͬ��MgO���ȶ����ڵ�����շֽ������º��ѷֽ�ȥ���������⾫���м��뻹ԭ��̼֮��MgO��ȥ���ͱ�ÿ��ܡ������̼���������£�����ܷ����ķ�Ӧ����[22-24]��
Mg=Mg(g)
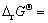 136931+99T (273-2073 K) (14)
136931+99T (273-2073 K) (14)
MgO+C=Mg(g)+CO(g)
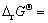 629567-299T (273-2073 K) (15)
629567-299T (273-2073 K) (15)
2MgO=2Mg(g)+O 2(g)
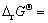 1483602-424T (273-2073 K) (16)
1483602-424T (273-2073 K) (16)
MgO+CO(g)=Mg(g)+CO2(g)
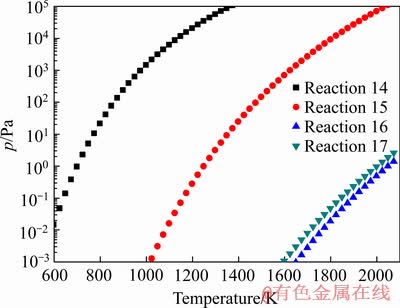
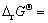 459481-125T (273-2073 K) (17)
459481-125T (273-2073 K) (17)
����þ���ܷ�����Ӧ��ƽ��ѹ�����¶ȵĹ�ϵ��ͼ5��ʾ����ͼ5���Կ�����Mg�Ļӷ������ף���ѹ��������1~100 Paʱ��Mg��773~860 K��Χ�ڼ��ɱ�ΪMg��������MgO�����ױ�̼��ԭ�����ɵ�Mg��������ʽ���ڣ������¯�б�����������¶ȵĽ���������MgOֱ�ӷֽ�õ�Mg��O2�ķ�Ӧ���ѽ��С���ˣ��⾫���е�MgO�����ױ�̼��ԭ��Mg������������ʽ�����ȥ����
ͼ5 ����þ���ܷ�����Ӧ��ƽ��ѹ�����¶ȵĹ�ϵ
Fig. 5 Equilibrium pressures of possible reactions of MgO vs temperature
2.4 Al2O3��C�ķ�Ӧ
�⾫���е�Al��Ҫ��Al2O3��ʽ���ڣ������⾫��Ʒλ�IJ�ͬ����Al2O3�ĺ���Ҳ����ͬ��Al2O3���ȶ����ڵ������ұ�������º���ȥ���������⾫���м��뻹ԭ��̼֮��Al2O3��ȥ��Ҳ��ÿ��ܡ��⾫���м���̼�ۺ�����������£�Al2O3���ܷ����ķ�Ӧ����[25-27]��
Al=Al(g)
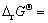 319448-119T (273-2073 K) (18)
319448-119T (273-2073 K) (18)
Al2O3+C=2AlO(g)+CO(g)
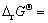 1405312-398T (273-2073 K) (19)
1405312-398T (273-2073 K) (19)
Al2O3+3C=2Al(g)+3CO(g)
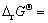 125497-561T (273-2073 K) (20)
125497-561T (273-2073 K) (20)
3Al2O(g) =4Al+Al2O3
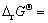 -1110913+583T (273-933 K) (21)
-1110913+583T (273-933 K) (21)
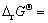 -1008089+476T (933-2073 K) (22)
-1008089+476T (933-2073 K) (22)
���������ܷ�����Ӧ��ƽ��ѹ�����¶ȵĹ�ϵ��ͼ6��ʾ����ͼ6��֪����ѹ����1~100 Pa��Χ��ʱ��Al2O3�ɱ�̼��ԭ����Al��������Al2O�������ʽ��ȥ����
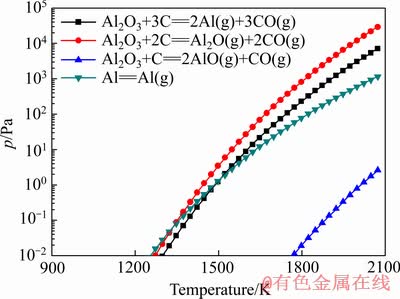
ͼ6 ���������ܷ�����Ӧ��ƽ��ѹ�����¶ȵĹ�ϵ
Fig. 6 Equilibrium pressures of possible reactions of Al2O3 vs temperature
��Al2O�绯��Ӧ�ļ���˹�����ܿ���֪������0~2073 K�¶ȷ�Χ�ڣ��伪��˹�����ܺ�Ϊ��������䷴Ӧ�������С�������Al2O���绯��Ӧ���������С�ķ�Ӧ�����ѹ�����ͻ���绯��Ӧ�Ľ��в���һ��Ӱ�졣��ͬѹ����Al2O�绯��Ӧ�ļ���˹�����ܿ���ʽ(23)���㣬�������õ��IJ�ͬѹ����Al2O�绯��Ӧ��Ӱ����ͼ7��ʾ��
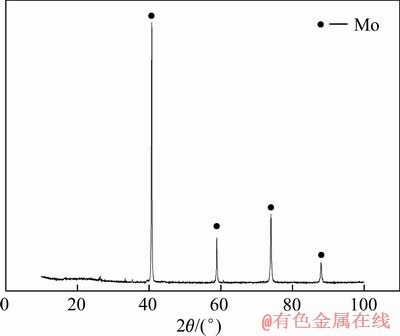
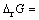 -1008089+476T-24.942
-1008089+476T-24.942 (23)
(23)
ͼ7 ��ͬѹ����Al2O�����绯��Ӧ�ļ���˹������
Fig. 7 Gibbs free energy of disproportionation reactions of Al2O vs temperature under different pressure
��ͼ7���Կ�������Ȼ����ѹ��������Al2O�绯��Ӧ������У���������ѹ��Ϊ10 Pa��100 Pa��101325 Paʱ��Al2O�����绯��Ӧ�ļ���˹�����ܾ�Ϊ������ˣ����Ʒֽ�ѹ��Ϊ10~100 Paʱ��Al2O���绯��Ӧ���Է�����
��ˣ��⾫���е���������̼���ڵ������£��ɱ���ԭ��Al�������Al2O���屻ȥ��������Al2O�ᷢ���绯��Ӧ�������¶��������绯��Ӧ������С������Ʒֽ�ѹ��Ϊ10~100 Paʱ��Al2O�ᱻ������������¶ȵĽ��ͷ����绯��Ӧ��
3 ���ұ�������о�
3.1 ʵ�鷽��
���⾫�������̼�۰���һ��������Ͼ��ȣ�����������ճ������������������423 K�¸���2 h��Ȼ��ȡ�����á�ȡ����õ����ŷ������ұ��¯�У�������1773 K������2 h�����������б���Ŀ��ѹ��Ϊ30~50 Pa�����ֽ����ʱ���������ұ��¯�ڵ�ѹ��ʹ������¯��ȴ�����£�Ȼ��ȡ��������
��ȡ������Ʒ�Լ��ܱ��ϵĻӷ�����л�ѧ�ɷ֡����������
ʵ������л���̼�۵ļ���������SiO2��CaO��MgO��Al2O3��̼��Ӧ��ȥ���Ļ�ѧ��Ӧ�����ȼ��룬�����̼����������mC:more=5:100��
3.2 �������Ʒ����
���õ��Ľ������Ʒ����ò��ͼ8��ʾ��
��ͼ8���Կ���������֮���������սᣬ��ɫΪ��ɫ�н��������������һ���̶ȵ�����������Ҫ���������е�������ӵĻ���̿�ڸ������ұ�������б�ȥ�����¡�

ͼ8 �������Ʒ��ò
Fig. 8 Morphology of metal molybdenum product
��ͼ8�е����Ž���XRD�����������ͼ9��ʾ����ͼ9���Կ��������õ��IJ�ƷΪ�����⣬˵�����õ��IJ�Ʒ�������Ѻ��٣������⺬���ܸߡ�
ͼ9 ���ò�Ʒ��XRD��
Fig. 9 XRD pattern of metal molybdenum product
�����õ��Ľ������Ʒ���л�ѧ�������ɵõ��仯ѧ�ɷ����3���С�
��3 ���õ�������Ļ�ѧ�ɷ�
Table 3 Chemical composition of metal molybdenum products (mass fraction, %)
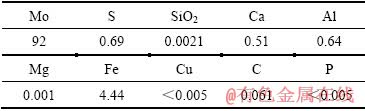
�ɱ�3���Կ������������е��⺬���ﵽ��92%��S��������0.69%����Ҫ����Ԫ��SiO2����0.0021%��Cu��0.005%��P����С��0.005%������̼������Ԫ�ؾ������½���������Ϊ4.44%������û��ȥ��������Al��δ����ȫȥ�������Al��Ȼ��Al2O3����ʽ���ڣ�Al2O3����ԼΪ1.21%�����⣬���ò�Ʒ������ܴ�����������[15]��
3.3 �ӷ������
�ڷֽ�����У������ұ��¯�ܱ��ϳ������������֮�⣬���кܶ�Ļӷ�����ڣ�����ò��ͼ10��ʾ����ͼ10���Կ������ӷ���ճ�������¯�ܵĸ����ͷ�ϣ�����Ϊ�ƺ�ɫ���ڲ�Ϊ��ɫ���ʣ�������Ϊ������ջ�ԭ�ֽ�����в����������ڶ�ͷ�������õ��ġ�������������������XRD����ͼ11��ʾ����ͼ11���Կ������õ������ʳʷǾ�̬�������ԵĹİ����Ա���İ���λ���Լ�������λ�ã��ɵõ��˻ӷ�����ҪΪSiO2�����Ǿ�̬����̬�п��������ڸ����µ������ڱõ������±�������ڵ�����������ȴ����ɵġ�������гɷַ������ɵõ��仯ѧ�ɷ����4���С�

ͼ10 �ܱ��ϵĻӷ���
Fig. 10 Morphology of volatile matters
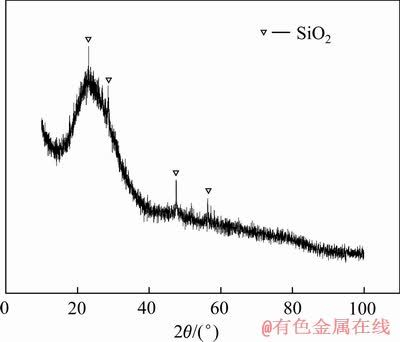
ͼ11 �ܱ��ϻӷ����XRD��
Fig. 11 XRD pattern of volatile matters
��4 �ӷ������Ҫ��ѧ�ɷ�
Table 4 Chemical composition of volatile matters (mass fraction, %)
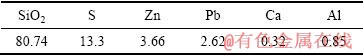
�ɱ�4�п��Կ�������Ҫ�ɷ�ΪSiO2������SiO2�ĺ����ɴﵽ80.74��������Ҫ�ɷ�ΪS��Zn��Pb��Ca��Al�ȡ����ڻӷ����е�Si��ҪΪSiO2�����ǰ�������ѧ������֪������Ҫ��������̼���ڵ�����£�SiO2��̼������Ӧ��������SiO���屻��������ڳ�������У������¶Ƚ��ͣ�SiO���������������绯��Ӧ������SiO2��Si�����ӷ����д��ڵ�Si����������������Ӧ������SiO2��
�����Ա�ԭ�����Ʒ�е����ʺ���������Si���ѳ���Լ�ﵽ100%��Mg���ѳ���Լ�ﵽ99.7%��Al���ѳ���Լ�ﵽ78.44%������̼���������ӣ����ѳ��ʿ��ܻ��һ����ߡ�Ca���ѳ���ԼΪ9.8%��Ca ���ѳ��ʽϵͣ����п�������û����ȫ��̼������Ӧ��Ϊ������ȥ�����������⾫���е�S������Ӧ����CaS������CaS��ʽ���ڡ�CaS��һ�ֺ���ȥ�������ʣ���ֽ���Ҫ���ߵ��¶Ⱥ��͵�ѹ���������ڽ������Ʒ��CaS�ij��֣�Ҳ��Ȼ��ʹ����Ӧ����Ӱ�죬���Ӧ��������CaS�ij��֡�
�ۺ�������������֪�������⾫���м���̼�ۣ����������е�����SiO2��CaO��MgO��Al2O3��ȥ��������Ϊ��ȥ�����е�SiO2��CaO��MgO��Al2O3�����������̼�ۣ����ڷֽ�������ֲ���ʹ̼ȫ����Ӧ��ϣ���Ȼ��������ղ�Ʒ��̼�����ϸߣ�����ʹ�ֽ�õ���Mo����̼��������Mo2C����MoC��Ӱ�����Ʒ������
4 ����
1) ���⾫�����ұ�������м���̼�ۣ����������е�����SiO2��CaO��MgO��Al2O3��ȥ��������Si���ѳ��ʴﵽ��Լ100%��Mg���ѳ��ʴﵽ��Լ99.7%��Al���ѳ��ʴﵽԼ78.44%������̼���������ӣ����ѳ��ʿ��ܻ��һ����ߡ�Ca���ѳ������ԼΪ9.8%��
2) ����ƷλΪ48%�ĵ�Ʒλ�⾫��Ϊԭ�ϣ��ڼ���̼�����ұ���������£��õ��Ľ������е��⺬���ﵽ��92%��S��������0.69%����Ҫ����Ԫ��SiO2����0.0021%��Cu��0.005%��P����С��0.005%��Mg����0.001%��Al����0.64%��Ca����Ϊ0.51%������̼������Ԫ�ؾ������½���������Ϊ4.44%������û�б�ȥ����
3) SiO2��̼������Ӧ������SiO���屻��������ڳ�������У������¶Ƚ��ͣ�SiO���������������绯��Ӧ������SiO2��Si��Al2O3�ɱ���ԭ��Al�������Al2O���壬��ȥ��������Al2O�ᷢ���绯��Ӧ��MgO�����ױ�̼��ԭ��Mg������������ʽ�����ȥ����Ca���п���û����ȫ��̼������Ӧ��Ϊ������ȥ�������Ǵ����⾫���е�S������Ӧ����CaS������CaS��ʽ���ڡ�
4) ���ռ����Ļӷ�����з�������Ҫ�ɷ�ΪSiO2������SiO2�ĺ����ɴﵽ80.74%��������Ҫ�ɷ�ΪS��Zn��Pb��Ca��Al�ȡ�
REFERENCES
[1] ������, ������. ����ұ��[M]. ����: ұ��ҵ������, 2005: 163-237.
ZHANG Qi-xu, ZHAO Qin-sheng. Metallurgy of molybdenum and tungsten[M]. Beijing: Metallurgical Industry Press, 2005: 163-237.
[2] �����, ������, �� ��. �����ֱ���ԭ���յ�����ѧ�о�[J]. ��ɫ����(ұ������), 2010(3): 2-4.
WANG Duo-gang, GUO Pei-min, ZHAO Pei. Thermodynamic analysis on direct reduction process of molybdenite with hydrogen[J]. Nonferrous Metals (Metallurgy Part), 2010(3): 2-4.
[3] ������, �����, �� ��. �������������չ��յ�����ѧ����[J]. ��ɫ����(ұ������), 2010(2): 6-8.
GUO Pei-min, WANG Duo-gang, ZHAO Pei. Thermodynamic analysis on non-oxidation of molybdenite roasting process[J]. Nonferrous Metals (Metallurgy Part), 2010(2): 6-8.
[4] Ф ��, Ф����, �� ��, �� ��, �ߴӈ�. MoS2-CaO-O2ϵ����ѧ������Ӧ��[J]. ϡ�н���, 2016, 40(4): 356-362.
XIAO Chao, XIAO Lian-sheng, XIA Yun, ZENG Li, GAO Cong-kai. Thermodynamic analysis of MoS2-CaO-O2 System and its application[J]. Rare Metal, 2016, 40(4): 356-362.
[5] ������, ��ѧ��, ������, �����, ������, ��С��. ������ۺ����ù��̼��о���״[J]. ϡ�н���, 2012, 36(2): 153-160.
WANG Ming-yu, WANG Xue-wen, JIANG Chang-jun, MA Yi-qian, FAN Ye-ye, XIANG Xiao-yan. Comprehensive utilization process and research status of Ni-Mo ore[J]. Chinese Journal of Rare Metals, 2012, 36(2): 153-160.
[6] BLANCO E, SOHN H Y, HAN G, HAKOBYAN K Y. The kinetics of oxidation of molybdenite concentrate by water vapor[J]. Metallurgical and Materials Transactions B, 2007, 38(4): 689-693.
[7] AFSAHI M M, SOHRABI M, KUMAR R V, EBRAHIM H A. A study on the kinetics of hydrogen reduction of molybdenum disulfide powders[J]. Thermochimica Acta, 2008, 473(1/2): 61-67.
[8] WANG Ming-shuang, WEI Chang, FAN Gang, DENG Zhi-gan, WANG Si-fu, WU Jun. Molybdenum recovery from oxygen pressure water leaching residue of Ni-Mo ore[J]. Rare Metals, 2013, 32(2): 208-212.
[9] EBRAHIMI-KAHRIZSANGI R, ABBASI M H, SAIDI A. Molybdenite alkali fusion and leaching: Reactions and mechanism[J]. International Journal of Minerals, Metallurgy and Materials, 2010, 17(2): 127-131.
[10] ������, �½���, �� ��. ͭ�����������������о���״����չ[J]. ϡ�н���, 2012, 36(5): 822-829.
YANG Xiao-long, WEN Jian-kang, WU Biao. Research status and process in bioleaching of Cu-Ni polymetallic sulphidedeposite[J]. Chinese Journal of Rare Metals, 2012, 36(5): 822-829.
[11] CAO Zhan-fang, ZHONG Hong, QIU Zhao-hui, LIU Guang-yi, ZHANG Wen-xuan. A novel technology for molybdenum extraction from molybdenite concentrates[J]. Hydrometallurgy, 2009, 99(1/2): 2-6.
[12] ZHOU Qiu-sheng, YUN Wei-tao, XI Jun-tao, LI Xiao-bin, QI Tian-gui, LIU Gui-hua, PENG Zhi-hong. Molybdenite- limestone oxidizing roasting followed by calcine leaching with ammonium carbonate solution[J].Transactions of Nonferrous Metals Society of China, 2017, 27(7): 1618-1626.
[13] ������, �ӽ���, �� ��. ��һ����ұ�����������������Ʒ�Ŀ���[J]. ��ɫ����(ұ������), 2012(6): 54-57.
GUO Pei-min, PANG Jian-ming, ZHAO Pei. New technology of molybdenum metallurgy and development of new steelmaking molybdenum product[J]. Nonferrous Metals (Metallurgy Part), 2012(6): 54-57.
[14] ��ά��, ��ά��, ������. �⾫����շֽ��Ʊ��ߴ�������ķ���: �й�ר��, 200810230851.X[P]. 2010-09-29.
ZHAO Wei-geng, ZHAO Wei-bao, GUO Pei-min. Preparation of high molybdenum oxide by vacuum decomposition from molybdenum concentrate: China Patent, 200810230851.X[P]. 2010-09-29.
[15] �� ��, ������, �ӽ���, �� ��. �⾫����շֽ�����е����༰��ò�仯[J]. ϡ�н���, 2016, 40(1): 64-70.
WANG Lei, GUO Pei-min, PANG Jian-ming, ZHAO Pei. Phase and morphology evolution in vacuum decomposition process of molybdenum concentrate[J]. Chinese Journal of Rare Metals, 2016, 40(1): 64-70.
[16] WANG Lei, GUO Pei-min, PANG Jian-ming, LUO Lin-gen, ZHAO Pei. Phase change and kinetics of vacuum decomposition of molybdenite concentrate[J]. Vacuum, 2015, 116: 77-81.
[17] �� ��, ������, �ӽ���, �� ��. �⾫����շֽ������ѧ����[J]. �й���ɫ����ѧ��, 2015, 25(1): 190-196.
WANG Lei, GUO Pei-min, PANG Jian-ming, ZHAO Pei. Thermodynamic analysis of vacuum decomposition process of molybdenum concentrate[J]. The Chinese Journal of Nonferrous Metals, 2015, 25(1): 190-196.
[18] ��Ӣ��, ������. ��������ѧ�����ֲ�[M]. ����: ������ѧ������, 1993: 240-241.
LIANG Ying-jiao, CHE Chang-yin. Inorganic chemical thermodynamics manual[M]. Shengyang: Northeastern University Press, 1993: 240-241.
[19] Ҷ����, ������. ʵ����������ѧ�����ֲ�[M]. ����: ұ��ҵ������, 2002: 1-30.
YE Da-lun, HU Jian-hua. Practical inorganic chemical thermodynamics data manual[M]. Beijing: Metallurgical Press, 2002: 1-30.
[20] LOUTZENHISER P G, TUERK O, STEINFELD A. Production of Si by vacuum carbothermal reduction of SiO2 using concentrated solar energy[J]. JOM, 2010, 62(9): 49-54.
[21] HU Fa-ping, PAN Jia, MA Xin, ZHANG Xi, CHEN Jie, XIE Wei-dong. Preparation of Mg and Ca metal by carbothermic reduction method�CA thermodynamics approach[J]. Journal of Magnesium and Alloys, 2013, 1(3): 263-266.
[22] YANG Cheng-bo, TIAN Yang, QU Tao, YANG Bin, XU Bao-qiang, DAI Yong-nian. Analysis of the behavior of magnesium and CO vapor in the carbothermic reduction of magnesia in a vacuum[J]. Journal of Magnesium and Alloys, 2014, 2(1): 50-58.
[23] TIAN Yang, XU Bao-qiang, YANG Bin, YANG Chen-bo, QU Tao, LIU Da-chun, DAI Yong-nian. Magnesium production by carbothermic reduction in vacuum[J]. Journal of Magnesium and Alloys, 2015, 3(2): 149-154.
[24] TIAN Yang, XU Bao-qiang, YANG Cheng-Bo, YANG Bin, QU Tao, LIU Hong-xiang, DAI Yong-nian, LIU Da-chun. Analysis of magnesia carbothermic reduction process in vacuum[J]. Metallurgical and Materials Transactions B, 2014, 45(5): 1936-1941.
[25] YU Wen-zhan, YANG Bin, CHEN Xiu-min, JIANG Wen-long, YU Qing-chun, XU Bao-qiang. Thermodynamic calculation and experimental investigation on the products of carbothermal reduction of Al2O3 under vacuum[J]. Vacuum, 2012, 86(12): 2005-2009.
[26] VISHNEVETSKY I, EPSTEIN M. Solar carbothermic reduction of alumina, magnesia and boria under vacuum[J]. Solar Energy, 2015, 111: 236-251.
[27] VISHNEVETSKY I, BEN-ZVI R, EPSTEIN M, BARAK S, RUBIN R. Solar carboreduction of alumina under vacuum[J]. JOM, 2013, 65(12): 1721-1732.
Behavior analysis of main impurity elements in vacuum smelting of molybdenum concentrate with carbon
WANG Lei1, 2, GUO Pei-min1, 2, KONG Ling-bing1, 2, ZHAO Pei1, 2, TIAN Zhi-ling1, 2
(1. CISRI SUNWARD Technology Co., Ltd., Beijing 100081, China;
2. State Key Laboratory of Advanced Steel Process and Products, Central Iron and Steel Research Institute, Beijing 100081, China)
Abstract: In order to further reduce the impurities content of SiO2, MgO, Al2O3 and CaO in the vacuum smelting process of molybdenite concentrates, a method of adding carbon powder in the vacuum smelting process of molybdenite concentrates was adopted. Thermodynamic calculation results show that SiO2, MgO, Al2O3 and CaO may react with carbon to generate gaseous substances which can be removed by vacuum pump. The results show that the addition of carbon powder in the vacuum smelting of molybdenite concentrate can significantly reduce the contents of Si, Mg, Al and Ca. The removal rates of Si, Mg, Al can reach about 100%, 99.7%, and 78.44%, respectively. The max removal rate of Ca can reach about 9.8%. When 48% low-grade molybdenite concentrate are used as raw material in the vacuum smelting process, the content of Mo in the metal product can reach 92%, and the content of S decreases to 0.69%. The main impurity SiO2 decreases to 0.0021%, and the contents of Cu and P are all less than 0.005%, and the contents of Mg, Al and Ca are 0.001%, 0.64% and 0.51%, respectively.
Key words: molybdenite concentrates; carbon; vacuum smelting; main impurities; metal Mo
Foundation item: Project(U1560201) supported by the National Natural Science Foundation of China
Received date: 2018-09-20; Accepted date: 2019-07-20
Corresponding author: WANG Lei; Tel: +86-18811105273; E-mail: wangleivictory@sina.com
(�༭ ������)
������Ŀ��������Ȼ��ѧ����������Ŀ(U1560201)
�ո����ڣ�2018-09-20�������ڣ�2019-07-20
ͨ�����ߣ��� �ڣ�����ʦ����ʿ���绰��18811105273��E-mail��wangleivictory@sina.com