文章编号:1004-0609(2007)06-1008-06
颗粒活性炭对乳酸钠的吸附及其特性
王 璞,闵小波,柴立元,王云燕,方 艳,常 皓,袁 林
(中南大学 冶金科学与工程学院,长沙 410083)
摘 要:将颗粒活性炭碾磨处理后用于吸附乳酸钠,并采用单因子实验考察溶液pH值、温度对活性炭吸附量的影响。对吸附等温线的分析表明,碾磨时间不同的活性炭对乳酸钠的吸附行为均可用Freundlich方程描述,对比吸附常数和固相?水分配系数发现,碾磨30 min后活性炭的吸附能力最强;碾磨活性炭吸附乳酸钠的最佳pH为7.0,且吸附量受温度的影响不大。
关键词:颗粒活性炭;乳酸钠;碾磨;吸附
中图分类号:X 703 文献标识码:A
Adsorption of sodium lactate on modified active carbon and its characteristics
WANG Pu, MIN Xiao-bo, CHAI Li-yuan, WANG Yun-yan, FANG Yan, CHANG Hao, YUAN Lin
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: Four kinds of milled granule active carbons were used to adsorb sodium lactate through batch experiments. The adsorption isothermal curve, pH value of solution, and temperature were studied using one-factor experiment. The adsorption isotherms were analyzed. The results show that with the regression analysis of data, the adsorption behaviors of sodium lactate can be well described by Freundlich equation. The adsorption constant and distribution coefficient show that the adsorption capacity of granular active carbon(GAC) milled for 30 min is the strongest, the best pH value is 7.0, and the effect of temperature on adsorption capacity is little.
Key words: granular active carbon; sodium lactate; mill; adsorption
内聚营养源SRB污泥固定化技术是一项新的重金属废水处理技术,它将SRB生长所需的有机碳源经固定化后,与SRB污泥共同包埋于同一颗粒小球内部,构造SRB污泥生长良好的内部环境,所以该技术不仅具有生物法处理成本低、环境友好、处理效果好等特点[1?4],消除游离重金属离子对SRB的毒害[5?6],也解决人为添加有机碳源产生新污染的问题[7],同时更有利于SRB对营养物质的利用,可实现重金属水低廉价高效处理。前期实验研究发现,内聚营养源SRB污泥固定化处理重金属废水的效果明显优于游离SRB污泥和普通包埋SRB污泥[8],因此该技术极具应用潜力。
颗粒活性炭(GAC)因其大比表面积、高吸附能力和高表面活性而成为独特的多功能吸附剂[9?11],是一种理想的营养源固定化材料。此外,在制备培养基时常用乳酸钠作碳源[12?13],由于乳酸钠呈液体状态且易溶于水的,将它作为营养源吸附到活性炭中是一种可行的方案。本文作者在前期实验工作的基础上,研究不同颗粒活性炭固定乳酸钠的效果,选择适宜的乳酸钠固定化载体,并考察环境因子对乳酸钠固定化效果的影响,为营养源的固定化及营养源内聚技术提供理论依据,具有重要的理论与实践意义。
1 实验
1.1 实验试剂与仪器
实验所用试剂有:颗粒活性炭(AR)(国药集团化学试剂有限公司),乳酸钠(AR)(天津市科密欧化学试剂开发中心)。实验所用仪器有:HH?6化学耗氧量测定仪(江苏江分电分析仪器有限公司);HZ?9212S恒温振荡器(太仓市科教器材厂);AB204?N电子天平(METTER?TOLEDO GROUP);XPM?120三头球磨机(武汉探矿机械厂)。
1.2 样品制备
取一定量的颗粒活性炭放入三头球磨机碾磨,设定碾磨时间为10、20、30和40 min,碾磨后过过孔径1.18 mm的筛子,与之对应的筛选活性炭标记为样品B、C、D和E,最后将活性炭密封保存备用。未碾磨的活性炭标记为A。
1.3 吸附平衡
在6个250 mL锥形瓶中分别加入一定量的活性炭,再向每个锥形瓶中加入一定浓度的乳酸钠溶液,将各个锥形瓶分别放在振荡箱中,在温度(25±0.5) ℃时恒温振荡,定时取出分取滤液,测定滤液中的COD值,直至前后几次的COD值不变为止。同时进行仅加乳酸钠溶液但不加活性炭的空白实验以作对比。根据空白液和滤液中COD的差值计算吸附量,计算公式为:

1.4 乳酸钠的测定方法
经典的重铬酸法存在试剂费用高、二次污染、耗时等缺点,已不能适应日益繁重的环境污染监测需要。HH?6化学耗氧量测定仪采用密封催化消解法测定COD值:在强酸性溶液中,加入一定量的重铬酸钾作氧化剂,在专用复合催化剂存在下,于165 ℃恒温加热消解水样10 min,重铬酸钾被水中有机物还原为Cr3+,在波长610 nm处测定Cr3+含量,再根据Cr3+的量换算出消耗氧的质量浓度。
经过30个实验值取平均得出1 g/L乳酸钠溶液的COD值为234.5 mg/L,以此为根据换算乳酸钠的量。
2 结果与分析
2.1 不同活性炭的表面形貌
由于活性炭的吸附绝大部分发生在微孔内,因此吸附量受微孔的数量支配。尽管如此,大孔和中孔的作用也不能忽视。Dubinin等[14]的研究表明,只有少数微孔直接通向外表面,在绝大多数情况下,活性炭的孔隙结构主要按下列方式排列:大孔直接通向活性炭的外表面,过渡孔是大孔的分支,微孔又是过渡孔的分支。微孔的吸附作用是以大孔的通道作用和中孔的过渡作用为基础。因此,吸附性能好的活性炭在孔结构上应有充分发育的微孔,同时又有数量及排列均适宜的过渡孔和大孔。
活性炭B、C、D和E的表面形貌如图3所示。由图3可以看出,颗粒活性炭表面孔的结构会随碾磨时间的变化而发生改变。其中碾磨30 min后的活性炭,表面孔径、数量均比较均匀,Dubinin等的研究结果一致,而且从图2的结果来看,活性炭D对乳酸钠的吸附性能最好。
2.2 吸附性能
不同活性炭吸附量随时间的变化如图2所示。由图2可见,活性炭B、C、D和E对乳酸钠的吸附量分别为103.8、105.6、122.7和115.9 mg/g,并且达到平衡时所用的时间没有较大差别。随着吸附时间的延长,活性炭对乳酸钠的吸附量增大,但吸附速度减小,吸附10 min后基本达到平衡。故选定活性炭B、C、D和E的吸附平衡时间都为10 min。从吸附量来看,活性炭D对乳酸钠的吸附量最大。同时,颗粒活性炭经过适当碾磨有助于提高其吸附容量,但是如果碾磨时间超过30 min,活性炭的吸附容量将会降低。而未经碾磨的活性炭A对乳酸钠的吸附量(51.9 mg/g)仅为其他活性炭吸附量的一半左右,且COD值出现波动,故不再进行实验。
2.3 Freundlich吸附等温线
Freundlich等温式为

式中 qe为平衡时吸附剂对溶质的吸附量,mg/g;ce为平衡时水相中溶质的质量浓度,mg/L;KF为Freundlich吸附容量常数;1/n为等温线的线性因子,一般n值越大,吸附的非线性越大。
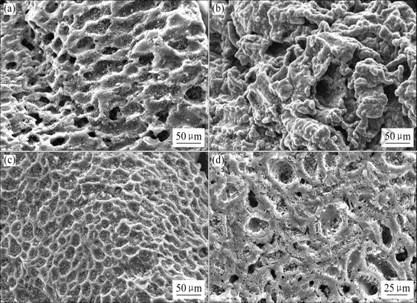
图1 不同活性炭的表面形貌图
Fig.1 Surface morphologies of different kinds of active carbons
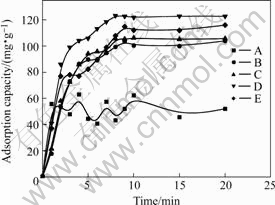
图2 不同活性炭的乳酸钠吸附量―时间曲线
Fig.2 Absorbed amounts―times curves of different milled granule active carbons for sodium lactate
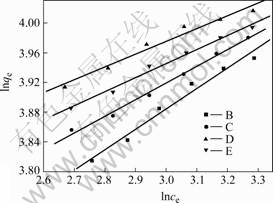
图3 不同活性炭的吸附等温线
Fig.3 Absorption isotherm curves of different kinds of active carbons
温度为(25±0.5)℃时活性炭B、C、D和E吸附乳酸钠的实验数据见表1。
表1 4种活性炭的等温吸附实验结果
Table 1 Isothermal absorption experimental results of four kinds of active carbons
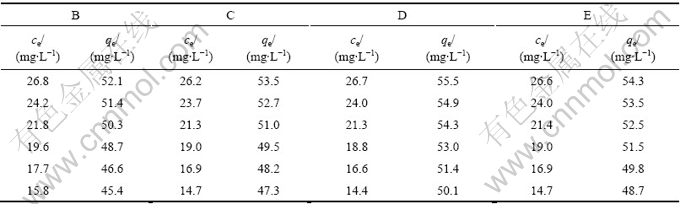
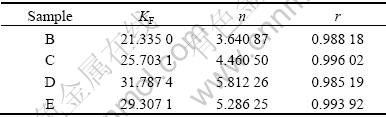
运用回归分析法即可求出活性炭B、C、D、E的Freundlich常数KF、1/n值,相应的参数列于表2中。活性炭B、C、D和E对乳酸钠的吸附等温线如图3所示。
表2 不同活性炭的Freundlich常数
Table 2 Absorption constants of different kinds of active carbons for Freundlich
活性炭的吸附形成有两种,线性吸附和非线性吸附。如果每一个微观吸附都为线性吸附,则总的吸附为线性吸附。相反,若其中如有一项或几项吸附为非线性吸附,那么整个吸附等温线将是非线性的形式。总之,线性部分的吸附服从相分配机理,而非线性部分则与表面反应有关[14]。从吸附数据可以看出,Freundlich模型可以很好地拟合吸附数据(R2>0.98),所有样品的吸附等温线均呈现出非线性,其中对乳酸钠的吸附量由大到小的样品顺序为:活性炭D>活性炭E>活性炭C>活性炭B,非线性由大到小的样品顺序为:活性炭D>活性炭E>活性炭C>活性炭B。
2.4 固相?水分配系数
为了评价在平衡条件下活性炭?溶液中乳酸钠与活性炭的缔合程度[15],需要了解乳酸钠在活性炭和水溶液中的总平衡浓度的比率(Kd)。这种比率定义为固相?水分配系数。

将式(4)代入式(2)中,即可得到Kd随乳酸钠浓度变化的规律,即

因此可以求得在不同水相平衡浓度下的固相?水分配系数。活性炭B、C、D和E的Kd随溶液浓度变化趋势见图4。
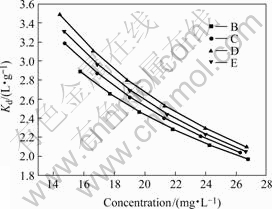
图4 不同活性炭的Kd随乳酸钠浓度的变化曲线
Fig.4 Variation curves of Kd with sodium lactate concentration of different kinds of active carbons
图4中曲线的变化趋势表明,随着乳酸钠在溶液中浓度的增大,Kd值变小,活性炭中乳酸钠的浓度也随之变小。活性炭B、C、D和E的Kd曲线变化平缓,所以当溶液中乳酸钠浓度低时,活性炭D的Kd值最大。
2.5 环境因子对营养源固定化的影响
2.5.1 pH值对营养源固定化的影响
取一定浓度的乳酸钠溶液分别加入锥形瓶中,然后在每个锥形瓶中加入一定量的活性炭B、C、D和E,调节pH到设定值(2.0、4.0、6.0、7.0、8.0、10.3和12.0)后将其置于25 ℃恒温水浴箱中,振荡10 min后取样分析。实验测定的结果如图5所示。由图5可以看出,当pH<7.0和pH>7.0时,大量的氢离子和氢氧根离子占据了活性炭的孔穴,不利于活性炭吸附乳酸钠。实验结果表明,pH 7.0是活性炭B、C、D和E对乳酸钠吸附的最佳pH值。
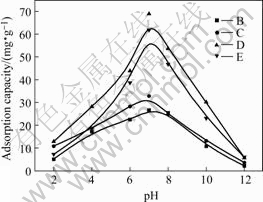
图5 pH值对乳酸钠吸附量的影响
Fig.5 Effect of pH on adsorption capacity of sodium lactate
2.5.2 温度对营养源固定化的影响
保持乳酸钠溶液的自然pH 值(6.98),调节恒温水浴箱温度到设定值(20、25、30、35和40 ℃),其后的实验步骤同2.5.1。实验结果见图6。从图6可知:在20~40 ℃范围内,温度对活性炭B、C、D和E吸附乳酸钠的影响不显著。但是如果温度超过40 ℃,那么活性炭对乳酸钠的吸附量将会有所下降。
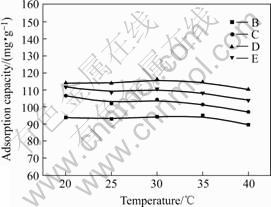
图6 温度对乳酸钠吸附量的影响
Fig.6 Effect of temperature on adsorption capacity of sodium lactate
3 结论
1) 乳酸钠静态吸附实验发现,经不同时间碾磨后的活性炭达到吸附平衡的时间约为10 min,不仅时间较短,而且吸附量大,其中碾磨30 min的活性炭的吸附量最大(122.7 mg/g)。未经碾磨的活性炭对乳酸钠的吸附效果不好。
2) 对吸附等温线分析发现Freundlich方程可以较好地描述乳酸钠在碾磨后的活性炭上的吸附行为。活性炭的Kd曲线变化平缓,说明低乳酸钠浓度有利吸附。
3) 适当碾磨可改变颗粒活性炭的孔结构和分布。由扫描电镜图可知,碾磨30 min后的活性炭孔径、数量均比较均匀,适合吸附乳酸钠。
4) 环境pH值变化对活性炭吸附乳酸钠的影响较大,pH7.0是最佳pH值。温度在20~40 ℃范围内对颗粒活性炭吸附乳酸钠无显著影响,但温度超过40 ℃时,吸附量则减少。
REFERENCES
[1] 沈 杰,张朝晖,周晓云,董丽辉. 生物法去除水中重金属离子的研究[J]. 水处理技术,2005, 31(3): 5?8.
SHEN Jie, ZHANG Zhao-hui, ZHOU Xiao-yun, DONG Li-hui. Removal of heavy metal ions by microorganism[J]. Technology of Water Treatment, 2005, 31(3): 5?8.
[2] 李长波,赵国峥,张洪林,蒋林时,苗 磊. 生物吸附剂处理含重金属废水研究进展[J]. 化学与生物工程,2006, 23(2): 10?12.
LI Chang-bo, ZHAO Guo-zheng, ZHANG Hong-lin, JIANG Lin-shi, MIAO Lei. The research development of treatment of wastewater with heavy metals using biological adsorbent[J]. Chemistry and Bioengineering, 2006, 23(2): 10?12.
[3] Arica M Y, Bayramoglu G, Yilmaz M, Bektas S, Genc O. Biosorption of Hg2+, Cd2+, and Zn2+ by Ca-alginate and immobilized wood-rotting fungus Funalia trogii[J]. Journal of Hzarzrdous Materials, 2004, 109(1/3): 191?199.
[4] Vilar Vitor J P, Botelho Cidalia M S, Boaventura Rui A R. Equilibrium and kinetic modeling of Cd(Ⅱ) biosorption by algae gelidium and agar extraction algal waste[J]. Water Research, 2006, 40(2): 291?302.
[5] Ueki K, Ueki A. Removal of sulfate and heavy metal from acid mine water by anaerobic treatment with cattle waste: effects of heavy metals on sulfate reduction[J], Environmental Science and Engineering, 1991, 26(8): 1471?1489.
[6] 冯易君,谢家理,向 芹,李福德. 共存离子对硫酸盐还原菌(SRB)处理含铬废水的影响研究[J]. 环境污染与防治,1995, 17(4): 15?17.
FENG Yi-jun, XIE Jia-li, XIANG Qin, LI Fu-de. Influences of coexistence ions on the treatment of Cr(Ⅵ) wastewater by sulfate reduce bacteria(SRB)[J]. Environmental Pollution and Control, 1995, 17(4): 15?17.
[7] Maree J P, Gerber A, Hill E. An integrated process for biological treatment of sulphate-containing industrial effluents[J]. WPCF, 1987, 59(12): 22?27.
[8] 唐 宁. 内聚营养源SRB污泥固定化技术处理高浓度含锌废水[D]. 长沙:中南大学,2004.
TANG Ning. The study on immobilized SRB sludge of inner cohesive nutrient source[D]. Changsha: Central South University, 2004.
[9] 赵振业,孙 伟,章诗芳,肖贤明. 活性炭对不同有机物吸附性能的影响[J]. 水处理技术,2005, 31(1): 23?25.
ZHAO Zhen-ye, SUN Wei, ZHANG Shi-fang, XIAO Xian-ming. Effect of active carbon on adsorption performance of different organic compounds[J]. Technology of Water Treatment, 2005, 31(1): 23?25.
[10] 解 强,张香兰,李兰廷,等. 活性炭孔结构调节:理论、方法与实践[J]. 新型炭材料,2005, 20(2): 183?190.
XIE Qiang, ZHANG Xiang-lan, LI Lan-ting, et al. Porosity adjustment of active carbon: theory, approaches and practice[J]. New Carbon Materials,2005, 20(2): 183?190.
[11] 李青刚,张启修,周康根. 活性炭去除工业钽液中有机物的研究[J]. 稀有金属与硬质合金,2004, 32(4): 1?3.
LI Qing-gang, ZHANG Qi-xiu, ZHOU Kang-geng. Study of organic matter removal from industrial H2TaF7 solution by active carbon[J]. Rare Metals and Cemented Carbides, 2004, 32(4): 1?3.
[12] 钱 卫,王肇颖,韩 波,肖 敏,杜桂彩,李永贵. 光合细菌中番茄红素的研究[J]. 山东大学学报(理学版),2004, 39(3): 111?115.
QIAN Wei, WANG Zhao-ying, HAN Bo, XIAO Min, DU Gui-cai, LI Yong-gui. Studies of lycopene from photosynthetic bacteria[J]. Journal of Shandong University, 2004, 39(3): 111?115.
[13] 姜 伟,赵德华,李 颖,田杰生,王珍芳,李季伦. 固氮条件下Greifswald磁螺菌的深层培养及其固氮活性的调节[J]. 科学通报,2002, 47(22): 1722?1725.
JIANG Wei, ZHAO De-hua, LI Ying, TIAN Jie-sheng, WANG Zhen-fang, LI Ji-lun. Submerged culture magnetospirillum gryphiswaldense under nitrogen-fixation and its nitrogen active adjustment[J]. Chinese Science Bulletin, 2002, 47(22): 1722?1725.
[14] Smisek M, Cerny S. Active carbon[M]. New York: Elservier, 1970.
[15] 水和废水监测分析方法编委会. 水和废水监测分析方法[M]. 第4版. 北京:中国环境科学出版社,2002.
Monitoring and Analysis Means of Water and Wastewater Editorial Board. Monitoring and analysis means of water and wastewater[M]. 4th ed. Beijing: Chinese Environment Science Press, 2002.
基金项目:国家自然科学基金资助项目(50508044);湖南省科技计划攻关重大专项基金资助项目(05SK1003-1)
收稿日期:2006-06-20;修订日期:2007-01-18
通讯作者:王 璞,电话:0731-8836804;E-mail: wangpu8123@163.com
(编辑 龙怀中)