����ʪ��ѧ��������̶���ѧ
Ф���������ƣ��δ��������壬���
(���ϴ�ѧ ұ���뻷��ѧԺ������ ��ɳ��410083)
ժҪ���������Ƶ���������Ż���������ղ������ȽϾ�̬�������붯̬�������Ч����ͨ���Ը������������Һ���෴Ӧ����ѧ���̵ķ����������2����������Ч�������ԭ���о�������������������������Ϊ60%����Ӧ�¶�Ϊ60 �棬����������Һ�̱�Ϊ30 mL/g�Լ�ʯ�ͽ�����С��106 ��mʱ�����þ�̬������ʱ��Ϊ24 h���������Ϊ53%�����ö�̬������ʱ��Ϊ12 h�������ʸߴ�72%�������ھ�̬�����µ��������ʿ��Ʋ���Ϊ����ɢ���ƣ���̬����������Ӧ�ı��ۻ��(Ea)Ϊ2.62 kJ/mol(ԶС��13.00 kJ/mol)��˵���ù��̵����ʿ��Ʋ���Ϊ����ɢ���ơ�
�ؼ��ʣ�����ʪ��ѧ���������ʣ�����ѧ����ɢ����
��ͼ����ţ�TF111.1 ���ױ�־�룺A ���±�ţ�1672-7207(2014)10-3339-05
Kinetics of high-sulfur petroleum coke desulfurization by wet-chemical method
XIAO Jin, DENG Songyun, HE Chuan, LAI Yanqing, LI Jie
(School of Metallurgy and Environment, Central South University, Changsha 410083, China)
Abstract: Using home-made desulfurizer and the optimized parameters of the desulfurization process, the static desulfurization process and dynamic process were compared, and the differences of the two desulfurization processes were elaborated by analyzing the kinetics. The results show that at the parameters (mass fraction of 60%, reaction temperature of 60 ��, liquid-solid rate of 30 mL/g, granularity <106 ��m), the static desulfurization rate is 53% after 24 h, while only 12 h later, the dynamic desulfurization rate can be up to 72%. The desulfurization of petroleum coke under static conditions is a reaction of external diffusion control, while this process under dynamic conditions is a reaction of internal diffusion control with apparent activation energy (Ea) of 2.62 kJ/mol (<13.00 kJ/mol).
Key words: high-sulfur petroleum coke; wet-chemical method; desulfurization rate; kinetics; diffusion-controll
�����������������⼰̿�ع�ҵ�����Խ��Խ��ij��[1-2]���о������������Ը����� ��⼰̿�ز��ϵ�������������������������ijɱ����ƽ�����ҵ�Ŀɳ�����չ������Ҫ����[3-7]��Ŀǰ ʯ�ͽ�������Ҫ�и������������������������ܼ����ᷨ�����������������ʪ��ѧ�������������(BDS)��[8-14]��Paul��[15-16]��ʯ�ͽ������������о������ֵ������¶ȸ���1 723 Kʱ��ʯ�ͽ��������Ե�����Ч�������¶����ߵ�1 923 Kʱ��ʯ�ͽ��������ʿ��Դﵽ90%���ϣ�Shlewit��[17]�����α���(�����������)�ķ�����ʯ�ͽ����������������о������У����Ƿ���ʯ�ͽ���400 ���½��м�����α��գ�ʯ�ͽ�������ѳ��ʿ��Դﵽ92%���ϣ����ͬʱ������������ʪ��ѧ���������Ѿ���չ�˴������о�[18-19]��ʵ����������ͨ���������Ƶ������Լ�����ʹ��ʯ�ͽ�����������߿ɴﵽ72%���ϡ�ʪ��ѧ����������2��������Ⱦ��кܶ��ŵ㣬�練Ӧ�����º͡�����ɱ��ϵ͡�ʵ�����̶����ײ����ȣ���Ϊͻ����������Ч�ѳ��������������ʽ���ڵ������ȶ����л���ʹ�ø������Ը�������������Ҫ����[20-22]������������ǰ���Ż��˹��������Ļ����ϣ��ȽϾ�̬�����붯̬����2�ַ�ʽ������Ч����Ӱ�죬Ȼ��ֱ���������������������Ӧ�¶ȡ�����������Һ�̱ȡ�����������ΪӰ�����ӶԸ������������Һ���෴Ӧ����ѧ���̽��з����������ض���ѧ�����þ�̬(��Ӧ��ϵ��ֹ)�Ͷ�̬(���ٽ��跴Ӧ��ϵ) 2������¸���ʪ��ѧ������Ӧ�Ŀ��Ʋ��衣
1 ����ʪ��ѧ������Ӧ�������
ʪ��ѧ������Ӧ���Կ����������������еĹ�̬�����������Ӧ���ڷ����о�������������ķ�Ӧ����ѧʱ������Ҫ���˽�һ�������·�Ӧ����ɲ�������ʱ���ʽ���ٰ�����̬����ԭ������������̣���ȷ����Ӧ���������Ʋ��輰�����ʽ��Ȼ��һ��������������·�Ӧ���ʻ�Ӧ��һ���̶������ʱ�䣬�������������ض��ٶȵ�Ӱ��[23]���������������Һ�̷�Ӧ���̿��ܵĿ��Ʋ���������ɢ���ơ���ѧ��Ӧ���ơ�����ɢ���ƻ����ǻ�Ͽ��ơ���ѧ��Ӧ�ɹ�������������У���Ӧ��Ͳ���֮�������ԵĽ��棬���ŷ�Ӧ�Ľ��У�������������ӣ���δ��Ӧ�ķ�Ӧ���������С����ˣ��������������Һ���෴Ӧ�������Ϊ��1) �������ҺĤ��ɢ��������(����ɢ)��2) ������ɸ�������ɢ����Ӧ��(����ɢ)��3) ������ڷ�Ӧ���Ͻ�������ѧ��Ӧ(���滯ѧ��Ӧ)��4) ��Ӧ��Ŀ�������ɢ�����ı��棻5) �����Բ��ᆳҺĤ����ɢ����Һ�С�
�����������Һ-���෴Ӧ�������������������еģ��ܵķ�Ӧ�ٶ�ȡ���ڿ��Ʋ��衣
�����Ʋ���Ϊ����ɢʱ����Ӧ����ѧ����ʽ(��Ӧ������ʱ��Ĺ�ϵʽ)Ϊ
Xb=K1t (1)
�����Ʋ���Ϊ���滯ѧ��Ӧʱ����Ӧ����ѧ����ʽΪ
1-(1-Xb)1/3=K2t (2)
�����Ʋ���Ϊ����ɢʱ����Ӧ����ѧ����ʽΪ
1-3(1-Xb)2/3+2(1-Xb)=K3t (3)
����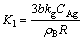 ��
�� ��
�� ��XbΪ�����з�����Ӧ�������������tΪ��Ӧʱ�䣻��Ϊ�����к������Ħ���ܶȣ�KgΪ����ϵ����KsΪ��һ�ױ��淴Ӧ���ʳ�����CAgΪҺĤ���������Ũ�ȣ�RΪ�������뾶��DΪ��ɢϵ����bΪ��Ӧ������
��XbΪ�����з�����Ӧ�������������tΪ��Ӧʱ�䣻��Ϊ�����к������Ħ���ܶȣ�KgΪ����ϵ����KsΪ��һ�ױ��淴Ӧ���ʳ�����CAgΪҺĤ���������Ũ�ȣ�RΪ�������뾶��DΪ��ɢϵ����bΪ��Ӧ������
Ϊ��ȷ���������������Ӧ����ѧ���̼�����Ʋ��裬ʵ���зֱ���������������������Ӧ�¶ȡ�����������Һ�̱ȡ���������������ΪӰ�����ӶԸ������������Һ���෴Ӧ����ѧ���̽��з�����
2 ʵ��
ʵ��ѡ�ù���ij�������ṩ�ĸ���ʯ�ͽ���Ϊԭ�ϣ�����Ҫ�ɷ����1��ʾ��ʵ����ʹ�õ���Ҫ������HDS3000��ȫ�Զ��������Լ���ո�����ȡ�
��1 ʵ���ø���ʯ�ͽ�����Ҫ�ɷ�(��������)
Table 1 Components of high-sulfur petroleum coke %

ʵ�����ȶ�ԭ�ϸ�����������ĥ��������150 ��m���£�Ȼ��ֱ���þ�̬���Ͷ�̬������̬���ǽ�װ�и��ۺ�Һ��������Ĺ�Һ���������ˮԡ���о�ֹ���Ȳ�����һ��ʱ�䣻��̬���ǽ�װ�и��ۺ�Һ��������Ĺ�Һ���������ˮԡ���м��ȱ��£������Ͻ����Һ����
3 ���������
3.1 ����Ը��������ʵ�Ӱ��
����ǰ�ڵ��Ż�����ʵ�������̶��������������Ϊ60%����Һ��Ϊ30 mL/g����Ӧ�¶�Ϊ60 �棬�ֱ���ö�̬�;�̬�ķ�ʽ��������ʵ�顣2�ַ�ʽ�·�Ӧʱ���������ʵĹ�ϵ��ͼ1��ʾ����ͼ1���Կ��������þ�̬��(�����跴Ӧ��ϵ)������Ȼ�������淴Ӧʱ����ӳ�������ߣ����ǣ���ߵķ��Ⱥ�С����Ӧʱ���6 h�ӳ���24 h�������ʴ�46%ֻ���ӵ���53%�������ö�̬��(���ٽ��跴Ӧ��ϵ)ʱ����Ӧ6 h�������ʾߴ�58%������Ӧʱ���ӳ���12 hʱ�������ʸߴ�72%������������ԭ���Ǹ�����������Ӵ��ᷢ��Һ�̷�Ӧ�����������������ʵ����ɡ�����Ӧ��ϵ���ھ�ֹ״̬ʱ�����ŷ�Ӧʱ����ӳ����������ݻ��Զ��ų�������һ�������ݻ�����ڸ��������棬��ֹ���������һ��������ڲ���϶����ɢ���������ø��ٻ�е����ʱ����Ӧ���������ݻ�Ѹ��ת�ƣ��Ӷ�Ϊ������������������ɢ�����ṩ�˷��㡣�ɴ˿����ƶϣ��ھ�̬�����£�ʪ��ѧ��������̵����ʿ��Ʋ���Ϊ����ɢ���ƣ��ڶ�̬�����£��ù��̵����ʿ��Ʋ��費��������ɢ���ƣ���Ӧ���ǻ�ѧ��Ӧ���ƻ�������ɢ���ơ�

ͼ1 ��Ӧʱ������������ʵĹ�ϵ
Fig. 1 Desulfurization rate of high-sulfur petroleum coke at different reaction time
3.2 ��̬������ʪ��ѧ������Ӧ����ѧ����
Ϊ��ȷ����̬�����¸���ʪ��ѧ������Ӧ�����ʿ��Ʋ��裬�ֱ������������������Һ�̱ȡ����������Լ���Ӧ�¶�ΪӰ�����ӷ�����������Ӧ����ѧ���̡��ڴ�״̬������Ӧ���ܻ�ѧ��Ӧ���ƻ�����ɢ���ƣ����ݻ�ѧ��Ӧ���ƺ�����ɢ���Ƶķ�Ӧ������ʱ��Ĺ�ϵʽ(2)��(3)���ֱ�����1-(1-Xb)1/3��1-3(1-Xb)2/3+2(1-Xb)��ʱ��t��ͼ��������������ϡ�ͼ2~9��ʾ�ֱ�Ϊ�����Ũ�ȡ�Һ�̱ȡ����������Լ���Ӧ�¶��뷴Ӧʱ��Ĺ�ϵ����ѧ��Ӧ���ƺ�����ɢ���ƵĶ���ѧ��ϵ���ͼ��
����ͼ2��ͼ9��֪���ڶ�̬�����£����ò�ͬ���������������Һ�̱ȡ����������Լ���Ӧ�¶�ʱ������Ӧ�����뷴Ӧʱ�䣬���ն���ѧ����ʽ(2)��(3)�������ݴ�������Ϻ���뷴Ӧʱ������õ����Թ�ϵ���ɴ˿�����Ϊ���ڶ�̬�����£�ʪ��ѧ������Ӧ�д��ڻ�ѧ��Ӧ���ƻ�����ɢ���ơ�

ͼ2 �����Ũ���뷴Ӧʱ�䰴��ѧ��Ӧ���Ƶ����ͼ
Fig. 2 Curves of 1-(1-Xb)1/3 versus t at different concentrations

ͼ3 �����Ũ���뷴Ӧʱ�䰴����ɢ���Ƶ����ͼ
Fig. 3 Curves of 1-3(1-Xb)2/3+2(1-X) versus t at different concentrations

ͼ4 Һ�̱��뷴Ӧʱ�䰴��ѧ��Ӧ���Ƶ����ͼ
Fig. 4 Curves of 1-(1-X)1/3 versus t at different liquid-solid rates

ͼ5 Һ�̱��뷴Ӧʱ�䰴����ɢ���Ƶ����ͼ
Fig. 5 Curve of 1-3(1-X)2/3+1(1-X) versus t at different liquid-solid rates

ͼ6 ���������뷴Ӧʱ�䰴��ѧ��Ӧ���Ƶ����ͼ
Fig. 6 Curve of 1-(1-X)1/3 versus t at different granularities
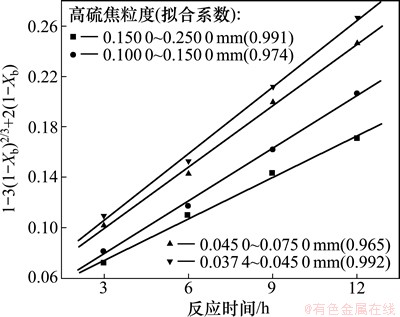
ͼ7 ���������뷴Ӧʱ�䰴����ɢ���Ƶ����ͼ
Fig. 7 Curve of 1-3(1-X)2/3+1(1-X) versus t at different granularities

ͼ8 ��Ӧ�¶��뷴Ӧʱ�䰴��ѧ��Ӧ���Ƶ����ͼ
Fig. 8 Curve of 1-(1-X)1/3 versus t at different temperatures
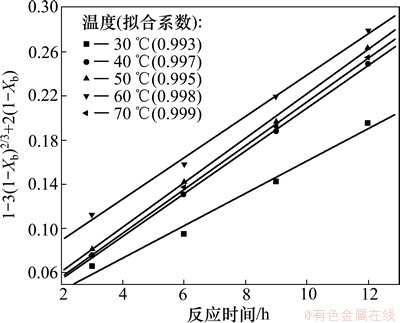
ͼ9 ��Ӧ�¶��뷴Ӧʱ�䰴����ɢ���Ƶ����ͼ
Fig. 9 Curve of 1-3(1-X)2/3+1(1-X) versus t at different temperatures
�����ڶ�̬�����µ�ʪ��ѧ������Ӧ���ջ�ѧ��Ӧ����������ɢ���ƶ���ѧ���̼������ʱ�����ֳ����õ����Թ�ϵ�����������һ�¶�������k��Ϊ��������kֻΪ�¶ȵĺ���������ͼ9�����ݣ�����lnk��1/T��ͼ���õ�����Arrhenius��ʽ������ͼ(ͼ10)����ͼ10�����ݣ�����Arrhenius��ʽ��������ۻ��Ea=2.62 kJ/mol�����ڱ��ۻ��Ea��С(Ea��13.00 kJ/mol)���ڶ�̬�����£�ʪ��ѧ���ѳ�ʯ�ͽ�����ķ�Ӧ������ɢ���ơ�

ͼ10 ln K-103K/T�Ĺ�ϵͼ
Fig. 10 Curve of ln K versus 103K/T
4 ����
1) ����ʪ��ѧ������ʱ�����������������Ϊ60%����Һ��Ϊ30 mL/g����Ӧ�¶�Ϊ60 �棬��Ӧʱ��Ϊ12 h�Լ�ʯ�ͽ�����Ϊ106 ��mʱ��ʯ�ͽ��Ķ�̬��������߿ɴ�72%������ͬ������ʱ���£���̬�����µ������ʱȾ�̬������Ҫ��20%���ϣ���ˣ����ٽ��跴Ӧ��ϵ�����ڸ�������Ŀ����ѳ���
2) �ھ�̬���������£�����������̵����ʿ��Ʋ���Ϊ����ɢ���ƣ���̬���������£�����Arrhenius��ʽ����ó�ʪ��ѧ������Ӧ�ı��ۻ��Ea=2.62 kJ/mol(��13.00 kJ/mol)������������̵����ʿ��Ʋ���Ϊ����ɢ���ơ�
�ο����ף�
[1] Edwards L C, Neyrey K J, Lossius L P. A review of coke and anode desulfurization[J]. Light Metals, 2007: 895-900.
[2] Salvador S, Commandre J M, Stanmore B R. Reaction rates for the oxidation of highly sulphurised petroleum cokes: The influence of thermogravimetric conditions and some coke properties[J]. Fuel, 2003, 82: 715-720.
[3] Vogt F, Tonti R, Hunt M, et al. A preview of anode coke quality in 2007[J]. Light Metals, 2004: 489-493.
[4] CHEN Xiping. The influence of petroleum coke��s calcining process on its desulfurizing[C]//2nd International Carbon Conference in China. Kunming, 2006: 46-49.
[5] Shlewit H, Alibrahim M. Extraction of sulfur and vanadium from petroleum coke by means of salt-roasting treatment[J]. Fuel, 2006, 85: 878-880.
[6] ������, κ��ΰ, ������, ��. ʯ�ͽ������»���Ԥ��������Σ��������[J]. ̿�ؼ���, 2010, 29(1): 52-55.
JI Yanxin, WEI Xinwei, LI Xianlei, et al. Damage of the declining quality of petroleum coke to pre-baked anode and its control[J]. Carbon Techniques, 2010, 29(1): 52-55.
[7] Tran K N, Berkovich A J, Tomsett A, et al. Influence of sulfur and metal microconsitituents on the reactivity of carbon anodes[J]. Energy & Fuels, 2009, 23: 1909-1924.
[8] Al-Haj Ibrahim H, Monla Ali M. The effect of increased residence time on the thermal desulfurization of Syrian petroleum coke[J]. Periodica Polytechnica Chemical Engineering, 2004, 48: 53-62.
[9] Adams A, Cahill R, Belizile Y, et al. Minimizing impact of low sulfur coke on anode quality[J]. Light Metals, 2009: 957-962.
[10] �Ա�, ��Ӣ��, ����ΰ, ��. ʯ�ͽ��������о���չ[J]. ̿�ؼ���, 2011, 30(2): 30-32.
ZHAO Bin, LUO Yingtao, SU Ziwei, et al. Development on the petroleum coke desulfurization[J]. Carbon Technioques, 2011, 30(2): 30-32.
[11] Al-Haj-Ibrahim H, Morsi B. Desulfurization of petroleum coke: A review[J]. Ind Eng Chem Res, 1992, 31(1): 1835-1840.
[12] GUO Zhancheng, FU Zhinxin, WANG Shenxiang. Sulfur distribution in coke and sulfur removal during pyrolysis[J]. Fuel Processing Technology, 2007, 88(10): 935-941.
[13] Syunyaev Z I, Gimaev R N, Abyzgildin Y M, et al. Reactions of organosulfur compounds in petroleum coke[J]. Khim Seraorg Soedin, Soderzh Neftyakh Nefteprod, 1968, 8: 381-386.
[14] Lossius L P, Neyrey K J, Edwards L C. Coke and anode desulfurization studies[J]. Light Metals, 2008: 881-886.
[15] Paul C A, Herrington L E, P E. Desulfurization of petroleum coke beyond 1 600 ��[J]. Light Metals, 2001: 597-601.
[16] Radenovic A. Sulphur separation by heat treatment of petroleum coke[J]. NAFTA, 2009, 60(3): 171-175.
[17] Shlewit H, Alibrahim M. Extraction of sulfur and vanadium from petroleum coke by means of salt-roasting treatment[J]. Fuel, 2006, 85: 878-880.
[18] Ф��, ��˼ε, ������, ��. ��ѧ�������ѳ�ʯ�ͽ��е���[J]. ��������, 2010, 30(3): 199-202.
XIAO Jin, YANG Siwei, LAI Yanqing, et al. Removal of sulfur from petroleum coke by chemical oxidation process[J]. Environmental Protection of Chemical Industry, 2010, 30(3): 199-202.
[19] Ф��, ����, �δ�, ��. ����ʯ�ͽ������Ƚ�[J].���ϴ�ѧѧ��(��Ȼ��ѧ��), 2013, 44(3): 880-884.
XIAO Jin, WU Qian, LAI Yanqing, et al. Comparison of removal of sulfur from high-sulfur petroleum coke[J]. Journal of Central South University (Science and Technology), 2010, 30(3): 199-202.
[20] Al-Haj Ibrahim H, Monla Ali M. Thermal desulphurization of syrian petroleum coke[J]. Journal of King Sand University, Sciences, 2005(17): 199-212.
[21] Aly I M H, Magdy Y H, Barakat N A M. Desulfurization of egyptian petroleum coke[J]. Developments in Chemical Engineering and Mineral Processing, 2003, 11: 395-406.
[22] Hay S J, Metson J B, Margaret M. Hyland. Sulfur speciation in aluminum smelting anodes[J]. Industrial & Engineering Chemistry Research, 2004, 43: 1690-1700.
[23] ����. ұ��ԭ��[M]. ����: ��ѧ������, 2005: 291-304.
LI Honggui. Metallurgy[M]. Beijing: Science Press, 2005: 291-304.
(�༭ ���˱�)
�ո����ڣ�2013-12-30�������ڣ�2014-04-16
������Ŀ(Foundation item)��������Ȼ��ѧ����������Ŀ(51374253)(Project (51374253) supported by the National Natural Science Foundation of China)
ͨ�����ߣ�������(1983-)���У����������ˣ���ʿ�о�����������ɫұ������ǽ��������о����绰��0731-88876454��E-mail:dengsongyun1@163.com