DOI: 10.11817/j.ysxb.1004.0609.2020-39349
废铅酸蓄电池铅膏碳酸盐转化工艺及其反应动力学
刘文科1,秦庆伟1,李登奇1,高运明1,刘 昱1,陈精智2
(1. 武汉科技大学 钢铁冶金及资源利用教育部重点实验室,武汉 430081;
2. 湖北金洋冶金股份有限公司,谷城 441705)
摘 要:碳酸盐转化工艺作为湿法回收废铅膏的关键步骤具有重要的研究意义。在对废铅膏组分分析的基础上,采用碳酸盐转化方法对比探讨同一条件下不同转化剂的脱硫效果,对转化产物进行XRD表征;同时探讨了(NH4)2CO3脱硫过程的动力学机理。结果表明:转化脱硫率从大到小依次为Na2CO3、(NH4)2CO3、NH4HCO3,以(NH4)2CO3和NH4HCO3作为脱硫剂,PbSO4转化生成PbCO3;而采用Na2CO3转化脱硫时,产物中存在NaPb2(CO3)2OH杂质物相。以(NH4)2CO3作为脱硫剂的最佳工艺条件是(NH4)2CO3浓度0.50 mol/L,反应温度50 ℃,反应时间60 min,搅拌速度500 r/min,液固比5:1,在此最佳工艺条件下脱硫率可达95.66%。PbSO4在(NH4)2CO3溶液中的转化服从缩核模型,过程反应速率受扩散控制,计算出表观活化能为16.471 kJ/mol,并最终建立了该脱硫过程的动力学方程式。
关键词:铅膏;碳酸盐转化;脱硫率;反应动力学
文章编号:1004-0609(2020)-08-1934-08 中图分类号:TF812 文献标志码:A
现代废铅蓄电池的破碎、分选过程是将铅分成金属、氧化物和硫酸盐等部分,将有机物分成壳体和隔板部分[1-2]。有机物中的聚丙烯可以回收利用,而含铅废料大部分是采用火法冶炼的方式处理[3]。由于火法处理会造成大量铅烟气和二氧化硫的排放,不但降低铅的直收率,还增加了后续收尘工序的处理难度,造成布袋粘结、设备腐蚀、环境污染等诸多问题[3-5]。因此,湿法回收路线成为研究的重点,而碳酸盐转化工艺作为湿法再生技术的首要步骤,具有重要研究意义以及对后续铅的回收具有重要影响。
对于湿法回收废铅膏的研究,主要集中在直接采用氯盐体系、柠檬酸盐、乙酸浸出等[6-9]方面。SHU等[10]采用NaCl-HNO3混合溶液作为浸出剂,首先将铅膏中的铅转化为[PbCl4]2-,然后加入草酸钠和分散剂聚乙二醇将其转化为PbC2O4,分步去除铅膏中的Fe和Si杂质元素,最终焙烧得到超细氧化铅粉。GOLPAYEGANI等[11]采用NaCl-FeCl3体系作为浸出剂,分别从热力学和动力学方面系统研究了熔炉铅渣的浸出机理和主要影响条件,通过基于中心复合设计(CCD)模型的响应面方法学(RSM)详细探讨了各参数对浸出率的影响,获得了最佳工艺条件。此外,SONMEZ等[12-13]采用柠檬酸和柠檬酸钠作为浸出液制取柠檬酸铅,进而焙烧分解生成氧化铅产品,此工艺虽然消除了火法熔炼的高污染和电解提铅高能耗等问题,但柠檬酸价格昂贵,投资成本较高,产业化困难。近年来,针对铅化合物的碳酸盐转化研究,国内外也有研究,CHEN等[14]采用NH4HCO3作为脱氯剂,系统研究了PbCl2转化为PbCO3的动力学机理,得到以下结论:PbCl2与NH4HCO3之间的化学转化遵循缩核模型,反应初始pH值和NH4HCO3溶液浓度对脱氯率影响明显,且反应初始pH值对转化产物的物相影响非常显著,这对采用碳酸盐探讨铅膏转化机理的研究思路给了不少启发。
目前,铅膏碳酸盐湿法转化工艺得到了国内外学者的广泛关注[15-17],舒月红等[18]和丁希楼等[19]分别采用Na2CO3、NH4HCO3、(NH4)2CO3等碳酸盐作为脱硫剂对铅膏进行脱硫处理,获得了良好的浸出效果。但针对分析脱硫剂影响产物的物相组成和探讨脱硫过程反应动力学的报道较少,因为脱硫产物的物相会影响后续的铅回收工艺,且探明动力学控制步骤对浸出过程的参数控制具有良好的指导作用。为此,本工作以废铅膏为研究对象,对比分析了不同脱硫剂对铅膏脱硫效率及产物的物相组成影响,进一步优化了脱硫工艺并详细探讨了碳酸铵转化脱硫过程的动力学机理,以期对冶金领域废铅蓄电池回收工艺具有一定的指导意义。
1 实验
1.1 实验原料
原料制备:本实验所用铅膏来自湖北金洋股份有限公司,将废铅膏研成粉末状后,用蒸馏水反复水洗去除其中所含硫酸等残留物,之后将铅膏放入干燥箱内在120 ℃下干燥处理;干燥后的铅膏经手工研钵研细,再放置在ZKF040真空干燥箱干燥12 h,备用。采用Mastersizer2000型粒度分析仪进行粒度分析,结果如图1所示,可以看出粒径在15 μm以下的占大多数,因此,用筛子淘洗过筛后,用于后续动力学实验测试。通过化学分析的方法测定其各组分含量见表1,并对其进行XRD和扫描电镜分析,结果如图2和图3所示。
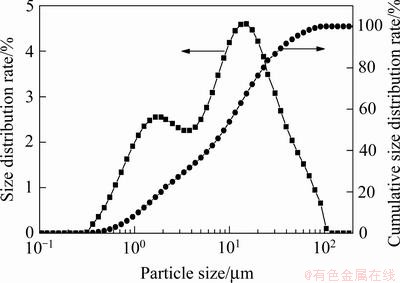
图1 铅膏粒径分布率
Fig. 1 Size distribution rate of lead paste
表1 废铅膏化学成分
Table 1 Chemical composition of waste lead paste (mass fraction, %)
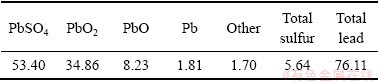

图2 原始铅膏的XRD谱
Fig. 2 XRD pattern of original lead paste
结合表1和图2可以看出,废铅膏主要含有PbSO4、PbO2、PbO和少量的单质铅,其中PbSO4占大部分,因此转化脱硫是回收废铅膏的必要步骤。图3所示为原始铅膏的SEM像。由图3可以看出,原始铅膏颗粒大小分布不均匀,呈条形状或方形。

图3 原始铅膏的SEM像
Fig. 3 SEM image of original lead paste
1.2 实验方法
首先在烧杯中配置一定浓度的脱硫转化液,将烧杯置于DF -101S集热式恒温加热磁力搅拌器中,调至已设定的转速和温度,当温度到达设定值后,加入已称量好的铅膏开始计时,反应结束后,固液分离,滤液经蒸发、结晶后可作为副产品回收,对滤渣检测分析。固体产物经100 ℃真空干燥12 h,利用X射线衍射仪(Germany Bruker-AXS D8 Advance)对其物相组成进行分析,探讨不同条件下PbSO4的物相转化规律,同时多次取样测定产物中平均S含量,通过计算脱硫率(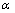 )来表征脱硫转化反应进行的程度,铅膏脱硫计算公式如下:
)来表征脱硫转化反应进行的程度,铅膏脱硫计算公式如下:
 (1)
(1)
式中:m1为脱硫前铅膏的质量,g;w1为脱硫前铅膏中硫酸铅的质量分数,%;m2为脱硫后铅膏的质量,g;w2为脱硫后铅膏中硫酸铅的质量分数,%。
2 结果与讨论
2.1 铅膏脱硫
2.1.1 转化剂种类的影响
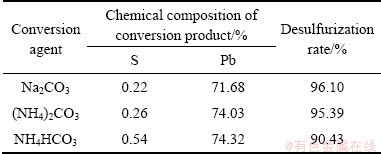
通过前期实验研究[20],分别采用碳酸钠、碳酸铵、碳酸氢铵作为脱硫剂对铅膏转化脱硫,选择反应初始条件:铅膏10 g,转化剂浓度0.50 mol/L,温度50 ℃,反应时间70 min,液固比5:1,搅拌速度500 r/min。考察了不同转化剂对铅膏脱硫规律的影响,分析结果见表2。由表2可知,在相同反应条件下,不同转化剂脱硫效果由大到小为Na2CO3、(NH4)2CO3和NH4HCO3,碳酸钠和碳酸铵的脱硫率分别为96.10%和95.39%,其中脱硫产物中S含量分别为0.22%和0.26%,均低于0.5%,符合工业生产指标,而碳酸氢铵的脱硫率较低,只有90.43%,且产物中S含量为0.54%,工业生产不达标。
表2 不同转化剂脱硫产物分析结果
Table 2 Chemical composition of desulfurized products by different conversion agents
为进一步研究不同脱硫剂对产物的物相组成影响,对各转化产物进行XRD表征,其结果如图4所示。由图4可以看出,采用不同转化剂,脱硫产物的衍射峰主要由PbCO3和PbO2组成,没有了PbSO4的衍射峰,这表明3种转化剂都具有良好的脱硫效果。当以碳酸铵、碳酸氢铵作为转化剂时,脱硫产物的物相主要由PbCO3和PbO2组成,而采用碳酸钠进行脱硫时,由于转化液浓度较高,导致初始pH值过高,转化生成的PbCO3再与Na2CO3结合生成NaPb2(CO3)2OH杂质物相,这种物相的生成不仅增加了转化剂的耗 费,而且给后续加工和副产品的回收利用造成困难[21-22]。不同转化剂脱硫的化学反应式如下:
PbSO4+Na2CO3→PbCO3+Na2SO4 (2)
PbSO4+(NH4)2CO3→PbCO3+(NH4)2SO4 (3)
PbSO4+2NH4HCO3→PbCO3+(NH4)2SO4+CO2↑+H2O (4)
3PbSO4+4Na2CO3+2H2O→Pb3(CO3)2(OH)2+3Na2SO4+2NaHCO3 (5)
2Pb(CO3)2(OH)2+2Na2CO3→3NaPb2(CO3)2OH+NaOH (6)
PbSO4+2NaHCO3→PbCO3+Na2SO4+CO2↑+H2O (7)
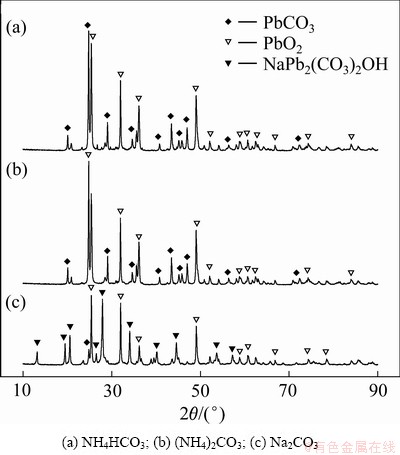
图4 不同转化剂脱硫产物的XRD谱
Fig. 4 XRD patterns of desulfurized products with different conversion agents
为了避免脱硫产物中NaPb2(CO3)2OH的生成,控制合理的转化剂浓度和调节溶液pH值是一种可行的方法。ZHU等[23]常温下向脱硫后膏糊矿浆中通入CO2调节反应pH值,在反应进行30 min后,固液分离,将滤渣烘干后测量S含量并进行物相分析,发现脱硫效果良好且消除了杂质物相NaPb2(CO3)2OH。但此方法操作复杂、可控性低,因此,本实验采用复合脱硫剂,通过调节Na2CO3、NaHCO3的添加比例来控制溶液初始pH值为9.5,既保证了较高的脱硫率,又避免了NaPb2(CO3)2OH副产物的生成,产物的物相只包含PbCO3和PbO2,对产物进行XRD分析,其结果如图5所示。
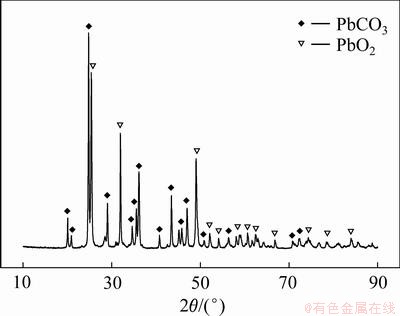
图5 复合脱硫产物的XRD谱
Fig. 5 XRD pattern of complex desulfurization product
综上所述可知,在工艺条件相同时,碳酸钠和碳酸铵脱硫效果比碳酸氢铵更好,但碳酸钠脱硫产物中含有杂质物相,且处理工序繁琐,因此,后续实验中,以碳酸铵作为最佳转化脱硫剂进行详细的条件实验探究。
2.1.2 (NH4)2CO3浓度的影响
反应初始条件:铅膏10 g,反应温度50 ℃,搅拌速度500 r/min,液固比5:1,随着反应时间增加,考察了不同(NH4)2CO3浓度对铅膏脱硫效果的影响,结果如图6所示。由图6可以看出,反应时间小于30 min时,各反应浓度下反应速度都很快,之后脱硫反应放缓,在60 min内基本达到反应平衡。(NH4)2CO3浓度从0.36 mol/L增加到0.54 mol/L时,脱硫率明显增加,当(NH4)2CO3浓度为0.36 mol/L时,在80 min内脱硫率只有70.41 %,而当(NH4)2CO3浓度为0.50 mol/L时,在40 min内脱硫率就达到96.42%,表明随着(NH4)2CO3浓度的增加,转化反应耗时减少且脱硫率增加。这是因为增加转化液浓度,使得转化液与铅膏接触几率增加,脱硫速度加快,脱硫更完全。因此,综合考虑原料成本及脱硫率等问题,选择0.50 mol/L (即(NH4)2CO3:PbSO4摩尔比为1.4:1)作为最佳浓度。
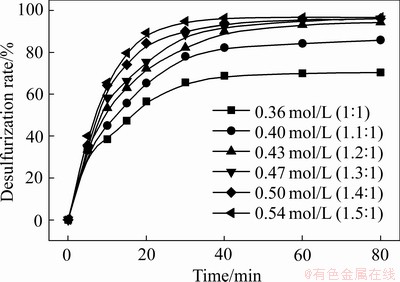
图6 (NH4)2CO3浓度对脱硫率的影响
Fig. 6 Effect of (NH4)2CO3 concentration on desulfurization rate
2.1.3 温度的影响
反应初始条件:铅膏10 g,(NH4)2CO3浓度为0.50 mol/L、液固比5:1、搅拌速度500 r/min,随着反应时间增加,考察了不同反应温度对铅膏脱硫效果的影响,其结果如图7所示。由图7可以看出,反应30 min内,各反应温度下脱硫率有明显的增加,在60 min内达到平衡。当反应温度为30 ℃时,在80 min内脱硫率达到92.04%,而当温度为70 ℃时,在40 min内脱硫率就达到92.45%,再随着反应时间的增加,脱硫率有下降的趋势,这是因为温度过高导致少量碳酸铵分解,致使脱硫率下降。可以看出,当温度为50 ℃时,在60 min内脱硫率可达95.66%,脱硫率高且时间消耗短,因此考虑到脱硫率和原料利用率等问题,选择最佳温度为50 ℃。
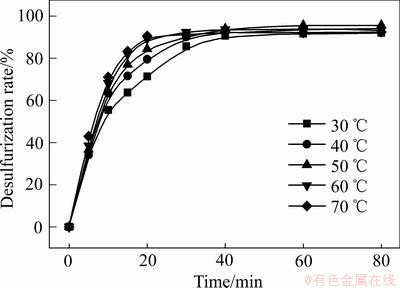
图7 温度对脱硫率的影响
Fig. 7 Effect of temperature on desulfurization rate
2.1.4 搅拌速度的影响
反应初始条件:铅膏10 g,(NH4)2CO3浓度为0.50 mol/L、液固比5:1、反应温度50 ℃,随着反应时间延长,考察了不同搅拌速度对铅膏脱硫效果的影响,结果如图8所示。由图8可以看出,随着搅拌速度从200 r/min加快到500 r/min,铅膏脱硫率有明显的升高,但当搅拌速度高于500 r/min后,再加快搅拌速度,对铅膏脱硫率的影响不明显。这是因为加快搅拌速度使得反应物充分接触,同时促进反应物向脱硫转化液中扩散,进而在一定程度上增加铅膏脱硫率。因此,综合考虑经济成本和设备处理能力,选择500 r/min作为最佳搅拌速度。
2.2 转化脱硫过程动力学分析
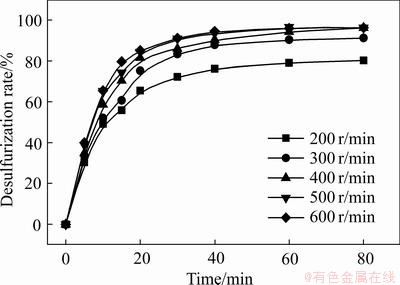
图8 搅拌速度对脱硫率的影响
Fig. 8 Effect of stirring speed on desulfurization rate
PbSO4和(NH4)2CO3溶液反应的局部化学性质表明,转化速率可以用收缩核模型描述[22]。利用PbSO4与(NH4)2CO3溶液的化学反应,以及通过在粒子上形成不断增厚的产物层扩散来分析动力学过程,将转化数据拟合到速率控制方程上。经验方程如下:其中式(8)表示化学反应控制,式(9)表示扩散控制。
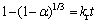 (8)
(8)
 (9)
(9)
式中: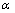 为脱硫率(%);t为反应时间(min);kr、kd为反应速率常数。
为脱硫率(%);t为反应时间(min);kr、kd为反应速率常数。
不同(NH4)2CO3浓度的两种速率控制方程数据拟合见表3。由表3可以看出,经过方程(9)拟合的数据相关系数更高,相关度可以达到98.18%。因此,可以推断出脱硫转化反应属于扩散控制过程,并通过速率常数kd作为考察反应速率的指标。
绘制不同(NH4)2CO3浓度、不同温度和不同搅拌速度随时间变化的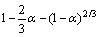 拟合图,结果如图9所示。由图9可以看出,不同(NH4)2CO3浓度、反应温度和搅拌速度的条件下,铅膏脱硫过程都比较符合扩散控制过程。
拟合图,结果如图9所示。由图9可以看出,不同(NH4)2CO3浓度、反应温度和搅拌速度的条件下,铅膏脱硫过程都比较符合扩散控制过程。
表3 不同(NH4)2CO3浓度的两种速率控制类型数据拟合
Table 3 Data fitting of two rate control types for different (NH4)2CO3 concentrations
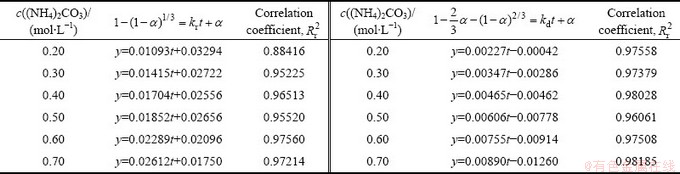
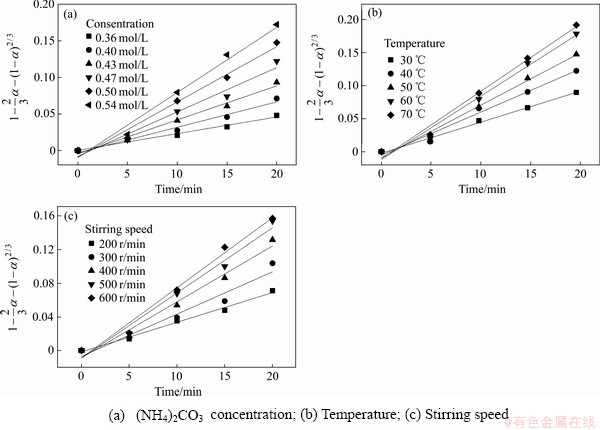
图9 不同(NH4)2CO3浓度、温度和搅拌速度下随时间变化的 关系
关系
Fig.9 Plots of t versus  at different operation parameters
at different operation parameters
为了定量地确定(NH4)2CO3浓度、反应温度和搅拌速度对反应动力学的影响,建立如下脱硫动力学半经验模型:
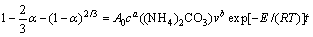 (10)
(10)
式中:A0为频率因子;a、b为常数。
由图9(a)得到不同(NH4)2CO3浓度转化的反应 速率常数,绘制如图10所示的函数关系图, 是不同碳酸铵浓度对应直线的斜率,计算得到a=3.38,同理得到b=0.809。可以看出,随着(NH4)2CO3浓度从0.36 mol/L增加到0.54 mol/L,脱硫速率也平稳有序的增加。不同浓度下的反应关系式如下:
是不同碳酸铵浓度对应直线的斜率,计算得到a=3.38,同理得到b=0.809。可以看出,随着(NH4)2CO3浓度从0.36 mol/L增加到0.54 mol/L,脱硫速率也平稳有序的增加。不同浓度下的反应关系式如下:
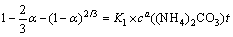 (11)
(11)
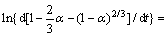
 (12)
(12)
式中:K1为反应速率常数; 为(NH4)2CO3浓度。
为(NH4)2CO3浓度。
通过图9(b)中不同温度下的的反应速率常数得到如图11所示的Arrhenius图。计算出活化能为16.471 kJ/mol,这进一步证实了碳酸铵转化脱硫过程是由扩散控制的,对废铅膏脱硫回收工艺有一定的理论指导价值。反应关系式如下:
 (13)
(13)
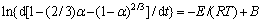 (14)
(14)
式中:E为表观活化能(kJ/mol);R为摩尔气体常数(J/(mol×K);T为温度(K);B为常数。
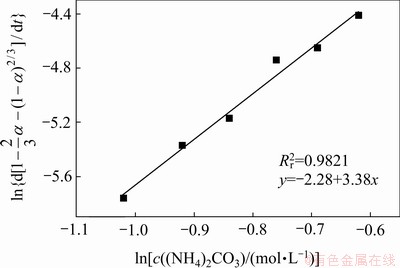
图10 (NH4)2CO3浓度对PbSO4转化率的影响
Fig. 10 Plot of values of 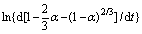 versus different (NH4)2CO3 concentration
versus different (NH4)2CO3 concentration

图11 不同温度下PbSO4转化的Arrhenius图
Fig. 11 Arrhenius plot for conversion of PbSO4 at different temperatures
综上所述,将a、b、E代入式(10),同时结合最佳脱硫条件,计算得出A0=0.2286 s-1,得到脱硫反应的动力学方程为

 (15)
(15)
3 结论
1) 通过实验研究,在同一工艺条件下对比不同转化剂的脱硫效果,转化脱硫率从大到小依次为Na2CO3、(NH4)2CO3、NH4HCO3,以(NH4)2CO3作为脱硫剂的最佳工艺条件:(NH4)2CO3浓度0.50 mol/L,反应温度50 ℃,液固比5:1,搅拌速度500 r/min,反应时间60 min,在最佳工艺条件下脱硫率可达95.66%。
2) 通过对不同脱硫剂的转化产物的物相分析,发现以(NH4)2CO3 和NH4HCO3作为脱硫剂时PbSO4能转化为纯度较高的PbCO3,而Na2CO3的脱硫产物中有NaPb2(CO3)2OH物相生成,得出pH值过高是形成此物相的原因,采用Na2CO3和NaHCO3作为复合脱硫剂,通过配比二者的用量来调节溶液pH值为9.5,可以避免了杂质物相的生成。
3) 通过对(NH4)2CO3脱硫过程的动力学分析,得出实验数据与扩散控制速率方程相关性更好,表明PbSO4在(NH4)2CO3溶液中的转化过程符合固膜扩散控制的缩核模型,得到动力学方程为 0.2286c3.38v0.809exp{-16470.53/(RT)}t。
0.2286c3.38v0.809exp{-16470.53/(RT)}t。
REFERENCES
[1] 李卫锋, 蒋丽华, 湛 菁, 张传福. 废铅酸蓄电池铅再生技术现状及进展[J]. 中国有色冶金, 2011, 40(6): 53-56.
LI Wei-feng, JIANG Li-hua, ZHAN Jing, ZHANG Chuan-fu. Status and progress of lead recycling technology of waste lead-acid battery[J]. China Nonferrous Metallurgy, 2011, 40(6): 53-56.
[2] CHANG Yu, MAO Xian-xian, ZHAO Yan-fang, FENG Shao-li, CHEN Hong-yu, FINLOW D. Lead-acid battery use in the development of renewable energy systems in China[J]. Journal of Power Sources, 2009, 191(1): 176-183.
[3] SUN Zhi, CAO Hong-bin, ZHANG Xi-hua, LIN Xiao, ZHENG Wen-wen, CAO Guo-qing, SUN Yong, ZHANG Yi. Spent lead-acid battery recycling in China―A review and sustainable analyses on mass flow of lead[J]. Waste Management, 2017, 64: 190-201.
[4] ZHANG Wei, YANG Jia-kuan, WU Xu, HU Yu-chen, YU Wen-hao, WANG Jun-xiong, DONG Jin-xin, LI Ming-yang, LIANG Sha, HU Jing-ping, KUMAR R V. A critical review on secondary lead recycling technology and its prospect[J]. Renewable and Sustainable Energy Reviews, 2016, 61: 108-122.
[5] TIAN Xi, WU Yu-feng, HOU Ping, LIANG Sai, QU Shen, XU Ming, ZUO Tie-yong. Environmental impact and economic assessment of secondary lead production: Comparison of main spent lead-acid battery recycling processes in China[J]. Journal of Cleaner Production, 2017, 144: 142-148.
[6] 齐美富, 郑园芳, 桂双林. 废铅酸蓄电池中铅膏氯盐体系浸取铅的动力学研究[J]. 矿冶工程, 2010, 30(6): 61-64.
QI Mei-fu, ZHENG Yuan-fang, GUI Shuang-lin. Kinetic study on leaching lead from waste lead-acid batteries for lead plaster chloride system[J]. Mining and Metallurgical Engineering, 2010, 30(6): 61-64.
[7] ZHANG Rong-liang, ZHANG Xiao-fei, TANG Shu-zhen, HUANG Ai-dong. Ultrasound-assisted HCl-NaCl leaching of lead-rich and antimony-rich oxidizing slag[J]. Ultrasonics Sonochemistry, 2015, 27: 187-191.
[8] KIM E, HORCKMANS L, SPOOREN J, BROOS K, VRANCKEN K C, QUAGHEBEUR M. Recycling of a secondary lead smelting matte by selective citrate leaching of valuable metals and simultaneous recovery of hematite as a secondary resource[J]. Hydrometallurgy, 2017, 169: 290-296.
[9] VOLPE M, OLIVERI D, FERRARA G, SALVAGGIO M, PIAZZA S, ITALIANO S, SUNSERI C. Metallic lead recovery from lead-acid battery paste by urea acetate dissolution and cementation on iron[J]. Hydrometallurgy, 2009, 96(1): 123-131.
[10] SHU Yue-hong, MA Cheng, ZHU Long-guan, CHEN Hong-yu. Leaching of lead slag component by sodium chloride and diluted nitric acid and synthesis of ultrafine lead oxide powders[J]. Journal of Power Sources, 2015, 281: 219-226.
[11] GOLPAYEGANI M H, ABDOLLAHZADEH A A. Optimization of operating parameters and kinetics for chloride leaching of lead from melting furnace slag[J]. Transactions of Nonferrous Metals Society of China, 2017, 27(12): 2704-2714.
[12] SONMEZ M S, KUMAR R V. Leaching of waste battery paste components. Part 1: Lead citrate synthesis from PbO and PbO2[J]. Hydrometallurgy, 2009, 95(1/2): 53-60.
[13] SONMEZ M S, KUMAR R V. Leaching of waste battery paste components. Part 2: Leaching and desulphurization of PbSO4, by citric acid and sodium citrate solution[J]. Hydrometallurgy, 2009, 95(1): 82-86.
[14] CHEN Yong-ming, YE Long-gang, XUE Hao-tian, YANG Sheng-hai. Conversion of lead chloride into lead carbonate in ammonium bicarbonate solution[J]. Hydrometallurgy, 2017, 173: 43-49.
[15] LYAKOV N K, ATANASOVA D A, VASSILEV V S, HARALAMPIEW G A. Desulphurization of damped battery paste by sodium carbonate and sodium hydroxide[J]. Journal of Power Sources, 2007, 171(2): 960-965.
[16] ZHANG Jun-feng, YI Liang, YANG Liu-chun, HUANG Yan, ZHOU Wen-fang, BIAN Wen-jing. A new pre-desulphurization process of damped lead battery paste with sodium carbonate based on a “surface update” concept[J]. Hydrometallurgy, 2016, 160: 123-128.
[17] NING Peng, PAN Jun-qing, LI Xue, ZHOU Yue, CHEN Jian-feng, WANG Jie-xin. Accelerated desulphurization of waste lead battery paste in a high-gravity rotating packed bed[J]. Chemical Engineering & Processing Process Intensification, 2016, 104: 148-153.
[18] 舒月红, 马 成, 高 倩, 陈红雨. 碳酸盐对废铅酸蓄电池中铅膏脱硫转化的研究[J]. 蓄电池, 2014, (6): 248-252.
SHU Yue-hong, MA Cheng, GAO Qian, CHEN Hong-yu. Study on desulfurization process of lead paste of used lead-acid batteries with carbonate as desulfurizer[J]. Battery, 2014, (6): 248-252.
[19] 丁希楼, 谢 伟. 铅膏硫酸盐转化为碳酸盐的实验研究[J]. 安徽化工, 2011, 37(4): 41-46.
DING Xi-lou, XIE Wei. Experimental study on the conversion of lead paste sulphate into carbonate[J]. Anhui Chemical Industry, 2011, 37(4): 41-46.
[20] 刘文科, 秦庆伟, 李登奇, 高运明, 刘 昱, 陈精智, 李顺海. 用碳酸盐从废铅酸蓄电池铅膏中脱硫试验研究[J]. 湿法冶金, 2019, 38(1): 56-59.
LIU Wen-ke, QIN Qing-wei, LI Deng-qi, GAO Yun-ming, LIU Yu, CHEN Jing-zhi, LI Shun-hai. Desulfurization from lead paste of spent lead-acid battery using (NH4)2CO3 and NH4HCO3[J]. Hydrometallurgy of China, 2019, 38(1): 56-59.
[21] ARAI K, TOGURI J M. Leaching of lead sulphate in sodium carbonate solution[J]. Hydrometallurgy, 1984, 12(1): 49-59.
[22] GONG Y, DUTRIZAC J E, CHEN T T. The conversion of lead sulphate to lead carbonate in sodium carbonate media[J]. Hydrometallurgy, 1992, 28(3): 399-421.
[23] ZHU Xin-feng, LI Lei, SUN Xiao-juan, YANG Dan-ni, GAO Lin-xia, LIU Jian-wen, KUMAR R V, YANG Jia-kuan. Preparation of basic lead oxide from spent lead acid battery paste via chemical conversion[J]. Hydrometallurgy, 2012, 117: 24-31.
Carbonate transformation process and reaction kinetics of lead paste from spent lead-acid batteries
LIU Wen-ke1, QIN Qing-wei1, LI Deng-qi1, GAO Yun-ming1, LIU Yu1, CHEN Jing-zhi2
(1. Key Laboratory for Ferrous Metallurgy and Resources Utilization, Ministry of Education, Wuhan University of Science and Technology, Wuhan 430081, China;
2. Hubei Jinyang Metallurgical Incorporated Co., Ltd., Gucheng 441705, China)
Abstract: Carbonate conversion process has important research significance as the crucial step of recovering spent lead paste via hydrometallurgical methods. Based on the analysis of lead paste component from spent lead-acid batteries, the desulfurization efficiencies of different conversion agent in the same condition was determined as follow from high to low: Na2CO3, (NH4)2CO3, NH4HCO3. The transformation products were characterized by XRD. The kinetics mechanism of desulfurization process by (NH4)2CO3 was discussed. The results show that PbSO4 can be transformed into pure PbCO3 through (NH4)2CO3 and NH4HCO3. However, the transformation product desulfurized by Na2CO3 contains impurities phase NaPb2(CO3)2OH. The optimum processing conditions using (NH4)2CO3 as transforming agent are also detected and determined as follows: c((NH4)2CO3) of 0.5 mol/L, reaction temperature of 50 ℃, reaction time of 60 min, stirring speed of 500 r/min, L/S of 5:1, more than 95.66% of PbSO4 is transformed in this optimum condition. The apparent activation energy is calculated as 16.471 kJ/mol and the reaction obeyed shrinking-core model based on the diffusion controlled, as well as the general equation of kinetics of the desulfurization process is established.
Key words: lead paste; carbonate transformation; desulfurization rate; XRD characterization; reaction kinetics
Foundation item: Project(2014-36) supported by the Key Industries Innovation Team of Hubei Province, China; Project(2011-763) supported by the New Century Excellent Talent Program of Hubei Province, China; Project(2018-21) supported by Xiang yang Longzhong Talent Support Program in 2017, China
Received date: 2019-05-20; Accepted date: 2020-01-10
Corresponding author: QIN Qing-wei; Tel: +86-18971621606; E-mail: qingweiqin@126.com
(编辑 龙怀中)
基金项目:湖北省重点产业创新团队项目(2014-36);湖北省新世纪高层次人才工程专项经费资助项目(2011-763);2017年度“隆中人才支持计划”项目(2018-21)
收稿日期:2019-05-20;修订日期:2020-01-10
通信作者:秦庆伟,副教授,博士;电话:18971621606;E-mail:qingweiqin@126.com