���±�ţ�1004-0609(2015)-03-0806-09
�����̳���������-���Ƽ��Խ�������
�� �ʯ �������컪����ѧ��
(���ϴ�ѧ ұ���뻷��ѧԺ����ɳ 410083)
ժ Ҫ��������������-���ƽ�����ϵ�Ը����̳����������о�������������������̳�������Ϊ0.5������������̳���������Ϊ0.2��Һ��������Ϊ5:1����Ӧ�¶�Ϊ90 �桢��Ӧʱ��Ϊ2.0 h�������ٶ�Ϊ400 r/min�����£���Ľ�����Ϊ89.64%����Ľ�����Ϊ10.11%��Ǧ�Ľ�����Ϊ1.16%������������ĺ���Ϊ0.89%�����Һ��������-��ȴ�ᾧ���������ƣ��ᾧĸҺ���������������ƺ����Ʒ��ؽ���������ѭ�����ã�����������ֱ�ӷ���Ǧ������Ǧ�ࡣ�������鹤�ձ�·ѭ����ʵ���˸����̳�������������������Ч���롣
�ؼ��ʣ������̳������Խ��������飻ʪ��ұ��
��ͼ����ţ�TF09���� ���ױ�־�룺A
Arsenic removal from high-arsenic dust by NaOH-Na2S alkaline leaching
YI Yu, SHI Jing, TIAN Qing-hua, GUO Xue-yi
(School of Metallurgy and Environment, Central South University, Changsha 410083, China)
Abstract: The high-arsenic dust is produced from the jamesonite in pyrometallurgical process, and contains large amount of valuable metals, such as lead, antimony and indium. Because of the complex composition and high content of arsenic in high-arsenic dust, the current main processing is stockpiling. Arsenic was leached from high-arsenic dust by sodium hydroxide and sodium sulfide mixed solution. The optimum conditions were determined as follows: alkali material ratio 0.5, ratio of sodium sulfide to high-arsenic dust 0.2, leaching temperature 90 ��, leaching time 2 h, liquid-to-solid ratio 5 and stirring speed 400r/min. Under these conditions, the leaching efficiencies of arsenic, antimony and lead are 89.64%, 10.11% and 1.16%, respectively, and the content of arsenic in leaching residue is 0.89%. The leaching residue can be returned to lead smelter for recycling lead and antimony. The leaching solution was treated by hydrogen peroxide oxidation and cooled to recover sodium arsenate. The filtrate was recycled with additional sodium hydroxide and sodium sulfide to alkaline leaching step. NaOH-Na2S alkaline leaching process provides a simple and highly effective way for the removal of arsenic from high-arsenic dust.
Key words: high arsenic dust; alkaline leaching; arsenic removal; wet metallurgy
����Ǧ����ڻ�ұ�������в��������������ϸߵ�Ǧ���̳�(���¼�Ƹ����̳�)�����д�����Ǧ���ࡢ�����м۽��������нϸߵľ��ü�ֵ�����ڸ����̳��ɷָ��ӡ��麬���ϸߣ����Ż���Ҫ��Խ��Խ�ϸ������մ����̳�Խ��Խ���ѣ�Ŀǰ������ұ������ཫ��������̳����жѴ档һ���棬�����̳���Ǧ���ࡢ����Ԫ�غ������ܸߣ��Ѵ����ý�������Դ�ļ����˷ѣ���һ���棬�����̳��ڶѳ����ʱ��������ˮ��ˢ�����ܡ��������õȻ��ʹ�����ܽ���ˮ�壬������ɶ�����Ⱦ[1-2]�������̳��Ի�������Ⱦ��Ҫ��������ˮ��ˢ���̳��еĿ��������Ρ��ؽ������ӱ��ܽ⣬һ������ر�ˮ���������Ⱦ��һ���������������ö������������ˮ����ˮ������Ǩ����ɢ����ɺ����̳����������ڵ���ˮ����ˮ�麬�����ߣ�һ�������������Ǩ�ơ�ת�������Ⱦ��ʹũ���������ũ���Ʒ�к��������ߣ���ͨ��ʳ�������������Σ��������Ⱦ����̬��������ƻ����Ի������������Ⱦ������Ⱥ������������Σ��������������������в[3]����ˣ���չ�����̳������о������ո����̳��е�Ǧ����м۽�����ʹ�����̳���Դ�����������̳��Ѵ��������������Ϳ��Ƹ����̳���Ⱦ���м�����Ҫ�����塣
��Ժ�������������ѳ����⣬������ѧ�߿�չ��һϵ���г�Ч���о�����Ҫ��Ϊ�������顢ʪ����������ͻ�-ʪ�����Ϲ��ա�����������Ҫ���ڸ�����ʹ���������е������������������̬�ӷ���ʹ���������м۽������룬��ͨ�������ճ��õ����������������Ʒ�����ݺ�����������ĸ���״̬�������������Է�Ϊֱ�ӱ��ջӷ���[4]���������շ�[5]�ͻ�ԭ���շ�[6-7]������������гɱ��͡����̶̡����ռʹ�����ģ����ص㣬������������ʽϵͣ�Ͷ�ʴ�ԭ�����÷�ΧС����ҵ�����ϲ�Դ�����Ⱦ���ص�ȱ�㣬�ҵõ��������������Ʒ���Ƚϵͣ�����Ҫ��һ����������ˣ������˻��������Ӧ�á�ʪ������������Ҫ��ָʹ�ú��ʵĽ����������ȡ�������ϣ�ʹ��ӹ���ת�ƽ������Һ�У����ս�����������һ����Է�Ϊ��ˮ����[8]���������[9]�ͼ������[10]�������ӽ���Һ�з��븻����ķ���һ��������Ũ���ᾧ[11]��ʯ�ҳ�����[12]�����γ�����[13]�����Ƴ�����[14]��������[15]�ȡ������������ȣ�ʪ������������������ʸߡ�������Ⱦ�ᡢ���÷�Χ�㡢�ܺĽϵ͵��ŵ㣬���ڽ���Һ�ĺ������������л�����ֱ���Ʊ���ͬ����ϵ�в�Ʒ[16]��������ڽ���Һ�Ĵ������̽ϳ�������ȽϷ�������ҵ��ˮ�������ѵ�ȱ�㡣��-ʪ�����Ϲ���[17]��Ҫ��ָ���ô���/�ռ��Ȼ��ˮ�����飬���������������ܺĽϸߡ�����/�ռ�������������Ⱦ�Ƚ����ء���ˣ���μ������ؽ�������̳������������м۽����ķ����ǵ�ǰؽ����������⡣
���о������漰�ĸ����̳��ɷָ��ӣ������̳�����ķֲ��ȽϷ�ɢ�����������Σ��������������������ˣ��������߲�����������-���ƽ�����ϵ�Ը����̳�����ѡ����ǿ���������飬��Ǧ�������ڽ������У����������麬���ͣ�����ֱ�ӷ���Ǧ������Ǧ�ࣻͬʱ�����ò�ͬ��̬���ڸ����Һ���ܽ�ȵIJ��죬�Լ��Һ��������-��ȴ�ᾧ���������������Ʋ�Ʒ��ĽᾧĸҺ���Է��ظ����̳��Ľ������������˼��Һ�е������ֱ����˺����ˮ�IJ���������������ʵ���˱�·ѭ����
1 ʵ��
1.1 ԭ��
���о����ø����̳����Թ�����Դ��ұ����˾Ǧұ����ͭ�����ķ�¯�������̲������̳���������̳��Ѵ������������ˮ�ֺ����ϸߣ��ʽ�����105 ��ķ����24 h��������0.6 mm�����Է���ܷ��װ�����á������̳��Ļ�ѧ�ɷֺ�XRD�ֱ����1��ͼ1���ӱ�1���Կ����������̳��ɷֱȽϸ��ӣ�������1%���ϵ�Ԫ����Ǧ���ࡢ�顢����п��ͭ�����������麬���Ƚϸߡ���ͼ1�п��Կ���4�����࣬�ֱ�ΪPbS��Pb5(AsO4)3OH��Sb2O3��Pb5O8��
��1 �����̳��Ļ�ѧ�ɷ�
Table 1 Chemical composition of high arsenic dust (mass fraction, %)


ͼ1 �����̳���XRD��
Fig. 1 XRD pattern of high arsenic dust
���û�ѧ���������[18]�Ը����̳�����Ĵ�����̬�����˷��������÷�ˮ��ȡ�����顢�������ȡ����п��EDTA��ȡ����Ǧ���������ƽ�ȡ���飬�õ������̳�����ĸ�������̬�������������2��ʾ���ӱ�2���Կ����������̳�������Ҫ������Ǧ�����������ʽ���ڣ����������������п����ʽ���ڡ�
��2 �����̳�����Ļ�ѧ����������
Table 2 Chemical phase analysis of arsenic in high arsenic dust (mass fraction, %)

1.2 ʵ��ԭ��
�����̳��е�����Ǧ�����������п��������ˮ���黯����, �ڼ�����Һ����ת�������ζ�����������Һ�У����������Ϊ�������������ˮ���������ڼ��������������ƺ������ƣ������̳��е���Ǧ����������������Һ������Ǧ����������������Һ������ͨ���������ƽ���ת��Ϊ��Ǧ�Ӷ���Ǧ���������У������̳��е��������������������������Һ����ˣ�������������-���ƽ�����ϵ����ѡ���Եؽ��������̳��е��飬����Ǧ����м۽��������ڽ������У��Ӷ�ʵ�ָ����̳�������Ǧ�����Ч���롣
�����̳������������п��ܷ�������Ҫ��ѧ��Ӧ������ʾ��
Pb5(AsO4)3OH+5Na2S=5PbS+3Na3AsO4+NaOH (1)
As2O3+2NaOH=2NaAsO2+H2O (2)
As2O5+6NaOH=2Na3AsO4+3H2O (3)
Pb5O8+8Na2S+8H2O=5PbS+16NaOH+3S (4)
ͨ��������ػ������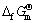 ������õ�����Ӧʽ��
������õ�����Ӧʽ��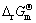 ��ʽ(1)~(4)�ı�����˹�����ܱ仯
��ʽ(1)~(4)�ı�����˹�����ܱ仯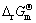 �ֱ�Ϊ-333.99��-46.3��-282.3��-769.08 kJ/mol��
�ֱ�Ϊ-333.99��-46.3��-282.3��-769.08 kJ/mol��
���ݵ��·��� ��ʽ(1)~(4)��ƽ�ⳣ��
��ʽ(1)~(4)��ƽ�ⳣ��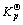 �ֱ�Ϊ3.51��1058��1.31��108��1.04��1054��6.38��10134����
�ֱ�Ϊ3.51��1058��1.31��108��1.04��1054��6.38��10134����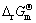 ��
��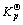 ��ֵ��֪��Ӧ(1)~(4)������ѧ���ǿ��еġ�
��ֵ��֪��Ӧ(1)~(4)������ѧ���ǿ��еġ�
1.3 ʵ�鷽������������
��ȡһ�����ĸ����̳�����500 mL�Ŀ���ƿ�У�Ȼ��������úõļ��Խ����������Ŀ���ƿ�������������趨ֵ�ĺ���ˮԡ���У������������ȴˮ�����趨�¶��½��������������������ȳ��ˣ�������ˮֱ����©��������ϴ�ӽ������������������ȡ����������Һ��ϴ��Һ�ϲ�����ϣ���¼�����ȡ�����ữ�����ݡ�����Խ���Һ�м���һ������˫��ˮ����������Ȼ����ȴ�����½��нᾧ���ᾧ��������ˡ�����õ������ƾ��壻���˺�õ��ĽᾧĸҺ�к��д����������������ƺ��������飬���䷵�ظ����̳��Ľ�����ʹ��õ����գ������������Ƶõ�ѭ�����á�����Ҫ����������ͼ2��ʾ��
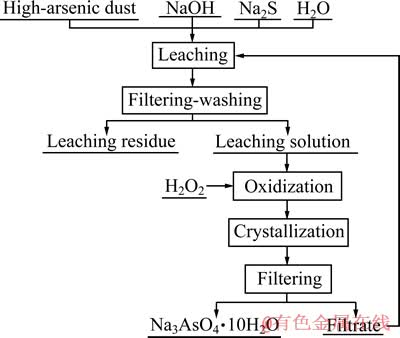
ͼ2 �����̳����Խ�����������ͼ
Fig. 2 Process chart for alkaline leaching of high arsenic dust
����ຬ��ʹ��AFS-2202Eԭ��ӫ���ȼƽ��з�����Ǧ������Ԫ�غ���ʹ��WFX-130Bԭ�����շֹ��ȼƽ��з�������Ľ����ʰ������㣬����Ԫ�صĽ����ʰ���Һ���㡣
2 ���������
2.1 ���ϱȶԽ����ʵ�Ӱ��
�ڸ����̳�Ϊ60 g����������Ϊ10 g����Ӧ�¶�Ϊ80 �桢��Ӧʱ��Ϊ2 h��Һ��������Ϊ5:1�������ٶ�Ϊ400 r/min�������£������˼��ϱȶԽ��������顢�ࡢǦ�����ʵ�Ӱ�죬������ͼ3��ʾ��
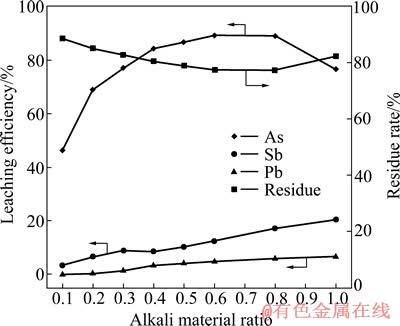
ͼ3 ���ϱȶԽ����ʵ�Ӱ��
Fig. 3 Effect of alkali material ratio on leaching efficiency
��ͼ3��֪������������ż��ϱȵ����������Ӻ��С�������ϱ�С��0.6ʱ������������ż��ϱȵ�������46.21%Ѹ��������89.26%�������ϱȴﵽ1.0ʱ��������ʽ�����76.62%��Ǧ����������ż��ϱȵ����Ӷ������ӣ��ֱ���2.99%��0.02%������20.49%��6.52%���������ż��ϱȵ�����������88.67%������77%��Ȼ��������82.17%����ʵ������У������ϱȴﵽ0.6�Ժ��ڳ��˹����У��������濪ʼ���ְ�ɫ�ᾧ������ż��ϱȵ����������࣬�������ְ�ɫ�ᾧ����Ҫ�ɷ�Ϊ�����ƣ������ϱȴﵽ1.0�Ժ���Һ��ʼ���ճ��������Һ�Ĺ������ܶ�������[19-20]��֪��As2O5��NaOH��Һ�еĵ��ܽ������NaOHŨ�ȵ����Ӷ����ͣ��������¶ȵĽ��Ͷ����͡���ˣ����ż��ϱȵ����ӣ��Ӹ����̳��н������Һ�е����������ӣ�����Һ�е���Ũ�������ӣ�����������ż��ϱȵ����Ӷ����ӣ��ڼ��ϱȴﵽ0.6�Ժ����ż��ϱȵĽ�һ�����ӣ�����Һ�е�NaOHŨ�����ӣ�����Һ��As(��)Ũ�ȴﵽ�˱��ͣ���As(��)���ܽ�����ͣ����½������Һ�е��������ͣ�����������ż��ϱȵ����ӷ�����С�������Һ�����Ũ�Ȼ����Ͻӽ����ͣ��ڳ��˹�������Ϊ�¶ȵĽ��͵����������ƽᾧ��������ȷ���ϸߵ�������ʺͽϵ͵�Ǧ������������£�ͬʱ��˽���Һ�Ĺ������ܣ�ѡ����ϱ�Ϊ0.5�ȽϺ��ʡ�
2.2 ���������Խ����ʵ�Ӱ��
�ڸ����̳�Ϊ60 g�����ϱ�Ϊ0.5����Ӧ�¶�Ϊ80 �桢��Ӧʱ��Ϊ2 h��Һ��������Ϊ5:1�������ٶ�Ϊ400 r/min�������£����������������Խ�����������Ǧ�����ʵ�Ӱ�죬������ͼ4��ʾ��
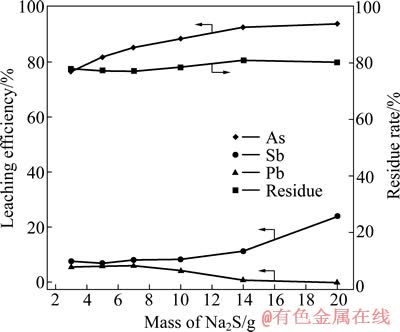
ͼ4 ���������Խ����ʵ�Ӱ��
Fig. 4 Effect of Na2S addition on leaching efficiency
��ͼ4��֪��������������������������Ӷ����ӣ�����������С��14 gʱ�����������76.48%����������92.61%���������������������������ӣ�����Һ�еĿ�����Ǧ��ת��Ϊ���ܵ���Ǧ�������ٽ�����Ǧ�ܽⷴӦ�����ҽ��У��������������ӵ�14 gʱ������������ӷ������ͣ���Ľ�����Ӧ����ƽ�⡣Ǧ�����������������������Ӷ����ͣ���������������14 g����Һ�е�Ǧ���ӻ����ϱ�������ȫ�������̳��е�Ǧ�����϶��������ڽ������У������������������ӣ�Ǧ�����������ֵ��5.95%������0.02%��������������������������Ӷ����ӣ��������������ӵ�10 g�Ժ�����������ӵķ���Խ��Խ���������������������������ӣ�����Һ�е�Ǧ����Ũ�����ͣ�����Һ�е�����Ũ�������ӣ������̳��е��������ڸ�Ũ�ȵ�������Һ�п�ʼת��Ϊ�����Ե���������ƣ�������Ľ�������6.63%Ѹ��������24.01%�����ʻ�����û�б仯���ۺϿ��ǣ�ѡ����������Ϊ14 g�ȽϺ��ʡ�
2.3 ��Ӧ�¶ȶԽ����ʵ�Ӱ��
�ڸ����̳�Ϊ60 g�����ϱ�Ϊ0.5����������Ϊ14 g��Һ��������Ϊ5:1����Ӧʱ��Ϊ2 h�������ٶ�Ϊ400 r/min�������£������˷�Ӧ�¶ȶԽ�����������Ǧ�����ʵ�Ӱ�죬������ͼ5��ʾ��
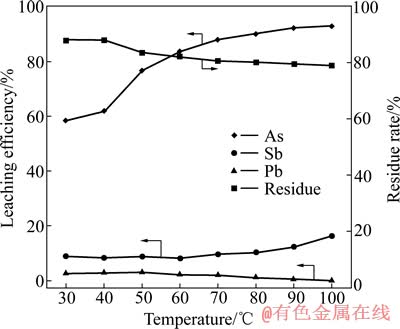
ͼ5 ��Ӧ�¶ȶԽ����ʵ�Ӱ��
Fig. 5 Effect of temperature on leaching efficiency
��ͼ5��֪������������ŷ�Ӧ�¶ȵ����Ӷ����ӣ���90 ��֮ǰ�����������58.48%����������92.11%��һ���棬��������������Һ�е��ܽ�������¶ȵ����Ӷ�����[20]����һ���棬����Ǧ�ķֽⷴӦ�����ȷ�Ӧ����ˣ����ŷ�Ӧ�¶ȵ����ߣ���Ӧƽ�����������ƶ���������������ӡ���90 ��֮������Ǧ�����Ϸֽ���ȫ��������ʵ���������ƽ��������������ŷ�Ӧ�¶ȵ����Ӷ����ӣ���60 ��֮ǰ�����������8%���Ҳ���������Ӧ�¶ȴ�60 �������90 ��ʱ�����������8.08%������12.26%����90 ��֮��������ʿ���������16.17%���������������������ת��Ϊ��������Ƶķ�Ӧ�ڸ��¸����������йأ���Ǧ�ij����������ȷ�Ӧ����ˣ����ŷ�Ӧ�¶ȵ����ӣ�Ǧ�ij�����Ӧƽ�����������ƶ���Ǧ���������ͣ���90 ��֮����Һ�еĿ�����Ǧ�����ϳ�����ȫ��Ǧ�����������ֵ��3%������0.09%���������ŷ�Ӧ�¶ȵ����Ӷ����ͣ����������ȶ����ۺϿ��ǣ�ѡ��Ӧ�¶�Ϊ90 ��ȽϺ��ʡ�
2.4 ��Ӧʱ��Խ����ʵ�Ӱ��
�ڸ����̳�Ϊ60 g�����ϱ�Ϊ0.5����������Ϊ14 g��Һ��������Ϊ5:1����Ӧ�¶�Ϊ90 �桢�����ٶ�Ϊ400 r/min�������£������˷�Ӧʱ��Խ�����������Ǧ�����ʵ�Ӱ�죬������ͼ6��ʾ��
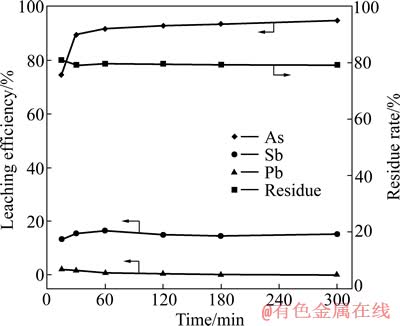
ͼ6 ��Ӧʱ��Խ����ʵ�Ӱ��
Fig. 6 Effect of time on leaching efficiency
��ͼ6��֪������������ŷ�Ӧʱ������Ӷ����ӣ���2 h��ǰ������������ŷ�Ӧʱ���������74.61%����������92.88%������2 h�Ժ�����������ӵķ������ͣ�������Ӧ�����ȶ���Ǧ���������ŷ�Ӧʱ������Ӷ����ͣ�����2 h֮ǰ��Ǧ��������1.56%������0.22%������2 h֮��Ǧ������������0.01%������������ŷ�Ӧʱ������������Ӻͣ����������1 hʱ������16.45%���ﵽ���ֵ��Ȼ������ʱ������ӣ�������ʻ���������15%���ҡ���������ڴﵽ���ֵ�������ͣ���������������������������ʽ�������Һ���ಿ�ֱ�����������������ˮ�������ƣ��������ƽ���������дӶ�����������ʵĽ��ͣ��Ż�ʵ���м������XRD���п��Եõ���֤����ȷ���ϸߵ�������ʺͽϵ͵�Ǧ������������£��ۺϿ����ܺġ����ܵ����أ���Ӧʱ��ѡ��2 h�ȽϺ��ʡ�
2.5 Һ�̱ȶԽ����ʵ�Ӱ��
�ڸ����̳�Ϊ60 g�����ϱ�Ϊ0.5����������Ϊ14 g����Ӧʱ��Ϊ2.0 h����Ӧ�¶�Ϊ90 �桢�����ٶ�Ϊ400 r/min�������£�������Һ�������ȶԽ�����������Ǧ�����ʵ�Ӱ�죬������ͼ7��ʾ��
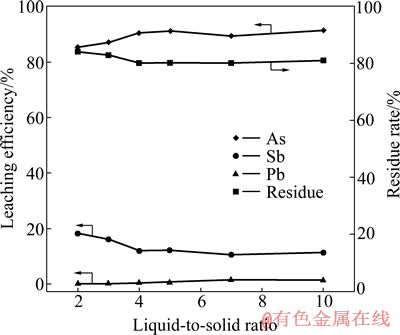
ͼ7 Һ�̱ȶԽ����ʵ�Ӱ��
Fig. 7 Effect of liquid-to-solid ratio on leaching efficiency
��ͼ7��֪�������������Һ�̱ȵ�����������Ȼ�������ȶ�����Һ�̱�С��5.0ʱ�����������85.43%����������91.25%����Һ�̱ȴ���5.0ʱ����Ľ�����Ӧ����ƽ�⡣�����������Һ�̱ȵ����Ӷ����ͣ���Һ�̱�С��4.0ʱ�����������18.24%���ٽ���11.62%����Һ�̱ȴ���4.0ʱ��������������ȶ���Ǧ����������Һ�̱ȵ����Ӷ��������ӣ���Һ�̱�Ϊ7.0ʱ��Ǧ�����ʴﵽ���ֵ(1.23%)�������ϱ�һ��ʱ������Һ�̱ȵĽ��ͣ�����Һ���������Ƶ�Ũ�������ӣ�����As(��)������������Һ�е��ܽ�����ż�Ũ�ȵ����Ӷ����ͣ�ʹ�ý���Һ�п����ɵ��������ͣ�ͬʱ������Һ�̱ȵĽ��ͣ�������ϵ�������ӣ�Һ�̷�������н������д���ʧ���������ӡ������Ƶ�����һ��ʱ������Һ�̱ȵ����ӣ�������ϵ�����Ƶ�Ũ�����ͣ���������������ת��Ϊ�����Ե���������Ƶ�ת����Խ��Խ�ͣ������ڲ��ܹ�ת����ͬʱ������Һ��S2-���ӵ�Ũ�Ƚ��Ͳ���������Ǧ�Ľ�������ʹ����Һ��Pb2+����Ũ�������ӡ�����߲��ܺͽ����ܺĵĽǶȣ�ѡ��ϵ͵�Һ�̱��Ǻ��ʵģ���Һ�̱ȹ���ʱ���ڹ�Һ������������¶ȵĽ��������������ƽᾧ�������ۺϿ��ǣ�Һ��������ѡ��5.0�ȽϺ��ʡ�
2.6 �����ٶȶԽ����ʵ�Ӱ��
�ڸ����̳�Ϊ60 g�����ϱ�Ϊ0.5����������Ϊ14 g��Һ��������Ϊ5:1����Ӧ�¶�Ϊ90 �桢��Ӧʱ���Ϊ2.0 h�������£������˽����ٶȶԽ�����������Ǧ�����ʵ�Ӱ�죬������ͼ8��ʾ��
��ͼ8��֪������������Ž����ٶȵ����Ӷ��������ӣ��������ٶ�С��350 r/minʱ�����������91.74%����93.22%���������ٶȴﵽ350 r/min֮�����������93%���Ҳ�����������ƽ�⡣����������Ž����ٶȵ����Ӷ����ͣ���18.56%������12.52%��Ǧ�����϶��������ڽ������У�Ǧ�������������㡣�ۺϿ��ǣ������ٶ�ѡ��400 r/min�ȽϺ��ʡ�
2.7 �Ż�ʵ��
ͨ�����ϵ�ϵ��ʵ���о����ɵó������̳����Խ������Ż���������������Ϊ0.5������������̳�������Ϊ0.2��Һ��������Ϊ5:1����Ӧ�¶�Ϊ90 �桢��Ӧʱ���Ϊ2.0 h��������Ϊ400 r/min���ڴ��Ż���������������3��ʵ�飬��ʵ�������3��4���С��������XRD����ͼ9��ʾ��
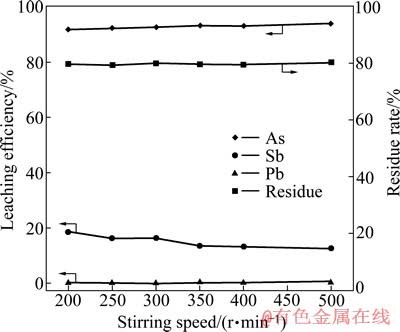
ͼ8 �����ٶȶԽ����ʵ�Ӱ��
Fig. 8 Effect of stirring speed on leaching efficiency
�ɱ�3��4���Կ��������Ż�ʵ�������£����ƽ��������Ϊ89.64%�����Խ����������ƽ������Ϊ0.89%������Һ���ࡢǦ������п��ͭ������ƽ�������ֱ�Ϊ1.83��1.08��1.39��1.69��0.002��0.005 g/L���ࡢǦ������п��ͭ������ƽ�������ʷֱ�Ϊ10.11%��1.16%��26.18%��35.82%��0.11%��0.14%����ͼ9�п��Կ���3�����࣬�ֱ�ΪPbS��Sb2O3��NaSb(OH)6���Աȸ����̳���XRD���Կ������ڼ������XRD���У�Pb5(AsO4)3OH��Pb5O8����������������ʧ�ˣ�����仯��֤ʵ��ʵ��ԭ����������4����Ӧ��˵���ڼ������������Ǧ������������Ǧת��Ϊ��Ǧ��NaSb(OH)6�����ij���˵�������̳��е�Sb2O3�ڼ����������һ����ת��Ϊˮ�������ơ�
��3 �Ż�ʵ����
Table 3 Experiment results of optimal experiment

��4 �Ż�ʵ���и�Ԫ�صĽ�����
Table 4 Leaching efficiencies of elements based on composition of leaching liquor

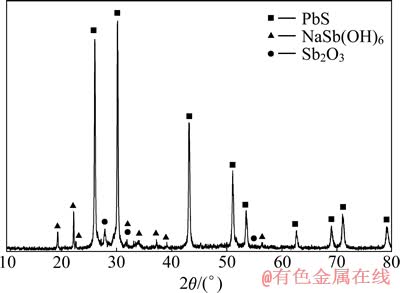
ͼ9 �������XRD��
Fig. 9 XRD pattern of alkali leaching residue
���Ż�ʵ������֪���ڸ����̳���������-���Ƽ��Խ��������У�90%������뵽����Һ�У�90%���ࡢ99%��Ǧ��74%������64%��п�ͼ���ȫ����ͭ���������˽������У��Ӷ�ʵ������������������Ч�����Ŀ�ģ�����������Ҫ�ɷ�ΪPbS�����麬���ϵͣ�����ֱ�ӷ���Ǧ�����սṤ������
2.8 ���Һѭ������ʵ��
�ڸ����̳����Խ��������У�Ϊ�˱�֤�ϸߵ�������ʣ������������������ԶԶ���������������������������Һ����������Ũ����80 g/L���ҡ���ˣ������Һ����ظ����̳��Ľ������Խ�Լ�������Ƶ�ʹ������ͬʱ�����ˮ�IJ������ŷš����Һ�е������As(��)��ʽ���ڣ�����һ������˫��ˮ��As(��)������As(��)��Ȼ����ȴ�����½��нᾧ���ս���Һ�е��飬�ᾧĸҺ���ظ����̳��Ľ�����
ѭ������ʵ����̣�ȡ60 g�����̳��������Ż�ʵ���������н�����������������ȹ��ˣ�����Һ�м���3 mL˫��ˮ����20 min��Ȼ����ȴ�����½ᾧ2 h���ᾧ��������ˣ��õ���ɫ�����ƽᾧ�ͽᾧĸҺ�������Ż�ʵ���������ᾧĸҺ���������������ƺ����Ʒ��ظ����̳������������ᾧ�����ɫ�����ƽᾧ��40 ���µ��º�ɣ��仯ѧ�ɷֺ�XRD�ֱ����5��ͼ10��ʾ�����Һ����3��, �Կɵõ��Ϻõ�����Ч����ѭ������ʵ�������6��ʾ��
��5 ��ɫ�ᾧ�Ļ�ѧ�ɷ�
Table 5 Compositions of white crystalline (mass fraction, %)

ͼ10 ��ɫ�ᾧ��XRD��
Fig. 10 XRD pattern of white crystalline
�ӱ�5��ͼ10���Կ���������-��ȴ�ᾧ�����ĺ��黯����ΪNa3AsO4��10H2O���ᾧ���麬��Ϊ17.8%���Ե���Na3AsO4��10H2O �������麬��(19.31%)������������������ᾧ��������У����Һ�е����౻�������������ƽᾧ�С�
�ɱ�6���Կ������ᾧĸҺ���ظ����̳��ļ��Խ���������Ľ�����Ӱ�첻���Һ����3�κ����̳�����Ľ��������ܴﵽ90%���ң�����Һ�����Ǧ��Ũ�ȷֱ���1.8 g/L���Һ�0.95 g/L���ң�����п��Ũ�ȷֱ���1.40 g/L��1.51 g/L��������3.26 g/L��3.76 g/L���������ᾧ��������У�����Һ�е��顢����������ƽᾧ�У����Һ����Ľᾧ�ʿɴﵽ90%���ң���Ľᾧ�ʿ��Դﵽ97 %���ң���Ǧ������п�Ƚ���Ԫ�������ڽᾧĸҺ�С�
��6 �����̳�ѭ������ʵ����
Table 6 Experiment results of circulation leaching of high-arsenic dust
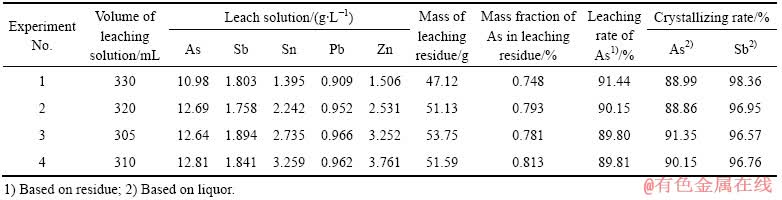
���ż��Һ�ķ��ؽ�������ϵ�е�����п���ϻ��ۣ��ᾧĸҺ�е�����п����Ũ�������ӣ���ˣ���Ҫ������п����ϵ�п�·�ų����ڸ�ȵ���Һ�У������Բ���Ca(OH)2�������ѳ���п��Ǧ���Բ���Na2S�������ѳ�[21]��ʵ��������ڵ��Ĵ�ѭ���У�����-�����ᾧĸҺ����������2.5����������Ca(OH)2��1����������Na2S���ֱ���80 ��������·�Ӧ���ᾧĸҺ�е�����Ǧ��п���Էֱ��ѳ���0.5��0.05��0.03 g/L��
3 ����
1) ������������-���ƻ��Һ���������̳������Һ��������-��ȴ�ᾧ���������ƣ��ᾧĸҺ���ظ����̳��Ľ������̣�ʵ���˸����̳������������м۽����ķ��룬�ù��չ��������ж�����������������鹤�����̶��ұ�·ѭ������ˮ�������ŷš�
2) ͨ����������̳����Խ��������и����ضԽ������̵�Ӱ�죬ȷ���˸����̳����Խ����������ѹ�����������������������̳�������Ϊ0.5������������̳�������Ϊ0.2��Һ��������Ϊ5:1����Ӧ�¶�Ϊ90 �桢��Ӧʱ���Ϊ2.0 h��������Ϊ400 r/min���ڴ������£���Ľ�����Ϊ89.64%����Ľ�����Ϊ10.11%��Ǧ�Ľ�����Ϊ1.16%������������ĺ���Ϊ0.89%������������ֱ�ӷ���Ǧ������Ǧ�ࡣ
3) ���Һ��������-��ȴ�ᾧ���������ƣ����Һ����Ľᾧ�ʿɴﵽ90%���ң���Ľᾧ�ʿ��Դﵽ97%���ң��ᾧĸҺ���ظ����̳��ļ��Խ���������Ľ�����Ӱ�첻�����̳�����Ľ��������ܴﵽ90%���ҡ����ѭ�������ᾧĸҺ�л��۵�����п���Էֱ����ʯ�ҳ��������Ƴ����ѳ����Ա�����Ը����̳��������̵�Ӱ�졣
REFERENCES
[1] �� ��, �Ź�ƽ, �� ��, �� ��, κ����. �������������������Sb��As��Ǩ�Ƽ�����Ӱ��[J]. ������ѧ�о�, 2009, 22(6): 682-687.
LI Ling, ZHANG Guo-ping, LIU Hong, XIANG Meng, WEI Xiao-fei. Antimony and arsenic migration and environmental impacts on river draining in the Dachang multi-metalliferous mine area in Guangxi, China[J]. Research of Environmental Sciences, 2009, 22(6): 682-687.
[2] �� ��, Ҧ��, ������, ������. �����̻�������״[J]. ������ɫ����, 2013, 29(5): 41-44.
HU Bin, YAO Jin-jiang, WANG Zhi-you, ZHOU Zuo-dong. The review of arsenic removal technologies of arsenic ashes[J]. Hunan Nonferrous Metals, 2013, 29(5): 41-44.
[3] �� ��, ����չ. �����±����Ŵ��ı����°����õ��о���չ[J]. �й��ط���ѧ����, 2012, 31(1): 107-110.
LING Min, LIU Qi-zhan. Arsenic due to epigenetic changes and carcinogenesis studies progress[J]. Chinese Journal of Endemiology, 2012, 31(1): 107-110.
[4] Ԭ����. �����̳�����ȡ����ʵ�鼰����ѧ�о�[J]. ����ұ��, 2011, 40(6): 27-34.
YUAN Hai-bin. Thermodynamics research and experiment of white arsenic extraction from high arsenic fume by pyrometallurgy[J]. Yunan Metallurgy, 2011, 40(6): 27-34.
[5] �� ��, ����, ��Ԫ��, �����, ����, �����. ��������������Ԥ����-����ԭ���չ�������Ļӷ���Ϊ[J]. ���ϴ�ѧѧ��: ��Ȼ��ѧ��, 2010, 41(1): 1-7.
JIANG Tao, HUANG Yan-fang, ZHANG Yuan-bo, HAN Gui-hong, LI Guang-hui, GUO Yu-feng. Behavior of arsenic in arsenic-bearing iron concentrate pellets by preoxidizing-weak reduction roasting process [J]. Journal of Central South University: Science and Technology, 2010, 41(1): 1-7.
[6] �����, �� ��, �� ��. ��������ʯ������̵�����ѧ[J]. �й���ɫ����ѧ��, 2011, 21(7): 1705-1712.
ZHANG Shu-hui, L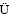 Qing, HU Xiao. Thermodynamics of arsenic removal from arsenic-bearing iron ores[J]. The Chinese Journal of Nonferrous Metals, 2011, 21(7): 1705-1712.
Qing, HU Xiao. Thermodynamics of arsenic removal from arsenic-bearing iron ores[J]. The Chinese Journal of Nonferrous Metals, 2011, 21(7): 1705-1712.
[7] �� ��, ������, �δ���, ʯ��. ͭ����¯�̻ұ��������о�[J]. ��ɫ����: ұ������, 2011(1): 9-11.
LIANG Yong, LI Liang-xing, LIAO Chun-fa, SHI Yu-chen. Study on de-arsenic from dust of flash smelting furnace[J]. Nonferrous Metals: Extractive Metallurgy, 2011(1): 9-11.
[8] ����Դ, ֣�Ӷ�, ���и�. ����ƽ��ұ����ʪ�����鹤�����[J]. ��ɫ����, 2003, 55(3): 62-64.
ZHOU Xiao-yuan, ZHENG Zi-en, LI You-gang. Design of arsenic extraction with hydrometallurgical process for northern Pyongyang smelter in Korea[J]. Nonferrous Metals, 2003, 55(3): 62-64.
[9] CHEN Ya, LIAO Ting, LI Gai-bian, CHEN Bai-zhen, SHI Xi-chang. Recovery of bismuth and arsenic from copper smelter flue dusts after copper and zinc extraction[J]. Minerals Engineering, 2012, 39: 23-28.
[10] YU Guo-lin, ZHANG Ying, ZHENG Shi-li, ZOU Xing, WANG Xiao-hui, ZHANG Yi. Extraction of arsenic from arsenic- containing cobalt and nickel slag and preparation of arsenic- bearing compounds[J]. Transaction of Nonferrous Metals Society of China, 2014, 24(10): 1918-1927.
[11] PENG Ying-lin, ZHENG Ya-jie, ZHOU Wen-ke, CHEN Wen-mi. Separation and recovery of Cu and As during purification of copper electrolyte[J]. Transaction of Nonferrous Metals Society of China, 2012, 22(9): 2268-2273.
[12] LI Yu-hu, LIU Zhi-hong, LI Qi-hou, ZHAO Zhong-wei, LIU Zhi-yong, ZENG Li, LI Li. Removal of arsenic from arsenate complex contained in secondary zinc oxide[J]. Hydrometallurgy, 2011, 109: 237�C244.
[13] SULLIVAN C, TYRER M, CHEESEMAN, CHRISTOPHER R, GRAHM, NIGEL J D. Disposal of water treatment wastes containing arsenic��A review[J]. Science of the Total Environment, 2010, 408: 1770�C1778.
[14] ��ѧ��, �ι���, �����, ½ �. �����̳����������о�[J]. ʪ��ұ��, 2010, 29(3): 99-202.
JIANG Xue-xian, HE Gui-xiang, LI Xu-guang, LU Jing. Experimental research on dearsenization of high arsenic fume[J]. Hydrometallurgy of China, 2010, 29(3): 199-202.
[15] MOHAN D, PITTMAN C U Jr. Arsenic removal from water/wastewater using adsorbents: A critical review[J]. Journal of Hazardous Materials, 2007, 142(1/2): 1-53.
[16] ֣�Ž�, ��ʤ��, �� ��. ����������Դ������ͭ������¹���[J]. �й���ɫ����ѧ��, 2013, 23(10): 2985-2992.
ZHENG Ya-jie, ZHANG Sheng-hua, GONG Chang. Novel technique for recovery of copper and arsenic from arsenic-containing waste acid[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(10): 2985-2992.
[17] ���Ԫ. �������ϵ�NaOH�������鹤��[J]. �й���ɫ����ѧ��, 1998, 8(2): 451-453.
WU Guo-yuan. Removing arsenic from the high arsenic material by NaOH roasting[J]. The Chinese Journal of Nonferrous Metals, 1998, 8(2): 451-453.
[18] ������. ��ķ�����ѧ[M]. ����: �й�������ѧ������, 1986: 178-180.
FENG Shu-ping. Analytical chemistry of arsenic[M]. Beijing: China Environmental Science Press, 1986: 178-180.
[19] URAZOV G G, LIPSHITS B M. The solubility isotherms of Na2O-H2O-As2O5 system at 75 ��[J]. Russian Journal of Inorganic Chemistry, 1960, 5(4): 950-952. (in Russian)
[20] GUERIN H, MATTRAT P. Study on the alkaline arsenates of As2O5-Na2O-H2O system at 25 ��[J]. French Bulletin of Chemical Society, 1957, 2: 323-329. (in French)
[21] �� ��, ���ɲ�, �Թ���. �������ƽ���-�����������Ʊ�Ǧп�����¹���[J]. ʪ��ұ��, 2010, 29(1): 32-36.
LIU Qing, ZHAO You-cai, ZHAO Guo-dong. A novel process for preparation of zinc and lead concentrates by alkaline leaching and precipitation[J]. Hydrometallurgy of China, 2010, 29(1): 32-36.
(�༭ ����)
������Ŀ�������Ƽ����ؼƻ�������Ŀ(��ƹ�12300001-2)
�ո����ڣ�2014-05-28�������ڣ�2014-12-29
ͨ�����ߣ���ѧ�棬���ڣ���ʿ���绰��0731-88877863��E-mail: xyguo@csu.edu.cn