���±�ţ�1004-0609(2014)05-1352-07
����������˾������ؽ�����Ⱦ����Ķ���ѧ
�� ӱ1, 2��л־��2��Ѧ �2��������2���� ��2���� ��2
(1. �Ӻ���ѧ dzˮ�����ۺ���������Դ�����������ص�ʵ���ң��Ͼ� 210098��
2. �Ӻ���ѧ ����ѧԺ���Ͼ� 210098)
ժ Ҫ���������������˾�����(T. f)���˷������ؽ�����Ⱦ�������ʵ���о������÷���ҡ�����������������������˹�����Fe2+Ũ�ȶԵ����ữ������������Fe2+�����Լ��������ؽ����ܳ��ʵ�Ӱ�죻����Monod���̵õ���ͬFe2+Ũ��������������˾��������������ʼ����ͳ�����ͨ�����鷽���Ƶ�����ͬFe2+Ũ�����ؽ�������Cu2+��Zn2+���ܳ����ʳ����������������Fe2+Ũ����2.0 g/L���ӵ�10.0 g/Lʱ������������˾�����������������0.126 h-1������0.159 h-1�����ͳ�����0.881 g/L�½���0.327 g/L���ؽ������ܳ����ʳ�����Fe2+Ũ�ȳ�����أ���Fe2+Ũ�ȳ���10.0 g/Lʱ������������˾��������������ʽ��ͣ������ͳ�����������Fe2+Ũ�ȵ�����Fe2+�������������ۺϸ�������ѧ������֪��Fe2+Ũ��Ϊ10.0 g/L������������ϵ����ѵ���Ũ�ȡ�
�ؼ��ʣ��ؽ���������������˾����������ˣ�����ѧ
��ͼ����ţ�X524 �� �� ���ױ�־�룺A
Bioleaching kinetics of heavy metal from contaminated sediment by Thiobacillus ferrooxidans
XU Ying1, 2, XIE Zhi-gang2, XUE Lu2, FENG Yue-yang2, CHEN Yu2, SUN Ying2
(1. Key Laboratory of Integrated Regulation and Resource Development on Shallow Lake of
Ministry of Education, Hohai University, Nanjing 210098, China;
2. College of Environment, Hohai University, Nanjing 210098, China)
Abstract: The bioleaching kinetics of heavy metal from contaminated sediment was studied by batch experiments with Thiobacillus ferrooxidans (T. f). The effects of Fe2+ concentrations on the sediment acidification, the growth of T. f, Fe2+ oxidation, and solubilization ratio of heavy metal during the bioleaching process were investigated. Monod equation was used to derive the maximum specific growth rate and the saturation constant of the T. f with different Fe2+ concentrations. An empirical equation was also used to derive the rate constants of heavy metal ions (Cu2+ and Zn2+) solubilization with different Fe2+ concentrations. The results show that when Fe2+ concentration increases from 2.0 g/L to 10.0 g/L the maximum specific growth rate of T. f increases from 0.129 h-1 to 0.159 h-1, the saturation constant reduces from 0.881 g/L to 0.327 g/L and the rate constant of heavy metals solubilization is linearly dependent on the Fe2+ concentrations. When Fe2+ concentrations is over 10.0 g/L, the maximum specific growth rate of the T. f reduces, while the saturation constant increases. The Fe2+ oxidation rates increase with increasing the Fe2+ concentrations. Taking all the kinetics parameters into account, the optimal concentration of Fe2+ is found to be 10.0 g/L.
Key words: heavy metal; Thiobacillus ferrooxidans; bioleaching; kinetics
������Ϊ���Ƴ���ˮ����˾ӻ����������ҹ�����Ӻ������˽ϴ��ģ���迣�����ٵ���Ĵ����ѳ�Ϊ����������һ������[1]�������迣���ຬ�д�����Ӫ������ԣ��������ó�Ϊ�����迣�������Ч;�������ڳ��кӺ��������������и�Ũ�ȵ��ؽ������ڵ����������ú��ؽ�����Ǩ��ת������Σ�����ཡ���ͻ�����ȫ����ˣ�����������ǰȥ�����������ؽ����dz���Ҫ��Ŀǰ���ؽ�����ȥ��������Ҫ�����綯���������������˷�����ѧ�Լ����ᷨ��ֲ����ȡ���Լ����ӽ��������������������ȡ����У���ͳ�Ļ�ѧ����ȥ��Ч�����ԣ����������ýϸߣ�������ʵ�����ձ�Ӧ��[2]��
�������˷��ǹ����Ͻ����������һ��dz���ǰ���Ľ������Ἴ�����÷�����Ҫ������Ȼ����һЩ�����ֱ�����û����л����ļ�����ã��������ؽ�������������Ӷ��ﵽ����Ч�����뻯ѧ���ᷨ��ȣ��������˷����з�Ӧ�º͡������١����гɱ��ϵ͵��ŵ�[3-4]���Ѿ��ɹ���������ˮ���༰���շɻ����ؽ���ȥ�����ؽ�����Ⱦ���������������������ҵ���������ؽ����ѳ������ؽ����Ļ��յȷ���[5-8]���й����������˷����о���������Ҫ�漰�������˴�����ˮ���ࡢ�ӵ����༰���շɻ����ؽ�����Ӱ���� ���о�[9-11]�����ڴӶ���ѧ�Ƕ��о�����Ũ�ȶ����������ؽ�����Ⱦ������о��������١���������Ӧ�ý϶�ľ���Ϊ��������˾�(Thiobacillus thiooxidans, T. t)������������˾�(Thiobacillus ferrooxidans, T. f)����������˾���С�����л����������������������á������и������ܽ����л����Ƿ������������������в�������������˵�Ч��ֱ����ء���ˣ��ڵ�������ж���������������Fe2+����������ѧ�����о������ڽ�ʾϸ�����������ƣ����ϸ���������ʣ��Ż��������˵���Ĺ�������������Ҫ�IJο���ֵ��
���������о����÷���ҡ��������������������������˾��������˹�����Fe2+Ũ�ȶԵ����ữ������������Fe2+�����Լ��������ؽ����ܳ��ʵ�Ӱ�죬����Monod�����о���ͬ����Ũ�������������Ķ���ѧ������ͨ�����鷽���������ͬFe2+Ũ����Cu2+��Zn2+���ܳ����ʳ�������������Ũ�ȶԵ������ؽ����ܽ����ʵ�Ӱ�죬Ϊ��������������Ⱦ���༼���ṩ֧�š�
1 ʵ��
1.1 ��Ʒ�ɼ���������
���о��вɼ��Ͼ����ػ��ӵ������ʵ�飬����pH 7.38���ܵ�����0.223%��������0.004%���л��ʺ���5.03%(��������)��Cu����99.28 mg/kg��Zn����422.59 mg/kg��
1.2 ��Ʒ��������
�ܵ��������ÿ������ⶨ����������������-�����ɫ���ⶨ���л��ʺ������õ��������ظ��������-��ɫ���ⶨ��Cu��Znʹ��ICP-AES�����ⶨ��pH��������ԭ��λ(ORP)����pH/ORP�Ʋⶨ��Fe2+���������ڷƆ����ֹ��ȷ��ⶨ���������Ѫ�������������������ؽ�����̬��BCR����ȡ���ⶨ[12-13]��
1.3 ����������˾���ѱ��
����������˾�(���Ͼ���ѧ�����ѧ�빤��ѧԺ�ṩ)������9K�������У���ʢ��Һ����ƿ�������ҡ���У���30 �桢180 r/min���������������ڼ��pH�仯����pH����2����ʱ����ȡ20 mL��Һ��������180 mL��20 g/L�����9K�������У���30 ������������pH����2����ʱֹͣ������ѱ��3�����õ�ѱ����Һ��Ϊ������������ʵ��Ľ����
1.4 ��������ʵ���������
��ȡ4 g�������ĥ������150 ��mɸ�ĵ������ӵ�500 mL�ྻ����ƿ�У���8��ɴ����ţƤֽ��ڣ������ѹ���������121 �����ʪ�����30 min����ȴ��ȷ��ȡ180 mL Fe2+Ũ�ȷֱ�Ϊ2.0��4.0��6.0��8.0��10.0��12.0��20.0 g/L�����9K����Һ(pHΪ3)�������ƿ�У�������20 mL����Һ����ʢ�л��Һ����ƿ�������ҡ���У���30 �桢180 r/min�����½����������������������˷�Ӧ��ϵ��ȡһ����������Һ���ÿ�0.45 ��m����Ĥ���ˣ�Ȼ��ⶨ����Cu2+��Zn2+��Fe2+������(FeT)��Ũ�ȣ�ͬʱȡ����Һ��������������ⶨ��Ӧ��ϵ�е�pH��ORP��ÿ��ʵ�鷴������3�Σ�ͬʱ��Fe2+Ũ��Ϊ10.0 g/L�����־�Һ�Ķ���ʵ�顣
2 ���������
2.1 ��ͬFe2+Ũ����pH��ORP��ʱ��ı仯
����������˾����������е��ؽ�����2�����û���[14]��ֱ�ӻ����ķ�ӦʽΪ
MS+2O2 M2++
M2++ (1)
(1)
����ֱ�ӻ����������еĽ�������ͨ�����������ֱ�ӱ�����������˾������ɿ����ԵĽ��������ν�������ӻ����ķ�ӦʽΪ
2FeSO4+0.5O2 +H2SO4 Fe2(SO4)3 +H2O (2)
Fe2(SO4)3 +H2O (2)
4Fe2(SO4)3+2MS+4H2O+2O2��2MSO4+8FeSO4+4H2SO4 (3)
���ռ�ӻ���������������˾����Ƚ���������������������(ʽ(2))��Ȼ�����������������������ɽ��������ν���(ʽ(3))����Ӧʽ(2)��(3)����������-��ԭ��ѭ��ϵͳ��ʹԽ��Խ����ؽ����ܽҺ�࣬��Ӧʽ(3)�����ɵ����ή����������ϵ��pHֵ���ӿ��˵������ؽ������ܽ⡣ORP��������Ҫ��������������˾��Ĵ��������ã����м���ﻹԭ̬�������������Լ���Fe2+������Fe3+����ˣ�pH��ORP�DZ���������������ǿ������Ҫָ�꣬pH���ͱ�����������������ORP������������������������ϸ��������ֳ[15]��
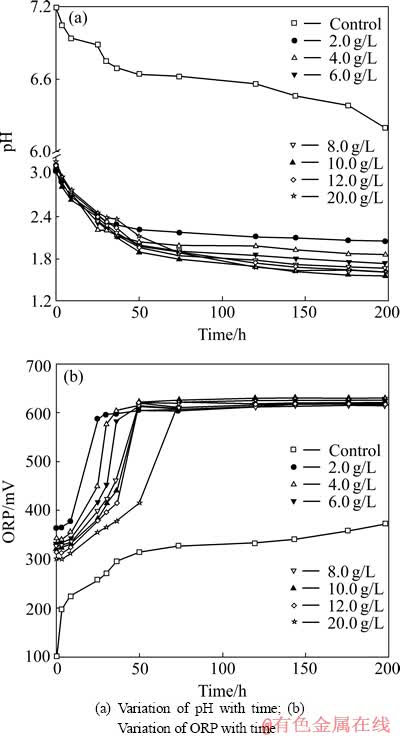
ͼ1 ��ͬ��ʼFe2+Ũ����pH��ORP��ʱ��ı仯����
Fig. 1 Changing curves of pH and ORP with time at different initial Fe2+concentrations
ͼ1��ʾΪ��ͬFe2+Ũ����pH��ORP��ʱ��ı仯����ͼ1��֪��������pH�ϸߣ���ORP����������������ΪFe2+��ѧ��������Զ�������������� ��[16]����ͬ����Ũ���¸�ʵ����ij�ʼpH������ͬ������ʼORP����Fe2+Ũ�ȵ����߶����н��͡����������˹����У�Fe2+Ũ����2.0 g/L������10.0 g/Lʱ��pH���½����ʼ�ORP�������ʾ�������Fe2+Ũ�ȳ���10.0 g/L��pH���½����ʼ�ORP�����������ͣ����������Fe2+Ũ�ȹ�������������������˾��Ļ��ԡ�
2.2 Fe2+Ũ�ȶ�����������˾�������Ӱ��
���������˵�ʵ������У���һ����ʱ�����ⶨ����������˾�����������������������˾�������ʱ��仯����(��ͼ2)��Ȼ��������ֵ�ַ���ʽ(4)������������ʣ�
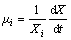 (4)
(4)
ʽ�У���i��Xi�ֱ�Ϊtiʱ���������������(h-1)����������(mL-1)��
���Ϧ�i��tiʱ��Fe2+��Ũ�ȣ����Ʋ�ͬ��ʼFe2+Ũ����tiʱ��Fe2+Ũ�����i�Ĺ�ϵ(��ͼ3)����ͼ3�е����ݴ���Monod����[16-17]��
 (5)
(5)
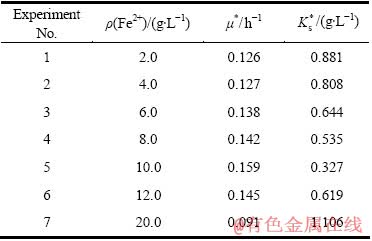
ʽ�У���*�� ��S�ֱ�Ϊ������������(h-1)�����ͳ���(��=1/2��*ʱFe2+��Ũ�ȣ�g/L)��tiʱ��Fe2+��Ũ��(g/L)���������(Levenberg-Marquardt, LM)�������з�������ϣ��õ���ͬ��ʼFe2+Ũ���µ������������ʼ����ͳ���(����1)������1�еĦ�*��
��S�ֱ�Ϊ������������(h-1)�����ͳ���(��=1/2��*ʱFe2+��Ũ�ȣ�g/L)��tiʱ��Fe2+��Ũ��(g/L)���������(Levenberg-Marquardt, LM)�������з�������ϣ��õ���ͬ��ʼFe2+Ũ���µ������������ʼ����ͳ���(����1)������1�еĦ�*�� ֵ���뷽��(5)�õ�ͼ3�е����ߣ���ͼ3�ɼ������ֵ��ʵ�������ǺϽϺá�
ֵ���뷽��(5)�õ�ͼ3�е����ߣ���ͼ3�ɼ������ֵ��ʵ�������ǺϽϺá�
��1 ��ͬ��ʼFe2+Ũ����T. f�Ķ���ѧ����
Table 1 Kinetic parameters obtained at different initial Fe2+concentrations for T.f
����������������ϸ����������ϸ�������ı�����ϵ������������Խ��ϸ���������ٶ�Խ�죻 ��ʾ�����Ӫ����������ԣ�
��ʾ�����Ӫ����������ԣ� ԽС������Խǿ�����ݱ�1������Fe2+Ũ�ȵ����ӣ���*���������Ӻ��½������ƣ���
ԽС������Խǿ�����ݱ�1������Fe2+Ũ�ȵ����ӣ���*���������Ӻ��½������ƣ��� �Ĺ������*�෴��˵������Fe2+Ũ�ȵ����ӣ�ϸ���������ʼӿ죬Fe2+����������Ҳ�ӿ죬����Fe2+Ũ�����ӵ�һ���̶�ʱ��������������������������ã����������������ʽ��͡�
�Ĺ������*�෴��˵������Fe2+Ũ�ȵ����ӣ�ϸ���������ʼӿ죬Fe2+����������Ҳ�ӿ죬����Fe2+Ũ�����ӵ�һ���̶�ʱ��������������������������ã����������������ʽ��͡� �DZ���ϸ������������֮һ��
�DZ���ϸ������������֮һ�� �Ĵ�С������ϸ���������Ե��������ԵĴ�С�ɷ��ȣ������������ʴ����ֵʱ��
�Ĵ�С������ϸ���������Ե��������ԵĴ�С�ɷ��ȣ������������ʴ����ֵʱ�� �����ֵ����ʱϸ����Fe2+��������ǿ��������ϸ�����ʺ��������ۺ϶���ѧ������*��
�����ֵ����ʱϸ����Fe2+��������ǿ��������ϸ�����ʺ��������ۺ϶���ѧ������*�� �ı仯���ɿɼ���������������ϵ��Fe2+10.0 g/L��ϸ������������Ũ�ȡ�
�ı仯���ɿɼ���������������ϵ��Fe2+10.0 g/L��ϸ������������Ũ�ȡ�

ͼ2 ��ͬ��ʼFe2+Ũ��������������˾�����������
Fig. 2 Growth curves of T. f at different initial Fe2+ concentrations
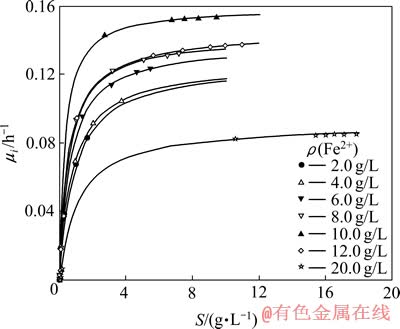
ͼ3 ��ͬ��ʼFe2+Ũ����tiʱ��Fe2+Ũ�����i�Ĺ�ϵ
Fig. 3 Relationship between Fe2+concentration and ��i at different initial Fe2+concentrations
2.3 Fe2+Ũ�ȶ�Fe2+�������ʵ�Ӱ��
ͼ4(a)��ʾΪFe3+Ũ����ʱ��ı仯���ߣ��������������Fe3+�IJ�����ʱ���������أ�������ʽ(6)[18]�ɵ�Fe2+����������(����2)��Fe2+������������ʱ��ı仯������ͼ4(b)��ʾ��

ͼ4 ��ͬ��ʼFe2+Ũ����Fe3+������Fe2+����������ʱ��ı仯
Fig. 4 Variations in Fe3+ production and Fe2+ oxidation rate with time at different initial Fe2+concentrations
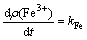 (6)
(6)
�ɱ�2��ͼ4(b)��֪��Fe2+����������kFe��Fe2+Ũ�ȵ����Ӷ����ӣ���Fe2+������������Fe2+Ũ�ȵ����ӳ��������Ե��ӳ��ڡ�������Ϊ��Fe2+Ũ�Ƚϵ�ʱ����������ں������ܵ���Ũ�ȵ����ƣ�Fe2+��������ƫ�ͣ���Fe2+Ũ�����ߵ�һ���̶Ⱥ�������������˾������������������ã�����������˾���Ҫ��������Ӧ�ڣ�����ӳ�������������������ں�Fe2+�������ʽϸߡ���ΪFe2+��������������ͬ�������ԣ�Fe2+�������ӳ����ܷ�ӳ���������״�����ɼ������������˹������ʵ����Fe2+Ũ������������������˾���������������ϵ��Fe3+Ũ������Fe2+Ũ�ȵ����Ӷ����ӣ�����Fe3+����Ч�����ؽ����Ľ�������Fe3+���������ڵ�pHʱ����ˮ�⣬���ɻ���������(MFe3(SO4)2(OH)6��M=K+��Na+��NH4+��)�����ڳ����谭�������Fe3+������н��������ֱ�ӽӴ�������������������Ч�ʣ�������������ϵ�������ؽ������Ӳ��������������͵������ؽ�����ȥ���ʡ���ˣ��������˹������轫Fe2+Ũ�ȿ����ں��ʷ�Χ�ڡ�
��2 ��ͬ��ʼFe2+Ũ����Fe2+����������
Table 2 Variation of Fe2+ oxidation rate at different initial Fe2+concentrations

2.4 Fe2+Ũ�ȶ��ؽ����ܳ��ʵ�Ӱ��
�ؽ������ܳ����ʿ��ɾ��鷽��[19]��ʾ��
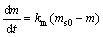 (7)
(7)
ʽ�У�kmΪ�ؽ����ܳ������ʳ���(h-1)��ms0Ϊԭ�������ؽ���������(mg)��mΪ��ʱ��Һ�����ؽ����IJ�ͬ��ʼ����(mg)��tΪʱ��(h)��
��ͬ��ʼFe2+Ũ�����ؽ������ܳ�����ͼ5��ʾ������ͼ5���ݣ�����ʽ(7)�õ���ͬ����Ũ�����ؽ����ܳ������ʳ���km(����3)��
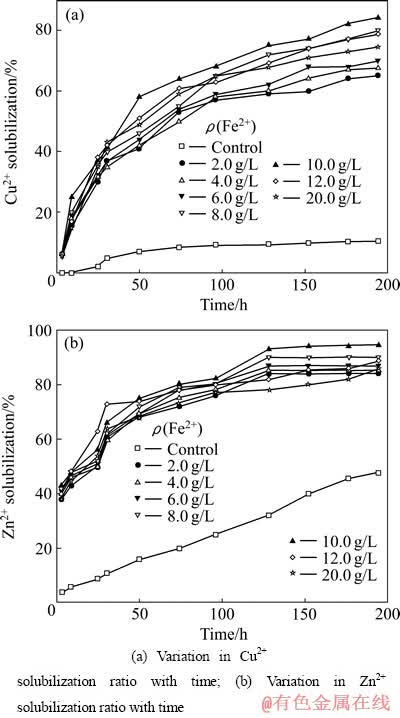
ͼ5 ��ͬ��ʼFe2+Ũ�����ؽ������ܳ���
Fig. 5 Heavy metal solubilization ratio from sediment at different initial Fe2+ concentrations
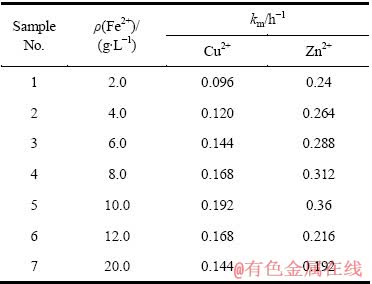
��3 ��ͬ��ʼFe2+Ũ�����ؽ����ܳ������ʳ���
Table 3 Rate constants of heavy metal solubilization at various concentrations of initial Fe2+
��4 ��������ǰ��������ؽ�������̬�ĺ���
Table 4 Contents of different forms of heavy metal in sediment before and after bioleaching

��5 �ؽ����ܳ������ʳ�����Fe2+Ũ�ȵĹ�ϵ
Table 5 Relationship between rate constant of heavy metal solubilization and initial Fe2+concentration

�ɱ�3֪����ͬһ����Ũ���£�������Zn2+�ܳ������ʳ���km��������Cu2+�ģ�˵��Zn2+��Cu2+�����ܳ���������Ϊԭ������Zn2+�Ĵ������ȡ̬(F1)�Ϳɻ�ԭ��ȡ̬(F2)�ĺ�����������Cu2+��(����4)����������̬�����ܳ�������������ȡ̬(F3)������̬(F4)��ֱ���ǿ�����Լ�ǿ��������²����ܳ��������ȶ�̬��Ҫ�������ȶ�̬���ؽ����ܳ���Ҫ���͵�pH���ߵ�ORP�����ŵ���Ũ�ȵ����ӣ�km����С����Ȼ�����ɴ��С����Fe2+Ũ��С��10.0 g/Lʱ��Cu2+��Zn2+��km��Fe2+Ũ�ȳ��������(����5)�����Է��̵�б����һ���̶��Ϸ�ӳ��Fe2+Ũ�ȶ��ؽ����ܳ��ʵ�Ӱ�졣��Cu2+��Zn2+��km���Է��̿ɼ���Fe2+Ũ�ȶ�Zn2+�ܳ��ʵ�Ӱ���Դ���Cu2+��Fe2+Ũ�ȴ���10.0 g/L��Cu2+��Zn2+��km�½�����ԭ��Ϊ����Ũ�ȹ��߶�����������������ã���ʱ����Ե���������½���������������ʽ��ͣ���������ؽ����ܳ����ʵ��½����������˺�����е�Cu��Ҫ�Բ���̬����ʽ���ڣ�Zn�Ĵ������ȡ̬�������ͣ�������̬�������ӣ��������˺�������ؽ�����������������Խ��͡������Ϸ����ɼ����ʵ����ӵ���Fe2+Ũ�ȿ�����ߵ������ؽ������ܳ����ʣ�������������˾���ֳ��������������ͣ��ʱ�䳤����������ģӦ�õ���Ҫ���ء�����跨ǿ��������ϵ���Ķ�ЧӦ��ʹ������治�ϸ��£�����������ϵ�е���ɢ�������ʣ��ٽ���������˾��Ե���Fe2+�����ã���Ҳ������ؽ����ܳ�Ч�ʵ���Ч;����
3 ����
1) ����Monod�����о��˲�ͬFe2+Ũ�������������Ķ���ѧ������Fe2+Ũ��Ϊ10.0 g/Lʱ������������˾��������������ʺͱ��ͳ����ֱ�����ֵ����Сֵ��˵������������������״����ѡ�
2) ��Fe2+Ũ�ȵ����ӣ�Fe2+����������kFe���ӣ���Fe2+����������Fe2+Ũ�ȵ����ӳ������Ե��ӳ��ڣ�������ΪFe2+Ũ�����ߵ�һ���̶Ⱥ�������������˾����������������ã�����������˾���Ҫ��������Ӧ�ڡ�
3) �ڵ���Fe2+Ũ��Ϊ2.0~10.0 g/Lʱ��Zn2+�ܽ����ʳ���km������Cu2+�ģ�����Zn2+�ڵ����еĴ�����̬�йء�Fe2+Ũ��С��10.0 g/Lʱ��Fe2+Ũ����Cu2+��Zn2+���ܽ����ʳ���km��ֱ����ء�
REFERENCES
[1] ZHU H N, YUAN X Z, ZENG G M, JIANG M, LIANG J, ZHANG C, YIN J, HUANG H J, LIU Z F, JIANG H W. Ecological risk assessment of heavy metals in sediments of Xiawan Port based on modified potential ecological risk index[J]. Transactions of Nonferrous Metals Society of China, 2012, 22(6): 1470-1477.
[2] ����, ������. �������˷�����ˮ�������ؽ���ȥ��Ч���о�[J]. ̫ԭ������ѧѧ��, 2011, 42(4): 383-386.
CUI Jia-li, WANG Zeng-zhang. Removal of heavy metals in urban sewage sludg by bioleaching[J]. Journal of Taiyuan University of Technology, 2011, 42(4): 383-386.
[3] PATHAK A, DASTIDAR M G, SREEKRISHNAN T R. Bioleaching of heavy metals from sewage sludge: A review[J]. Journal of Environmental Management, 2009, 90(8): 2343-2353.
[4] BAYAT B, SARI B. Comparative evaluation of microbial and chemical leaching processes for heavy metal removal from dewatered metal plating sludge[J]. Journal of Hazardous Materials, 2010, 174(1/3): 763-769.
[5] ASHISH P, DASTIDARA M G, SREEKRISHNAN T R. Bioleaching of heavy metals from sewage sludge by indigenous iron-oxidizing microorganisms using ammonium ferrous sulfate and ferrous sulfate as energy sources: A comparative study[J]. Journal of Hazardous Materials, 2009, 171(1/3): 273-278.
[6] WANG Q H, YANG J, WANG Q, WU T J. Effects of water-washing pretreatment on bioleaching of heavy metals from municipal solid waste incinerator fly ash[J]. Journal of Hazardous Materials, 2009, 162(2/3): 812-818.
[7] REN W X, LI P J, ZHENG L, FAN S X, VERHOZINA V A. Effects of dissolved low molecular weight organic acids on oxidation of ferrous iron by acidithiobacillus ferrooxidans[J]. Journal of Hazardous Materials, 2009, 162(1): 17-22.
[8] CHEN S Y, LIN J G. Enhancement of metal bioleaching from contaminated sediment using silver ion[J]. Journal of Hazardous Materials, 2009, 161(2/3): 893-899.
[9] ��ռƽ, �ž���. ��������ȥ��ũ���������ؽ�����Ч��������[J]. ũҵ����ѧ��, 2009, 25(2): 177-182.
CAO Zhan-ping, ZHANG Jing-li. Removal and process of heavy metals in sludge by microbiological leaching for agricultural use[J]. Transactions of the Chinese Society of Agricultural Engineering, 2009, 25(2): 177-182.
[10] ̷����, Ԭ����, ������, ��÷��, �� ��, �� ��. ˿״������������ȥ���������ؽ����Ĵٽ�����[J]. ��������ѧ��, 2010, 4(12): 2853-2859.
TAN Xian-yi, YUAN Xing-zhong, ZENG Guang-ming, ZHOU Mei-fang, JIANG Min, LI Peng. Promotion effect of filamentous bacteria on removal of heavy metals during bioleaching from contaminated sediment[J]. Chinese Journal of Environmental Engineering, 2010, 4(12): 2853-2859.
[11] ��ͥ��, ��Ⱥ��, �� ��, ����־. ������Ӧ�淨�Ż��������˷ɻҴ����������о�[J]. �й�������ѧ, 2009, 29(7): 738-744.
WU Ting-ji, WANG Qun-hui, YANG Jie, MA Hong-zhi. Optimization on bioleaching factors of municipal solid waste incineration fly ash using response surface methodology[J]. China Environmental Science, 2009, 29(7): 738-744.
[12] ����Ƽ, �� ��, �� ��, �� ��, �� ��, ף����, �� ΰ. ���������ؽ�����̬���������о���չ[J].��ѧ��������, 2006, 15(4): 72-74.
FENG Su-ping, JU Li, SHEN Yong, QIU Na, LI Xin, ZHU Pei-ming, WANG Wei. Study on sepciation analysis method of heavy metal in sediments[J]. Chemical Analysis and Meterage, 2006, 15(4): 72-74.
[13] MIN X B, XIE X D, CHAI L Y, LIANG Y J, LI M, KE Y. Environmental availability and ecological risk assessment of heavy metals in zinc leaching residue[J]. Transactions of Nonferrous Metals Society of China, 2013, 23(1): 208-218.
[14] TYAGI R D, COUILLARD D, TRAN F. Heavy metals removal from anaerobically digested sludge by chemical and microbiological methods[J]. Environmental Pollution, 1988, 50(4): 295-316.
[15] ������, �� ��, ��˳��, ����վ, ����÷. ������������˾�ȥ���Ƹ������и����о�[J]. ������ѧ, 2004, 25(1): 62-66.
ZHOU Li-xiang, FANG Di, ZHOU Shun-gui, WANG Dian-zhan, WANG Shi-mei. Removal of Cr from tannery sludge by Acidophilic Thiobacilli[J]. Environmental Science, 2004, 25(1): 62-66.
[16] CHARTIER M, COUILLARD D. Biological processes: The effects of initial pH, percentage inoculum and nutrient enrichment on the solubilization of sediment bound metals[J]. Water Air and Soil Pollution, 1997, 96(1/4): 249-267.
[17] CABRERA G, GOMEZ J M, CANTERO D. Kinetic study of ferrous sulphate oxidation of Acidithiobacillus ferrooxidans in the presence of heavy metal ions[J]. Enzyme and Microbial Technology, 2005, 36(2/3): 301-306.
[18] ISHIGAKI T, NAKANISHI A, TATEDA M, IKE M, FUJITA M. Bioleaching of metal from municipal waste incineration fly ash using a mixed culture of sulfur-oxidizing and iron-oxidizing bacteria[J]. Chemosphere, 2005, 60(8): 1087-1094.
[19] CHEN S Y, LIN J G. Effect of substrate concentration on bioleaching of metal-contaminated sediment[J]. Journal of Hazardous Materials, 2001, 82(1): 77-89.
(�༭ ������)
������Ŀ��������Ȼ��ѧ����������Ŀ(51079049)
�ո����ڣ�2013-05-10�������ڣ�2013-12-25
ͨ�����ߣ��� ӱ�����ڣ��绰��13912963190��E-mail: xyhohai@163.com