DOI:10.19476/j.ysxb.1004.0609.2018.12.19
NH3-NH4Cl-H2O体系低品位硫化铜矿氧化浸出-脉冲电积工艺
李树超,杨建广,陈 冰, 丁 龙,南天翔
(中南大学 冶金与环境学院,长沙 410083)
摘 要:采用单因素试验法,研究某低品位硫化铜精矿(Cu 7.42%(质量分数))在NH3-NH4Cl-H2O体系中的氧化浸出行为。结果表明:在液固比 4:1、[NH3・H2O]=1 mol/L、[NH4Cl]=3 mol/L、氧化剂过量系数1.4、原料粒度94~124 μm、浸出时间2 h、温度30℃的条件下,该低品位硫化铜矿浸出率98.89%;并在此基础上开展了从该低品位硫化铜精矿铜氨浸出液中直接脉冲电积铜的工艺优化试验。结果表明:在[NH4Cl]=3 mol/L、[NH3・H2O]=1.5 mol/L、[Cu2+]=20 g/L、明胶0.06 g/L、硫脲0.05 g/L、脉冲电流密度600 A/m2、占空比90%的条件下,可以获得平整光滑且有金属光泽的阴极铜,阴极电流效率87.97%。阴极铜XRD分析结果表明:氨-氯化铵体系中脉冲电积铜晶体主要沿(220)晶面生长,其余晶面未见明显反射峰,表现出类单晶结构。SEM分析显示:该阴极铜表面光滑致密且无瘤状物产生,铜在阴极表面的生长方式呈与阴极面垂直的一维方向生长。
关键词:低品位硫化铜精矿;氨性氧化浸出;脉冲电积
文章编号:1004-0609(2018)-12-2558-10 中图分类号:TF811 文献标志码:A
我国是世界重要的铜冶炼生产国之一,但我国铜冶炼原料大部分依赖进口,原料对外依存度超过80%。随着铜矿资源的过度开采,国内外高品位铜矿资源日益减少,从各类低品位、复杂多金属伴生硫化铜矿及硫氧混合铜矿中高效提铜已成为目前铜提取冶金的重要发展方向[1-2],本领域研究人员就此开展了诸多研究。
张振健[3]针对东川汤丹铜精矿,研究了“焙烧-氨浸-萃取-电积”提铜工艺,采用氨-硫酸铵体系浸出铜。在最优浸出条件下,铜浸出率92%以上,且萃取后的富铜液符合电积要求;刘维[4]采用Me(Ⅱ)-NH4Cl-NH3-H2O(MACA)浸出体系处理高碱性脉石氧化铜精矿,建立了各氧化铜矿相在该体系中溶解的热力学模型,并对Cu-En-NH4Cl-NH3-H2O体系直接电积铜工艺进行了探索性研究,发现各因素对电流效率和槽电压的影响规律较为复杂:由于亚铜离子的影响,其直接电积的电流效率一般低于80%;铜离子浓度过高或过低也会使电流效率发生大幅下降。针对难选含硫化物的低品位氧化铜矿,刘志雄等[2]以过硫酸铵为氧化剂,采用氨-硫酸铵体系浸出铜,研究了氨/硫酸铵浓度、粒度等因素对铜浸出率的影响规律。在优化条件下,铜浸出率达87.7%。于霞等[5]采用氨-硫酸铵体系浸出铜锌精矿焙砂及浸出液直接电积生成铜板,在最优化条件下,电积过程的电流效率85.66%;并指出电流效率低的主要原因是在阴极表面还原生成的Cu(NH3)2+经溶液扩散作用扩散至阳极表面发生氧化反应:
Cu(NH3)42++Cu=2Cu(NH3)2+ (1)
Cu(NH3)2++2NH3-e=Cu(NH3)42+ (2)
诸多研究结果表明,在处理高碱性脉石成分铜矿时,氨浸工艺比酸浸工艺具有更高的选择性且其试剂消耗量更少[6]。在氨法浸出过程中有价金属铜与氨发生络合反应形成铜氨络合物从而与脉石组分相分离,而其他金属杂质如铁、砷等则不与氨发生络合反应。另外,添加(NH4)2CO3、乙二胺等与氨形成缓冲体系,可以维持浸出液中的游离氨在较高浓度,减少氨的挥发,维持浸出液的pH值稳定在较高范围内,有利于浸出过程的进行[7]。氨性氧化提铜率通常可以达到90%以上。目前研究的焦点主要集中在如何从浓度相对较低的铜氨([Cu2+]<20 g/L)溶液中直接电积获得高质量的阴极铜,并克服铜氨溶液直接电积时溶液中因溶液扩散作用引起Cu(NH3)42+  Cu(NH3)2++2NH3+e的循环,获得较高的电流效率。在前期研究的基础上,本研究以云南某低品位复杂硫化铜精矿为研究对象,采用氨-氯化铵体系对原料中有价金属铜进行选择性浸出,之后以脉冲电积法从浸出液中直接电积铜,以实现从低品位复杂硫化铜精矿中高效提铜的目的。本文主要介绍该过程工艺条件优化试验内容。
Cu(NH3)2++2NH3+e的循环,获得较高的电流效率。在前期研究的基础上,本研究以云南某低品位复杂硫化铜精矿为研究对象,采用氨-氯化铵体系对原料中有价金属铜进行选择性浸出,之后以脉冲电积法从浸出液中直接电积铜,以实现从低品位复杂硫化铜精矿中高效提铜的目的。本文主要介绍该过程工艺条件优化试验内容。
1 实验
1.1 试验原料
试验所用低品位复杂硫化铜精矿原料由云南某公司提供。该铜矿的主要化学组成分析和化学物相分析如表1和2所示,其中铜的化学物相由长沙矿冶研究院公司分析检测中心分析。
表1 低品位铜精矿的主要化学组成
Table 1 main chemical compositions of low grade copper sulfide concentrate (mass fraction, %)

表2 铜精矿中铜的化学物相分布
Table 2 Copper occurences in copper sulfide concentrate

由表1可知,该铜精矿属于低品位铜矿,铜矿中铁和硫的含量分别为31.31%和39.92%,铜含量为7.42%。由表2可知,总铜中次生硫化铜的含量最高,占总铜的83.06%,另外还含有少量的自由氧化铜、结合氧化铜和原生硫化铜。综上所述可知,该原料为低品位硫化铜矿,主要脉石成分为黄铁矿,难以采用现行铜火法熔炼工艺处理。
1.2 工艺流程
本研究采用的“氨性氧化浸出-脉冲电积”低品位硫化铜精矿处理工艺流程示意图如图1所示。
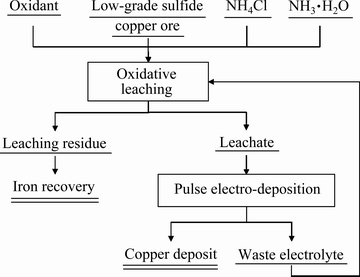
图1 低品位硫化铜矿“氨性氧化浸出-脉冲电积”工艺流程示意图
Fig. 1 Schematic flowchart of low grade copper sulfide concentrate “oxidative ammonia leaching-pulse electro- deposition” process
1.3 试验方法
1.3.1 氨性氧化浸出试验
配制一定浓度的氨-氯化铵溶液于锥形瓶中,在恒温水浴锅中加热至一定温度并调节转速。待温度达到设定值,称量一定量的铜精矿原料加入至锥形瓶中;开始记录时间并每间隔一定时间加入一定量漂白粉进行氧化浸出,定义漂白粉加入量与氧化铜精矿中全部CuS所需漂白粉理论量的比值为氧化剂过量系数。浸出完毕后抽滤分离固液,所得滤液用碘量法滴定其中铜的浓度;所得滤渣在烘干箱中烘干8 h,留作金属平衡分析。浸出条件试验规模铜粗矿原料每次50 g,综合条件试验铜精矿原料每次100 g。
1.3.2 铜氨溶液脉冲电积试验
在浸出液中配入一定浓度的氨-氯化铵以调整溶液中氨-氯化铵至适当浓度。加入一定量的明胶和硫脲及配位剂乙二胺,在恒温水浴锅中加热至一定温度并调节转速。待温度达到设定值,以石墨为阳极,不锈钢(301)为阴极,极距4 cm,脉冲直流电源作为电源,进行铜电积实验。实验完毕后,分别用低浓度氨水、蒸馏水冲洗阴极铜片,并在烘干箱中烘干30 min,并根据实验前后阴极的质量差计算阴极电流效率。
2 结果与讨论
2.1 实验原理
2.1.1 氨性氧化浸出原理
在氨性氧化浸出硫化铜矿过程中[2],铜精矿中的硫元素最终被氧化为SO42+。漂白粉中的次氯酸钙在溶液中会和液相中或者空气中的CO2反应,生成具有强氧化性的次氯酸;次氯酸不稳定,易分解而产生活性[O]。其反应方程式如下:
Ca(ClO)2+CO2+H2O=CaCO3+2HClO (3)
2HClO=2HCl+O2 (4)
在氨-氯化铵体系中,次氯酸钙以ClO-形式参与反应,则铜精矿的氨性氧化浸出反应方程式:
2Cu5FeS4+37ClO-+36NH3+H2O+4NH4Cl=10Cu(NH3)42++2Fe(OH)3+8SO42-+41Cl- (5)
2.1.2 脉冲电积原理
在传统直流电积过程中,电沉积速度一般较低,主要是由于在扩散控制下阴极表面的金属离子被还原,而周围的离子不能得到及时的补充,阴极与电解液界面存在一个较厚的扩散层。在直流电沉积下,如果电流密度过高时,不仅不能提高金属离子的电沉积速度,反而会产生一些不利影响,如阴极氢气析出量的增加,金属材料出现氢脆现象,电流效率降低,镀层表面起泡、结晶变得粗糙或产生树枝状形貌,严重时会使镀层烧焦等。研究发现,采用脉冲电沉积,有利于减小电积过程中浓差极化,减小离子扩散层对阴极电流效率的影响,提高电流密度,提高金属的沉积速率。其原理主要是利用脉冲电压或脉冲电流的张弛(间隙工作),增强阴极表面镀液的活性极化,降低阴极表面镀液的浓差极化,从而有效地改善电沉积层的外观质量和其物理化学特性,其电流效率也相对更高[8]。
本研究引入脉冲电沉积技术对浸出液电沉积铜,以实现从低浓度铜氨溶液中直接电积提铜。在Cu(Ⅱ)-En-NH3-NH4Cl-H2O脉冲电沉积体系中,Cu2+和Cu+的存在形态可能为Cu(NH3)42+、Cu(En)+、Cu(En)22+等。阴极可能的反应[9-11]为
Cu(En)22++e=Cu(En)++En (6)
Cu(NH3)42++e=Cu(NH3)2++NH3 (7)
Cu(En)++e=Cu+En (8)
阳极反应为析氮反应[11-12]:
8NH3-6e=N2↑+6NH4+ (9)
2.2 氨性氧化浸出试验
2.2.1 氨水用量和液固比对铜浸出率的影响
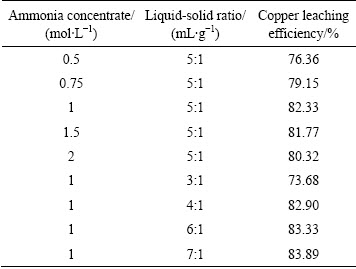
在氯化铵4 mol/L、氧化剂过量系数1、原料粒度124~250 μm、浸出时间2 h、温度30 ℃条件下,考察不同氨水摩尔浓度和液固比对铜浸出率的影响,试验结果如表3所示。
试验结果表明,氨水摩尔浓度从0.5 mol/L增加至1 mol/L时,铜浸出率由76.36%升高至82.33%;继续增加氨水摩尔浓度至2 mol/L后,铜浸出率稳定在82%左右。SABAH等[13]曾在研究从铜蚀刻液中回收氯化铜时发现,铜氨溶液中铜离子以平面四方结构Cu(NH3)4(OH)2的形式存在,理论上全部形成该络合物时所需氨水摩尔浓度为0.92 mol/L。本研究试验结果与该研究结论大致吻合。因此,后续试验确定氨水摩尔浓度为1 mol/L。
由表3可知,随着液固比由3:1增加到4:1后,铜浸出率有一定程度增加;但液固比继续增大到7:1后,铜浸出率无明显增加。且由于高液固比导致浸出液体积增大,溶液中铜浓度降低,不利于后续电积回收,因此,本研究选择液固比为4:1作为最佳条件进行后续试验。
表3 氨水浓度和液固比对铜浸出率的影响
Table 3 influence of ammonia concentrate and liquid-solid ratio on copper leaching efficiency
2.2.2 氯化铵浓度和氧化剂过量系数对铜浸出率的影响
在液固比为4:1、[NH3・H2O]=1 mol/L、原料粒度0.124~0.25 mm、浸出时间2 h、温度30℃条件下,考察不同氯化铵浓度和氧化剂过量系数对铜浸出率的影响,试验结果如表4所示。
表4 氯化铵浓度和氧化剂过量系数对铜浸出率的影响
Table 4 influence of ammonium chloride concentration and stoichiometric oxidant dosage on copper leaching efficiency
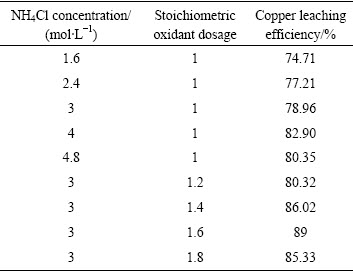
由表4可知,随着氯化铵浓度由1.6 mol/L增加到4.8 mol/L,铜浸出率从74.71%增加至80.35%。姚雅伟[14]在研究从PCB污泥中浸析铜时曾发现,在氨浸过程中,氨水浓度对铜浸出率的影响程度比铵盐的更大。溶液中氯化铵可与氨形成缓冲体系,维持溶液中的游离氨在较高浓度范围内从而减少氨的挥发;但氯化铵浓度的增加对于提高铜浸出率的作用不明显。综上考虑可得,本研究选择氯化铵浓度为3 mol/L作为最佳条件。
由表4可知,随着氧化剂过量系数由1逐渐增加至1.4,铜浸出率由78.96%增加至86.02%;当氧化剂过量系数由1.4增加至1.8时,铜浸出率的升高趋势不大。可见,本研究中氧化剂(漂白粉)的加入量对铜浸出率的影响至为重要,这是由于原料中硫化铜占总铜质量的88.52%,在无氧化剂时原料中的硫化铜难以被氧化溶解浸出,但氧化剂(漂白粉)用量增加时,渣量也随之上升。综合各因素可知,本研究中选择氧化剂过量系数为1.4。
2.2.3 原料粒度和浸出时间对铜浸出率的影响
在液固比为4:1、[NH3・H2O]=1 mol/L、氯化铵3 mol/L、氧化剂过量系数1.4、温度30 ℃条件下,考察不同原料粒度和浸出时间对铜浸出率的影响,试验结果如表5所示。
表5 原料粒度和浸出时间对铜浸出率的影响
Table 5 influence of particle size and contact time on copper leaching efficiency
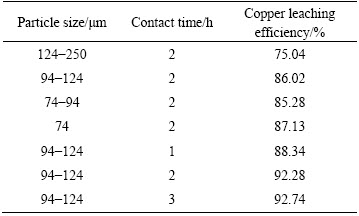
由表5可知,随着铜精矿粒度由124~250 μm减少至94~124 μm,铜浸出率显著增加;但继续减少原料粒度,铜浸出率增长趋势不明显。且粒度越细,对应的球磨能耗越高,综合考虑,本研究选择原料粒度为94~124 μm作为最佳粒度条件。
由表5可知,在浸出时间为2 h时,铜精矿中已有92.28%铜溶解浸出。延长浸出时间,铜浸出率的增长趋势不大;且随着浸出时间的延长,氨水的挥发量增加,不利于浸出反应的进行。因此,本研究选择2 h为最佳浸出时间条件。
综上所述可得,氨性氧化浸出低品位硫化铜矿的最佳工艺条件:液固比(L/S)=4:1、[NH3・H2O]=1 mol/L、氯化铵3 mol/L、氧化剂过量系数1.4、原料粒度124~250 μm、浸出时间2 h、温度30 ℃。
2.2.4 综合条件试验
在上述优化条件下,开展了氨性氧化浸出低品位硫化铜矿综合条件试验及循环浸出试验,结果如下表6和7所示。
表6 综合试验及循环浸出试验结果
Table 6 results of confirmed experiments and circulating leaching experiments

表7 循环浸出试验浸出液的主要化学成分
Table 7 Main chemical contents of leachate in circulating leaching experiment (g/L)

经过2次综合条件验证试验,得到氨性体系氧化浸出低品位硫化铜矿中铜的浸出率分别为91.36%和92.19%;经循环浸出3次后,浸出液中铜浓度可富集到16.57 g/L,杂质Pb浓度0.01 g/L,此时铜浸出率可达到98.89%。
2.3 脉冲电积试验
以上述浸出液为电解液,开展了浸出液直接脉冲电积条件优化试验。分别研究了添加剂明胶、硫脲、乙二胺浓度、脉冲电流密度、氯化铵浓度、氨水浓度、占空比、铜离子浓度等因素对阴极铜形貌及电流效率的影响规律。试验中通过加入氨-氯化铵溶液、氧化铜等调整溶液中铜离子浓度。
2.3.1 添加剂明胶、硫脲浓度的影响
在电流密度400 A/m2、脉冲电源占空比80%、氯化铵4 mol/L、[NH3・H2O]=1.0 mol/L、乙二胺0.4 mol/L、 [Cu2+]=20 g/L条件下,考察添加剂明胶和硫脲浓度对阴极电流效率和阴极电积铜形貌的影响规律。试验结果如图2和3所示。
由图2(a)可知,随着明胶浓度由0.02 g/L升高至0.06 g/L,阴极电流效率略有增加;但继续提高明胶浓度,电流效率略微下降。明胶浓度从0.02 g/L增加至0.04 g/L时,槽电压升高至最大值,约2.55 V;之后,随着明胶浓度的继续增加,槽电压小幅度下降。由图3(a1)~(a4)可以看出,随着明胶浓度的改变,阴极铜表面的条纹没有明显改善。综上所述可知,明胶在氨性体系电积铜中对阴极铜的形貌和阴极电流效率无明显影响。选择明胶浓度为0.06 g/L作为最佳明胶浓度。
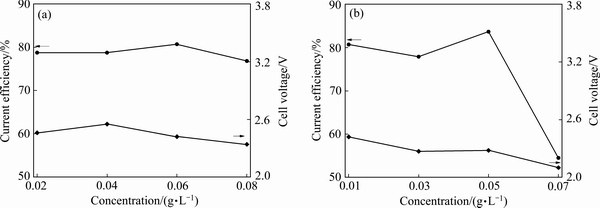
图2 明胶和硫脲浓度对阴极电流效率和槽电压的影响
Fig. 2 influence of gelatin(a) and thiourea(b) concentrations on cathode efficiency and cell voltage
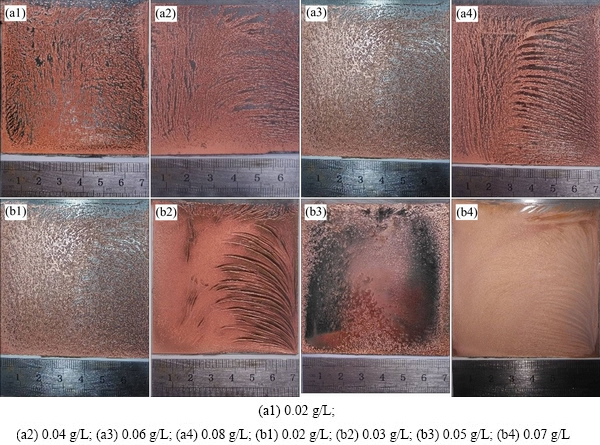
图3 不同明胶和硫脲浓度下阴极铜的形貌
Fig. 3 Surface morphologies of cathode copper at different gelatin((a1)-(a4)) and thiourea((b1)-(b4)) concentrations
由图2(b)可知,随着硫脲浓度由0.01 g/L升高至0.07 g/L,槽电压由2.42 V逐渐下降至2.9 V;而阴极电流效率在硫脲浓度增至0.05 g/L时,达到最大值,之后迅速下降。由图3(b1)~(b4)可看出,随着硫脲浓度的增加,阴极铜的形貌得到明显改善:在硫脲浓度为0.07 g/L时,阴极表面沉积物分散,较为平整;但在此浓度下,阴极电流效率大幅下滑。综上所述可知,硫脲在氨性体系电积铜中对阴极铜的形貌影响较大,在电解液中添加适量浓度的硫脲添加剂可以明显改善阴极铜表面的条纹缺陷,使阴极沉积物趋于平整。选择硫脲浓度0.07 g/L为最佳硫脲浓度。
2.3.2 配位剂乙二胺的影响
在电流密度400 A/m2、脉冲电源占空比80%、氯化铵4 mol/L、[NH3・H2O]=1.0 mol/L、[Cu2+]=20 g/L、明胶0.06g/L、硫脲0.05 g/L条件下,考察乙二胺浓度对阴极电流效率和阴极电积铜形貌的影响规律。试验结果如图4和5所示。
文献[11]中报道称,Cu(NH2(CH2)2NH2)22+配合物[Cu(NH3)42+配合物的结构更稳定且有很大的极化值,使得铜配合物分解趋势减小,可有效抑制一价铜配合物的形成[11],因而对于阴极电流效率和阴极铜形貌具有很大影响。由图4可知,乙二胺浓度对于阴极电流效率的影响较为复杂,浓度太高或者太低都不利于阴极效率的提高;在乙二胺摩尔浓度为0.4 mol/L时,阴极电流效率达到最高值,为79.27%。另外,乙二胺配位剂对于槽电压的影响微小。由图5可以看出,随着乙二胺浓度增加,阴极铜表面更加细致光亮;在乙二胺浓度为0.6 mol/L时,阴极可以得到较为平整且光滑的铜沉积物。综上所述可知,选择乙二胺浓度为0.4 mol/L进行后续实验。
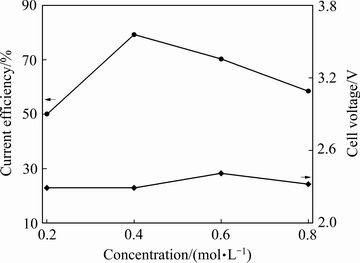
图4 乙二胺对阴极电流效率和槽电压的影响
Fig. 4 influence of ethylenediamine concentration on cathode efficiency and cell voltage
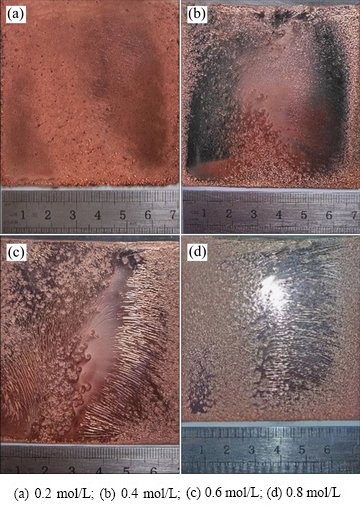
图5 不同乙二胺浓度下阴极铜的形貌
Fig. 5 Surface morphologies of cathode copper at different ethylenediamine concentrations
2.3.3 脉冲电流密度的影响
在脉冲电源占空比80%、氯化铵4 mol/L、[NH3・H2O]=1.0 mol/L、[Cu2+]=20 g/L、明胶0.06 g/L、硫脲0.05 g/L、乙二胺0.4 mol/L条件下,考察对阴极脉冲电流密度阴极电流效率和阴极电积铜形貌的影响规律,试验结果如图6所示。
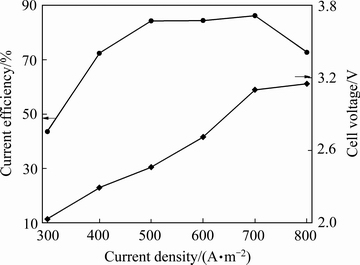
图6 脉冲电流密度对阴极电流效率和槽电压的影响
Fig. 6 influence of pulse current density on cathode current efficiency and cell voltage
由图6可知,随着阴极脉冲电流密度从300 A/m2增加至500 A/ m2,阴极电流效率迅速升高;阴极电流密度增加至700 A/ m2时,阴极电流效率逐渐增加至86.17%,但增加趋势减缓;阴极电流密度继续增加时,阴极电流效率呈下降趋势。但由于电流密度过大时槽电压过高,电积副反应效应增大。本研究选择阴极脉冲电流密度600 A/m2进行后续实验。
2.3.4 氯化铵和氨水的影响
在电流密度600 A/m2、脉冲电源占空比80%、[Cu2+]=20 g/L、明胶0.06 g/L、硫脲0.05 g/L、乙二胺0.4 mol/L条件下,考察对氯化铵和氨水浓度对阴极电流效率和阴极电积铜形貌的影响规律,试验结果如图7所示。
由图7(a)可知,随着氯化铵浓度升高,槽电压逐渐减小至2.70 V左右并不再变化,阴极电流效率逐渐升高。氯化铵浓度的增加使得导电离子增加,电解液的电导率也随之升高,因而槽电压呈下降趋势。氯化铵可以与氨水形成缓冲体系,维持电解液的稳定性,因而阴极电流效率也有一定程度的增加。
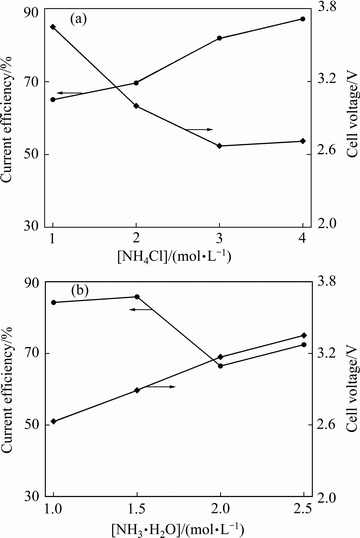
图7 氨水浓度对阴极电流效率和槽电压的影响
Fig. 7 influence of concentration of ammonium hydroxide on cathode efficiency and cell voltage
由图7(b)可知,随着氨水浓度由1.0 mol/L增加至1.5 mol/L时,阴极电流效率没有变化;但继续增加氨水浓度(>1.5 mol/L)时,阴极电流效率下降。随着氨水浓度由1.0 mol/L升高至2.5 mol/L,槽电压呈线性增长趋势。
综上所述可知,选择氯化铵浓度3 mol/L、氨水浓度1.5 mol/L为最佳条件进行后续试验。
2.3.5 占空比和二价铜浓度的影响
在电流密度600 A/m2、氯化铵3 mol/L、[NH3・H2O]=1.5 mol/L、明胶0.06 g/L、硫脲0.05 g/L、乙二胺0.4 mol/L条件下,考察脉冲占空比和二价铜离子浓度对阴极电流效率和阴极电积铜形貌的影响规律。试验结果如图8所示。
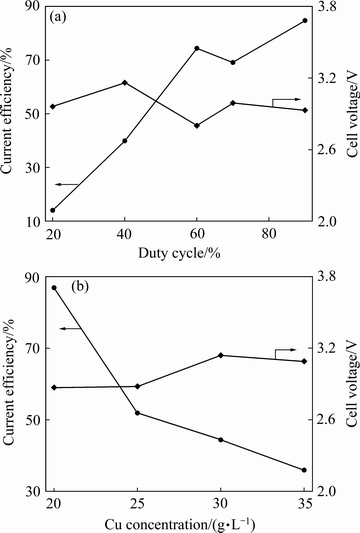
图8 占空比和铜离子浓度对阴极电流效率和槽电压的影响
Fig. 8 influence of duty cycle(a) and Cu2+ concentration(b) on cathode efficiency and cell voltage
由图8(a)可知,随着占空比由20%增加至90%时,阴极电流效率呈升高趋势;占空比由20%增加至60%时,阴极电流效率增加趋势较大,之后,增加趋势减缓。占空比增加至60%时,阴极铜表面条纹显著减少,阴极铜表面光滑致密且有金属光泽。
由图8(b)可知,随着阴极铜浓度由20 g/L增加至35 g/L,阴极电流效率降低趋势明显。这是由于电解液中二价铜离子浓度的升高加剧了阴极铜的反溶反应,使得阴极已沉积的铜又与溶液中Cu2+反应进入溶液。本研究选择占空比90%、铜浓度20 g/L为最佳条件。
2.3.6 综合条件实验
综上所述,采用单因素试验法获得从铜氨溶液中电积铜的优化工艺条件:1) 添加剂 明胶0.06 g/L、硫脲0.05 g/L,配位剂 乙二胺0.4 mol/L;2) 脉冲电流密度600 A/m2、占空比90%;3) 电解液组分:[NH4Cl]=3 mol/L、[NH3・H2O]=1.5 mol/L、[Cu2+]=20 g/L。在此条件下,阴极铜沉积物平整光滑且有金属光泽。在此条件下进行综合试验连续电积6 h后,得到了平整、光滑且具有金属光泽的铜阴极片18.78 g,此时阴极电流效率87.97%,槽电压为3.20 V。所得铜阴极片的XRD谱、光学图像和SEM像如图9~11所示。
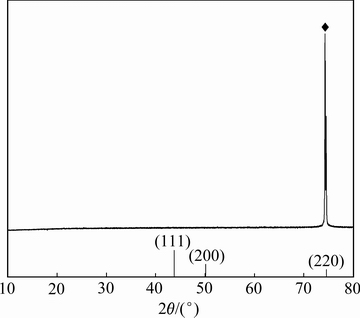
图9 综合条件下所得阴极铜的XRD谱
Fig. 9 XRD pattern of cathode copper layer on cathode under optimized conditions

图10 综合条件下阴极铜光学照片
Fig. 10 optical photo of cathode copper layer under optimized conditions

图11 综合条件下阴极铜的SEM像
Fig. 11 SEM images of copper layer under optimized conditions
XRD谱的结果表明,本研究氨-氯化铵体系脉冲电积所得阴极铜晶体主要沿(220)晶面生长,其余晶面,如(111)、(200)等未见明显反射峰,表现出类单晶结构(见图9)。由图10可知,阴极铜表面光滑平整且有金属光泽。由图11(a)可知,所得阴极铜表面光滑致密且无瘤状物产生;由图11(b)的阴极铜片的剖面图可知,铜沉积物为纤维状,铜在不锈钢极板表面的生长方式为呈与阴极面垂直的一维方向生长。
3 结论
1) 以漂白粉为氧化剂,研究了某低品位硫化铜精矿在NH3-NH4Cl-H2O体系中的氧化浸出行为,得到了最佳浸出条件:液固比(L/S)=4:1、[NH3・H2O]=1 mol/L、氯化铵3 mol/L、氧化剂过量系数1.4、原料粒度94~124 μm、浸出时间2 h、温度30 ℃。在此条件下,该低品位硫化铜精矿铜浸出率达98.89%。
2) 采用单因素实验法优化了从铜氨溶液中直接电积铜的工艺,得到了最佳电积条件:添加剂为0.06 g/L明胶、0.05 g/L硫脲,配位剂为0.4 mol/L乙二胺;脉冲电流密度600 A/m2、占空比90%;电解液组分:[NH4Cl]=3 mol/L、[NH3・H2O]=1.5 mol/L、[Cu2+]=20 g/L。在此条件下进行电积试验,得到了平整、光滑且具有金属光泽的铜阴极片,阴极电流效率为87.97%。
3) 对综合条件所得阴极铜进行XRD分析结果表明,氨-氯化铵体系中脉冲电积铜晶体主要沿(220)晶面生长,其余晶面未发现明显反射峰,表现出类单晶结构;对阴极进行SEM分析表明,所得阴极铜表面光滑致密且无瘤状物产生,铜在阴极表面的生长方式为为呈与阴极面垂直的一维方向生长。
REFERENCES
[1] 邓会娟, 季根源, 易锦俊, 尚 磊, 姜爱玲. 中国铜矿资源现状及国家级铜矿床实物地质资料筛选[J].中国矿业, 2016, 25(2):143-148.
DENG Hui-juan, JI Gen-yuan, YI Jin-jun, SHANG Lei, JIANG Ai-ling. Current status of copper-ore resources in China and screening of national copper-ore geological material data[J]. China Mining Magazine, 2016, 25(2):143-148.
[2] 刘志雄, 尹周澜, 胡慧萍, 陈启元. 低品位氧化铜矿氨-硫酸铵体系过硫酸铵氧化浸出[J]. 中国有色金属学报, 2012, 22(5):1488-1496.
LIU Zhi-xiong, YIN Zhou-lan, HU Hui-ping, CHEN Qi-yuan. Oxidative leaching of low-grade copper ore in ammonia- ammonium sulfate solution with ammonium persulfate[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(5): 1488-1496.
[3] 张振健. 汤丹铜精矿焙烧-氨浸-萃取电积新工艺研究[J]. 有色金属(冶炼部分), 1999(4): 16-20.
ZHANG Zhen-jian. Study on the new method of processing Tangdan copper concentrate by roasting-ammonia leaching- extraction eletrodeposition[J]. Nonferrous Metals (Smelting Part), 1999(4): 16-20.
[4] 刘 维. MACA体系中处理低品位氧化铜矿的基础理论和工艺研究[D]. 长沙: 中南大学, 2010: 46-75, 132-139.
LIU Wei. Theoretical and technological study on treating low grade copper oxide ore in the system of MACA[D]. Changsha: Central South University, 2010: 46-75, 132-139.
[5] 于 霞, 甘雪萍, 杨声海, 唐谟堂. Cu(Ⅱ)-NH3-(NH4)2SO4- H2O体系浸出-电积生产铜的工艺研究[J]. 湖南有色金属, 2001, 17(6): 18-20.
YU Xia, GAN Xue-ping, YANG Sheng-hai, TANG Mo-tang. The study on leaching-electrodeposition in NH3-(NH4)2SO4-H2O system[J]. Hunan Nonferrous Metals, 2001, 17(6): 18-20.
[6] BINGOL D, CANBAZOGLU M, AYDOGAN S. Dissolution kinetics of malachite in ammonia/ammonium carbonate leaching[J]. Hydrometallurgy, 2005, 76: 55-62.
[7] 赵洪冬. 高碱性脉石低品位氧化铜矿浸出工艺及氨浸动力学研究[D]. 长沙: 中南大学, 2014: 9-11.
ZHAO Hong-dong. Study on the leaching of low-grade oxidized copper ore with high alkalinity gangue and it’s kinetics of ammonia leaching[D]. Changsha: Central South University, 2014: 9-11.
[8] ZHOU Long-ping, DAI Ya-tang, ZHANG Huan, et al. Nucleation and growth of bismuth electrodeposition from alkaline electrolyte[J]. Bulletin of the Korean Chemical Society, 2012, 33(5): 1541-1546.
[9] Jorge V A, Isabel L. Electrochemical study of binary and ternary copper complexes in ammonia-chloride medium[J]. Electrochimic Acta, 2007, 52: 6106-6177.
[10] Darko G, Batric P. Reaction and nucleation mechanisms of copper electrodeposition from ammoniacal solutions on vitreous carbon[J]. Electrochimic Acta, 2005, 50: 4426-4443.
[11] 郑永勇. 废弃线路板中铜的提取与资源化工艺研究[D]. 杭州:浙江工业大学, 2010: 22-25, 30-32.
ZHENG Yong-yong. Research on recycling process of Cu from scrap printed circuit boards[D]. Hangzhou: Zhejiang University of Technology, 2010: 22-25, 30-32.
[12] 杨声海. Zn(Ⅱ)-NH3-NH4Cl-H2O体系制备高纯锌理论及应用[D]. 长沙: 中南大学, 2003: 32-33.
YANG Sheng-hai. Theory and application studies on preparing high purity zinc in the system of Zn(Ⅱ)-NH3-NH4Cl-H2O[D]. Changsha: Central South University, 2003: 32-33.
[13] Sabah M, Adbel B. Recovery of cupric chloride from spent copper etchant solutions: A mechanistic study[J]. Hydrometallurgy, 2003, 69: 135-143.
[14] 姚雅伟. 氨性体系浸析含铜废物中铜的技术研究[D]. 济南: 山东大学, 2015: 21-22, 28-30.
YAO Ya-wei. Study on the leaching of copper by ammoniacal solution from copper-containing waste[D]. Ji’nan: Shandong University, 2015: 21-22, 28-30.
Oxidation leaching and pulse electro-deposition of low-grade copper sulfide ore in NH3-NH4Cl-H2O system
LI Shu-chao, YANG Jian-guang, CHEN Bing, Ding Long, Nan Tian-xiang
(School of Metallurgy and Environmental, Central South University, Changsha 410083, China)
Abstract: The oxidative leaching behaviors of a low grade copper sulfide concentrate in NH3-NH4Cl-H2O were investigated by using single-factor experiment method. The results show that 98.89% copper can be leached under the conditions of liquid-solid ratio 4:1, NH3・H2O concentration 1.0 mol/L, ammonium chloride concentration 3.0 mol/L, 1.4 times stoichiometric oxidant dosage, particle size 94-124 μm, contact time 2 h and temperature 30℃. In addition, the optimization experiments of direct pulse copper electro-deposition from this cuprammonia leach solution were carried out. A flat and metallic luster cathode copper plate with cathode current efficiency 87.97% is obtained under the optimized conditions NH4Cl concentration 3 mol/L, NH3・H2O concentration 1.5 mol/L, Cu2+ concentration 20 g/L, gelatin concentration 0.05 g/L, thiourea concentration 0.06 g/L, pulse current density 600 A/m2 and duty cycle 90%. XRD analysis results of the resultant cathode copper show that the copper crystal in the ammonia system grow mainly along (220) crystal surface, and there is no obvious reflection peak on the other crystal faces, which show that the cathode copper is analogous to single crystal structure. SEM analysis results show that the surface of the cathode copper is smooth, compact and without tumor on the surface. The growth of copper on the cathode surface is in one-dimensional direction perpendicular to the cathode surface.
Key words: low grade copper sulfide concentrate; oxidative ammonia leaching; pulse electrodeposition
Foundation item: Project(51574294) supported by the Natural Science Foundation of China; Project(2015CX001) supported by the Innovation-driven Plan of Central South University, China
Received date: 2017-06-23; Accepted date: 2017-11-13
Corresponding author: YANG Jian-guang; Tel: +86-731-88830470; E-mail: jianguang_y@163.com
(编辑 李艳红)
基金项目:国家自然科学基金资助项目(51574294);中南大学创新驱动计划资助项目(2015CX001)
收稿日期:2017-06-23;修订日期:2017-11-13
通信作者:杨建广,教授,博士;电话:0731-88830470;E-mail:jianguang_y@163.com