DOI: 10.11817/j.issn.1672-7207.2016.02.003
甲烷还原氧化球团过程中的渗碳行为
王振阳,张建良,邢相栋,刘征建,刘兴乐
(北京科技大学 冶金与生态工程学院,北京,100083)
摘要:通过固定床热重反应器,利用X线衍射(XRD)、热重(TG)以及扫描电镜-能谱(SEM-EDS)等分析方法,研究纯CH4气体还原球团过程中的渗碳行为。研究结果表明:甲烷还原铁氧化物依靠其裂化产生的H2与吸附碳;CH4还原5 min时,金属铁相产生,但由于吸附碳参与还原反应,故基本不存在积碳,由于金属铁层在球团颗粒表面逐渐增厚以及铁碳固溶体颗粒中碳质量分数逐渐增加,阻碍吸附碳的还原并抑制碳向固溶体颗粒内的进一步扩散,故积碳在还原5 min后出现,20 min后浮士体相消失且吸附碳质量分数逐渐增加;反应初期吸附碳对还原速率有一定促进作用,但当吸附碳大量沉积时,则阻碍还原气H2与还原产物H2O与CO的扩散,降低CH4还原速率。
关键词:甲烷;直接还原;球团;渗碳;微观结构
中图分类号:TF554 文献标志码:A 文章编号:1672-7207(2016)02-0373-07
Carburization behavior in reduction of oxide pellets by methane
WANG Zhenyang, ZHANG Jianliang, XING Xiangdong, LIU Zhengjian, LIU Xingle
(School of Metallurgical and Ecological Engineering, University of Science and Technology Beijing, Beijing 100083, China)
Abstract: With thermogravimetric fixed bed reactor, the analysis methods of X-ray diffraction (XRD), thermogravimetric (TG) and scanning electron microscopy (SEM) energy dispersive spectrometer (EDS) were used to investigate the carburization behavior in reduction of oxide pellets by CH4. The results show that CH4 reduction of iron oxide is mainly through the adsorption carbon and cracking H2. In 5 min, the metallic iron phase appears and since adsorption carbon takes part in the reduction, there is no carbon. However, with the metallic iron layer thickening gradually, it hinders the reduction and internal diffusion of adsorption carbon. Thus, deposition carbon appears after 5 min. After 20 min, FexO disappears and adsorption carbon increases gradually. The adsorption carbon can diffuse from the external of metallic iron particles to the center and produce iron carbon solid solution with metallic iron. The adsorption carbon has a positive effect on reduction rate at initial reduction stage. When large amounts of adsorption carbon deposits, it hinders the spread of reducing gas H2 and reduction product H2O and CO, which reduces the reduction rate of CH4.
Key words: methane; direct reduction; pellets; carburization; microstructure
Energiron-ZR是目前较为先进的直接还原工艺,可直接使用天然气、煤制气和焦炉煤气。但未经重整的还原气中甲烷含量很高,故在竖炉的入口处,还原气需要与喷入的氧气发生部分燃烧反应,以减少还原气中的甲烷含量,但仍有15%~25%(体积分数)的甲烷进入竖炉,依靠金属铁的催化作用进行自重整,若促使该过程生成的活性炭与金属铁发生渗碳反应,则可阻碍成品海绵铁在空气中的再氧化[1-3]。因此,有必要对甲烷直接还原氧化球团的作用机理进行探究。国内外学者已展开相关研究,DONG等[4] 研究了Fe-C固溶体、γ-Fe以及Fe3C三者之间的物相转变,指出Fe3C或吸附碳可以阻碍Fe-C固溶体和γ-Fe的氧化。NATHANIEL等[5-6]的研究表明:甲烷在还原锰氧化物过程中,其裂化产生的活性炭会被还原和渗碳反应所消耗,但若大量产生活性炭以至于沉积在氧化物表面时,会对还原产生强烈的抑制作用。HAYASHI等[7]研究了H2-CH4混合气还原赤铁矿球团的过程,指出升温和加压有利于渗碳反应的进行。但利用纯甲烷气体,对其在还原球团过程中的作用机理和微观研究则极少见诸报道。本文作者通过在固定床反应器内利用纯甲烷气体还原氧化球团,采用热重(TG)、X线衍射(XRD)以及扫面电镜-能谱(SEM-EDS)等分析方法,研究了氧化球团在甲烷还原过程中的物相转变及微观结构变化,为海绵铁渗碳及防氧化工艺提供了理论基础。
1 实验
1.1 原料
实验所用氧化球团来自国内某大型钢铁企业,利用化学分析方法对该球团的成分进行检测,结果见表1。
表1 氧化球团化学成分(质量分数)
Table 1 Chemical composition of oxidized pellets %

由表1可知:实验用球团全铁(TFe)的质量分数为63.1%,有害元素S和P含量较低,但酸性脉石含量较高,SiO2与Al2O3总质量分数接近6.4%,经直接还原,金属化球团中酸性脉石质量分数将超过8.5%。考虑到我国自产铁矿品位普遍偏低,二氧化硅等脉石含量较高,该种球团符合我国球团现状,故选用表1所示球团作为实验原料。为了解原料球团的主要物相组成,对其进行XRD分析,结果见图1。
由图1可知:原料球团中铁的主要物相为赤铁矿(Fe2O3),基本不存在磁铁矿(Fe3O4);硅主要以二氧化硅(SiO2)形式存在,并未出现铁橄榄石相(FeO・SiO2),说明该球团在预热焙烧过程中的氧化反应较为充分,且未出现低熔点的硅酸盐物相。

图1 原料球团XRD图谱
Fig. 1 XRD pattern of pellets before methane reduction
1.2 方法与设备
取粒度为10.0~12.5 mm的若干球团为一组,并保证各组球团质量相近,将筛分后的球团置入恒温干燥箱中,在105 ℃下烘干4 h,以充分脱除其中的吸附水。程序还原炉以5 ℃/min的速率进行升温,整个过程通入氩气,以最大限度排出恒温区内的氧气。在Energiron实际生产工艺中,为避免海绵铁之间的黏结,会控制反应最高温度以最大限度的降低液相的生成,故反应温度一般在900~950 ℃之间,本文选择了较低的反应温度以获得较低的裂化速度,从而利于研究甲烷的渗碳行为。炉温升至900 ℃后开始保温,将装有球团的钼丝篮置于恒温区,待炉温稳定30 min后,将氩气切换至甲烷气体,还原反应开始。有研究表明[8]:还原气体流速的增大有利于加快还原反应速率,但是当气流线速度大于0.050 m/s时,还原率随时间的变化不再受到还原气体流速增加的影响,即外部对流传质此时对还原速率不产生影响,实验所用管式炉刚玉管的内径为45 mm,还原气流量选取5 L/min,此时还原气线速度为0.052 m/s。为进一步说明甲烷还原球团的特点,也进行了H2和CO还原球团的质量损失实验作为对比,还原实验设备见图2。
通过电子天平连续测量和计算机记录,系统会每隔12 s记录一次球团在实验中的质量损失情况,达到预定还原时间后取出钼丝篮,迅速放入充满氩气的容器中直至冷却,对不同还原时间的球团进行XRD检测,并对其中心切面进行SEM-EDS分析,得到甲烷还原过程中的球团物相转变和微观结构变化。还原实验升温制度及CH4还原后的球团宏观形貌见图3。
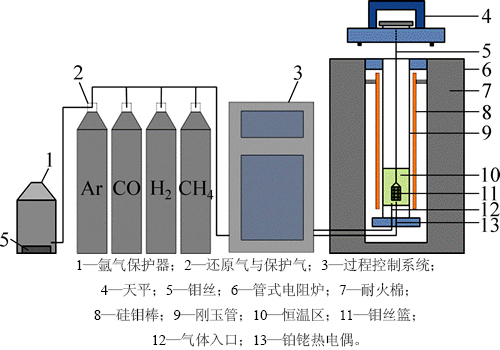
图2 实验装置示意图
Fig. 2 Sketch map of experimental device
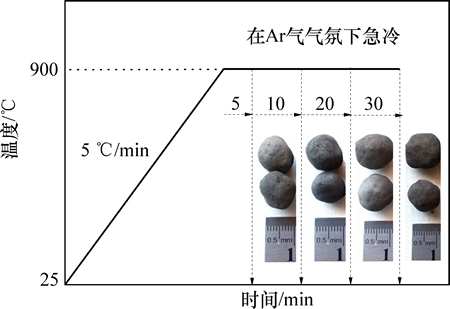
图3 甲烷还原实验温度控制制度
Fig. 3 Temperature control process in methane reduction
2 结果与分析
2.1 球团在CH4还原过程中的物相分析
甲烷还原球团实验过程中,在反应进行至5,10,20和30 min时对球团取样,进行XRD物相分析,结果见图4。
由图4可知:在反应进行至5 min时,原料球团中的主要物相Fe2O3与少量存在的Fe3O4基本还原为浮士体FeO,并有少量金属铁生成。这是由于在赤铁矿还原至金属铁的过程中,Fe2O3还原至FeO的失氧量仅占总失氧量的33%,且还原势要求较低,相比FeO还原至Fe更易进行,故还原进行5 min后,赤铁矿与磁铁矿相基本消失,少量浮士体还原为金属铁。当反应进行至10 min时,浮士体进一步被还原,金属铁含量增加,由于甲烷的裂化反应,导致球团局部生成吸附碳的速度大于碳的还原消耗,部分碳沉积在球团表面,且金属铁与吸附碳发生渗碳反应,从而铁碳固溶体相FexC开始出现。20 min时,浮士体相消失,还原反应结束,而铁碳固溶体与吸附碳的含量则继续增加。30 min时,金属铁的主峰强度有所下降,而铁碳固溶体与吸附碳的主峰强度增加明显,说明部分金属铁在吸附碳的作用下继续生成铁碳间隙固溶体FexC[9],从而导致金属铁相含量下降。通过对不同甲烷还原时间球团碳含量进行化学分析,结合XRD结果,得到不同反应时间的球团物相转变状态,见表2。
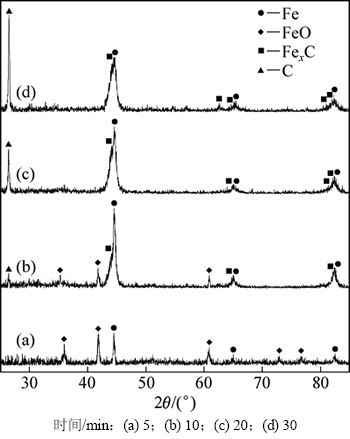
图4 甲烷还原过程中球团XRD图谱
Fig. 4 XRD pattern of pellets in process of methane reduction
表2 甲烷还原过程中物相转变
Table 2 Phase transformation in the process of methane reduction

甲烷裂化过程反应式如下[10-11]:
CH4(g)=CH4(ad) (1)
CH4(ad)=CH3(ad)+H(ad) (2)
CH3(ad)=CH2(ad)+H(ad) (3)
CH2(ad)=CH(ad)+H(ad) (4)
CH(ad)=C(ad)+H(ad) (5)
2H(ad)=H2(g) (6)
铁氧化物首先被裂化产生的H2以及反应式(5)产生的吸附碳还原至金属铁,而后金属铁与吸附碳反应生成铁碳固溶体,甲烷还原球团过程中含铁物相转变如图5所示,物相转变所需的还原势以w(H2)/[w(H2)+w(H2O)]表征。

图5 甲烷还原过程中铁的物相转变过程
Fig. 5 Iron phase transformation in the process of methane reduction
赤铁矿在微量还原势下即可还原至磁铁矿,且失氧量仅占总失氧的11.1%,说明在还原气氛下,Fe2O3极易转变为Fe3O4;同样地,磁铁矿也较易还原为浮士体,失氧比与还原势分别为22.2%和16.5%H2;而浮士体转变为金属铁最为困难,失氧量占总失氧的66.7%,且需要61.3%H2的还原势。甲烷裂化总反应可以用式(7)表达,若以式(8)中所示固态碳为标准状态,则式(7)中吸附碳的活度可以用式(9)表示:
CH4=C(ad)+2H2 (7)
CH4=C(solid)+2H2 (8)
 ;
;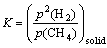 ;
;
 (9)
(9)
式中:ac为吸附碳C(ad)的活度;K为甲烷裂化反应的平衡常数;p(CH4)与p(H2)分别为甲烷与氢气的分压。实验中由于甲烷分压远大于氢气分压,所以[(p(CH4))/(p2(H2))]ad大于有固态碳存在且甲烷与氢气达到平衡时的[(p(CH4))/(p2(H2)]solid,因此,吸附碳的活度大于固态碳的活度,故实验中甲烷裂化产生的吸附碳易参与还原并且易与金属铁反应生成铁碳固溶体。
2.2 球团在CH4还原过程中的热重分析
甲烷还原球团实验中,由于存在球团失氧与甲烷裂化的叠加反应[12],故球团总质量损失如下式所示:
Δm=Δm(O)+Δm(C) (10)
式中:Δm(O)为还原失氧导致的质量减少;m(C)为甲烷裂化在球团表面形成吸附碳,造成的质量增加。若以质量损失折算还原度,则会造成还原度失真,因此,采用质量损失率(η)为本实验的分析指标,而以质量损失速率表征反应速率,计算方法如下:
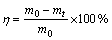 (11)
(11)
 (12)
(12)
式中:mt为t时刻球团质量,g;m0为初始球团质量,g;Δm为微小时间内的质量损失,g;Δt为微小时间,min。
由式(11)可知:反应温度为900 ℃时,H2,CH4和CO还原球团的质量损失率曲线以及除去吸附碳的CH4还原球团质量损失率曲线,另根据球团化学成分,得到球团内铁氧化物全部还原成磁铁矿、浮士体和金属铁的质量损失率分别为2.89%,8.90%以及26.93%,见图6(a),根据球团在H2与CH4还原过程中的质量损失,结合式(12),可得H2还原球团的质量损失速率以及CH4还原球团的质量损失速率及其导数曲线,见图6(b)。
由图6(a)可知:对比H2,CO和CH4还原球团质量损失率曲线,可得H2还原球团速率较快,赤铁矿在5 min内全部还原为浮士体,且有部分浮士体被还原为金属铁,当反应进行至15 min时,还原反应基本完成;而CO还原球团的速率相对较慢,在30 min内反应仍未结束,这主要与H2与CO的扩散能力有关,相关研究较为成熟[13-15]。CH4在0~17 min内质量损失率略比H2的低,但显著比CO的高,在17 min后出现质量增加现象,质量损失率曲线下降明显。对于除去吸附碳的CH4质量损失率曲线,由于CH4主要通过高温裂化产生的H2还原铁氧化物,因此,CH4质量损失曲线明显比CO的高,且与H2的相差不大;但由于该过程会在铁氧化物表面形成吸附碳,对CH4裂化产生的H2还原铁氧化物产生阻碍作用,故CH4质量损失曲线略比H2的低。
由图6(b)可知:H2作为还原气时的反应速率在整个还原过程中均呈现下降趋势,且根据速率曲线斜率的不同可分为3个阶段,这主要是控速限制环节不同所致,3个阶段分别为化学反应控速、化学反应与内扩散混合控速和内扩散控速。CH4虽然主要依靠裂化产生的H2进行还原,但由于吸附碳的存在,对反应过程造成了一定影响,因此,与H2反应速率曲线有所不同。在CH4还原球团初期,反应速率逐渐下降,这是由于生成的产物铁层阻碍了还原气H2以及还原产物H2O的扩散所致,且此时甲烷裂化产生的碳量较少,不能完全提供直接还原所需碳量;但当反应进行至约4.2 min时,反应速率呈现增加的趋势,这是由于甲烷裂化产生吸附碳含量增加且进一步扩散至球团内部,吸附碳与铁氧化物发生了充分的直接还原反应,其对还原的促进作用大于了产物铁层和吸附碳层对还原的抑制作用(对还原气H2与还原产物H2O和CO扩散的阻碍),故反应速率有所提高,这里CH4反应速率的反常提升有可能是由于新生成的活性金属铁对裂化H2还原铁氧化物的催化作用所致,但对比纯H2反应速率曲线则排除了这一可能性;当反应进行至约8.5 min时,反应速率出现极大值点,在该时刻还原失重与CH4裂化积碳达到平衡;当反应进行至17 min时,随着球团内铁氧化物还原殆尽以及裂化产生的碳在金属铁的催化作用下大量吸附在球团内,导致CH4质量损失率曲线出现拐点并下降,球团开始质量增加;当反应进行至约21.8 min后,反应速率基本恒定,此时还原反应基本结束,只存在甲烷裂化反应。

图6 CH4还原球团质量损失率曲线和CH4还原球团质量损失速率及其导数曲线
Fig. 6 Mass loss rate curve and CH4 reduction mass loss speed and its derivative curve
2.3 球团在CH4还原过程中的微观变化
取不同甲烷还原时间的球团,利用扫描电镜对其中心切面的微观变化进行检测,其在不同还原时间的SEM以及甲烷还原30 min后球团内某一铁颗粒不同部位的EDS见图7。
由图7可知:当CH4还原球团至5 min时,球团各颗粒之间基本没有积碳形成,由未反应核模型可知,在反应初期,球团颗粒表面的铁氧化物还原度较低,裂化产生的吸附碳易与铁氧化物颗粒发生直接还原反应生成CO气体,因此球团颗粒表面基本不存在吸附碳。而随着还原反应的进行,氧原子浓度由球团颗粒内部至表面逐渐降低,金属铁层在球团颗粒表面逐渐增厚,阻碍了吸附碳与铁氧化物发生直接还原反应,且球团内部铁碳固溶体颗粒中碳含量逐渐增加,抑制了碳向固溶体颗粒内的进一步扩散,但甲烷裂化反应仍在进行,CH4扩散至球团内部并裂化产生吸附碳,故碳在球团颗粒之间及表面逐步沉积,形成图7所示的反应进行至10~30 min时的SEM。
通过高倍数条件下观测甲烷还原30 min时的金属化颗粒并对其进行EDS分析可知:金属化颗粒中含有一定量以铁碳固溶形式存在的碳,且从边缘至中心碳含量逐渐降低,说明甲烷在还原铁氧化物过程中,碳不只是吸附在金属化颗粒表面,而是由颗粒外部向中心逐渐扩散,并与金属铁以固溶体的形式生成铁碳化合物。由DONG等[4]的研究可知:该种海绵铁可以有效地阻碍氧化,故在Energiron-ZR工艺中,还原气含有部分CH4可以有效降低海绵铁的再氧化。EDS能谱中有微弱的Au峰,这是为了使SEM显示结果更加清晰可辨,在球团截面处溅射了一层Au,对显示结果不产生影响。

图7 不同甲烷还原时间下球团SEM像与EDS谱
Fig. 7 SEM images and EDS spectrum of pellets for different methane reduction time
3 结论
1) 甲烷还原球团过程中,反应进行至5 min时,有金属铁相生成;10 min时吸附碳沉积在球团表面并与金属铁发生渗碳反应,有少量铁碳固溶体相产生;20 min后浮士体相消失,还原反应基本结束,但吸附碳与铁碳固溶体含量继续增加,金属铁质量分数下降。
2) 甲烷还原铁氧化物主要依靠其裂化产生的H2,由于吸附碳的产生,其质量损失曲线略低于H2还原质量损失曲线,但显著高于CO还原质量损失曲线;甲烷还原反应初期,其裂化产生的吸附碳对还原有一定促进作用,之后反应速率逐渐下降,主要是由于铁氧化物质量分数的降低,产物铁层的增厚以及沉积在球团表面的吸附碳对气体扩散的阻碍所致。
3) 反应5 min内,由于吸附碳与铁氧化物发生了还原反应,故在球团表面基本不存在积碳,5 min后,金属铁层在球团颗粒表面逐渐增厚,阻碍了吸附碳与铁氧化物的还原反应,同时铁碳固溶体颗粒中碳质量分数逐渐增加,抑制了碳向固溶体颗粒内的进一步扩散,致使碳在球团颗粒之间及表面逐步沉积;反应30 min时金属化颗粒中碳含量由边缘至中心逐渐降低,说明吸附碳可由金属铁颗粒的外部向中心扩散,并与金属铁生成铁碳固溶体,可有效降低海绵铁的再氧化。
参考文献:
[1] VOLPATTI A, FRANCO B, MARTINIS A. Energiron direct reduction process: The forefront technology[C]//AISTech 2012 Iron and Steel Technology Conference and Exposition. Atlanta, 2012: 615-624.
[2] 特诺恩. 联合钢厂采用无碳排放的ENERGIRON直接还原方案减少温室气体的排放[J]. 世界钢铁, 2012, 4(3): 1-8.
TE N N. Decrease of GHG emissions through the carbon free emissions Energiron DR scheme in integrated mills[J]. World Iron & Steel, 2012, 4(3): 1-8.
[3] 李志远, 米万良, 苏庆泉. 重整气中CO深度去除方法[J]. 北京科技大学学报, 2010, 32(1): 100-104.
LI Zhiyuan, MI Wanliang, SU Qingquan. Deep removal of CO in reformate[J]. J Univ Sci Technol Beijing, 2010, 32(1): 100-104.
[4] DONG X L, ZHANG Z D, ZHAO X G. Mossbauer effect in ultrafine particles with Fe-C solid solution, γ-Fe and Fe3C phases[J]. J Mater Sci Technol, 1998, 14(5): 441-446.
[5] NATHANIEL A, OLEG O, GANGULY S. Reduction of manganese oxides by methane-containing gas[J]. ISIJ int, 2004, 44(9): 1480-1487.
[6] NATHANIEL A, OLEG O, GANGULY S. Reduction of manganese ores by methane-containing gas[J]. ISIJ int, 2004, 44(10): 1615-1622.
[7] HAYASHI S, IGUCHI Y. Formation behavior of iron carbide in a pellets with pressurized H2-CH4 gas mixtures containing traces of H2S[J]. Tetsu to Hagane: Journal of the Iron and Steel Institute of Japan, 2003, 89(11): 1099-1106.
[8] 刘建华, 张家芸, 周土平. CO及CO-H2气体还原铁氧化物反应表观活化能的评估[J]. 钢铁研究学报, 2000, 12(1): 5-9.
LIU Jianhua, ZHANG Jiayun, ZHOU Shiping. Assessment of apparent activation energies for reducing iron oxides by CO and CO-H2[J]. J Iron Steel Res, 2000, 12(1): 5-9.
[9] 陈维青, 杜振民, 吴平, 等. Fe-C基三元合金相图计算[J]. 北京科技大学学报, 1992, 14(6): 672-676.
CHEN Weiqing, DU Zhenmin, WU Ping, et al. Zhang W J. Calculation of Fe-C base alloy ternary phase diagrams[J]. J Univ Sci Technol Beijing, 1992, 14(6): 672-676.
[10] GRABKE H J. Evidence on the surface concentration of carbon on gamma iron from the kinetics of the carburization in CH4-H2[J]. Metall Mater Trans B, 1970, 1(10): 2972-2975.
[11] GHOSH D, ROY A K, GHOSH A. Reduction of ferric oxide pellets with methane[J]. ISIJ Int, 1986, 26(3): 186-193.
[12] ARMAN R, NASSER T. The effect of lime coating of hematite pellets on soot formation and reduction rate with CH4/H2[J]. ISIJ Int, 2009, 49(3): 349-354.
[13] EGASHIRA M, MAEDA T, NISHIOKA K, et al. Synthesis of iron carbide from hematite pellets with H2-CH4 gas mixture[J]. J Iron Steel Inst Jpn, 2000, 86(6): 375-380.
[14] ONO-NAKAZATO H, YONEZAWA T, USUI T. Effect of water-gas shift reaction on reduction of iron oxide powder packed bed with H2-CO mixtures[J]. ISIJ Int, 2003, 43(10): 1502-1511.
[15] 左晓剑, 王静松, 安秀伟, 等. 高还原势气氛下球团矿还原行为的研究[J]. 钢铁钒钛, 2013, 34(2): 46-53.
ZUO Xiaojian, WANG Jinsong, AN Xiuwei, et al. Reduction behaviors of pellets under high reduction potential[J]. Iron Steel Vanadium Titanium, 2013, 34(2): 46-53.
(编辑 杨幼平)
收稿日期:2015-02-10;修回日期:2015-05-25
基金项目(Foundation item):国家自然科学基金委员会与宝钢集团有限公司联合资助项目(51134008)(Project (51134008) supported by the National Natural Science Fund Committee and Baosteel Group Corporation of China)
通信作者:张建良,博士,教授,博士生导师,从事低成本炼铁等研究;E-mail:Zhang.jianliang@hotmail.com