DOI: 10.11817/j.ysxb.1004.0609.2020-37507
���ڽ����϶�����Ͳ�ָ����������ʽ﮿���Һ����ص绯ѧ���������о�
�� �࣬�� ����������
(�Ϻ����´�ѧ �̴�ѧԺ���Ϻ� 201306)
ժ Ҫ������˾��н����϶�����ṹ������ʽ﮿���Һ����أ�������Һ���������Һѭ������Ͻ����϶�����ṹ��ǿ���缫�ڲ�Li+��O2��ɢ�ͽ�������������缫�ۻ�������COMSOL Multiphysics 5.3��������ά�绯ѧģ�ͣ���Darcy���ɡ�Butler-Volmer���̺�������˹�ʽ�����ڽ����϶�����ṹ(��=0.55+��X��)�µ缫�ڲ����Һ�������������绯ѧ��Ӧ�����Һ��Li+��O2Ũ�ȳ��ֲ�������Li2O2������������϶�ڣ��缫�ȱ�����½�������Carman-Kozeny������������K���о������϶�ʡ�ѹǿ�����������������ȼ�����ѧ����ϵ���Ըõ�طŵ�����Ӱ�졣����������ڷŵ�����ܶ�0.1 mA/cm2����رȵ������DZ���ʽ�ṹ��2.5�������=0.85-0.1X��ȣ����æ�=0.55+��X�ṹ�ĵ绯ѧ���ܽϼѣ��ڷŵ�����ܶ�0.1 mA/cm2�£��������Ϊ500~750 ��m����طŵ����ܽϺá�
�ؼ��ʣ�﮿���Һ����أ�����ʽ�ṹ�������϶�ʣ���ֵ����
���±�ţ�1004-0609(2020)-03-0629-11���� ��ͼ����ţ�TM911 ���� ���ױ�־�룺A
1996��ABRAHAM��[1]����˵�һ�����з�ˮ����ʵ�﮿������ϵͳ������ѧ���������˶�﮿�������о��ȳ�[2]��﮿�����طŵ��������̼���ϲ���(�����ݡ������ȱ����)�й�[3]��ZHOU��[4]�Ʊ�����ʯīϩ������[5]Ϊ����Ŀ�������������ص���ά��֧�Žṹʵ����10000 mA��h/g�ķŵ�ȵ�������WANG��[6]�Ʊ�����ά��ṹ�������Ru��������ʯīϩ��̼���ϣ��õ��ϵͳ�ŵ�������ߴ�17710 mA��h/g��DAI��[7]�Ʊ��˾���ɺ��״�ṹ��N����̼��ά��������1000 mA��h/g�£������Ȧѭ������Ч�ʸߴ�90%������������Ȼ�ʹ��رȵ��������ӣ�����ѭ��ʹ������[8]�Լ�������ɢ���ʻ����½�[9]���о�������缫�ڲ��������Ե�����Ũ���ݶ�[10]������Ũ�ȸ�Li2O2�����ߣ��缫�ۻ�����[11]��XIA��[12]�о��˲�����ʪ�ķֲ��������ṹ���ڷŵ�����ܶ�Ϊ0.1 mA/cm2ʱ���õ缫����ڴ�����״̬�缫�ȵ����������60%��HU��[13]�о���һ��3.4 mm��ķֲ���ľ�������������ڷŵ�����ܶ�Ϊ0.1 mA/cm2���������ŵ�ȵ������ߴ�56 mA��h/cm2��
Ŀǰ���ٹ�����ѧ�߶�����Һ�����չ����ģ���о�[14-16]��SHAH��[17]������ȫ��Һ����ص�˲̬ģ�ͣ��о������٣�������Ũ�ȼ��缫��϶�ʶԵ�����ܵ�Ӱ�졣ZHENG��[18]�����﮿���Һ����ظ��ģ���ڲ�ͬ�������Һ[19]�£�������������ܶ��ܴ�140 W��h/kg��1100 W��h/kg��CHEN��[20]ͨ��ʵ��֤����﮿���Һ����ؿ��Ա��ָ߹���������ڷŵ�����ܶ�Ϊ4 mA/cm2ʱ����ص������ܶȿɴ�7.64 mW/cm2��
���������һ�ֻ��ڽ����϶�����ṹ��﮿���Һ�����ϵͳ��ģ���о��˽����϶�ʣ�ѹǿ�������ȣ�����ѧ���ʳ���������Ũ�ȼ���ɢϵ���Ըõ��ϵͳ�ŵ�����Ӱ�졣
1 ϵͳ����������ģ��
1.1 ϵͳ����
�õ��ϵͳ��﮽����缫������Ĥ�������϶��������Һ�á������úʹ�Һ����ɡ���ͼ1(a)~(b)��ʾ�������е�O2�������ô��봢Һ���У�ʹ�ô�Һ���е��Һ�ܽ����ﵽ���ͣ�Ȼ��ͨ����Һ�ý�����в�ָ�������Ľ����϶�����ڣ�������������ѹ����������£����Һ��������缫�ڲ���������϶�ڵ��Һ�е�Li+��O2��ַ�Ӧ������Li2O2����ɷŵ绯ѧ��Ӧ��������Һ���������Һѭ������Ͻ����϶�����ṹ��ǿ���缫��϶�ڲ����Һ��Li+��O2��ɢ�ͽ��������ʹ�õ�ؾ��и��ߵıȵ��ݡ�
1.2 ����ģ��
�ö�ά����ģ��ͼ��ͼ2��ʾ�������ҷֱ���﮽����缫������Ĥ�������϶�����Ͳ�ָ�����������ͼ1(b)�в�ָ�������ṹ�����������ĶԳ��ԣ��������������ںͳ���ͨ����һ�롣�ڼ����У��߸������������2/5(40%�Ŀ�����)��
�ڽ���������У������� ���Ա���X��xȡֵ��Χ��ͼ2������ԭ��0��0*��ѡȡ�ܽ��ڱ�1��������
���Ա���X��xȡֵ��Χ��ͼ2������ԭ��0��0*��ѡȡ�ܽ��ڱ�1�������� ��ʽ(1)ȷ����
��ʽ(1)ȷ����
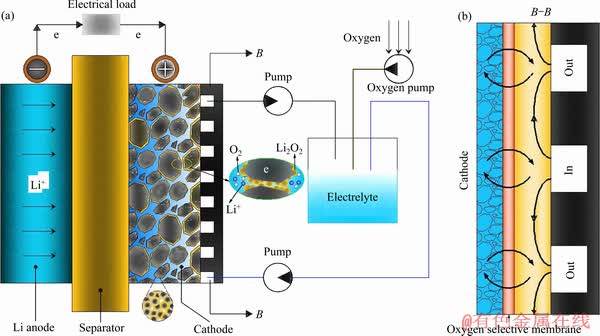
ͼ1 ����ʽ﮿���Һ�����ϵͳ�Ͳ�ָ�����������ͼ
Fig. 1 Lithium-air liquid flow battery system(a) with active cathode and cross section view(b) of interdigital channel

ͼ2 ģ�͵ļ�������
Fig. 2 Computational domain of model
��1 ����������
Table 1 Variable description

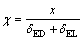 (1)
(1)
ʽ�У� Ϊ������ȣ�
Ϊ������ȣ� Ϊ����Ĥ�ĺ�ȡ�
Ϊ����Ĥ�ĺ�ȡ�
1.3 ���۽�ģ
��������Darcy���ɡ�Butler-Volmer���̺�������˹�ʽ�����ڽ����϶�����ṹ(��=0.55+��X��)�µ缫�ڲ�������������������绯ѧ��Ӧ�����Һ��Li+��O2Ũ�ȷֲ�������Li2O2������������϶�ڣ����µ缫�ȱ�����½�������Carman-Kozeny������������K��
1.3.1 ģ�ͼ���
Ϊ��ģ�ͣ�ģ�ͽ��������в������¼��裺�������Һ�ڵ�����ʼ�մ��ڱ���״̬��Li+����ɢʹ��Ũ��Һ��������ۣ���缫���г���Һ�����ʣ�������Li2O2�ǵ�طŵ������Ψһ����(�����Ǹ���Ӧ�Լ�LiO2��Li2CO3����)��
1.3.2 Li+��O2Ũ������
������������غ㷽�̼�Darcy����[21]��
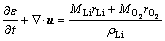 (2)
(2)
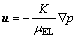 (3)
(3)
ʽ�У���Ϊ������϶�ʣ�tΪʱ�䣻MiΪ����i����Է���������ri��ʾ����i�������ʣ���LiΪLi+���ܶȣ���ELΪ�������Һ�����ȣ�KΪ��ϵ����uΪ�����ٶȣ�pΪѹǿ��
Li2O2������������϶�ڲ�����ϵ��K��֮�ı䣬����ʽ���Carman-Kozeny����[21]��
 (4)
(4)
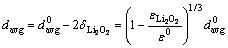 (5)
(5)
ʽ�У���0Ϊ������ʼ��϶�ʣ�dPΪ������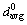 Ϊ�����ٶ�dP=davg������K��ʽ(6)ȷ����
Ϊ�����ٶ�dP=davg������K��ʽ(6)ȷ����
 (6)
(6)
��������i��Ũ�ȿ��Ʒ��̿�дΪ��
 (7)
(7)
ʽ�У�ci��ʾ��Һ��������i��Ũ�ȣ�NiΪ����i��Ħ��ͨ��������ʽȷ����
 (8)
(8)
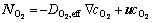 (9)
(9)
ʽ�У�t+ΪLi+��Ǩ������Di,effΪ����i����Ч��ɢϵ����J2����Һ���е����ܶ���ʽ(10)ȷ����
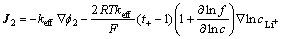 (10)
(10)
ʽ�У�keff�ǵ���ʵ���Ч�絼�ʣ���2Ϊ����ʵ�λ��FΪ�����ڳ�����
����ʽ(2)��(7)��(8)��(10)������ʽ(2)��(7)��(9)���ɷֱ�õ�Li+��O2���Ʒ��̣���ʽ(11)~(12)��ʾ��

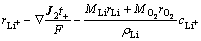 (11)
(11)
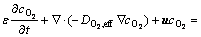
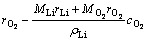 (12)
(12)
������Ӵ��������ܶ�J1���ŷķ����[22]���ڱ�ģ���й�Һ�������غ㣬��ʽ(14)��ʾ��

 (13)
(13)
ʽ�У���effΪ��缫��Ч�絼�ʣ���1Ϊ�����λ��
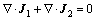 (14)
(14)
�ɷ����ڶ��ɿɵ�������������ri�ı���ʽ��
 (15)
(15)
ʽ�У�SiΪ����i��Ũ��Դ��
1.3.3 ����������ѧ����ʽ
���������绯ѧ��Ӧ��Ӧ��Butler-Volmer����[23]��
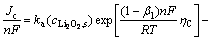
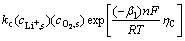 (16)
(16)
 (17)
(17)
ʽ�У�JcΪ�ֲ�ת�Ƶ����ܶȣ�ci,s�缫��������i��Ħ��Ũ�ȣ�ka��kcΪ�������������ʳ�������1�ǶԳ�����ȡ0.5��n�ǵ绯ѧ��Ӧ������ת�Ƶĵ���������CΪ����λ��RfilmΪŷķ�����������ĵ��裻E0Ϊ���ۿ�·��ѹ��
����﮽��������ĵ绯ѧ��Ӧ��Ӧ��Butler- Volmer���̣�
 (18)
(18)
ʽ�У�Ja���������������ܶȣ�J0Ϊ���������ܶȣ� Ϊ���������λ��
����������
��طŵ�ʱ��Li2O2��������϶�ڵĻ��ۣ��缫�ȱ�������٣���Ч�ȱ����ʽ(19)��ʾ[24]��
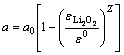 (19)
(19)
ʽ�У�a�������ȱ������a0Ϊ��ʼ��缫�������ZΪ�������ӣ��ڱ�ģ����ȡ0.4[24]��
1.3.4 ����Li2O2�ܽ���̿�϶�仯����
��cLi2O2,s��ccmax,Li2O2�����Һ��Li2O2Ũ�ȱ仯��ʽ(20)��ʾ����cLi2O2,s��ccmax,Li2O2��Li2O2������������϶�ڱ����ϣ������ֳ���Ĥ״����ʽ(21)��ʾ��
 (20)
(20)
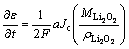 (21)
(21)
ʽ�У�cLi2O2,sΪLi2O2�ڵ��Һ�е�Ħ��Ũ�ȣ�ccmax,Li2O2ΪLi2O2�ڵ��Һ�е�����ܽ�ȡ�
1.4 �߽�����
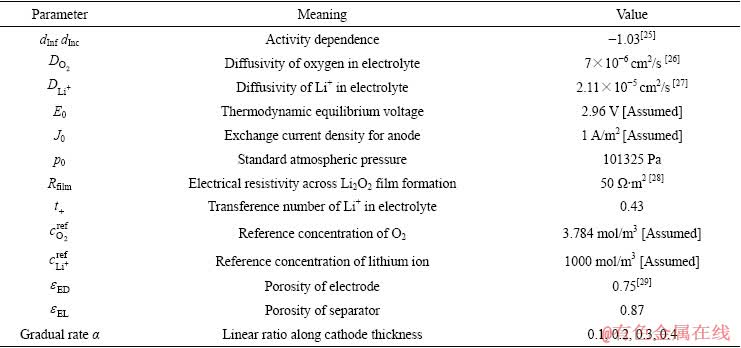
�߽��������2��ʾ��ͼ2����ģ����(����������)��߽�һһ��Ӧ���ڽ���������У����û������˵��������ͨ����ѹ����Ϊ0.4p0���������Ϊ750 ��m��
���Ľ����˶�ά˲̬�ǵ���ģ�ͣ�����COMSOL Multiphysics 5.3��﮿�����طŵ�ȵ��ݡ�����Li2O2���������O2��Li+Ũ�ȳ��ֲ���������Ԫ��������������������ǹ�����С�в(GMRES)[30]������ݲ�����Ϊ1��10-4��������������Ʒ���(2)~(21)���߽����������������϶�ʡ�������ȡ�����ѧ����ϵ����ѹǿ�O2Ũ�Ⱥ���ɢϵ���Ըõ��ϵͳ�ŵ����ܺʹ��ʹ��̵�Ӱ��(ע�������������J��ʾ�ŵ�����ܶ�)��
1.5 ģ����֤
��J=0.2 mA/cm2��J=0.5 mA/cm2ʱʵ��õ��ı���ʽ﮿�����طŵ�������ģ����б���ʽ�����ṹ��طŵ����߽��жԱȣ�����֤ģ�����ݵĿɿ��ԣ�ʵ��������������[31]����ͼ3���Կ�����ģ��������ʵ�������Ǻ϶Ƚϸߣ�����ģ�ͽ��������д��������裬�Լ��������Բ�����ѡȡ�����������һ���̶��ϻᵼ��ģ����������������ƫ�롣
1.6 �����������֤
��������������ֵ����ȷ��ʮ����Ҫ��Ϊ��ø��Ӿ�ȷ�ļ���������������ϸ������ģ��ʹ����������Ԫ����ɵķǽṹ������Ϊ�˲�������������Ӱ�죬��J=1.5 mA/cm2����=0.75����£��Ա������ֲ�ͬ���������ϴֻ�(437����Ԫ)���ֻ�(529����Ԫ)������(770����Ԫ)����ϸ��(2545����Ԫ)�����4��ʾ����������������������������ģ��������Ӱ�죬Ϊ��ʡ����ʱ�䣬��ģ�Ͳ��ý�ϸ������
��2 �߽��������ܱ�
Table 2 Summary of boundary conditions
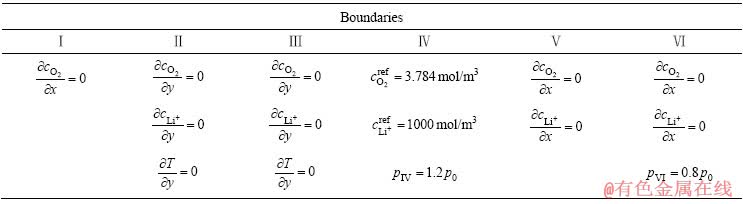
��3 ģ�Ͳ�����
Table 3 Parameters used in model
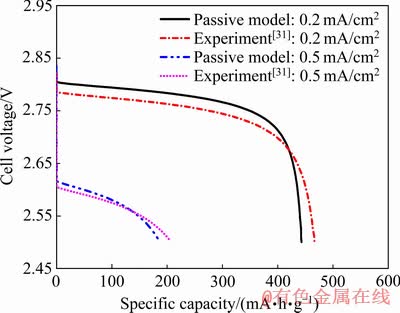
ͼ3 ﮿�����ص�����ŵ�����[31]��ģ�����Ա�
Fig. 3 Comparisons between experimental discharge curves[31] and passive model simulation curves of lithium-air batteries at J=0.2 mA/cm2, J=0.5 mA/cm2 and ��ED=800 ��m
��4 �ȵ����������������仯��
Table 4 Variations of specific capacity with grid number
2 ���������
2.1 ����ʽ������ʽ�����ṹ�Ƚ�
�ڷŵ��ֹ��ѹ��Ϊ2.5 V����£���������ʽ﮿���Һ����ز��ò�ָ��������ƣ�������������֮���ѹ����ǿ���缫�ڲ����Һ�Ĵ��ʹ��̣����Ƶ缫�ڲ�Li+��O2Ũ�ȷֲ���ʹ�õ缫��϶�ڵ��Һ��Li+�õ�������ã�����˵缫�����ʡ���ͼ4���Կ���������ʽ�����ṹ�ĵ�طŵ�ȵ�����Ϊ2045.6 mA��h/g��������ʽ�ṹ��Ϊ835.5 mA��h/g�������2.5�����������ʽ﮿���Һ������ܽϴ�̶���ǿ�����������������ӣ���ߵ�����ܡ�

ͼ4 ����ʽ������ʽ�缫�ṹ�ŵ�Ա�ͼ
Fig. 4 Comparison of cell voltage and specific capacity curves between lithium-air batteries with active and passive cathodes at J=0.1 mA/cm2 and ��=0.75
2.2 �㶨��϶���뽥���϶�ʱȽ�
��϶����Ӱ������������Ҫ��������ͼ5(a)���Կ�������=0.75+0.1X���=0.85-0.1X��ȣ���ŵ�ȵ�������446.4 mA��h/g���ӵ�698.2 mA��h/g�������56.4%���Ҧ�=0.75+0.1X���=0.85�ͦ�=0.75��ȣ���ŵ�ȵ������ֱ������9%��47.9%�������������æ�=0.75+0.1X�ṹ�������O2��Li+���缫���෴Ӧ���������ʹ�õ��Һ�е�Li+�õ�������ã����Ƶ�����ܡ����ڶ�ṹҲΪLi2O2�Ļ����ṩ�˳�������ͼ5(b)���Կ�������=0.75+0.1Xʱ��Li2O2�������ϴ��ҷֲ����ݶȱ仯���缫�����ʽϸߡ�����=0.85-0.1Xʱ�����ڿ����������϶�ʽ�С�����ŵ绯ѧ��Ӧ������Li2O2�����缫�������ڶλ���λ�㣬����O2��һ����ɢ���缫�ڲ�������O2��Li+�ڵ缫�ڴ��䷢���仯������ѧ���ͣ�Ũ�ȼ���������ˣ���=0.85-0.1X����ڦ�=0.75+0.1X����Li2O2�ֲ���Ϊ���ȣ��缫�����ʽϵ͡�

ͼ5 ��J=1.5 mA/cm2ʱ�㶨��϶���뽥���϶�ʽṹ��طŵ���������ͼ�Լ�����Li2O2�ֲ�ͼ
Fig. 5 Cell voltage vs specific capacity curves(a) and distribution of Li2O2 volume fractions(b) of active lithium-air batteries with gradual-change porosity and single porosity at J=1.5 mA/cm2
2.3 �����϶�ʽṹ�Ե������Ӱ��
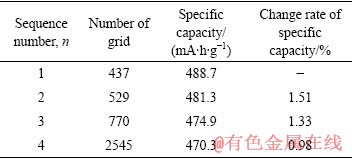
��ͼ6(a)��(c)���Կ���������flow=0.85����=(0.75, 0.65, 0.55)+��X�������ʦ���0.1����0.3ʱ����������702.4 mA��h/g����765.1 mA��h/g�������8.9%������flow=0.95����=(0.75,0.65,0.55)+��X�������ʦ���0.2����0.4ʱ����������1558.1 mA��h/g����1928.7 mA��h/g�������23.8%�����ұȵ��������������Ǧ�flow=0.85����µ�2.7����������ڿ�����������϶��һ�µ�����£������ʦ�Խ��ʱ����طŵ�����Խ���ҿ�����������϶��Խ��缫������Խ�ߡ����ڽ����ʦ����ӣ������Ա仯���Ʊ��������϶��O2��Li+��Ӧ���������Һ��Li+�õ�������ã�ʹ�ñ�����Һ������Һ��Ũ�ȼ�����С����������������ѧ����ͼ6(b)��(d)���Կ�����Li2O2�ֲ����ݶȱ仯��Խ��������ͨ������Li2O2����Խ�ࣻ�����ʦ�Խ��Li2O2�ֲ��ݶ�Խ��flow=0.95ʱ���flow=0.85ʱ��ȣ���Li2O2�ڵ缫��϶�ڻ���Խ�ࡣ����������϶�����ṹ���෴Ӧ��������ϴ��ܹ����ɸ����Li2O2����س����ŵ��������������ϼ�(ע����flowΪ��������ͨ������϶��)��
2.4 ѹǿ��Խ����϶�������ṹ�������Ӱ��
����ͨ����ѹǿ��Ĵ�С���طŵ������йء���ͼ7(a)�п��Կ���������=0.75+0.1X����pa��0.3p0���ӵ�0.5p0���ȵ�������500.5 mA��h/g���ӵ�850.9 mA��h/g�������70%����ͼ7(b)���Կ�������pa���ѹǿ����Li2O2Ũ�����Ը��ڵ�ѹǿ���µ�Ũ�ȡ��������ѹǿ����Ը��Ƶ缫�ڵ��Һ���ʼ�����ʹ�õ缫�ڲ�Li+��O2�����ֲ����ھ�һ������Ч��ɵ�طŵ绯ѧ��Ӧ����ߵ��Һ�����ʡ�����ģ��������ȡ��ָ����������ѹǿ�����������ұ���Ҳ���������ӡ���ˣ����ѹǿ��Ӧ���ۺϿ����������أ��Ӷ�ʹ��طŵ����ܴﵽ��ѡ�
2.5 ����Ũ�ȼ���ɢϵ���Խ����϶�������ṹ�������Ӱ��
����Ũ�ȼ���ɢϵ��������������������ء���ͼ8(a)���Կ�������O2Ũ�ȴ�3.78 mol/m3����15.14 mol/m3ʱ���ȵ�������697.1 mA��h/g�仯��1934.4 mA��h/g�������2.8����˵������Ũ��Խ�ߣ���صķűȵ�����Խ��صķŵ��ѹҲԽ�ߡ���ͼ8(b)���Կ�������O2��ɢϵ����7��10-10 m2/s����7��10-9 m2/sʱ���ȵ�������697.1 mA��h/g�仯��908.8 mA��h/g�������30.4%��˵����������ɢҲ�ǵ�ط�Ӧ�Ŀ��Ʋ��衣��ˣ�ѡȡ���ܽ�ȡ�����ɢϵ���ĵ������Һ�����Ż�﮿����ŵ����ܾ�����Ҫ���塣
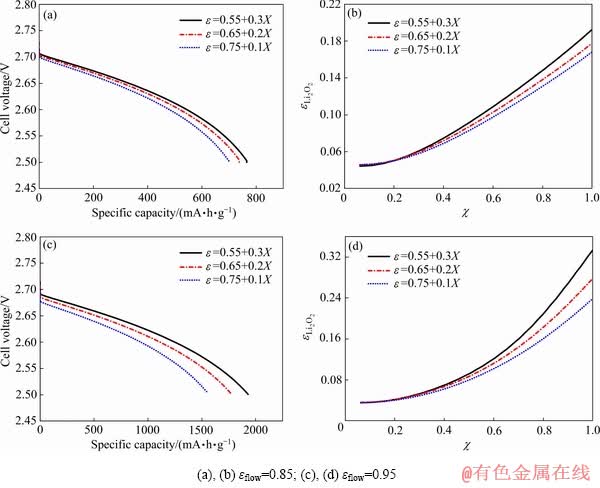
ͼ6 ��J=1.5 mA/cm2ʱ��ͬ���µ�طŵ���������ͼ�Լ�����Li2O2�ֲ�ͼ
Fig. 6 Cell voltage vs specific capacity curves((a), (c)) and distribution((b), (d)) of cathode Li2O2 with different �� at J=1.5 mA/cm2: (a), (b) ��flow=0.85; (c), (d) ��flow=0.95

ͼ7 ��ͬ��pa�µĵ�طŵ���������ͼ������Li2O2�ֲ�ͼ
Fig. 7 Cell voltage vs specific capacity curves(a) and distribution(b) of cathode Li2O2 with different pressure differences at J=1.5 mA/cm2 and ��ED=0.75+0.1X
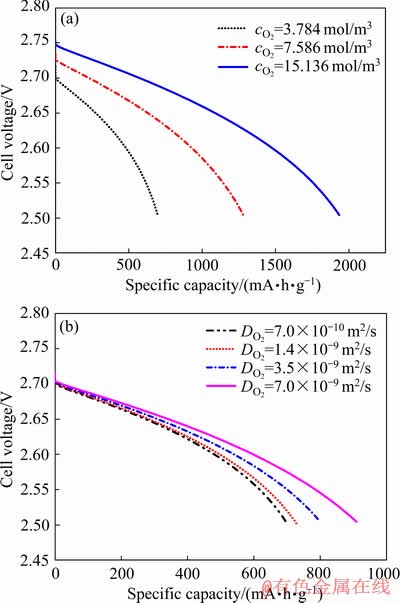
ͼ8 ��ͬ����Ũ�ȺͲ�ͬ������ɢϵ���µ�طŵ���������ͼ
Fig. 8 Battery discharge capacity curves under different oxygen concentrations(a) and different oxygen diffusion coefficients(b) (J=1.5 mA/cm2, ��=0.75+0.1X)
2.6 ������ȶԽ����϶�������ṹ�������Ӱ��
Ϊ�о�������ȶԵ�طŵ�����Ӱ�죬������������Damkohler(Da��)����ʽ(22)��ʾ:
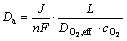 (22)
(22)
ʽ(22)�����绯ѧ��Ӧ������O2��ɢ����֮�ȡ���ͼ9(a)���Կ�����������ȴ�500 ��m�仯��1500 ��m���ȵ�������309.6 mA��h/g����948.84 mA��h/g��Da����13.90����41.70���ȵ����������3.2������Da��Ҳ�����3����������ȵ�����ʹ�ȵ�����������ߣ����ܽ�������ɢ����ԶԶС�ڵ绯ѧ��Ӧ���ʣ���������ܽ����ֲ������ȣ������˵��Һ�������ʡ���ͼ9(b)���Կ�����������ȴ�500 ��m�仯��750 ��m�������Ե��ݵ����������˵�������500~750 ��m֮�䣬��صķŵ����ܽϼѣ����Ŵ�0.65 ����0.85���ȵ�����������303.6 mA��h/g��ߵ�599.4 mA��h/g����Ҳ��߿�϶���µ�طŵ����ܽϺõĹ���һ�¡����5��ʾ���ڸߵ����ܶȸ���������£�Da��Զ����1�������ŵ�����ܶ�Խ����λʱ��μӷ�Ӧ�Ļ�������Խ�ࡣ���ڵ缫����O2��Li+���Ĺ��죬O2���������뵽�缫�ڲ���ͬʱ���ڿ�������ͨ������Li2O2�������谭��O2��ɢ�缫�ڲ������ʹ�õ缫�ڲ�Li+�ò���������ã����Һ�����ʵ͡���ͼ9(b)��֪��������ȴ�500 ��m�仯��750 ��mʱ���ȵ�����������࣬ͬʱ��J=0.1 mA/cm2ʱ��Da����С��O2�ڵ缫�ڲ��ֲ���Ϊ���ȣ���˸ù�����طŵ����ܽϼѡ�
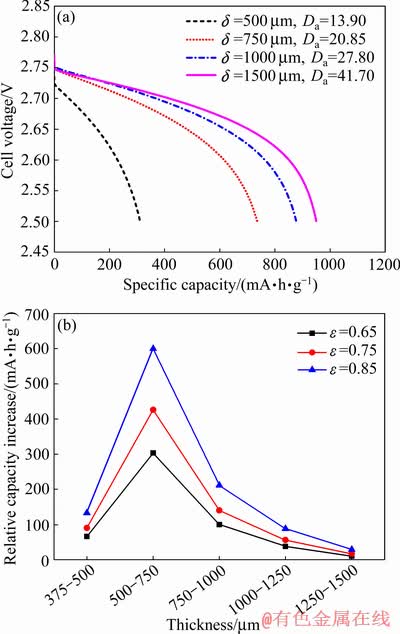
ͼ9 ��ͬ��������µ�طŵ���������ͼ�Ͳ�ͬ��϶���µ�رȵ��������ȱ仯���������������ͼ
Fig. 9 Cell voltage vs specific capacity curves(a) with different cathode thickness (J =1.0 mA/cm2, ��ED=0.75) and thickness vs relative capacity increase line chart(b) with different cathode porosity (J =1.0 mA/cm2, ��ED=750 ��m)
��5 ��ͬ�ŵ�����ܶȺ����������Damkohler����
Table 5 Comparison of Damkohler number at different current densities and cathode thickness

2.7 ����ѧ����ϵ���Խ����϶�������ṹ�������Ӱ��
�������Ը��Ƶ��ORR����ѧ��������λ���ٶ���Ӧ����ϵ���������ڲ��㶨�Ҿ��ȣ���ͼ10��ʾ����kc��3.49��10-18 m7/(s��mol2)�仯��3.49�� 10-16 m7/(s��mol2)����ʼ��ѹ��2.7 V��ߵ�2.8 Vʱ���ȵ�������746.9 mA��h/g���ӵ�1262.8 mA��h/g�������69.1%��������������[32]�еĽ���һ�£�˵�����и��ߴ����ԵĴ������������﮿���������ܡ����ڴ������Թ���ڹ����ź���������ȱ�ݶȣ�����Ч���͵�طŵ������Li2O2����ܣ�����ȱ��λ����Li2O2�ɺ˳����Ϊ����������Щ������������������Ӷ����Ƶ�����ܡ�

ͼ10 ��ͬ������Ӧ����ϵ���µ�طŵ�����ͼ
Fig. 10 Cell voltage vs specific capacity curves with different cathodic reaction rate coefficients at J=1.0 mA/cm2 and ��=0.75+0.1X
3 ����
1) ����ʽ﮿���Һ���������ڴ�ͳ��﮿�����ؿ���������ߵ�طŵ�ȵ���������J=0.1 mA/cm2������ʽ���ϵͳ�ȵ������DZ���ʽ�ṹ��2.5����
2) �����һ�ֽ����϶�������ṹ(����϶����������ȷ������Ե���)�������ʦ�Խ��صķŵ�����Խ�ѡ���J=1.5 mA/cm2ʱ����=0.75+0.1X���=0.85-0.1X��ȣ�������������56.4%����=0.75+0.1X���=0.85�ͦ�=0.75��ȣ���������ֱ������9%��47.9%��
3) ����ͨ����ѹǿ��Ĵ�СӰ��缫�ڲ�Li+��O2���ʹ��̡���J=1.5mA/cm2������=0.75+0.1Xʱ����pa��0.3p0���ӵ�0.5p0���ȵ����������70%��Ȼ����ѹǿ�����������ұ���ʧҲ���������ӣ���ˣ�Ӧ�ۺϿ��������������Ż�����ͨ������ѹ���
4) ����Ũ�ȼ���ɢϵ����Ӱ�����������Ҫ���ء���J=1.5 mA/cm2����O2Ũ�ȴ�3.784 mol/m3����15.136 mol/m3ʱ�������������2.8������O2��ɢϵ����7��10-10 m2/s����7��10-9 m2/sʱ�������������30.4%����������и��ܽ�ȡ�����ɢϵ���ĵ������Һ������Ч��ߵ��Һ���ܽ�������ɢ�������Ӷ����������ۻ������������Ҳ�ڵ绯ѧ��Ӧ��������Ҫ���á���J=0.1 mA/cm2�����������500 ��m��750 ��m֮��ʱ����طŵ����ܽϼѡ�
5) ���ʵĴ���������Ч����ORR����ѧ��������λ����J=1.5 mA/cm2����=0.75+0.1Xʱ��kc��3.49�� 10-18 m7/(s��mol2)�仯��3.49��10-16 m7/(s��mol2)����ʼ��ѹ��2.7 V��ߵ�2.8 V�������������69.1%��˵�����и��ߴ����ԵĴ������������﮿���������ܡ�
REFERENCES
[1] ABRAHAM K M, JIANG Z. A Polymer electrolyte-based rechargeable lithium/oxygen battery[J]. Journal of the Electrochemical Society, 1996, 143(1): 1-5.
[2] WOO H, KANG J, KIM J, KIM C, NAM S, PARK B. Development of carbon-based cathodes for Li-air batteries: Present and future. Electronic Materials Letters[J]. 2016, 12(5): 551-567.
[3] JIE X, WANG D H, XU W, WANG D Y, RALPH E W, LIU J, ZHANG J G. Optimization of air electrode for Li/air batteries[J]. Journal of the Electro-chemical Society, 2010, 157(4): 2057-2063.
[4] JIANG J, HE P, TONG S F, ZHENG M B, LIN Z X, ZHANG X P, SHI Y, ZHOU H S. Ruthenium functionalized graphene aerogels with hierarchical and three-dimensional porosity as a free-standing cathode for rechargeable lithium-oxygen batteries[J]. NPG Asia Materials, 2016, 8(1): 239-239.
[5] �� ��, ������, ������, �� ��, ��ҵ��. ʯīϩ������ӵ�ز��������Ż��е�Ӧ��[J]. �й���ɫ����ѧ��, 2016, 26(4): 807-820.
CAO Liang, WANG An-an, YAI Li-hua, JIA Ming, LIU Yei-xiang. Application of graphene in performance optimization of lithium ion battery materials[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(4): 807-820.
[6] SUN B, HUANG X D, CHEN S Q, MUNROE P, WANG G X. Porous graphene nanoarchitectures: An efficient catalyst for low charge-overpotential, long life, and high capacity lithium-oxygen batteries[J]. Nano Letters, 2014, 14(6): 3145-3152.
[7] SHUI J L, DU F, XUE C M, LI Q, DAI L M. Vertically aligned N-doped coral-like carbon fiber arrays as efficient air electrodes for high-performance nonaqueous Li-O2 batteries[J]. ACS Nano, 2014, 8(3): 3015-3022.
[8] FREUNBERGER S A. True performance metrics in beyond-intercalation batteries[J]. Nat Energy, 2017, 2: 17091.
[9] ANDREI P, ZHENG J, HENDRICKSON M, PLICHTA E J. Some possible approaches for improving the energy density of Li-air batteries[J]. Electrochemical Society, 2010, 157(12): 1287-1295.
[10] JIANG J, DENG H, LI X, TONG S F, HE P, ZHOU H S. Research on effective oxygen window influencing the capacity of Li-O2 batteries[J]. ACS Applied Materials Interfaces, 2016, 16(8): 10375-10382.
[11] SHUI J L, WANG H H, LIU D J. Degradation and revival of Li-O2 battery cathode[J]. Electrochemistry Communications, 2013, 34: 45-47.
[12] XIA C, BENDER C L, BERGNER B, PEPPLER K, JANEK J. An electrolyte partially-wetted cathode improving oxygen diffusion in cathodes of non-aqueous Li-air batteries[J]. Electrochemistry Communications, 2013, 26: 93-96.
[13] SONG Hui-yu, XU Shao-mao, LI Yi-ju, DAI Jia-qi, GONG A, ZHU Ming-wei, ZHU Chun-liang, CHEN Chao-ji, CHEN Ya-nan, YAO Yong-gang, LIU Bo-yang, SONG Jian-wei, PASTEL G, HU Liang-bing. Hierarchically porous, ultrathick, ��breathable�� wood-derived cathode for lithium-oxygen batteries[J]. Advanced Energy Materials, 2017, 8(4): 1701203.
[14] WEBER A Z, MENCH M M, MEYERS J P, ROSS P N, GOSTICK J T, LIU Qing-hua. Redox flow batteries: A review[J]. Journal of Applied Electrochemistry, 2011, 41: 1137-1164.
[15] ��˫��, ������, �� ��, �� ��, �ź���, �� ��, ��ҵ��. Բ������Ӷ�����ص������Է���[J]. �й���ɫ����ѧ��, 2014, 24(7): 1823-1830.
DU Shuang-long, LAI Yan-qing, JIA Ming, CHENG Yun, ZHANG Hong liang, ZHANG Kai, LIU Ye-xiang. Electrothermal characteristics simulation of cylindrical automotive lithium-ion battery[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(7): 1823-1830.
[16] ��˫��, ������, �� ��, �� ׳, ������, �� ��. ���ڵ绯ѧģ�͵�﮿�����ط���[J]. �й���ɫ����ѧ��, 2018, 28(6): 1143-1150.
DU Shuang-long, LAI Yan-qing, JIA Ming, CHENG Zhuang, AI Li-hua, AI Liang. Simulation for lithium air batteries based on electrochemical model[J]. The Chinese Journal of Nonferrous Metals, 2018, 28(6): 1143-1150.
[17] SHAH A A, WATT-SMITH M J, WALSH F. A dynamic performance model for redox-flow batteries involving soluble species[J]. Electrochemistry Acta, 2008, 53(27): 8087-8100.
[18] ZHENG J P, ANDREI P, HENDRICKSON M, PLICHTA E J. The theoretical energy densities of dual-electrolytes rechargeable Li-air and Li-air flow batteries[J]. Journal of the Electrochemical Society, 2011, 158(1): 43-46.
[19] �� ��, ������, �� ��, ������, �� ��, �� ��. ����������ӵ�ع��ܵ��Һ���о���չ[J]. �й���ɫ����ѧ��, 2017, 27(6): 1208-1221.
HONG Bo, YAN Xiao-lin, HONG Shu, LAI Yan-qing, LI Jie, JIANG Feng. Review of functional electrolyte for lithium-ion battery working in wide temperature scope[J]. The Chinese Journal of Nonferrous Metals, 2017, 27(6): 1208-1221.
[20] CHEN X J, SHELLIKERI A, WU Q, ZHENG J P, HENDRICKSON M A, PLICHTA E J. A high-rate rechargeable Li-air flow battery[J]. Journal of Electro- chemistry Society, 2013, 160(10): 1619-162.
[21] NIELD D A, BEJAN A. Convection in porous media[M]. New York: Springer, 2006: 1-778.
[22] UKRIT S, HUA Cheng, KEITH S. Modelling of electrolyte degradation and cycling behaviour in a lithium-air battery[J]. Journal of Power Sources, 2013, 243: 409-418.
[23] CANO M, RODRIGUEZ-AMARO R, FERNANDEZ- ROMERO A J. Use of Butler-Volmer treatment to assess the capability of the voltammetric ion sensors: Application to a PPy/DBS film for cations detection[J]. Electrochemistry Communications, 2008, 10: 190-194.
[24] LI X L, HUANG J, FAGHRI A. A critical review of macroscopic modeling studies on Li2O2 and Li-air batteries using organic electrolyte: Challenges and opportunities[J]. Journal of Power Sources, 2016, 332: 420-446.
[25] NYMAN A, BEHM M, LINDBERGH G. Electrochemical characterization and modelling of the mass transport phenomena in LiPF6-EC-EMC electrolyte[J]. Electrochemical Acta, 2008, 53(22): 6356-6365.
[26] READ J, MUTOLO K, ERVIN M. Oxygen transport properties of organic electrolytes and performance of lithium/oxygen battery[J]. Journal of the Electrochemical Society, 2003, 150(10): 1351-1356.
[27] STEWART S G, NEWMAN J. The use of UV/vis absorption to measure diffusion coefficients in LiPF6 electrolytic solutions[J]. Journal of the Electrochemical Society, 2008, 155(1): 13-16.
[28] LI Q, SUN H Y, TAKEDA Y, YAMAMOTO O. Interface properties between a lithium metal electrode and a poly (ethylene oxide) based composite polymer electrolyte[J]. Journal of Power Sources, 2001, 94(2): 201-205.
[29] REN X M, ZHANG S, TRAN D T, READ J. Oxygen reduction reaction catalyst on lithium/air battery discharge performance[J]. Journal of Materials Chemistry, 2011, 27(21): 10118-10125.
[30] LELE A F, KUZNIK F, OPEL O, RUCK W K L. Performance analysis of a thermochemical based heat storage as an addition to cogeneration systems[J]. Energy Conversion and Management, 2015, 106: 1327-1344.
[31] READ J. Characterization of the lithium/oxygen organic electrolyte battery[J]. Journal of Electrochemistry Society, 2002, 149(9): 1190-1195.
[32] CHENG H, SCOTT K. Carbon-supported manganese oxide nanocatalysts for rechargeable lithium-air batteries[J]. Journal of Power Sources, 2010, 195(5): 1370-1374.
Investigation on electrochemical performance of active gradual-change porosity cathode in interdigital flow channel of lithium-air flow battery
SHU Qing, CHEN Wei, KANG Jia-lun
(School of Merchant Marine, Shanghai Maritime University, Shanghai 201306, China)
Abstract: Lithium-air flow battery with active gradual-change porosity cathode was proposed in which more oxygen in the electrolyte and electrochemical reaction occured due to the utilization of solution pump to drive electrolyte recycled and gradual-change porosity to achieve better O2 migration in cathode. Based on COMSOL Multiphysics 5.3, a two-dimensional electrochemical model was established. The electrolyte flow, electrochemical reactions in the cathode and anode as well as the Li+ and O2 concentrations in the gradual-change porosity cathode of ��=0.55+��X etc, were described by Darcy��s law, Butler-Volmer equation and component transport formulae, respectively. The permeability K inside porous cathode changed with the electrochemical reaction as the occurrence of Li2O2 deposition in the pore, which was modified by Carman-Kozeny equation. The effects of discharge current density, porosity, pressure difference, oxygen parameters, cathode thickness and kinetic rate coefficient were investigated. The results show that the 2.5 times capacitance occurs in the active lithium-air battery at 0.1 mA/cm2 current density than that of a passive mode; more electrochemical reaction happens in the gradual-change porosity cathode of ��=0.55+��X in comparison with that of ��=0.85-0.1X; and better discharge performance can be obtained in the 500 ��m to 750 ��m thick cathode of active lithium-air battery at 0.1 mA/cm2 current density.
Key words: lithium-air flow battery; active cathode structure; gradual-change porosity; numerical simulation
Foundation item: Project(19ZR1422400) supported by the Shanghai Natural Science Foundation, China
Received date: 2019-03-13; Accepted date: 2019-10-08
Corresponding author: CHEN Wei; Tel: +86-21-383282921; E-mail: weichen@shmtu.edu.cn
(�༭ ��ѧ��)
������Ŀ���Ϻ�����Ȼ��ѧ����������Ŀ(19ZR1422400)
�ո����ڣ�2019-03-13�������ڣ�2019-10-08
ͨ�����ߣ��� �������ڣ���ʿ���绰��021-383282921��E-mail��weichen@shmtu.edu.cn