�й���ɫ����ѧ�� 2004,(05),836-841 DOI:10.19476/j.ysxb.1004.0609.2004.05.023
ͭ�Ͻ��临�ϲ������Ȼ��������еĸ�ʴ��Ϊ
ժ Ҫ��
ͨ���Ȼ���������ʴʵ��,���X��������(XRD)�͵���̽��(EPMA)����,�о���ͭ�Ͻ��临�ϲ������Ȼ��������еĸ�ʴ��Ϊ���������:��ʵ����ڲ��ϵĸ�ʴ�ٶ���ʱ����ӳ�������,Լ96h�Ժ�ʴ�ٶȻ������ٱ仯;BZn15 17�봿�����ϲ��ϵ���ʴ�����;ʵ����ںͺ��ڵĸ�ʴ������ɻ�����ͬ,2�ְ�ͭ�Ͻ����Ҫ��ʴ���ﶼ��CuCl2��2H2O,��ͭ�Ͻ����Ҫ��ʴ����ΪCuCl,���ΪCuCl2��2H2O��(CuZn)2(OH)3Cl;��ʴ��ò�仯�ϴ�
�ؼ��ʣ�
ͭ�Ͻ�;���ϲ���;��ʴ��Ϊ;�Ȼ�������;
��ͼ����ţ� TG172
����飺�ż���(1970),��,����ʦ.;����Ң,���о�Ա;�绰:02423893544;E mail:zhywang@imr.ac.cn;
�ո����ڣ�2003-09-02
Corrosion behavior of copper alloys and its composites in NaCl spray
Abstract��
The corrosion behavior of copper alloys and its composites was studied by means of NaCl spray test, with the analysis of XRD and EPMA. It is found that the average corrosion rates of the tested materials in the initial stage decrease with increasing time, and it keep approximately constant after 96 h. The composition of corrosion products is basically same during the whole experimental period, whereas the morphology of corrosion products changes. The main corrosion product of B25 and BZn15-17 is CuCl2��2H2O. And the main corrosion product of HSn72-1-1 is CuCl, subordination is CuCl2��2H2O and (CuZn)2(OH)3 Cl.
Keyword��
copper alloys; composite materials; corrosion behavior; NaCl salt spray;
Received�� 2003-09-02
ͭ����Ͻ���������ĵ��硢 ���ȡ� ��ʴ������, �ڹ��ý��������Ź㷺��Ӧ�á� 20����90�����, �ҹ�ͭ��������Ͷ��ʹ��, �����Ź���������ֵ���������, ͭ�Ͻ����ҹ��������ҵ�е�ʹ����Ҳ���������ӡ� Ŀǰ, ������һЩ��������ѹ㷺��չͭ����ϽDz�Ĵ�����ʴ�о�
����ʵ������á� ����˹����ٸ�ʴʵ��֮һ�� ���Ż�����ѧ�����ķ�չ�Լ��Թ�ҵ��Ʒ�ɿ���Ҫ������, ����ʵ���Ӧ�÷�ΧҲ�����㷺�� Ŀǰ, ����ʵ���Ѿ���չ�������л�Ϳ�㡢 ������֬�� ��������, ����Ԫ�����Լ���ȫװ��õ���̨�豸�Ժ����Դ�������Ӧ����, ��Ϊ��Ʒ����ʵ����Ŀ֮һ
1 ʵ��
1.1 ����ʵ��
ʵ�����Ϊ3��ͭ�Ͻ�3��ͭ�Ͻ�ֱ��봿�����ɵĸ��ϲ��ϡ� �ڴ�, ��1��6�Ŵ���6��ʵ�����, ����4�� 5�� 6�Ŵ���3��ͭ�Ͻ����, �仯ѧ�ɷ����1���С� 1�� 2�� 3�ŷֱ�Ϊ4�� 5�� 6�Ų����м�д����ĸ��ϲ���, ������Լ0.2 mm�� �����ߴ�Ϊ33.00 mm��(1.50��1.88)mm�� Ϊ��ʾ���ϲ�������ͭ�Ͻ�֮��Ľṹ��ϵ, ȡ���ϲ��������Ķ���, ĥ�Ƴɽ�������, ���������˫��ˮ��Һ��ʴ(��Ҫ�ǽ�ʴͭ�Ͻ�), ���Ͻṹ��ͼ1��ʾ�� ���Կ���, ����������ͭ�Ͻ�, �м������㡣 ǰ������360��ɰֽ��ĥ�� ��ϴ, ��ͭ����, ���ø�������24 h��, ���������� ��������������ˮ1��1���Һȥ����ʴ��� ÿ�ֲ���ÿ����3Ƭƽ������, ��GB/T 10125-1997
��1 3��ͭ�Ͻ�Ļ�ѧ�ɷ�
Table 1 Chemical composition ofthree kinds of copper alloys(mass fraction, %)
| Samples No. | Alloy | Cu | Ni | Zn | Other |
| 4 | B25 | 75 | 25 | - | - |
| 5 | BZn15-17 | 68 | 15 | 17 | - |
| 6 | HSn72-1-1 | 72 | 1 | 26 | 1 |
1.2 ��żʵ��
������¶�ߴ�Ϊ10 mm��10 mm, ���溸�ӵ��ߺ�, �û�����֬�ܷ⡣ �������Ϸֱ�ΪB25�� BZn15-17�� HSn72-1-1��Ni�� ��3%�Ȼ�����Һ�в�����λ��ʱ������, ��αȵ缫Ϊ���ʹ��缫�� ��B25�� BZn15-17�� HSn72-1-1�ֱ��Ni��ɵ�ż��, ��3%�Ȼ�����Һ�в�����ż������ʱ�����ߡ�
2 ���������
2.1 ��ʴ����
ͼ1 ���ϲ��������Ķ�����ò
Fig.1 Microstructure of cross surface of composites
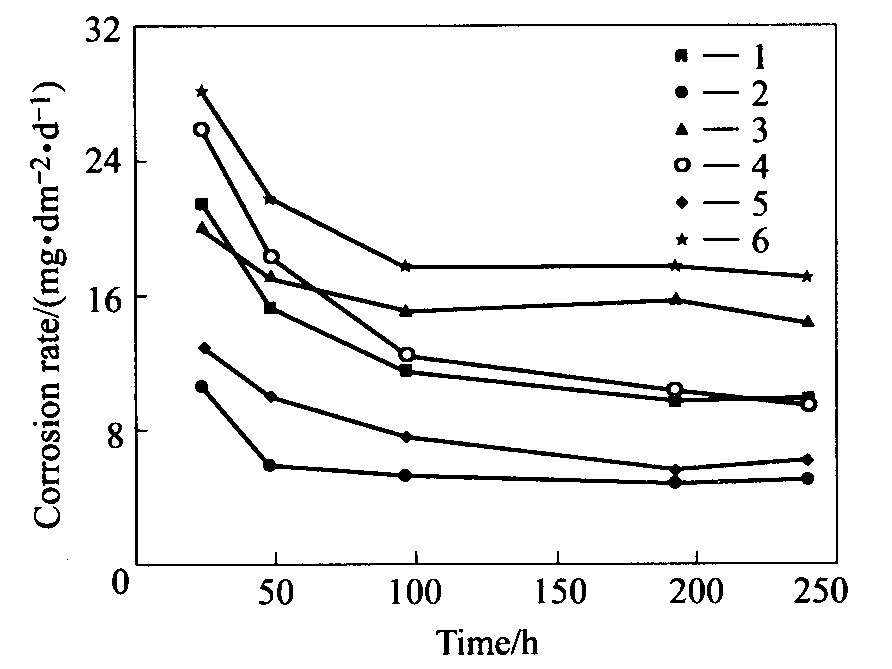
ͼ2��ʾΪ6�ֲ����ڲ�ͬʵ��ʱ���ڵ�ƽ����ʴ�ٶȡ� �ɴ˿�֪: 6�ֲ��ϵĸ�ʴ�ٶȾ��ڳ���ʱ��, ��������ʵ��ʱ����ӳ�����˥��, ����������������γɵľ���һ���������õ�ͭ���й�
ͼ2 ʵ����ϵ�ƽ����ʴ�ٶ���ʱ��ı仯
Fig.2 Change of average corrosion rates of tested materials with time
2.2 ��ż��
ͼ3��ʾΪ4��������3%�Ȼ�����Һ�еĵ�λ��ʱ�����ߡ� ��ͼ�п��Կ���, ��3%���Ȼ�����Һ��, ���ǵĵ�ż���������Ϊ: B25�� HSn72-1-1�� BZn15-17�� Ni, �����ڻ̬�� ����Խ���3��ͭ�Ͻ�ֱ��봿�����Ϻ����ʴ����Ӧ���������, ��Ϊ���ϲ��������м�Ĵ������������¶�ڸ�ʴ�����е�, ����һ����������������, ����, �������㼫��, �ټ��ϸ�ʴ���︲��, �������������� ������ѧ����˵, 2�ֽ�����3%�Ȼ�����Һ�����ż��ʱ, ���ߵĿ�·��λ��Խ��, ��ʴ�ƶ���ҲԽ��, ����ʵ�ʲ�õĽ��(ͼ4)���ɵ�ż����жϲ�����ȫһ�¡� ��B25�� BZn15-17�� HSn72-1-1�ֱ���Ni��ɵ�ż��ʱ, ����BZn15-17��Ni���ż�Եĵ�ż�����Ĵ�С���ż����жϻ���������һ��, ����ʴ�ƶ�����С, ��ż����Ҳ��С�� ��ͼ3Ҳ�����ж�, ��2�ְ�ͭ�Ͻ�(B25�� BZn15-17)�ֱ����ͭ�Ͻ�(HSn72-1-1)���ż��ʱ, ����֮���λ���С, ˵������֮��ĵ�ż��ʴ����С�����Ժ��Եij̶ȡ� ���õ�ż�����жϽ�����ż���еļ��Ժ�ʴ����ʱ, ��������������ѧ����Ԥ�ڸ�ʴ�����ķ�����ȶ���, ��û���漰����ѧ�����⡣
ͼ3 4��������3%�Ȼ�����Һ�е� ��λ��ʱ������
Fig.3 Potential��time curves of four kinds of materials in 3%NaCl solution
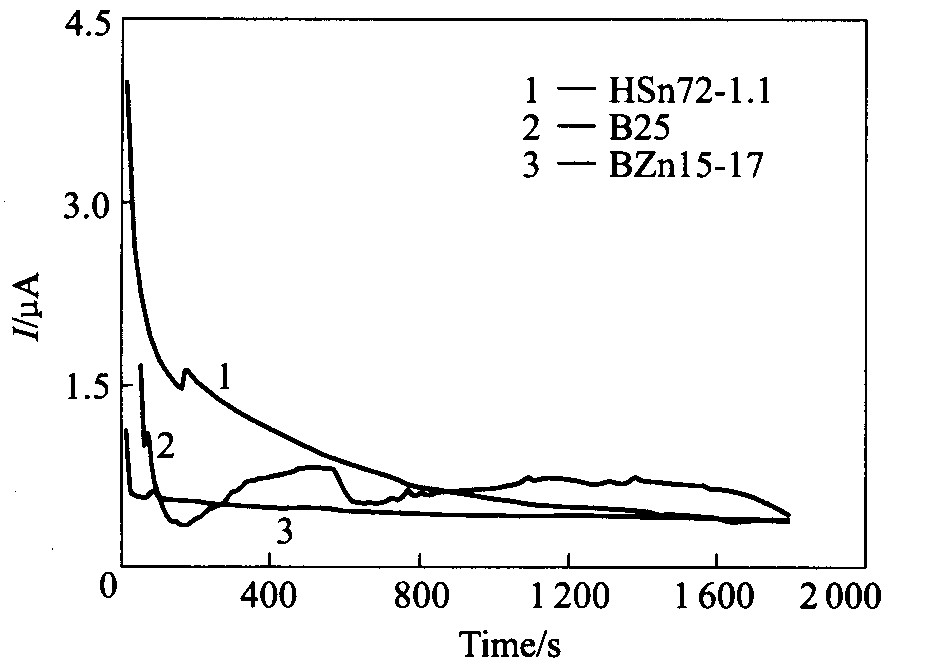
ͼ4 3��ż����3%�Ȼ�����Һ�е� ��ż������ʱ������
Fig.4 Galvanic current��time curves of three kinds of copper alloys coupled with nickel in 3%NaCl solution
2.3 ��ʴ�������
�����ձ���ѧD/MAX-RB��X���������Ƕ�6�ֲ�������ʵ��24 h��240 h�ĸ�ʴ������з����� ����ʵ��240 h�IJ��ֽ����ͼ5��ʾ�� ��֪1�� 2����������Ҫ��ʴ���ﶼ��CuCl2��2H2O,��3����������Ҫ��ʴ����ΪCuCl, ���ΪCuCl2��2H2O��(CuZn)2(OH)3Cl; 4�� 5�� 6����������Ҫ��ʴ����ֱ���1�� 2�� 3�ŵ���ͬ�� 24 h��240 h����ʵ�鸯ʴ����, ������Ժ��������в��졣
ͼ5 3�ֲ��ϸ�ʴ����X����������
Fig.5 XRD patterns of corrosion products of three kinds of tested materials (a)��Sample 1; (b)��Sample 2; (c)��Sample 3
�Ӻ�۹۲�, 6�ֲ��ϵĸ�ʴ�̶Ⱦ�����ʵ��ʱ����ӳ�������, ��������������ʧ�� ��ɫ�� ����, ��ʴ���������ӡ� 1�� 2�� 4�� 5��4�ֲ��ϵ�����������ֱ�ɫ�� ������ ��ʴ�ߵ�, ���ո�ʴ�ߵ�û�в�����������, ��ɫΪdz��ɫ; 3�ź�6����������Ͼ��ȵر�ɫ, ����Ϊ����ɫ, ��ʴ������Ȳ�������, ������4�ֲ��ϸ�ʴ���ء� ͭ�Ͻ���������Ӧ�ĸ��ϲ��ϲ�� �����ձ�����EP300����̽���1�� 2�� 3�Ž�������ʵ��24 h��240 h�ĸ�ʴ������ò����Ԫ�طֲ����з���, �����ͼ6��ͼ7��ʾ�� ���Կ���, 3��ͭ�Ͻ�ĸ�ʴ��ò��һ���IJ���, 3�ŵĸ�ʴ���Ա�����2�ֵ�����; ����ʵ��ʱ����ӳ�, ���港ʴ������ۻ�����������(ͼ6(b), (d), (f)), ����Ԫ����ֲ���֪�ȵĺ���Ҳ����Ϊ������(ͼ7)�� ��ʵ�����(ͼ6(a), (c), (e))�����ɼ���������ļӹ���ǰ�����ĺۼ���
��������������ຬ�Ȼ���СҺ������ɵ���ɢϵͳ, ��ʵ����ϴ��ڸû�����ʱ, ���������������γ�һ��ܱ��ĺ������Ȼ��Ƶ�ˮĤ, �����Ե绯ѧ��ʴ��ʽ����
������Ӧ: ������ˮ�����ӵ���ʽ������Һ, ���ѵ������ڽ�����, ���Ӵ�������������, ��:
Cu��Cu2+(��Cu+)+2e
ͼ6 ʵ����ںͺ��ڵĸ�ʴ��ò
Fig.6 Morphologies of corroded surfaces of different materials at different stages (a)��Sample 1, 24 h; (b)��Sample 1, 240 h; (c)��Sample 2, 24 h; (d)��Sample 2, 240 h; (e)��Sample 3, 24 h; (f)��Sample 3, 240 h
ͼ7 ʵ����ںͺ���B25�����������Ԫ�طֲ�
Fig.7 Surface distribution of Cl on alloy B25 at different stages (a)��24 h; (b)��240 h
Cu2++2H2O��Cu2+��2H2O
��
Cu+2H2O��Cu2+��2H2O+2e
������Ӧ: ��ͨ����ɢ��������������������ս����е�ʣ����Ӷ��γ�����������, ��:
1/2O2+H2O+2e��2OH-
�Ȼ������, ͬʱ�γɸ�ʴ����, ��
Cu2+��2H2O+2Cl-��CuCl2��2H2O
��
Cu++Cl-��CuCl
�ɴ˿ɼ�, ��������Һ�е������ż���Ҫ�����á� �����ŵ���������, �Խ���������������, ֻ�г����ڽ���������, �γɵ��ҺĤʱ�ŶԽ���������ʴ�� ����������������, ����������ʵ���ڼ�����������������������һ�µĵ��ҺĤ�� ʵ�����, ʵ����Ʒ��ȫ��¶, ��������ͨ����ɢ����������������, ��ʴ�ٶȽϿ�; ����ʵ��ʱ����ӳ�, �������港ʴ������ۻ���������, ��ʴ�ܵ�һ�����谭, ��ʴ�ٶȽ��͡� ����, һ��ʱ���Ժ�ʴ�ٶȻ������ٱ仯, �������������ӵİ뾶��С, ������ǿ, �����״�����������ĸ�ʴ�����, �����ڲ������ʴ, �����γ����ܽ�Ľ����Ȼ���, ���մﵽһ�ֶ�̬ƽ��, �Ի���һ���ĸ�ʴ�ٶȽ��С� ��������ͭ��ͭ�Ͻ��ڴ����еĸ�ʴ����, ����ʴ�ٶȴﵽ�ȶ�����Ҫ��ʱ�䳤��ȡ���ڲ���������ʵ�黷������
3 ����
1)
��ʵ�����ʵ����ϵĸ�ʴ�ٶȾ�����ʵ��ʱ���ӳ�������, ��Լ96h�Ժ�ʴ�ٶȻ�����������ʱ����ӳ����仯��
2) ʵ����ںͺ��ڵĸ�ʴ������ɻ�����ͬ:
2�ְ�ͭ�Ͻ����Ҫ��ʴ���ﶼ��CuCl2��2H2O, ��ͭ�Ͻ����Ҫ��ʴ����ΪCuCl, ���ΪCuCl2��2H2O��(CuZn)2(OH)3Cl, ��ʴ��ò�нϴ�ı仯��
3) 3��ͭ�Ͻ����ʴ˳��Ϊ:
BZn15-17�� B25�� HSn72-1-1, �봿�����Ϻ����ʴ˳��û��, ������ʴ������Ӧ�������, ��ʴ����õ�ΪBZn15-17�봿���ĸ��ϲ��ϡ�
�����
[4] ��Knotkova,BosekB,VlickovaJ.CorrosioninNaturalEnvironments,WestConshohocken[M].PA:ASTM,1974.52.
[5] ��CostasLP.AtmosphericCorrosionofCopperAlloysExposedfor15to20years[M].PA:ASTM,1982.106115.
[6] ��SantonB.TestingandprotectionofthenewUScoin[J].MaterialsPerformance,2000,39(5):2123.
[7] ��ISO9227 1990,Corrosiontestsinartificialatmospheressaltspraytests[S].
[4] ��Knotkova,BosekB,VlickovaJ.CorrosioninNaturalEnvironments,WestConshohocken[M].PA:ASTM,1974.52.
[5] ��CostasLP.AtmosphericCorrosionofCopperAlloysExposedfor15to20years[M].PA:ASTM,1982.106115.
[6] ��SantonB.TestingandprotectionofthenewUScoin[J].MaterialsPerformance,2000,39(5):2123.
[7] ��ISO9227 1990,Corrosiontestsinartificialatmospheressaltspraytests[S].