���±�ţ�1004-0609(2011)07-1728-06
��ת����̶Ժ��������Ȼ�������Ӱ��
���º�, ������, ������, ��־��
(���ϴ�ѧ ұ���ѧ�빤��ѧԺ����ɳ 410083)
ժ Ҫ�����Ȼ���CaCl2��2H2O�ļ�����Ϊԭ��������8%(���ȼ�)����ԭ����̿������Ϊԭ��������6%����������Ϊ5 ��/min�������£��Է��ɱ�������������Ȼ�����������TG-DTA��XRD�о����ɱ����������Ȼ�����������1 000 �漰��ȴ�����е�����ת�䡣������������������е�����������700 �濪ʼ��������ʯ�У��γɸ������ʯ�࣬�ƻ�����ʯ�ľ���ṹ��������Ļ��ԣ������������Ȼ������������Ȼ������ͷŵ��ȳ�Ϊ��Ǩ�Ƶ�ý�飻��ȴ����������û�з������Ա仯����������Fe3O4�ļ�����Ϊԭ���10%(��������)ʱ������������Ʒλ�ﵽ13.14%�������ʴﵽ80.12%����δ��Fe3O4ʱ�Ļ����������Լ10%��
�ؼ��ʣ�
�����������Ȼ�����������ת�������������
��ͼ����ţ�TD95���� ���ױ�־�룺A
Effect of phase transformation on
chloridizing segregation of laterite ores
LI Xin-hai, ZHANG Lian-xin, HU Qi-yang, WANG Zhi-xing
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: Under conditions of chlorinating agent dosage (CaCl2��2H2O) of 8% (vs mass of raw ore), reductant dosage of 6%(vs mass of raw ore) and heating rate of 5 ��/min, the chloridizing segregation of nickel laterite ores from Philippines was carried out, and the phase transformation of chloridizing segregation of nickel laterite ores at temperatures up to1 000 �� and the phase reversibility with cooling were investigated by TG-DTA and XRD. The results show that the Fe-rich forsterite is formed with the ferrous oxide entering into the serpentine at 700 ��. Therefore, the lattice structure of serpentine is failure, which is beneficial to chloridizing segregation, since the activity of Ni is enhanced, and the chlorine that is released from chlorinating agent acts as the medium of the transfer of iron. The phase is not changed obviously in the cooling process. When Fe3O4 adding in the raw materials is 10% (mass fraction), the grade in the concentrate of Ni reaches 13.14%, and the recovery achieves 80.12%, which increases by 10% compared with that without adding Fe3O4.
Key words: nickel laterite ores; chloridizing segregation; phase transformation; phase control
����������Ԫ�أ��ؿ���������0.008%(��������)������֪Ԫ�صĵ�24λ���ڵؿ����������ں���������������У����⣬��̽����Ҳ����һ��������[1]��������������ռ��������70%����ȻĿǰ��������Ȼ��������Ҫ��Դ���������Ÿ�Ʒλ������ļ��٣�Խ��Խ����˿�ʼ�о�����������ȡ���Ĺ���[2-3]��Ŀǰ����Լ��������չ����Ҫ�����ǹ��ղ����죬��������ijɷָ��ӡ���䣬������������о��Ƚ��ѷ�����ˣ��Ժ���������л����о��DZ�Ҫ�ġ�
�����������ǶԺ���������Ȼ��������̽�����������о���MA��PICKLES[4]��USLU��[5]�о���������������ȡ�LIU��[6]�о�����¯���ȹ����и��������籺���¶ȡ�����ʱ�䡢�Ȼ������ࡢ�Ȼ�����������ԭ������ͻ�ԭ�������ȶԺ��������Ȼ�������Ӱ�죬��δ�Ժ��������Ȼ��������̵�����仯�����о�������VALIX��CHEUNG[7]��LI��[8]��CHANG��[9]�Ժ��������ڻ�ԭ�����е�����仯�������о�����RHAMDHANI��[10-11]�о��˺��������ڻ�ԭ�����±��պ����Ľṹ������仯����Ӧ����ѧ�����Ժ���������Ȼ������������������Ϊ���Ȼ����������У��ȶ���������Ǩ������������Ҫ�����á�Ϊ�ˣ��������߲���TG-DTA��XRD�������о����ɱ����������Ȼ��������̵�����仯���������������������е����á��������Ӽ��������������̵�����仯����ȡ����ѵ�����Ч����
1 ʵ��
��ʵ�����ú�������Ϊ��������ʯ���̼��þ��ĸ߹衢��þ���������������仯ѧ�ɷּ���1��XRD������������ͼ1�� ԭ������Ϊ0.12~0.15 mm���Ȼ�������CaCl2��2H2O ����Ϊԭ��������8%(���ȼ�)����ԭ����������Ϊ0.18~0.25 mm�Ľ�̿��������Ϊԭ��������6%��
����ʵ������ͼ2��ʾ�Ĺ�ʽ¯�н��С�������0.1 L/min�����������ʽ¯������ۡ��Ȼ����ͻ�ԭ����Ͼ��ȣ���������ˮ����õ�����ֱ��Ϊ15~20 mm�����ϡ������Ϸ������ۺ��ٽ����۷����ʽ¯���룬Ȼ����5 ��/min��������������ָ���¶Ⱥ�Ѹ��ȡ��ˮ�㡣�Ա��յ���ͬ�¶ȵ����Ͻ���XRD���������
��1 ��������Ļ�ѧ�ɷ�
Table 1 Chemical composition of nickel laterite ores (mass fraction, %)

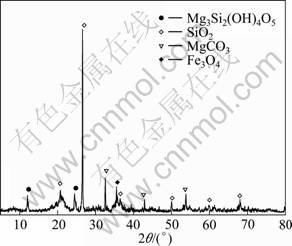
ͼ1 ���������XRD��
Fig.1 XRD pattern of nickel laterite ores
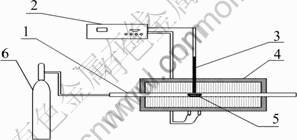
ͼ2 ����ʵ��װ��ͼ
Fig.2 Schematic diagram of roasting equipment: 1��Corundum tube; 2��Temperature control instrument; 3��Thermocouple; 4��Electric heat furnace; 5��Porcelain combustion boat; 6��Nitrogen steel bottle
�Ȼ�����ʵ�������Ȼ���CaCl2��2H2O�ļ�����Ϊԭ��������8%(���ȼ�)����ԭ����̿�ļ�����Ϊԭ��������6%���������Ӽ���ˮ��Ͼ�������õ����ϡ���5 ��/min�������ʽ���Ʒ���µ�1 000 �棬��1 000 �����60 min��ȡ��ˮ��ʪĥ��ɸ������Ϊ0.038~0.048 mm��Ȼ��0.3 T��ѡ�õ������β��ͨ����ѧ�����õ������β��������Ʒλ������� ���ʡ�
2 ���������
ԭ����CaCl2��6H2O(���ȼƣ�����Ϊԭ��������8%)�뽹̿(����Ϊԭ��������6%)��Ͼ������ϵ�TG-DTA������ͼ3��ʾ����ͼ3�ɼ���ԭ���DTA������77.92��275.42��543.44��641.09 �洦����4�����ȷ塣77.92 �洦�����շ��Ӧ����ˮ���ѳ���275.42 �洦�����շ��Ӧ������ˮ���ѳ���543.44 �洦�����շ�Դ��̼��þ�ķֽ⣻641.09 �洦�����շ����ǻ�����þ��ˮ�ֽ����¡�������������������Ӧ��
CaCl2��6H2O=CaCl2��2H2O+4H2O (30~80 ��) (1)
CaCl2��2H2O=CaCl2+2H2O (200~260 ��) (2)
������DTA������77.80 ����275.78 �洦�ķ���ԭ��ķ�������ǿ���������Ӧ��TG������������ʧҲ�������ӡ�ԭ������543.44 ��̼��þ�ķֽ�壬����Ͽ�����493.00 ��ͽ����ˣ�����Ҫ�������Ȼ��Ƶļ����̼��þ�ķֽ�����һ���Ĵٽ����á�
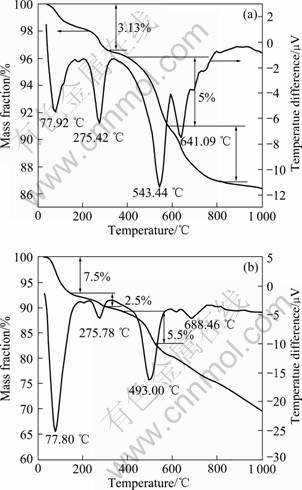
ͼ3 ԭ������ϵ�TG-DTA����
Fig.3 TG-DTA curves of raw ores(a) and raw materials(b)
�ڵ������������£����¹����к��������ڲ�ͬ�¶��µ�����仯��ͼ4��ʾ����ͼ4��֪��ԭ�����Ҫ����ΪʯӢ������ʯ���������̼��þ�����¶�Ϊ400~600 �棬̼��þ�ֽ⣻���¶�Ϊ600~700 ��ʱ������ʯ��ֽ���ʧ���γɸ����������ʯ�࣬���ڼ�������Ȼ��Ƶķֽ��Fe3O4����ʧ�������¶ȵļ������ߣ������Ƶ����ʯ�������࣬����Ҳ����������SiO2��ĺ������͡������¶����ߵ�800~900 ��ʱ������ʯӢ��(����)ת��Ϊ����ʯӢ��(����)[12-13]�����SiO2����2��=20���2��=40�㴦��ֵ���ߡ�
���¹����к��������ڲ�ͬ�¶��µ�����仯��ͼ5��ʾ��ͼ5�зֱ�Ϊ1 000 ��(1 000 �棬(a))��1 000 �����60 min(1 000 �棬(b))�����µ�900��800��700 ��ʱ���ϵ�XRD�ס���ͼ5���Կ������ڽ��¹����У���������Ŀ��ಢû�з������Ըı䣬���ԣ����������Ȼ������Ĺ����Dz�������̣��ڽ��¹������������ȶ��ġ���ֵ��ע����ǣ�������ƽ��¹��̵�����Ϊ����ԭ�����գ���ֹ�����Ͻ����������
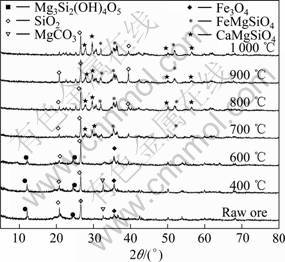
ͼ4 ���¹������Ȼ��������������XRD��
Fig.4 XRD patterns of chloridizing segregation of nickel laterite ores during temperature increase process
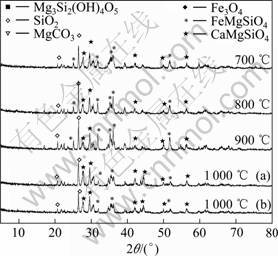
ͼ5 ���¹������Ȼ��������������XRD��
Fig.5 XRD patterns of chloridizing segregation of nickel laterite ores during temperature decrease process
��Ȼ���������Ȼ�������Ŀ�����������������Ϊ���Ļ��Ա����ĸߣ���ʯ������������������10~30������ˣ��о��������̱��뿼�����������������Ϸ�����֪�������������������ϵ�����仯������Ҫ�����ã���Ӧ����ʽ���£�
�������¶ȵ���560 ��ʱ������ת�����ط� ӦΪ
Mg3Si2(OH)4O5(s)=Mg3Si2O7(s)+2H2O(g) (3)
CaCl2(s) +H2O(g)+SiO2(s)=CaSiO3(s)+2HCl(g) (4)
CaCl2(s) +H2O(g)=CaO(s)+2HCl(g) (5)
Fe����ķ�ӦΪ
Fe3O4(s)+8HCl(g)=FeCl2(s)+2FeCl3(s)+4H2O(g) (6)
2FeCl3(s)![]() 2FeCl3(g)
2FeCl3(g)![]() Fe2Cl6(g) (7)
Fe2Cl6(g) (7)
Fe2Cl6(g)+2H2O(g)=2FeOCl(s)+4HCl(g) (8)
6FeOCl(s)+3H2O(g)+CO(g)=2Fe3O4(s)+
6HCl(g)+CO2(g) (9)
�������¶ȸ���560 �棬����ת�����ط�ӦΪ
Mg3Si2O7(s)+3FeO(s)+SiO2(s)=3(Mg,Fe)SiO4(s) (10)
Mg3Si2O7(s)+3CaO(s)+SiO2(s)=3(Mg,Ca)SiO4(s) (11)
Fe����ķ�ӦΪ
FeCl2(g)+H2O(g)=FeO(s)+2HCl(g) (12)
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) (13)
��ˮ���������£�CaCl2��550 ����SiO2��Ӧ����HCl[15]�����ǻ�����þ��ˮ��Ϊ���������Ȼ���Ǩ���ṩˮ���Ȼ��⡣��Ȼ���ڵ��·�Ӧ�����з���Fe3O4�� FeCl2 (FeCl3) ��Fe3O4ѭ�������ǣ�Fe3O4��λ�÷����˱仯�����ǻ�����þ����Ǩ�ƣ��������ɵ�Fe3O4��¶�ڿ�ʯ���棬���Խϸߣ������ױ���ԭ��FeO���Ӷ��ٽ�FeO�����þ��Ӧ���ɸ������ʯ�ࡣ����þ������ƻ��������Ƕ�ڹ���þ�����Ļ��ԣ���������һ��������[14]��
ͨ������ʵ�鼰���۷�����֪���ں��������Ȼ����������������ż�Ϊ��Ҫ�����ã�ͨ���������������þ��Ӧ���ɸ������ʯ���������ʯ�������Ļ��ԡ�Ϊ����ߵ�������þ��ʯ�������Ʒλ�ͻ����ʣ����������ں��������зֱ�����Fe3O4��Fe��,�����Ȼ����������е�����仯�������ɸ���ĸ������ʯ��Fe3O4�ļ������ֱ�Ϊԭ��������0��5%��10%��15%��20% ��25%�����۵ļ������ֱ�Ϊԭ��������0��0.1%��0.2%��0.3%��0.4%��0.6%��0.8% ��1.0%����������-��ѡ������Ʒλ�ͻ�������ͼ6 ��ʾ��
��ͼ6���Կ���������Fe3O4��������0���ӵ�25%����������Ʒλ�����Ӻͣ����Ļ����ʾ���ͬ���Ĺ��ɣ����ǣ������ʽ��͵ķ��ȱȽ�С������Ҫ����ΪFe3O4���Ȼ�Ǩ�ƺ���ԭΪ���������������þ�ľ���ʹ���Ļ������ߣ��Ӷ�ʹ����ʯ�е������Ȼ���������һ���Ļ��ԣ����ܱ��Ȼ�������ѡ�����ǣ�����Fe3O4���������ӣ�����ԭ���������������ӣ�����һ�𱻴�ѡ�����ԣ���������Ʒλ���������Ӷ����ͣ����ǣ��������Ļ����ʲ�û�����ԵĽ��ͣ���Ϊ�����ʽ��͵���Ҫԭ������������ʹ���������Ͻ�ճ���ڹ����α��棬��δ����ѡ��
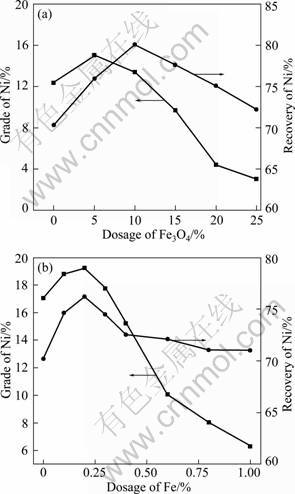
ͼ6 Fe3O4��Fe�۵ļ�����������Ʒλ�ͻ����ʵ�Ӱ��
Fig.6 Effect of dosages of Fe3O4 (a) and Fe (b) powders on grade and recovery of Ni
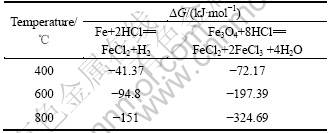
�Ա�ͼ6(a)��(b)���֣���Fe3O4�������Ϊ10%ʱ��������ѡ��������ƷλΪ13.14%�����Ļ����ʴﵽ���ֵ80.12%������Fe�۵ļ�����Ϊ0.2%ʱ��������ѡ��������ƷλΪ19.21%�����Ļ����ʴﵽ���ֵ76.23%������������������������ױ��Ȼ���Ǩ�ƣ�����������ߵĴٽ����ø�����������ͬ�¶���Fe��Fe3O4��HCl���巴Ӧ�ļ���˹�����ܼ� ��2��
��ԭ����������Ϊ0.12~0.15 mm���Ȼ���Ϊ�Ȼ��ơ��Ȼ����������ȼ���Ϊԭ��������10%����ԭ����̿����Ϊԭ��������8%������Ϊ0.18~0.25 mm��Fe3O4�ļ�����Ϊԭ��������10%�������¶�Ϊ1 000 �棬����ʱ��Ϊ60 min����ɰ��ѡ����Ϊ0.038~0.048 mm���ų�ǿ��Ϊ0.3 T����������£����ú����������β���XRD����ͼ7��ʾ����ͼ7���Կ������������Ҫ����ΪFe��NiFe��(Mg0.39Fe0.52Ca0.09)SiO3��(Fe1.04Mg0.94)SiO4��β�����Ҫ����ΪSiO2��Fe��(Mg0.39Fe0.52Ca0.09)SiO3��(Fe1.04Mg0.94)SiO4�����ڲ������������Ͻ������ʯճ����һ������ĥ������û�а�����ȫ����ˣ���������Ȼ���зǴ��Ե�(Mg0.39Fe0.52Ca0.09)SiO3��(Fe1.04Mg0.94)SiO4��
��2 ��ͬ�¶���Fe��Fe3O4��HCl���巴Ӧ�ļ���˹������
Table 2 Gibbs free energies for reactions between Fe or Fe3O4 and HCl

ͼ7 ���������º����������β���XRD��
Fig.7 XRD patterns of nickel laterites concentrate(a) and tailing (b) under optimal conditions
3 ����
1) FeO��700 �濪ʼ�������þ�����γɸ������ʯ�࣬����þԭ�еľ���ṹ���ƻ����Ӷ��������Ƕ�ڹ���þ���������Ļ��ԺͿ������ȡ�
2) �Ȼ���CaCl2���ͷŵ�����Ϊ��Ǩ�Ƶ�ý�飬���Ȼ����������дٽ�FeO��Ǩ�ƣ��Ӷ��ٽ�FeO�����þ��Ӧ���ɸ������ʯ�ࡣ
3) Fe3O4��Fe�۸������Ȼ�������Ǩ�ơ���Fe3O4�ļ�����Ϊԭ��������10%ʱ���Ȼ�����-��ѡ���þ���������ƷλΪ13.14%�����Ļ�����Ϊ80.12%�������δ����Fe3O4�Ȼ����������Ļ����������Լ10%��
REFERENCES
[1] LUO W, FENG Q M, OU L M, LU Y P,ZHANG G F. A comprehensive study of atmospheric pressure leaching of saprolitic laterites in acidic media [J]. Mineral Processing and Extractive Metallurgy, 2009, 118(2): 109-113.
[2] WEI L, QIMING F, LEMING O, GUOFAN Z, YIPING L. Fast dissolution of nickel from a lizardite-rich saprolitic laterite by sulphuric acid at atmospheric pressure[J]. Hydrometallurgy, 2008, 96(1/2): 171-175.
[3] ZHAI Yu-chun, MU Wen-ning, LIU Yan, XU Qian. A green rocess for recovering nickel from nickeliferous laterite ores[J]. Transactions of Nonferrous Metals Society of China, 2010, 20(1): 65-70.
[4] MA J, PICKLES C A. Microwave segregation process for nickeliferous silicate laterites[J]. Canadian Metallurgical Quarterly, 2003, 42(3): 313-325.
[5] USLU T, ATALAY U, AROL A I. Effect of microwave heating on magnetic separation of pyrite[J]. Colloids and Surfaces A: Physicochem Eng, 2003, 225: 161-167.
[6] LIU Wan-rong, LI Xin-hai, HU Qi-yang, WANG Zhi-xing, GU Ke-zhuan, LI Jin-hui, ZHANG Lian-xin. Pretreatment study on chloridizing segregation and magnetic separation of low-grade nickel laterites[J]. Transactions of Nonferrous Metals Society of China, 2010, 20(1): 82-86.
[7] VALIX M, CHEUNG W H. Study of phase transformation of laterites ores at high temperature [J]. Minerals Engineering, 2002, 15(8): 607-612.
[8] LI Jin-hui, LI Xin-hai, HU Qi-yang, WANG Zhi-xing, ZHOU You-yuan, ZHENG Jun-chao, LIU Wan-rong, LI Ling-jun. Effect of pre-roasting on leaching of laterite[J]. Hydrometallurgy, 2009, 99(1/2): 84-88.
[9] CHANG Yong-feng, ZHAI Xiu-jing, FU Yan, MA Lin-zhi, LI Bin-chuan, ZHANG Ting-an. Phase transformation in reductive roasting of laterite ore with microwave heating[J]. Transaction of Nonferrous Metals Society of China, 2008, 18(4): 969-973.
[10] RHAMDHANI M A, HAYES P C, JAK E. Nickel laterite (Part 1): Microstructure and phase characterizations during reduction roasting and leaching[J]. Transactions of the Institutions of Mining and Metallurgy, 2009, 118(3): 129-145.
[11] RHAMDHANI M A, HAYES P C, JAK E. Nickel laterite (Part 2): Thermodynamic analysis of phase characterizations during reduction roasting[J]. Transactions of the Institutions of Mining and Metallurgy, 2009, 118(3): 146-155.
[12] PICALES C A. Microwave heating behaviour of nickeliferous limonitic laterite ores [J]. Minerals Engineering, 2004, 17(6): 775-784.
[13] ���ĸ�, л��ɭ, ��־��, �� ��, �� ��. ��-��ʯӢ����Ӧ��������㼰���������[J]. �� ѹ �� �� ѧ ��, 2002, 16(4): 241-248.
ZHOU Wen-ge, XIE Hong-sen, ZHAO Zhi-dan, ZHOU Hui, GUO Jie. Calculation of the strain, stress and elastic energy for ��-�� quartz transition and its geological significance[J]. Chinese Journal of High Pressure Physics, 2004, 16(4): 241-248.
[14] ������, ��ѧ��, �����. ���Ͽ�ѧ����[M]. �人: �人������ѧ������, 2004: 497-498.
ZHANG Lian-meng, HUANG Xue-hui, SONG Xiao-lan. Fundamentals of materials science[M]. Wuhan: Wuhan University of Technology Press, 2004: 497-498.
[15] ASAKI K H, KONDO Z. Hydrolysis of fused calcium chloride at high temperature[J]. Metall Trans B: Process Metall1, 1978, 9(3): 477-483.
(�༭ ����Ƽ)
������Ŀ�������ص�����о���չ�ƻ�������Ŀ(2007CB613607)
�ո����ڣ�2010-06-18�������ڣ�2010-07-29
ͨ�����ߣ����º������ڣ���ʿ���绰��0731-88836633��E-mail: lianxin-zhang@126.com


