DOI: 10.11817/j.issn.1672-7207.2016.02.008
一锅法合成苯并噁唑类化合物
唐叶绿,杜宗波,江国防
(湖南大学 化学化工学院,湖南 长沙,410082)
摘要:以三氯氧磷(POCl3)为缩合剂,将邻氨基苯酚和羧酸在CHCl3中回流一锅法合成4个系列的2-烷基、2-芳基、2-苯乙烯基取代的苯并噁唑类化合物,并研究其可能的反应历程;通过考察反应过程中邻氨基苯酚和羧酸以及POCl3的物质的量比、羧酸的结构及活性、反应温度以及溶剂种类对目标化合物产率的影响,得到最佳的反应条件参数,并对目标化合物进行1HNMR和MS表征。研究结果表明:邻氨基苯酚和羧酸以及POCl3的物质的量比、羧酸的结构及活性对苯并噁唑的产率影响比较大;当温度达到或超过60 ℃时,所选的溶剂对其产率的影响比较小;2-烷基取代苯并噁唑的产率整体比2-芳基和2-苯乙烯基取代的苯并噁唑产率高;该方法是一种简便、高效的合成2-取代苯并噁唑类化合物的方法。
关键词:苯并噁唑;邻氨基苯酚;三氯氧磷;合成
中图分类号:O621.3 文献标志码:A 文章编号:1672-7207(2016)02-0408-06
A one-pot synthetic route to substituted benzoxazoles
TANG Yelü, DU Zongbo, JIANG Guofang
(College of Chemistry and Chemical Engineering, Hunan University, Changsha 410082, China)
Abstract: Aliphatic acids, aromatic acids and β-aryl-α,β-unsaturated acids were selected to react with o-aminophenol in the presence of phosphorus oxytrichloride (POCl3) in refluxing CHCl3 to afford four series of 2-alkyl,2-aryl and 2-styryl benzoxazoles,respectively, and a possible reaction mechanism for their synthesis was proposed. The reaction conditions including the molar ratio of substrates and POCl3, the structure and activity of carboxylic acid, the reaction temperature and the different solvents were optimized. All the structures of the target products were confirmed by 1HNMR and MS.The results show that the molar ratio of substrates and the different carboxylic acid structures play an important role in the yields of benzoxazoles. The impact of the selected solvent on yield is relatively small when the reaction temperature equals or surpasses 60 ℃. The yields of 2-alkyl substituted benzoxazoles are significantly higher than those of 2-phenyl and 2-styryl substituted benzoxazoles. The method is concise and efficient for the synthesis of 2-substituted benzoxazoles.
Key words: benzoxazole; o-aminophenol; phosphorus oxytrichloride; synthesis
苯并噁唑是一类是重要的杂环化合物,它具有抗炎、抗菌、抗肿瘤等多种生物活性,因而成为药物合成中重要的化学中间体[1-3]。苯并噁唑类化合物还具有较高的荧光量子产率而常被用于荧光增白剂和闪烁剂[4]。苯并噁唑类聚合物具有很强的耐热性和耐腐蚀性,可以被用作耐热材料[5]。鉴于苯并噁唑类化合物及其衍生物的用途广泛,其合成方法的研究也受到了化学工作者的广泛关注,近年来发展了一些合成苯并噁唑类化合物的方法[6]。通常苯并噁唑类化合物的合成路线是在较高温度下,利用邻氨基苯酚与醛或者羧酸及其衍生物在强酸如多聚磷酸(PPA)的作用下反应得到[7-9],或者是在微波辐射条件下发生成环反应[10]。该类反应需要强酸和较高温度(一般都高于100 ℃),甚至有些反应温度在450 ℃以上,反应条件较为苛刻。在催化剂的使用上,许多研究是利用重金属催化或是利用多聚磷酸催化[11-12],而多聚磷酸在加热时容易放出剧毒气体氧化磷,容易造成环境污染甚至对人体产生伤害,这些为反应的操作和处理带来了很大难度。此外,还有另一种合成苯并噁唑类化合物的方法是将邻二卤苯与酰胺或者是邻卤苯胺衍生物在金属Pd与Cu催化条件下发生偶联成环反应[13-15],该金属催化下的成环反应所用的催化剂是化学剂量的,其应用范围不广,产率偏低。利用邻氨基苯酚和羧酸为原料,以三氯甲烷为溶剂,在POCl3作用下发生成环反应,获得了一种简便、快速、高效的合成2-取代苯并噁唑类化合物的方法。反应温度是氯仿的回流温度62 ℃,相对于文献[12]报道的方法反应温度大大降低,同时所使用的试剂POCl3在反应过程中和后处理中不会产生有害物质,因而,此方法在合成苯并噁唑上有一定优势。利用该方法合成如图1所示的在2位和5位上含不同取代基团的4个系列苯并噁唑类化合物,共计22个目标化合物,并对其进行结构表征。
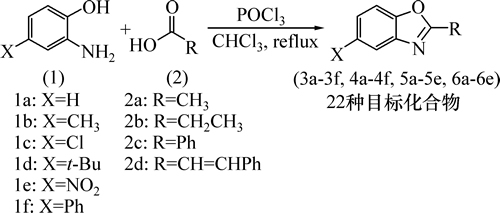
图1 苯并噁唑的合成
Fig. 1 Synthesis of benzoxazoles
1 实验
1.1 试剂与仪器
试剂为:邻氨基苯酚,分析级,上海山浦化工有限公司生产;2-氨基-4-氯苯酚,分析级,常州市恒瑞化工有限公司生产;2-氨基-4-甲基苯酚,分析级,浙江永泉化学有限公司生产;2-氨基-4-叔丁基苯酚,分析级,浙江永泉化学有限公司生产;2-氨基-4-硝基苯酚,分析级,石家庄市东胜化工厂生产;2-氨基-4-苯基苯酚,张家港康克国际贸易有限公司生产;三氯氧磷(POCl3),分析级,上海同方精细化工有限公司生产,重蒸后使用;氯仿(CHCl3),分析级,湖南师范大学化学试剂厂生产。其他试剂均为市售分析级或化学级,未经进一步处理。目标化合物的熔点采用XT-4双目显微熔点测定仪(北京泰克仪器有限公司)测定;核磁共振氢谱采用INOVA-400型核磁共振仪(美国Varian公司,TMS为内标)测定;质谱采用GCMS-QP2010型气质联用仪(日本岛津公司)测定。
1.2 目标化合物的合成
目标化合物(3a,见图1)的合成见图2。其过程为:在50 mL三颈瓶里加入邻氨基苯酚(1.09 g,10 mmol)和CHCl3 (10 mL),在搅拌下加入乙酸(0.86 mL,15 mmol),再加入POCl3 (2.76 mL,30 mmol),加热回流,TLC监测反应进程。反应结束后,冷至室温,在三颈瓶里加入少许碎冰和CHCl3 (10 mL),然后用5 mol/L NaOH溶液中和至反应液呈中性,分液,用CHCl3萃取(10 mL,萃取2次),合并有机相,用水洗涤(10 mL,萃取2次),再用饱和食盐水洗涤(10 mL),有机相用无水Na2SO4干燥,减压蒸出溶剂,将残余物进行硅胶柱层析分离,以CH2Cl2为洗脱剂,收集第1带,比移值Rf约为0.6。按照该方法还合成了另外21个目标化合物(见图1中3b~3f,4a~4e,5a~5e,6a~6e)。
2 结果和讨论
有机合成方法学的目标是反应条件温和、反应转化率高和选择性好。在最初的研究中,以10 mmol邻氨基苯酚(图1中1a)与10 mmol乙酸以及20 mmolPOCl3 在氯仿中回流2 h合成2-甲基苯并噁唑(见图2),反应进程由TLC实时监测。反应完成后,最终只得到产率为70%的2-甲基苯并噁唑。但此结果可足以证明邻氨基苯酚与羧酸可以在POCl3 的作用下有效地合成苯并噁唑类化合物。为了得到更好的反应结果,继续探索优化条件非常重要。
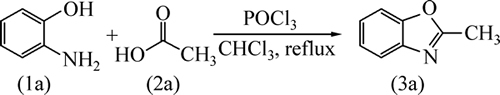
图2 2-甲基苯并噁唑(3a)的合成
Fig. 2 Synthesis of 2-methyl benzoxazole (3a)
2.1 反应历程
在研究优化条件之前,先对该反应历程进行研究。结合文献[16-19],该反应历程可能是首先由羧酸A在POCl3作用下转化为酰氯B,然后B在POCl3作用下与邻氨基苯酚反应生成化合物C,之后C经过环化反应,脱质子后生成目标化合物D,如图3所示。
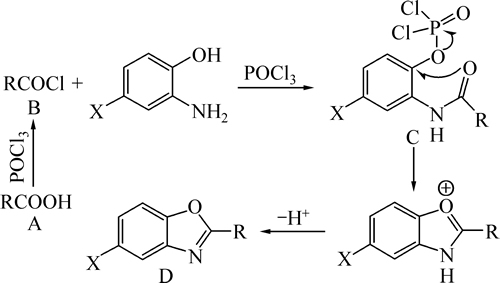
图3 合成苯并噁唑的可能反应历程
Fig. 3 Possible processes for synthesis of 2-substituted benzoxazoles
为了证明该反应历程,对2个反应进行研究:第1个反应是首先只让乙酸和POCl3反应0.5 h,此时乙酸已转化为乙酰氯,然后加入邻氨基苯酚,加热回流;第2个反应是直接利用乙酰氯和邻氨基苯酚在POCl3作用下发生反应,同样得到了目标化合物D。上述2个分步反应与同时加入乙酸、邻氨基苯酚和POCl3的反应结果是一致的。所以,可以认为该反应的历程是按照图3所示的历程进行的。
2.2 POCl3与羧酸的物质的量比对反应产率的影响
在反应过程中,羧酸首先转化成酰氯,再与邻氨基苯酚反应,然后成环。因此,在这个反应过程中,POCl3与羧酸的物质的量比会对目标化合物的产率造成较大影响。以合成2-甲基苯并噁唑为例,在不改变邻氨基苯酚的量的情况下,通过调节POCl3与乙酸的物质的量比进行实验。
根据反应历程(见图3),该反应过程中只有当氨基转化为酰胺时才能缩合,所以,应尽量使邻氨基苯酚转化为邻乙酰氨基苯酚。按照理论量计算,羧酸和邻氨基苯酚完全转化为苯并噁唑所需要的物质的量比即n(羧酸):n(邻氨基苯酚)应该是1:1,而POCl3所需要的量按照理论计算量应该是羧酸的2倍,因此,在第1次实验中,将邻氨基苯酚、乙酸和三氯氧磷三者物质的量比按照1:1:2在CHCl3中回流,反应至不再有HCl气体逸出时,TLC监测发现仍有部分邻氨基苯酚剩余。于是,继续增加羧酸的量,同时也按物质的量比增加POCl3的量,并将所得产物的产率进行比较,结果见表1。
表1 POCl3与羧酸的物质的量比对3a产率的影响
Table 1 Effect of POCl3 and carboxylic acid ratio on yield of 3a %
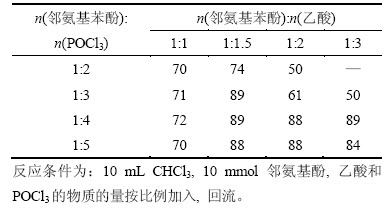
从表1可知:当邻氨基苯酚、乙酸的物质的量比为1:5,邻氨基苯酚、POCl3的物质的量比为1:3.0时获得的目标产物的产率达到最大,为89%;而后再继续增加其物质的量比时,2-甲基苯并噁唑的产率还是非常接近。所以,理想的邻氨基苯酚、乙酸的物质的量比为1:5,邻氨基苯酚、POCl3的物质的量比为1:3.0。
2.3 羧酸结构对反应产率的影响
将邻氨基苯酚与4种不同结构的羧酸在POCl3的作用下反应,得到的产率见表2。从表2可见:在利用乙酸和丙酸合成相应的化合物(3a和4a)的产率达到88%以上,而利用苯甲酸和肉桂酸合成相应的化合物(5a和6a)时的产率相对来说要低得多。产生这种现象的原因是羧酸首先生成酰氯,不同的酰氯的活性不一样,而苯甲酰氯和肉桂酰氯的活性相对乙酰氯和丙酰氯的活性低;此外,它们的羰基活性也较低,所以,
表2 不同羧酸的结构对反应产率的影响
Table 2 Effect of carboxylic acid structure on yield %

第2步成环时的效率比脂肪族羧酸的效率低。
2.4 不同溶剂和温度对反应产率的影响
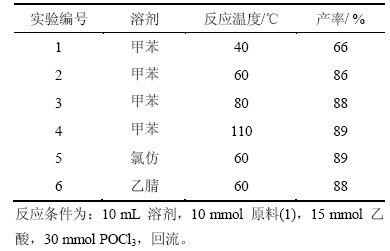
溶剂的沸点以及反应底物在溶剂中的溶解度会在一定程度上影响反应的进程和结果,因而,可以通过选用不同的溶剂研究其对反应所产生的影响。以合成2-甲基苯并噁唑为例,选用3种不同的溶剂即CHCl3,CH3CN和PhCH3,在反应过程中保持所需的温度恒定,得到的实验结果见表3。
由表3可知:当在40 ℃的甲苯中进行反应时,2-甲基苯并噁唑的产率相对较低,只有66%;当温度升至60 ℃时,产率达到86%;当温度高于60 ℃时,产率上升的幅度很小,在甲苯回流温度下反应也只得到89%的产率。因此,为了节约能源,最佳反应温度只需60 ℃即可。在确定好最佳温度后,对比不同溶剂下的反应结果。从表3可知:以60 ℃的CHCl3和CH3CN分别作溶剂的反应产率几乎与甲苯作溶剂的产率相当,并无太大变化,因此,可以确定溶剂对产物产率的影响比较小,主要影响因素还是邻氨基苯酚、乙酸和POCl3的物质的量比以及羧酸的结构。
表3 不同溶剂和温度对2-甲基苯并噁唑产率的影响
Table 3 Effect of reaction temperature and solvent on yield of 3a
由此可以认为选用CHCl3作为溶剂最合适,因为其沸点恰好是62 ℃,与最优温度非常接近。故只要选择其回流温度作为反应温度,就使得反应温度容易控制,且产率也最高。此条件最温和,节约能源,而且溶剂的沸点低,也使得反应的后处理比较简单。
2.5 苯并噁唑类化合物的合成
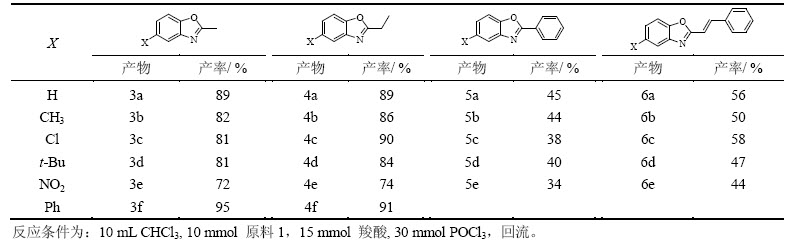
根据以上讨论,通过优化邻氨基酚与乙酸在POCl3中的反应条件,开发了一种合成2-取代苯并噁唑的新方法。其合成的最佳条件为邻氨基苯酚、乙酸、的物质的量比为 1.0:1.5,邻氨基酚、POCl3的物质的量比为1:3.0。以氯仿作溶剂回流反应。然后,在此优化条件下,考察不同结构的羧酸与含有不同取代基团的邻氨基酚反应(见图1)。所有实验步骤参照2-甲基苯并噁唑(3a)的合成进行,并获得较高的产率,实验结果见表4。
由表4可得:以不同取代的邻氨基苯酚和不同的羧酸为原料,CHCl3为溶剂,在POCl3作用下,2-烷基取代苯并噁唑(3a-3f和4a-4f)产率都非常高,其中除了X基团为NO2取代的苯并噁唑3e和4e的产率稍低(72%和74%)之外,其他的产率都高于81%,甚至在X被苯基取代时,3f产率达95%,4f的产率达91%。而2-苯基取代苯并噁唑(5a-5e)和2-苯乙烯基取代苯并噁唑(6a-6e)的产率明显比2-烷基苯并噁唑的产率低,即使通过延长反应时间或更换反应溶剂,或者再提高反应温度,依然没有能够使目标产物的产率得到明显提高。其原因可能是苯甲酰氯与肉桂酰氯的活性较低,而且位阻较大,导致在发生缩合反应时不能完全进行。
从表4还可看出:(6a-6e)的产率比(5a-5e)的产率要高。其原因可能是肉桂酰氯的活性稍高于苯甲酰氯的活性,由于苯环上碳链的增长,产生的酰氯位阻有所降低,使得其产率比2-苯基苯并噁唑的产率略高。因此,该方法对合成2-烷基取代的苯并噁唑是非常有效的。2-苯基和2-苯乙烯基取代的苯并噁唑的产率比2-烷基取代的苯并噁唑产率稍低,但该反应条件温和,简单操作,依然是一种可供选择的合成这类芳基取代苯并噁唑的方法。
表4 2-取代苯并噁唑类化合物的合成
Table 4 Synthesis of 2-substituted benzoxazole compounds
3 部分产物的结构表征
设δ为化学位移,J为耦合常数,d为单峰,m为多重峰,s为单峰,mp为熔点,t为三重峰,q为四重峰,dd为dd峰,m/z为质荷比。
1) 2-甲基苯并噁唑(3a),为黄色液体; 1H NMR (400 MHz, CDCl3)δ: 7.96 (d, J = 8.0 Hz, 1H, Ar-H),7.67 (d, J = 8.4 Hz, 1H, Ar-H), 7.47~7.55 (m, 2H, Ar-H), 2.56 (s, 3H, CH3); MS m/z (相对强度): 133 (M+, 100)。
2) 2-甲基-5-氯苯并噁唑(3c),为橙黄色固体; mp为54~55 ℃; 1H NMR (400 MHz, CDCl3) δ: 7.89 (d, J1=8.8 Hz,J2=1.6 Hz, 1H, Ar-H), 7.60 (d, J=8.8 Hz, 1H, Ar-H), 7.51 (dd, J=8.8, 1.6 Hz, 1H, Ar-H), 2.56 (s, 3H, CH3); MS m/z (相对强度): 167 (M+, 100)。
3) 2-乙基苯并噁唑(4a),为无色液体;1H NMR (400 MHz, CDCl3)δ:7.66~7.68(m, 1H, Ar-H),7.46~7.48 (m, 1H, Ar-H), 7.23~7.30 (m, 2H, Ar-H), 2.96 (q, J=8.0 Hz, 2H, CH2), 1.45 (t, J=8.0 Hz, 3H, CH3); MS m/z (相对强度): 147 (M+, 63), 146 (M-1, 100)。
4) 2-乙基-5-氯苯并噁唑(4c),为白色固体; mp 62.2~63.6 ℃; 1H NMR (400 MHz, CDCl3)δ: 7.65 (s, 1H, Ar-H), 7.40 (t, J=8.4 Hz, 1H, Ar-H), 7.28 (d, J=1.6 Hz, 1H, Ar-H), 2.97 (q, J=7.6 Hz, 2H, CH2), 1.45 (t, J=7.6 Hz, 3H, CH3); MS m/z (相对强度): 183 (M+2, 15), 182 (M+1, 40), 181 (M+, 60), 180 (M-1, 100)。
5) 2-苯基苯并噁唑(5a),为白色固体; mp 101~103 ℃; 1H NMR (400 MHz, CDCl3) δ: 8.26~8.32 (m, 2H, Ar-H), 7.72~7.87 (m, 1H, Ar-H), 7.51~7.64 (m, 4H, Ar-H), 7.34~7.45 (m, 2H, Ar-H); MS m/z(相对强度): 195 (M+, 100)。
6) 5-氯-2-苯基苯并噁唑(5c),为棕黄色固体; mp 98~100 ℃; 1H NMR (400 MHz, CDCl3)、δ: 8.26 (d, J=8.0 Hz, 2H, Ar-H), 7.77 (d, J=1.6 Hz, 1H, Ar-H), 7.51~7.58 (m, 4H, Ar-H), 7.34 (dd, J1=8.4 Hz,J2=1.2 Hz, 1H, Ar-H); MS m/z (相对强度): 231 (M+2, 33), 229 (M+, 100)。
7) 2-苯乙烯基苯并噁唑(6a),为白色固体; mp 81.5~83℃; 1H NMR (400 MHz, CDCl3)δ: 7.83 (d, J=16.4 Hz, 1H, =CH), 7.73 (t, J=4.8 Hz, 1H, Ar-H), 7.61 (d, J=6.8 Hz, 2H, Ar-H), 7.55 (t, J=4.0 Hz, 1H, Ar-H), 7.39~7.43 (m, 3H, Ar-H), 7.26~7.36 (m, 2H, Ar-H), 7.11 (d, J=16.4 Hz, 1H, =CH); MS m/z (相对强度): 221 (M+, 48), 220 (M-H, 100)。
8) 5-氯-2-苯乙烯基苯并噁唑(6c),为白色固体; mp 106~107 ℃; 1H NMR (400 MHz, CDCl3) δ: 8.85 (d, J=16.0 Hz, 1H, =CH), 7.71 (s, 1H, Ar-H), 7.61~7.63 (m, 2H, Ar-H), 7.43~7.48 (m, 4H, Ar-H), 7.30 (d, J=10.4 Hz, 1H, Ar-H), 7.08 (d, J=16.0 Hz, 1H, =CH); MS m/z (相对强度): 257 (M+2, 8), 256 (M+1, 35), 255 (M+, 25), 254 (M-1, 100)。
4 结论
1) 以含有不同取代基团的邻氨基苯酚和不同结构的羧酸以CHCl3为溶剂,在POCl3的作用下可以合成多种苯并噁唑类化合物。该方法与传统方法相比具有反应条件温和、操作简便、产率较高、反应底物易得等优点,是一种非常有效的合成苯并噁唑类化合物的方法。
2) 通过对物料比、温度及溶剂对目标产物产率影响的研究,确定了最为理想的反应条件如下:邻氨基苯酚、羧酸的物质的量比为1.0:1.5,邻氨基苯酚、POCl3的物质的量比为1:3.0,在氯仿溶剂中回流,并通过这个反应条件合成了一系列苯并噁唑类化合物。2-烷基取代苯并噁唑的产率较高,最高可达95%;2-苯基和2-苯乙烯基取代的苯并噁唑产率相对较低,位于34%~58%之间。
3) 羧酸的结构对目标化合物的产率影响比较大。在合成2位具有不同取代基团的苯并噁唑类目标化合物时,由于在反应过程中羧酸先转化为酰氯,在缩合反应中酰氯的活性和位阻的差别将决定所得目标化合物产率的差别。
参考文献:
[1] KAUR A, WAKODE S, PATHAK D P. Benzoxazole: The molecule of diverse pharmacological importance[J]. International Journal of Pharmacy and Pharmaceutical Sciences, 2015, 7(1): 16-23.
[2] SEENAIAH D, REDDY P R, REDDY G M, et al. Synthesis, antimicrobial and cytotoxic activities of pyrimidinyl benzoxazole, benzothiazole and benzimidazole[J]. European Journal of Medicinal Chemistry, 2014, 77: 1-7.
[3] 冯长君, 刘志国, 梁逸曾. 苯并噻(噁)唑酮衍生物杀虫活性的理论研究[J]. 中南大学学报(自然科学版), 2013, 44(11): 4399-4407.
FENG Changjun, LIU Zhiguo, LIANG Yizeng. Theoretical study on insecticidal activities and structural modification for N-arylaminocarbonyl-2-benzothiazolinone/benzoxazolone[J]. Journal of Central South University (Science and Technology), 2013, 44(11): 4399-4407.
[4] DICK P F, COELHO F L, RODEMBUSCH F S, et al. Amphiphilic ESIPT benzoxazole derivatives as prospective fluorescent membrane probes[J]. Tetrahedron Letters, 2014, 55(19): 3024-3029.
[5] WEE D, YOO S, KANG Y H, et al. Poly(imide-benzoxazole) gate insulators with high thermal resistance for solution- processed flexible indium-zinc oxide thin-film transistors[J]. Journal of Materials Chemistry C, 2014, 2: 6395-6401.
[6] 肖立伟, 高红杰, 孔洁, 等. 2-取代苯并噁唑类化合物的合成研究进展[J]. 有机化学, 2014, 34(6): 1048-1060.
XIAO Liwei, GAO Hongjie, KONG Jie, et al. Progress in the synthesis of 2-substituted benzoxazoles derivatives[J]. Chinese Journal of Organic Chemistry, 2014, 34(6): 1048-1060.
[7] SHARMA H, SINGH N, JANG D O. A ball-milling strategy for the synthesis of benzothiazole, benzimidazole and benzoxazole derivatives under solvent-free conditions[J]. Green Chemistry, 2014, 16(12): 4922-4930.
[8] BALASWAMY G, SRINIVAS K, PRADEEP P, et al. Synthesis, characterization and antimicrobial activity of novel substituted benzoxazole derivatives[J]. International Journal of Chemical Sciences, 2012, 10(2): 619-626.
[9] XIAO Liwei, ZHANG Min, SUN Wenhua. Efficient syntheses of 2-substituted benzimidazoles and benzoxazoles from β-keto esters[J]. Chemical Research in Chinese Universities, 2011, 27(2): 228-231.
[10] ANAND M, RANJITHA A, HIMAJA M. Silica sulfuric acid catalyzed microwave-assisted synthesis of substituted benzoxazoles and their antimicrobial activity[J]. International Research Journal of Pharmacy, 2011, 2(4): 211-213.
[11] SOARES A M S, COSTA S P G, GONCALVES M S T. Oxazole light triggered protecting groups: synthesis and photolysis of fused heteroaromatic conjugates[J]. Tetrahedron, 2010, 66(41): 8189- 8195.
[12] ENDO Y, BACKVALL J E. Biomimetic oxidative coupling of benzylamines and 2-aminophenols: synthesis of benzoxazoles[J]. Chemistry: a European Journal, 2012, 18(43): 13609-13613.
[13] MAO Zhifeng, WANG Zhe, XU Zhaoqing, et al. Copper(II)-mediated dehydrogenative cross-coupling of heteroarenes[J]. Organic Letters, 2012, 14(15): 3854-3857.
[14] Murali M G, Md A A, Tharamalingam P. Copper (Ⅱ)-catalyzed conversion of blasaryloxime ethers to 2-arylbenzoxazoles via C-H functionalization/C-N/C-O bonds formation[J]. Organic Letters, 2011, 13(5): 1194-1197.
[15] ACKERMANN L. Carboxylate-assisted transition-metal- catalyzed C-H bond functionalizations: Mechanism and scope[J]. Chemical Reviews, 2011, 111(3): 1351-1345.
[16] ANTON V D, RICHARD C L. Synthesis of o-(dimethylamino)aryl ketones: acridones, acridinium salts, and 1H-indazdes by the reaction of hydrazones and arynes[J]. Journal of Organic Chemistry, 2012, 77(24): 11232-11256.
[17] EGART B, CZEKELIUS C. Stereoselective bromocyclization of allylated allylated aldoxime ethers[J]. Chemistry-An Asian Journal, 2014, 9(8): 2088-2091.
[18] SURESH D, DHAKSHINAMOORTHY A, PITCHUMANI K. A green route for the synthesis of 2-substituted benzoxazole derivatives catalyzed by Al3+-exchanged K10 clay[J]. Tetrahedron Letters, 2013, 54(48): 6415-6419.
[19] CHEN Chengyi, Andreani T, LI Hongmei. A divergent and selective synthesis of isomeric benzoxazoles from a single N-Cl imine[J]. Organic Letters, 2011, 13(23): 6300-6303.
(编辑 陈灿华)
收稿日期:2015-06-04;修回日期:2015-08-10
基金项目(Foundation item):国家基础科学人才培养基金(J1210040);湖南省自然科学基金资助项目(2015JJ4018)(Project (J1210040) supported by the National Natural Basic Science Personnel Training Fund of China; Project (2015JJ4018) supported by the Natural Science Foundation of Hunan Province)
通信作者:江国防,博士,教授,从事有机合成研究;E-mail:gfjiang@hnu.edu.cn