文章编号:1004-0609(2013)04-1086-06
室温下多孔Mg(OH)2薄膜的电沉积制备及表征
吕 莹,张治安,赖延清,刘业翔
(中南大学 冶金科学与工程学院,长沙 410083)
摘 要:以SnO2导电玻璃为阴极,使用循环伏安法及计时电流法研究0.1 mol/L硝酸镁水溶液体系中氢氧化镁的电沉积过程,并对恒电势沉积法制备的多孔Mg(OH)2薄膜的形貌、物相及光学性质进行表征。结果表明:所得Mg(OH)2薄膜呈很明显的(011)面择优取向;随着沉积电势或初始pH值的增加,Mg(OH)2二次成核的数量增加;在沉积时间固定为10 min的情况下,沉积电势为-1.2、-1.3和-1.4 V的薄膜在可见光范围内(390~780 nm)的平均透过率依次为90.21%、69.39%和47.12%。
关键词:氢氧化镁;薄膜;电沉积;形貌;透过率
中图分类号:TB321;TQ153.3 文献标志码:A
Preparation and characterization of electrodeposited porous
Mg(OH)2 thin films at room temperature
L? Ying, ZHANG Zhi-an, LAI Yan-qing, LIU Ye-xiang
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: Electrodeposition process of Mg(OH)2 on SnO2 coated glass was studied by cyclic voltammetry and chronoamperometry in 0.1 mol/L aqueous magnesium nitrate solution at room temperature. Characterization of morphology, phase, optical properties of the porous Mg(OH)2 thin films was carried out by FESEM, GAXRD and UV-Vis. Results show that the thin films have (011) preferred orientation. The number of secondary nucleation increases with the increase of applied potential or solution pH. The average transmittances of the porous Mg(OH)2 films deposited at -1.2, -1.3 and -1.4 V over the visible region (390-780 nm) are 90.21%, 69.39% and 47.12% respectively.
Key words: Mg(OH)2; thin films; electrodeposition; morphology; transparency
收稿日期:2012-07-13;修订日期:2012-11-16
通信作者:赖延清,教授,博士;电话:0731-88876454;E-mail: laiyanqingcsu@163.com
Mg(OH)2薄膜材料被广泛用作阻燃剂、催化剂、添加剂、二氧化碳吸收剂和复合膜材料等[1-3]。同时, 由于Mg(OH)2可在较低的温度下转变为MgO且保持形貌不发生改变[4-5],故常用作制备MgO的前驱体,而MgO 具备高电阻率、高透过率、宽带隙、良好化学稳定性及高二次电子发射系数等优点,是一种重要的工业材料[6]。近年来,Mg(OH)2还被尝试用于一些新的领域,如CIGS太阳电池[7]和染料敏化太阳电 池[8]以及透明导电材料[9]等,这使得其应用范围得到进一步拓宽。
制备Mg(OH)2薄膜材料的方法主要包括氧化 法[10]、溶胶-凝胶法[11]、化学浴沉积法[12]、电化学法等。其中电化学法以其较低的加工温度、简单的工艺、低廉的成本等优点成为合成纳米薄膜材料的最受欢迎的方法之一。THERESE等[13]和DINAMANI等[14]以金属为基底使用恒电流法分别从硝酸镁溶液和氯化镁溶液中电沉积制备氢氧化镁薄膜,并考察pH值、前驱体浓度和电流密度等对电沉积氢氧化镁的影响。LI 等[15]在Pt基底上制备了氢氧化镁薄膜,并考察了沉积电压对薄膜形貌的影响,发现高电压下生成的是扁平状的薄膜,而低电压下生成的是多孔的薄膜。ZOU 等[16-17]以ITO玻璃为基底从硝酸镁溶液中制备了氢氧化镁薄膜,并考察了醋酸钠和水溶性离子对薄膜的 影响。
为了将电沉积Mg(OH)2薄膜应用于光电器件等领域,薄膜的均匀性和光学性质十分重要。为此,本文作者以SnO2导电玻璃为阴极,在0.1 mol/L的硝酸镁水溶液体系中制备了多孔氢氧化镁,使用循环伏安法及计时电流法研究了电沉积过程。在此基础上,对恒电势沉积法制备的多孔氢氧化镁薄膜的形貌、物相、光学性质进行了表征,考察了沉积电势对形貌和光学透过率的影响。
1 实验
用去离子水配制Mg2+浓度为0.1 mol/L的硝酸镁溶液,将SnO2导电玻璃(工作面积1.5 cm2)、Pt电极和饱和甘汞电极分别作为工作电极、对电极和参比电极。进行电化学测试及电沉积之前,工作电极用丙酮、乙醇和去离子水在超声波清洗机中分别清洗15 min。溶液温度是室温(298 K),溶液pH值使用硝酸调节至5。循环伏安扫描区间为从开路电压0.17 V (vs SCE)至-1.3 V (vs SCE),扫描速率为10 mV/s,循环次数为4。恒电势沉积的电势分别为-0.9,-1.0,-1.1,-1.2,-1.3和-1.4V (vs SCE)。沉积完成后,工作电极使用去离子水清洗,然后在空气中干燥至质量不再变化。
电沉积实验和电化学测试均使用PAR 2273电化学工作站进行。薄膜形貌分析采用场发射扫描电镜FESEM (Hitachi S4800)进行,工作电压为2 kV。对薄膜进行掠入射角X射线衍射分析(GAXRD),X’Pert Pro靶为Cu Kα1 (λ=0.154 06 nm),工作电压为40 kV,扫描区间为 10°≤2θ≤90°,步长为0.02°。采用紫外-可见光谱测试仪(SHIMADZU UV-2450 UV-Vis)表征薄膜的光学透过性能,扫描范围为300~900 nm。
2 结果与讨论
电化学沉积法制备Mg(OH)2的原理可由如下3个步骤加以描述:
1) 硝酸根得到电子生成亚硝酸根和氢氧根,
NO3-+H2O+2e→NO2-+2OH- (1)
2) 水分解生成氢气和氢氧根(HER),
2H2O+2e→H2+2OH- (2)
3) 溶液中Mg2+与生成的OH-发生反应生成Mg(OH)2薄膜,即
Mg2++2OH-=Mg(OH)2 (3)
2.1 电化学分析
2.1.1 循环伏安法
图1所示为硝酸镁水溶液在SnO2电极上的循环伏安扫描曲线。从图1可以看出,向负方向扫描时电流密度从-0.1 V开始增大,并在-0.6 V左右达到最大值,形成第一个还原峰(1),对应于硝酸根的还原反应: NO3-+H2O+ 2e→NO2-+2OH- (-0.232 V, vs SCE) 。从-1.04 V 开始电流密度的增大,对应于析氢反应(2): 2H2O+2e→H2+2H- (-1.07 V, vs SCE)。向正方向扫描时没有出现氧化峰,这说明生成的NO2-在此电势范围内(-1.3~0.17 V)并没有被氧化为NO3-。在第二个循环时,反应(1)的起始电位负移至-0.3 V,对应于NO3-在Mg(OH)2电极表面还原的起始电位。随着循环次数的增加,A峰的峰电流密度依次减小,这表明随着薄膜厚度的增加,薄膜的导电性有所降低;同时,NO3-的消耗也是导致出现这种现象的可能原因。
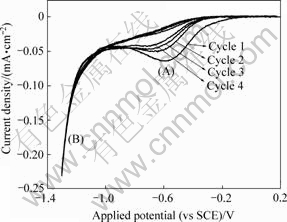
图1 硝酸镁水溶液在SnO2电极上的循环伏安扫描曲线
Fig. 1 Cyclic voltammetry of Mg(NO3)2 on SnO2 coated electrode at scanning rate of 10 mV/s
2.1.2 计时电流法
图2所示为不同电势下的计时电流曲线。由图2可知,随着阴极电压的增大,阴极电流密度增大。电流在施加阴极电压的初始阶段均先到达一个最大值,这是由测量电路的时间常数造成的。当沉积电势为-0.9、-1.0和-1.1 V时,电流密度在最大值后迅速减小并接近定值,由图1可知,这些电势下发生的主要是硝酸根的还原反应,电流密度较小;当沉积电势为-1.2 V时,电流密度在到达最大值后数秒内到达最小值,随后又开始平缓上升。这说明先生成的晶核覆盖在电极表面,使电流密度减小,随后发生的析氢反应(HER)将一部分电极表面冲刷开以使电化学反应顺利进行[15]。导电性良好的电极面积的变化导致电流密度变化,氢氧化镁晶体从留下来的晶核上生长,这就使得有良好导电性的电极面积基本维持不变,于是电流密度在300 s之后保持近似恒定。当沉积电势为-1.3 V时,电流密度随时间减小。当沉积电势为-1.4 V时,电流密度基本维持不变。
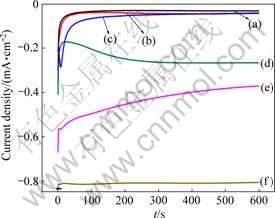
图2 氢氧化镁电沉积的计时电流曲线
Fig. 2 Chronoamperogram of Mg(OH)2 electrodeposition: (a) -0.9 V; (b) -1.0 V; (c) -1.1 V; (d) -1.2 V; (e) -1.3 V; (f) -1.4 V
2.2 表面形貌及其影响因素
2.2.1 初始溶液pH值对表面形貌的影响
当初始溶液pH低于2时,在阴极表面生成的氢氧根离子被溶液中的H+大量消耗,因此氢氧化物的产量很低,而初始溶液pH值大于7时,将发生化学沉淀从而降低薄膜的质量。当pH值在3~7时,产率几乎维持不变。因此,固定沉积电势为-1.4V,沉积时间为30 min,初始溶液pH值选为3,4,5,6和7,研究初始溶液pH值对表面形貌的影响。
图3所示为使用不同溶液初始pH值制备的Mg(OH)2薄膜的FESEM像。由图3可知,当pH为3时,沉积进行30 min后生成了均匀多孔的薄膜,与沉积300 s时生成的薄膜(图3(a))对比可知,薄膜均在初级晶核上生长(图3(b)),并没有二次结晶的出现。但随着溶液初始pH值的升高,二次结晶的数量增多,二次结晶区域面积逐渐增大(图3(c)~(f))。这一结果表明:在本实验条件下(Mg2+为0.1 mol/L,溶液温度为298 K,沉积时间30 min),当沉积电势为-1.4 V时,若初始溶液pH值大于3,将出现二次成核。
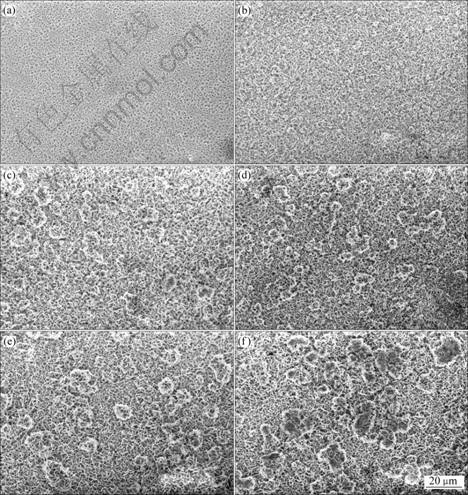
图3 不同初始溶液pH值制备的Mg(OH)2薄膜的FESEM像
Fig. 3 SEM images of electrodeposited Mg(OH)2 thin films (Mg2+: 0.1 mol/L, T=298 K, φ=-1.4 V, t=30 min): (a) pH=3, deposition for 300 s; (b) pH=3, deposition for 30 min; (c) pH=4; (d) pH=5; (e) pH=6; (f) pH=7
2.2.2 沉积电势对表面形貌的影响
图4所示为固定溶液初始pH值为5时,不同电势下制备的Mg(OH)2薄膜的FESEM像。在电势为-0.9、-1.0和-1.1 V时,只有界面处有少许沉积物,基底的其他部分没有成膜。其中当沉积电势为-1.1 V时(见图4(a)),从气固液界面(以虚线标识)向液体内部延伸1 mm左右(至实线处)的区域内有沉积物(见图4(a)中插图)。当电势为-1.2 V时(见图4(b)),整个基底上覆盖着由薄片组成连续的多孔薄膜。当电势为-1.3 V时(见图4(c)),在均匀的多孔薄膜上出现了不连续的结晶,形态与初级结晶接近,但尺寸比初级结晶大,这些结晶是二次成核形成的。由图2(e)可知,此时电流密度越来越小,这说明氢氧化镁的二次成核仅发生在初级结晶表面的活性中心,包围在这些活性中心周围的禁区在一定程度上会阻止二次成核的发生[18]。随着阴极电势的提高,薄膜上出现了越来越多的二次结晶。当电势为-1.4 V时(见图4(d)),在二次结晶的薄膜上出现了二次成核。由图2(f)可知,电流密度基本维持不变,这说明提高沉积电势使溶液过饱和度升高到一定程度后,二次成核的发生不再受到非活性中心的制约。通过高倍SEM照片(见图4(e))可以得知,纳米薄片的厚度大约是12 nm。图4(f)所示为沉积电势为-1.4 V时气液固三相界面的薄膜形貌。与液固界面的多孔形貌不同,三相界面的膜平整致密,这是由倾向于竖直生长的纳米薄片共同构成的。

图4 不同电势下制备的Mg(OH)2薄膜的FESEM像
Fig. 4 FESEM images of electrodeposited Mg(OH)2 thin films (Mg2+: 0.1 mol/L, pH=5.0, T=298 K, t=10 min): (a) -1.1 V; (b) -1.2 V; (c) -1.3 V; (d) -1.4 V; (e) High magnification image of Fig. 4(d); (f) Liquid-gas interface
当界面pH值的提高可以满足Mg(OH)2薄膜的生成时,初级成核和结晶即可发生,形成均匀多孔的Mg(OH)2薄膜。当采用较负的沉积电势或较高的初始溶液pH值时,均会得到较高的界面OH-浓度,即较高的溶液过饱和度,在一次结晶和溶液的界面处就会出现二次成核,且随着沉积电势和初始溶液pH值的提高,二次成核的数量增加。因此若要获得均匀多孔的Mg(OH)2薄膜,须控制合适的参数以防止二次结晶的出现。对比2.2.1节中结果与2.2.2节中结果可知,当沉积电势由-1.2 V调节至-1.4 V时,不发生二次成核的初始溶液pH值由5降至3;反之,当初始溶液pH值由5降至3时,不发生二次成核的沉积电势由-1.2 V调节为-1.4 V。这说明若采用高的沉积电势,可降低初始溶液pH值以防止二次成核,同样,若初始溶液pH较高,可适当降低沉积电势以防止二次成核。
2.3 物相分析
图5所示为制备的多孔Mg(OH)2薄膜的典型GAXRD测试谱。尖锐的衍射峰显示了薄膜良好的结晶度;除了基底上的衍射峰外,其他所有的衍射峰都与水镁石结构的氢氧化镁匹配(PDF#76-0667, a=b=3.142 ?, c= 4.766 ?)。(011)和(001)峰的衍射强度之比I(011)/I(001)为5.06,远高于PDF#76-0667中峰强比对应的数值(1.26),这表明生成的薄膜有很明显的(011)面择优取向。
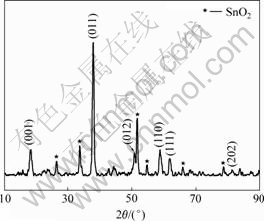
图5 Mg(OH)2薄膜的XRD谱
Fig. 5 XRD pattern of electrodeposited Mg(OH)2 thin films (Mg2+: 0.1 mol/L, pH=5, T=298 K, φ=-1.2 V, t=10 min)
2.4 光学性质
图6所示为在不同电势下制备出的Mg(OH)2薄膜的紫外-可见光光谱。由图6可知,在沉积时间固定为10 min时,沉积电势为-1.1 V和-1.2 V的薄膜在可见光范围内(390~780 nm)的平均透过率最大,分别为101.1%和90.21%。其中当沉积电势为-1.1 V时,当波长在340~680 nm之间时,Mg(OH)2/SnO2复合薄膜的透过率明显高于SnO2薄膜的透过率,这可能是由于Mg(OH)2薄膜厚度较小,在此波长范围内对SnO2薄膜有一定的增透作用造成的。但是由图4(a)可知,此时制备的薄膜未能将基底覆盖完全。因此,制备厚度适当且均匀覆盖于基底的薄膜并分析其对基底的增透作用是下一步需要开展的工作。其他电势下制备的薄膜在可见光范围内的平均透过率分别为69.39%(-1.3 V)和47.12%(-1.4 V)。Mg(OH)2薄膜的禁带宽度无法从测试数据中得出,因其带隙宽度(5.7 eV[19])远大于SnO2导电玻璃的可测范围。
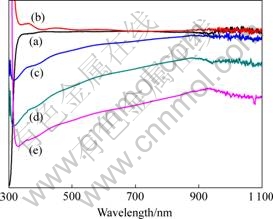
图6 Mg(OH)2薄膜的紫外-可见光光谱
Fig. 6 UV-Vis spectra of electrodeposited Mg(OH)2 film: (a) Blank SnO2 coated glass; (b) -1.1 V; (c) -1.2 V; (d) -1.3 V; (e) -1.4 V
3 结论
1) 随着沉积电势或初始pH值的增加,Mg(OH)2二次成核量增加。在采用较高的沉积电势时,可适当降低初始溶液pH以防止二次成核,同样,在采用较高的初始溶液pH时,可适当降低沉积电势以防止二次成核。
2) 在沉积电势低于-1.5 V的情况下,生成的Mg(OH)2薄膜有很明显的(011)面择优取向。
3) 当沉积时间固定为10 min时,沉积电势为-1.2、-1.3及-1.4 V的薄膜在可见光范围内(390~780 nm)的平均透过率分别为90.21%、69.39%和47.12%,表明提高沉积电势可降低薄膜的平均透过率。
REFERENCES
[1] MAO Q H, ZHANG L P, HUANG D H, WANG D, HUANG Y, XU H, CAO H T, MAO Z P. Preparation and characterization of flame-retardant lamellar Mg(OH)2 thin films on citric acid-treated cotton fabrics[J]. Surface and Interface Analysis. 2011, 43(5): 903-912.
[2] NDUAGU E, BERGERSON J, ZEVENHOVEN R. Life cycle assessment of CO2 sequestration in magnesium silicate rock―A comparative study[J]. Energy Conversion and Management, 2012, 55: 116-126.
[3] BAE T, LIU J, THOMPSON J A, KOROS W J, JONES C W , ANIR S. Solvothermal deposition and characterization of magnesium hydroxide nanostructures on zeolite crystals[J]. Microporous and Mesoporous Materials, 2011, 139(1/3): 120-129.
[4] MORRIS R M, KLABUNDE K J. Formation of paramagnetic adsorbed molecules on thermally activated magnesium and calcium oxides: Characteristics of the active surface sites[J]. Inorganic Chemistry, 1983, 22(4): 682-687.
[5] KLABUNDE K J, MATSUHASHI H. A comparison of electron donor and proton abstraction activities of thermally activated pure magnesium oxide and doped magnesium oxides[J]. Journal of the American Chemical Society, 1987, 109(4): 1111-1114.
[6] SHAND M A, WILEY J. The chemistry and technology of magnesia[M]. Wiley Online Library, 2006.
[7] YAMADA A, MIYAZAKI H, CHIBA Y, KONAGAI M. High-efficiency Cu(InGa)Se2 solar cells with a zinc-based buffer layer[J]. Thin Solid Films, 2005, 480/481: 503-508.
[8] YUM J H, NAKADE S, KIM D Y, YANAGIDA S. Improved performance in dye-sensitized solar cells employing TiO2 photoelectrodes coated with metal hydroxides[J]. Journal of Physical Chemistry B, 2006, 110(7): 3215-3219.
[9] HONJO T, KUJI T, THEMINERALS M M S T. Development of new transparent conductive material of Mg(OH)2-C [J]. The Surface Science Society of Japan, 2008, 6: 15-16.
[10] ZOU G, LIU R, CHEN W, XU Z. Preparation and characterization of lamellar-like Mg(OH)2 nanostructures via natural oxidation of Mg metal in formamide/water mixture[J]. Materials Research Bulletin, 2007, 42(6): 1153-1158.
[11] UTAMAPANYA S, KLABUNDE K J, SCHLUP J R. Nanoscale metal oxide particles/clusters as chemical reagents: Synthesis and properties of ultrahigh surface area magnesium hydroxide and magnesium oxide[J]. Chemistry of Materials, 1991, 3(1): 175-181.
[12] HUANG C H, JAN Y L, LEE W C. Investigation of Mg(O, OH) films prepared by chemical bath deposition as buffer layers for Cu(In,Ga)Se2 solar cells[J]. Journal of the Electrochemical Society, 2011, 158(9): H879-H888.
[13] THERESE G H A, KAMATH P V. Cathodic reduction of different metal salt solutions (Part Ⅰ): Synthesis of metal hydroxides by electrogeneration of base[J]. Journal of Applied Electrochemistry, 1998, 28(5): 539-543.
[14] DINAMANI M, KAMATH P V. Electrosynthesis of Mg(OH)2 coatings on stainless steel substrates[J]. Journal of Applied Electrochemistry, 2004, 34(9): 899-902.
[15] LI C F, HO W H, YEN S K. Effects of applied voltage on morphology and crystal orientation of Mg(OH)2 coating on Pt by electrochemical synthesis[J]. Journal of the Electrochemical Society, 2009, 156(2): E29-E34.
[16] 邹光龙. 氢氧化镁、氧化锌微/纳米结构的软化学合成与表征[D]. 杭州: 浙江大学, 2007.
ZHOU Guang-long. Soft chemical synthesis and characterization on micro/nanostructured magnesium hydroxide and zinc oxide[D]. Hangzhou: Zhejiang University, 2007.
[17] ZOU G L, LIU R, CHEN W X. Highly textural lamellar mesostructured magnesium hydroxide via a cathodic electrodeposition process[J]. Materials Letters, 2007, 61(10): 1990-1993.
[18] TULIO P, CARLOS I. Effects of SiC and Al2O 3 particles on the electrodeposition of Zn, Co and ZnCo (Ⅰ). Electrodeposition in the absence of SiC and Al2O3[J]. Journal of Applied Electrochemistry, 2009, 39(2): 283-291.
[19] KUMARI L, LI W Z, VANNOY C H, LEBLANC R M, WANG D Z. Synthesis, characterization and optical properties of Mg(OH)2 micro-/nanostructure and its conversion to MgO[J]. Ceramics International, 2009, 35(8): 3355-3364.
(编辑 龙怀中)