稀有金属 2013,37(05),778-782
Ca (OH) 2的加入量对锆英砂碱熔分解过程的影响
张亚增 陈伟东 闫淑芳 闫国庆
内蒙古工业大学材料科学与工程学院
摘 要:
在锆英砂与氢氧化钠质量比为1.0∶1.2时, 分别选取锆英砂含量0.2%, 0.4%, 0.6%, 0.8%和1.0%的Ca (OH) 2作为添加剂, 研究Ca (OH) 2加入量对锆英砂碱熔分解过程的影响。采用X射线衍射仪和差热-热重分析仪对反应物料的组成和反应体系热量变化进行分析。结果表明:在Ca (OH) 2加入量为1.0%时, 锆英砂的分解率达到最大值, 为96.4%, 碱熔过程中在590℃以后发生剧烈的放热反应, 锆英砂碱熔分解后的主要产物为Na2ZrO3和Na2SiO3。烧碱和添加剂复合分解锆英砂的适宜工艺条件为:烧结温度为750℃, 烧结时间为30 min。
关键词:
锆英砂;碱熔工艺;锆分解率;
中图分类号: TQ134.12
作者简介:张亚增 (1987-) , 男, 河南安阳人, 硕士研究生;研究方向:锆铪冶金;陈伟东, E-mail:weidongch@163.com;
收稿日期:2013-04-10
基金:教育部科学技术研究重点项目 (211031);内蒙古自然科学基金项目 (2011MS0709) 资助;
Influence of Ca ( OH) 2 Addition Amount on Zircon Alkali Fusion Decomposition Process
Zhang Yazeng Chen Weidong Yan Shufang Yan Guoqing
College of Materials and Engineering, Inner Mongolia University of Technology
Abstract:
With the zircon sand to sodium hydroxide mass ratio of 1. 0∶ 1. 2, and the Ca ( OH) 2additive amount of 0. 2%, 0. 4%, 0. 6%, 0. 8% and 1. 0% to zircon amount separately, the influence of Ca ( OH) 2on zircon alkali fusion decomposition process was studied. The composition of the reactant and heat changes of the reaction system were analyzed by X-ray diffraction ( XRD) and differential scanning calorimetry-thermal gravimetric analysis ( DSC-TG) . It was found that when the additive amount of Ca ( OH) 2reached1. 0%, the decomposition rate of zircon increased up to a maximum value of 96. 4%. When the temperature reached 590 ℃, the process of alkali fusion decomposition occurred a violent exothermic reaction, and the main products of zircon alkali fusion decomposition were Na2ZrO3and Na2SiO3. In addition, the results showed that the optimal sintering temperature and sintering time were about750 ℃ and 30 min respectively to decompose zircon with caustic soda and Ca ( OH) 2additive.
Keyword:
zircon; alkali fusion technology; zircon decomposition rate;
Received: 2013-04-10
氧氯化锆 (Zr OCl2・8H2O) 是重要的基础化工产品锆盐, 可制取氧化锆、硫酸锆和碳酸锆等, 也可直接用于锆铪分离制备原子能级氧化锆。随着国民经济, 特别是卫生陶瓷、电子、核电、汽车制造等行业的迅速发展, 对锆化学制品的需求日益增加。根据中国有色金属协会钛锆铪分会统计, 2011年我国氧氯化锆产量已经超过20万吨, 居世界第一[1,2,3,4]。
国内外氧氯化锆的工业化生产普遍采用锆英砂一酸一碱法生产工艺, 包括碱熔、水洗转型、酸化、浓缩结晶、酸浸除铁等工序[5,6]。锆英砂碱熔法与氯化法、石灰烧结法等相比具有生产规模大、效率高等特点, 是生产氧氯化锆的主要方法[7,8,9]。但是该方法存在氢氧化钠消耗量大, 能源利用率低, 废碱水处理量大等问题。借鉴熔盐和催化理论[10,11,12,13], 在反应体系中加入Ca (OH) 2作为添加剂, 有助于提高反应体系的活性, 使反应温度降低, 从而有助于分解反应的迅速进行[14,15,16]。因此本文提出在烧碱-锆英砂反应体系内加入Ca (OH) 作为添加剂, 研究烧碱和添加剂复合分解锆英砂的工艺条件, 期望在一定程度上减少烧碱的用量, 弥补传统工艺的不足。
1 实验
1.1 原料
实验所用锆英砂来源于澳大利亚艾璐卡资源有限公司, 其化学成分见表1。氢氧化钠采用片状固碱, 其化学成分见表2。
1.2 实验方法
将锆英砂与固体氢氧化钠按质量比为1.0∶1.2置于坩埚中, 然后再分别加入锆英砂含量的0.2%, 0.4%, 0.6%, 0.8%和1.0%的Ca (OH) 2, 混合均匀后在高温炉中按设定的温度和时间进行高温碱熔。实验各组工艺参数见表3。高温碱熔后称取一定量的烧结料, 置于锥形三角瓶中, 加入1.2 mol・L-1的盐酸, 放在电炉上加热溶解后加蒸馏水, 用EDTA络合滴定法测定锆英砂的分解率。
表1 锆英砂化学成分 (%, 质量分数) Table 1 Zircon sand chemical composition (%, mass fraction) 下载原图

表1 锆英砂化学成分 (%, 质量分数) Table 1 Zircon sand chemical composition (%, mass fraction)
表2 烧碱化学成分 (%, 质量分数) Table 2 Caustic soda chemical composition (%, mass fraction) 下载原图

表2 烧碱化学成分 (%, 质量分数) Table 2 Caustic soda chemical composition (%, mass fraction)
表3 实验工艺参数Table 3 Experimental process parameters 下载原图
表3 实验工艺参数Table 3 Experimental process parameters
采用荷兰飞利浦APD-10型全自动粉末衍射仪 (参数:Cu靶, 电流35 m A, 电压40 k V, 步进扫描0.02°) 测定烧结料的物相组成, 研究锆英砂碱熔过程中的物相变化。采用德国耐驰公司STA 409PC Luxx差热-热重同步分析仪对烧碱和添加剂复合分解锆英砂体系进行反应过程的热变化分析。测试温度从室温25℃升至1000℃, 升温速率为10℃・min-1。
2 结果与讨论
2.1 添加剂的加入量对锆英砂分解率的影响
图1是加入不同含量Ca (OH) 2的条件下得到锆英砂分解率的曲线。从图1中可以看出, 随着Ca (OH) 2加入量的增大, 锆英砂的分解率随之相应增加。在不添加Ca (OH) 2的情况下锆英砂的分解率为94.5%, 在Ca (OH) 2的加入量达到锆英砂含量的1%时, 锆英砂的分解率达到最大值, 为98.4%, 这说明Ca (OH) 2的加入有助于提高锆英砂的分解率。
2.2 温度对锆英砂分解率的影响
图2是有添加剂和无添加剂的情况下, 锆英砂分解率随温度变化的曲线图。对比可知, 在不添加Ca (OH) 2时 (见图2 (1) ) , 随着温度的升高, 锆英砂的分解率逐渐增加。当反应温度为750℃时, 锆英砂的分解率可达94.5%, 当温度超过750℃后, 锆英砂的分解率随着温度的升高而降低。而由Ca (OH) 2参与的锆英砂分解反应 (见图2 (2) ) , 随着温度升高, 锆英砂的分解率逐渐升高。当温度超过750℃时, 分解率增长趋势较为缓慢, 但过高的反应温度将消耗过多的能源, 也可能造成物料的烧结致使物料结块, 粘壁现象严重, 不利于后续的洗涤, 酸浸等处理, 由以上可知, 反应温度应控制在750℃左右较为适宜。

图1 Ca (OH) 2的加入量对锆英砂的分解率的影响Fig.1 Effect of Ca (OH) 2amount on decomposition rate of zircon
2.3 时间对锆英砂分解率的影响
图3是在加入添加剂的情况下, 反应温度为750℃时, 反应时间对锆英砂分解率的影响。由图3可知, 随着反应时间的延长, 锆英砂的分解率随之增加;当反应时间超过30 min后, 继续延长反应时间, 锆英砂的分解率增加较为缓慢。因此综合考虑锆英砂分解率和能源消耗, 反应时间为30 min左右较为合适。

图2 温度对锆英砂的分解率的影响Fig.2Effect of reaction temperature on decomposition rate of zircon
(1) No additive; (2) Adding 1%of Ca (OH) 2

图3 反应时间对锆英砂分解率的影响Fig.3Effect of reaction time on decomposition rate of zircon
2.4 烧碱和添加剂Ca (OH) 2复合分解锆英砂体系的差热-热重分析
图4是Ca (OH) 2加入量为1.0%时烧碱和Ca (OH) 2复合分解锆英砂体系的DSC-TG曲线。从图4中可知, 在70℃左右DSC曲线出现一个吸热峰, 这主要是由于在该温度下原料中水分吸收热量而汽化导致体系吸热。在300℃左右时DSC曲线又出现了一个吸热峰, 可以确定此吸热峰是由于氢氧化钠的融化而引起。当温度升高至590℃以上时DSC曲线出现明显放热峰, 并在840℃左右时, 放热反应最为激烈。对烧碱和添加剂Ca (OH) 2复合分解锆英砂体系的TG曲线分析表明, 反应体系在100℃左右时出现了明显的失重现象, 这是由于体系内存在的吸附水蒸发而导致体系失重。而在550℃后反应体系又出现明显失重, 此时对应于体系放热反应温度区间, 分析可知是由于体系中锆英砂发生分解反应, 并有水生成, 而在此温度范围内生成的水不断挥发导致体系重量下降。
图5是有添加剂和无添加剂情况下锆英砂分解反应体系的DSC曲线。对比两曲线可知, 锆英砂分解反应体系中加入Ca (OH) 2添加剂后, 体系DSC曲线在580℃出现了一个吸热峰 (见图5 (2) ) 。在590℃后有添加剂存在时, 反应体系的峰值温度更高, 峰面积更大。这说明添加剂加入后反应放热更剧烈, 且在该温度区间内不仅氢氧化钠与锆英砂发生反应, 而且氢氧化钙也与锆英砂发生了反应, 从而造成在该温度区域下化学反应较为剧烈。

图4 烧碱和Ca (OH) 2复合分解锆英砂反应体系的TG-DSC曲线Fig.4 TG-DSC curves of zircon decomposition reaction process with Ca (OH) 2-Na OH

图5 有添加剂和无添加剂情况下锆英砂分解反应体系DSC曲线Fig.5DSC curves of zircon decomposition reaction system with or without additive
(1) No additive; (2) Adding 1%of Ca (OH) 2
2.5 烧碱和添加剂Ca (OH) 2复合分解锆英砂体系XRD分析
图6是有添加剂和无添加剂情况下锆英砂分解反应体系的XRD图谱。从图5中可知, 无添加剂加入的锆英砂分解反应产物主要有Na2Zr O3和Na2Si O3, 而加入添加剂Ca (OH) 2的锆英砂分解反应产物主要有Na2Zr O3和Na2Si O3以及少量的Ca Zr O3和Ca Si O3。这说明添加剂Ca (OH) 2的加入参与了锆英砂的分解反应。
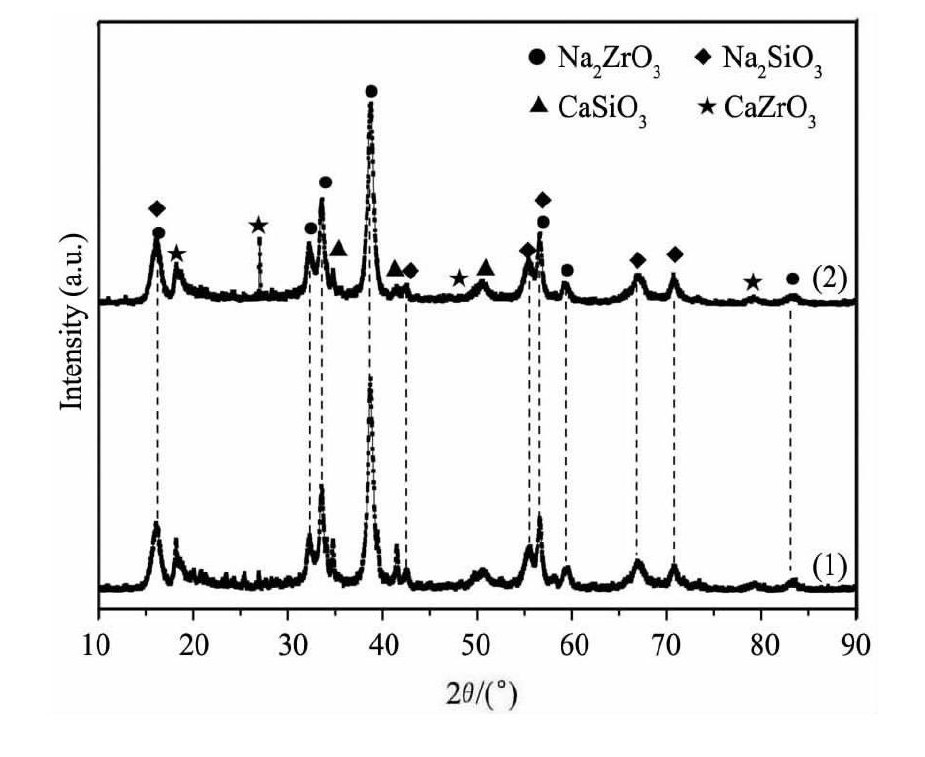
图6 有添加和无添加剂情况下锆英砂分解反应体系XRD图谱Fig.6XRD spectrum of zircon sand decomposition reaction system with or without additive
(1) No additive; (2) Adding 1%of Ca (OH) 2
3 结论
1.Ca (OH) 2添加剂的加入可提高锆英砂的分解率, 锆英砂分解率随Ca (OH) 2加入量的增加而增大。烧碱和Ca (OH) 2复合分解锆英砂的适宜工艺条件为:Ca (OH) 2加入量为1%, 烧结温度为750℃, 烧结时间为30 min。
2.通过差热分析表明, 锆英砂碱熔分解反应为放热反应, 反应体系在590℃以上开始放热。Ca (OH) 2加入使得反应体系的放热量增大, 放热峰温度范围变宽。
3.锆英砂碱熔分解反应的主要产物为Na2Zr O3和Na2Si O3, Ca (OH) 2添加剂加入后反应产物中出现少量的Ca Zr O3和Ca Si O3。
参考文献
[1] Xiong B K, Yang X M, Luo F C.Zirconium and Hafnium Metallurgy[M].Beijing:Metallurgical Industry Press, 2006.1. (熊炳坤, 杨新民, 罗方承.锆铪冶金[M].北京:冶金工业出版社, 2006.1.)
[2] Yu P.Analysis of import state for zircon and its concentration in China in recent two years[J].Rare Metals Letters, 2007, 26 (8) :20. (虞平.近两年我国锆英砂及其精矿进口情况分析报告[J].稀有金属快报, 2007, 26 (8) :160.)
[3] Lin Z H.Development problem and prospect of zirconium chemicals in China[J].Rare Metals Letters, 2007, 26 (1) :17. (林振汉.中国锆化学制品的发展及前景[J].稀有金属快报, 2007, 26 (1) :17.)
[4] Zeng W M, Qiu G Z.Research progress of chalcopyrite bioleaching mechanism[J].Metal Mine, 2012, (2) :94. (曾伟民, 邱冠周.黄铜矿生物浸出机制研究进展[J].金属矿山, 2012, (2) :94.)
[5] Abdelkader A M, Daher A, Emad EI-Kashef.Novel decomposition method for zircon[J].Journal of Alloys and Compounds, 2008, 460 (1-2) :577.
[6] Tong J Z, Zhang Y B.Preparation zirconiun oxychloride from concentrated Zr tails of Nb-Ta ore by lime[J].Chemistry World, 2003, 44 (2) :66.
[7] Luo X P, Wang X L, Luo L Y, Chen X M, LüL Z.Study on the flotation technology for Cu-Pb-Zn polymetallic sulphide ore in Qibaoshan[J].Metal Mine, 2012, (4) :68. (罗仙平, 王笑蕾, 罗礼英, 陈晓明, 吕玲芝.七宝山铜铅锌多金属硫化矿浮选新工艺研究[J].金属矿山, 2012, (4) :68.)
[8] Liu C H, Wang Z B, Wang L J.Technical and economical comparison of zirconium oxychloride by basic process chlorination[J].Rare Metals Letters, 2007, 26 (1) :97. (刘长河, 王泽斌, 王力军.碱熔法氯化法制备氧氯化锆的技术经济比较[J].稀有金属快报, 2007, 26 (1) :97.)
[9] Huang S J, Zhu Y G, Zhang B F.Experiment research on separation of Cu-Zn sulphide ore by flotation[J].Metal Mine, 2012, (1) :84. (黄思捷, 朱阳戈, 张保丰.某铜锌硫化矿浮选分离试验研究[J].金属矿山, 2012, (1) :84.)
[10] Biswas R K, Habib M A, Habib M A, karmakar A K, Islam M R.A novel method for processing of Bangladeshi zircon:Part I:baking, and fusion with NaOH[J].Hydrometallurgy, 2010, 103 (1-4) :124.
[11] Abdelkader A M, Daher A, Emad E.Novel decomposition method for zircon[J].Journal of Alloys and Compounds, 2008, 460 (1-2) :577.
[12] Rehim A, Aly M.A new technique for extracting zirconium form Egyptian zircon concentrate[J].International Journal of Mineral Processing, 2005, 76 (4) :234.
[13] Sun F.Suitable dressing process of a magnetic ore with copper and sulfur[J].Metal Mine, 2012, (10) :70. (孙放.某含铜硫磁铁矿石合理选矿工艺研究[J].金属矿山, 2012, (10) :70.
[14] Zhang J D, Wang L J, Jiang D M.Decomposition process of zircon sand concentrate with CaO-NaOH[J].Rare Metals, 2012, 31 (4) :410.
[15] Koji M, Ohgai M.Formation mechanism of hydrouszirconia particles produced by hydrolysis of ZrOCl2solutions[J].Am.Ceram.Soc., 2000, 83 (6) :1386.
[16] Zhu L, Luo Y H, Zhang J D, Zhang L, Wang L J.Decomposition process of zircon sand with mixed alkali of NaOH-KOH[J].Chinese Journal of Rare Metals, 2012, 36 (5) :799. (朱露, 罗远辉, 张建东, 张力, 王力军.NaOH-KOH混合碱分解锆英砂的工艺研究[J].稀有金属, 2012, 36 (5) :799.