���±�ţ�1004-0609(2008)06-1123-06
LiFe1-xMgxPO4���Ʊ�����绯ѧ����
�� �����Ľܣ����º�����־�ˣ�������
(���ϴ�ѧ ұ���ѧ�빤��ѧԺ����ɳ 410083)
ժ Ҫ�����øɷ�������ĥ-һ�����෴Ӧ�ϳ�LiFe1-xMgxPO4(x = 0��0.01��0.05��0.10��0.20)�������ϡ�����X���������ǡ�ɨ��羵������ɫɢ�ױ�����Ʒ�ľ���ṹ����ò��MgԪ�طֲ������о�Mg��������LiFePO4���ϵ绯ѧ���ܵ�Ӱ�졣����������Ʊ���LiFe1-xMgxPO4(0��x��0.10)Ϊ���࣬��LiFe1-xMgxPO4(x = 0��0.01��0.05��0.10��0.20)�����ߴ���������������������LiFe0.99Mg0.01PO4�ķŵ�������ѣ�����0.1C�����³�ŵ����״ηŵ�����Ϊ150.8 mA?h/g����ʹ��1C�����·ŵ�ʱҲ��129.9 mA?h/g��������ѭ�����ܽϺá�
�ؼ��ʣ�LiFePO4������ӵ�أ��������ϣ�þ����
�й�����ţ�TM 912.9 ���ױ�ʶ�룺A
Synthesis and electrochemical properties of LiFe1-xMgxPO4
LI Xu, PENG Wen-jie, LI Xin-hai, WANG Zhi-xing, GUO Hua-jun
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: LiFe1-xMgxPO4(x = 0, 0.01, 0.05, 0.10 and 0.20) cathode materials were synthesized by one-step solid-state reaction combined a dry high-energy ball milling. The crystalline structure, morphology and Mg distribution were characterized by XRD, SEM and EDS. The effect of amount of doped-Mg on the electrochemical properties of LiFe1-xMgxPO4 was investigated. The results show that the prepared LiFe1-xMgxPO4 (0��x��0.10) is pure, and with the increasing of x value, the crystalline size of LiFe1-xMgxPO4 (x=0, 0.01, 0.05, 0.10 and 0.20) increases. LiFe0.99Mg0.01PO4 sample has higher charge and discharge capacities than other samples��The initial discharge specific capacity of LiFe0.99Mg0.01PO4 is 150.8 mA?h/g at 0.1 C and ambient temperature, 129.9 mA?h/g at 1C, showing that it has good cycling behavior.
Key words: LiFePO4; lithium-ion battery; cathode materials; Mg doping
LiCoO2��1991�걻��ҵ��������������Ȼ������ӿɳ����е���Ҫ���ϣ���Ϊ�������ܶȸߣ�ѭ�����ܺã��ϳɼ�[1]����LiCoO2��������������Դϡ���ҳɱ������ж��������˸ò��ϴ�Χ��Ӧ�ã�����������������°�ȫ���ܷ������ʺ�������ߴ�Ķ�����Դ�����ϵ綯�����ö�����Դ�����ʹ��ܵ�Դ���綯�����õ�Դ��1997�꣬PADHI��[2]����Ծ�������Ϊ�Ǽܹ��ɵ����ʯ��LiFePO4�������ϣ������LiCoO2��˵�߱�ԭ���Ϸḻ���ɱ���������ȫ���ܸ�[3]�ͻ����Ѻò�������������ƣ���������170 mA?h/g��Դ�����۱������ͻ������෴Ӧ(LiFePO4|FePO4)3.4V(vs Li/Li+)�ķŵ�ƽ̨��ѹ������һ����ϣ�����������ϡ�
Ȼ����LiFePO4���������е͵��ӵ�����(10-10 S/cm)��Li+����������滺��������ɢ��ȱ�㣬�����䱶�����������������LiFePO4����������ʵ������ӵ���е�Ӧ�á�Ŀǰ�о���ʾ��ͨ��������ϵ�����[4-5]�����������ӵIJ���[6-8]���Ʊ���ϸ�ҿ����ߴ�ֲ����ȵ���Ʒ[9]�ܿ˷������ʵ͵����⡣CHIANG��[6]���ö������෴Ӧ�Ʊ��۽�������Liλ���ӵ�Li0.99M0.01FePO4(M = Mg2+��Al3+��Ti4+��Nb5+��W6+)�������ϣ������²�õ��ӵ����ʴ��� 10-2 S/cm���봿��(10-10 S/cm)������8��������������ʱ0.1C(15 mA/g)��������ŵ�����Լ142 mA?h/g�� ��1.1C�ϸ߱����·ŵ�Լ120 mA?h/g��������WANG��[7]ͨ���ܽ������ϳ�·���Ʊ�FeλTi���ӵ�LiTi0.01Fe0.99PO4�������ϣ�����C/8(17 mA/g)���ʷŵ�ʱ�����ӽ�160 mA?h/g����Щ���Ƶ����������ڲ���ʹLiFePO4�����ڲ����ṹȱ��(���ֿ�λ�����ӻ��Ѩ��)�������LiFePO4������ӵ����ʡ�Ȼ����Ϊ�˵õ���һ������ʯ�Ͳ�����������������ϣ�������Щ�������ڸ��ӵ��Ʊ�����ͳ�ʱ���ȴ����������⣬�������Ժ�ҵ��������
�ű���[10]������ʹ���Ҵ�����ɢ��������ĥ����-�������෴Ӧ�Ʊ�Mg����Feλ��LiFe1-x-MgxPO4�������ϣ��绯ѧ����Ҳ�õ��˸��ƣ����Dz���������δ֪���ࡣ�����о���ʾ���ںϳ�LiFePO4�������ϣ���е��ѧ���(MA)��Ϊ��һ����ϣ���ķ� ��[11-12]��FANG��[13-14]�����˻�е����ϳ�5 V�⾧ʯ��LiMn1.5Ni0.5O4�������ϵ���Ч�ԡ��ڸ����� ĥ-��е��ѧ��ڼ䣬�����������ĥ�������ܷ�������ײ�����롢����ײ���������·��������ͽ��ܵķ����ϣ�Ȼ�����ȴ��������෴Ӧ�õ����ࡣ��ˣ�����е��ѧ�����Ӧ�����Ʊ����ӵ�LiFePO4�������ϣ������ڴ�����·�̡������Ʊ����ڣ��õ���һ��ġ��绯ѧ���ܺõIJ���LiFePO4�������ϡ�
����������ʹ�øɷ�������ĥ-��е��ѧ��Ƶ�Mg�����������ǰ���壬�ڸ�����ĥ�ڼ�û�������κ���ĥ��ɢ��(������[6, 12]���ἰ�Ҵ����ͪ����Ϊ��ĥ���̵���ĥ��ɢ��)ʹ���Ʊ����ո��Ӱ�ȫ�ͼ�������Ӧ���ڹ�ҵ��������Ȼ����һ�����෴Ӧ�õ�������Ʒ������������������ò���������е绯ѧ���ܼ�⣬�����뱾�о�ǰ�ڱ���ʹ�ô�ͳ�������෨�Ʊ���þ�����������[10]�绯ѧ���жԱȡ�
1 ʵ��
1.1 ���ϵ��Ʊ�
ԭ��ʹ��Li2CO3(��ؼ������ȡ�99%)��NH4H2PO4 (��ؼ������ȡ�99%)��FeC2O4?2H2O(��ؼ������ȡ�99%)��MgO(������ĩ������������99%)����Li��Fe��Mg��P�Ļ�ѧ������1 (1- x)
(1- x)  x
x 1(x = 0��0.01��0.05��0.10��0.20)��������������ʽ��ĥ���ľ��ķ���ϩ�������������������Ϊ1?25���������ĥ5 h���õ�ǰ�����ĩ����ǰ��������ʽ���¹�ʽ¯�ڣ�ͨ�����������650 ���ս�18 h����¯��ȴ������ȡ�����õ����ֲ�������ͬ����������������ϡ�
1(x = 0��0.01��0.05��0.10��0.20)��������������ʽ��ĥ���ľ��ķ���ϩ�������������������Ϊ1?25���������ĥ5 h���õ�ǰ�����ĩ����ǰ��������ʽ���¹�ʽ¯�ڣ�ͨ�����������650 ���ս�18 h����¯��ȴ������ȡ�����õ����ֲ�������ͬ����������������ϡ�
1.2 ���Ϸ��������
����X����������(XRD)��ɨ��羵(SEM)������Ʒ�ľ���ṹ����ò��XRD���Բ��õ����ձ�Rigaku��˾��D/max 2550VB+18 kWת��X����������(X����ԴCu K��������300 mA���ܵ�ѹ40 kV������0.02?��ɨ������8 (?)/min�������ɨ�跶Χ10?~90?��SEM���Բ��õ���JEOL��˾��JSM-5600LVɨ��羵����20 kV�¹۲���Ʒ�ı�����ò��
1.3 ʵ������װ�Ͳ���
ʵ����������Ƭ���Ʊ�����m(��������)�s�������Ȳ�ں�ճ���PVDF��������8 1
1 1�������μ��л��ܼ�N-��������ͪ(NMP)���ɻ�Ͼ��ȵĽ��ϣ��پ���Ϳ����0.02 mm��ļ����������ϣ����������120 �����6 h���õ�������Ƭ������Ϊ�����Ƭ�����ҺΪ1 mol/L LiPF6/ EC+DMC+EMC(�����1
1�������μ��л��ܼ�N-��������ͪ(NMP)���ɻ�Ͼ��ȵĽ��ϣ��پ���Ϳ����0.02 mm��ļ����������ϣ����������120 �����6 h���õ�������Ƭ������Ϊ�����Ƭ�����ҺΪ1 mol/L LiPF6/ EC+DMC+EMC(�����1 1
1 1)�����Һ����ĤΪCelgard 2400�۱�ϡ��Ĥ���ڳ�������������յ�����������װ��CR 2025�Ϳ�ʽ��ز��Բ��ϵĵ绯ѧ���ܡ�ʵ�����������Ժ�ʵҵ����˾������BTS-51���ε�����ܼ�����Ͻ��г�ŵ���ԡ���ŵ緽ʽ���£�������Ժ���0.1C(1C = 140 mA/g)���(��ֹ��ѹΪ4.1 V)�����ѹ���(����ѹ4.1 V����ֹ����Ϊ��������0.01 C��ʱ��2 h)���ŵ��Ժ�����ʽ���У��ŵ����Ϊ0.1C��1C����ֹ��ѹΪ2.5 V��
1)�����Һ����ĤΪCelgard 2400�۱�ϡ��Ĥ���ڳ�������������յ�����������װ��CR 2025�Ϳ�ʽ��ز��Բ��ϵĵ绯ѧ���ܡ�ʵ�����������Ժ�ʵҵ����˾������BTS-51���ε�����ܼ�����Ͻ��г�ŵ���ԡ���ŵ緽ʽ���£�������Ժ���0.1C(1C = 140 mA/g)���(��ֹ��ѹΪ4.1 V)�����ѹ���(����ѹ4.1 V����ֹ����Ϊ��������0.01 C��ʱ��2 h)���ŵ��Ժ�����ʽ���У��ŵ����Ϊ0.1C��1C����ֹ��ѹΪ2.5 V��
2 ���������
2.1 LiFe1-xMgxPO4��Ʒ��X�����������
ͼ1��ʾΪ�ϳɵ�LiFe1-xMgxPO4(x = 0��0.01��0.05��0.10��0.20)��Ʒ��XRD�ף�����������XRD��(JCPDS��-190721)�Աȷ��֣��ϳɵ�LiFePO4��LiFe0.99Mg0.01PO4��LiFe0.95Mg0.05PO4��LiFe0.90Mg0.10- PO4Ϊ���࣬���ϳɵ�LiFe0.80Mg0.20PO4����δ֪���ʷ壬�����ǿ�Ⱥ�С��˵�����������ࡣ����������Ϊ������λþ���ӵ���Ϊ0��x��0.10ʱ��ʹ�øɷ�������ĥ-һ�����෨�Ʊ���LiFe1-xMgxPO4Ϊ���࣬�����о�ǰ�ڱ����Ĵ�ͳ�������෨�Ʊ�LiFe1-xMgxPO4(x = 0.01��0.05��0.10��0.15)[10]�����������ɣ�����ܹ鹦�ڸɷ�������ĥ���������ͽ��ܵķ������ܵõ����Ӿ���һ�µ�ǰ���塣

ͼ1 LiFe1-xMgxPO4��Ʒ��XRD��
Fig.1 XRD patterns of LiFe1�C xMgxPO4 samples
����XRD���ݼ���õ��IJ�����Ʒ���������;���������ڱ�1���ӱ����ܿ���������Mg������x������������a��b�;������V����С�����ơ�����Mg2+�İ뾶(0.066 nm)С��Fe2+�İ뾶(0.074 nm)������������������ϵ���ʯ��LiFePO4(�ռ�Ⱥ��Pnma)������Fe2+ռ�ݰ�����4c λ[15-16]ƽ����a��bƽ�������У���������Mg2+ռ��M2(Fe)λ�����࣬��������a��b��С���¾������VҲ��С��
��1 LiFe1-xMgxPO4��Ʒ�ľ��������;������
Table 1 Lattice parameters and lattice volume of LiFe1-x- MgxPO4 samples

2.2 LiFe1-xMgxPO4��Ʒ��ɨ��羵����
ͼ2��ʾΪ�ϳɵ�LiFe1-xMgxPO4(x = 0��0.01��0.05��0.10��0.20)��Ʒ��ɨ��羵��ͼ�п��Կ��������������Ƚ�С(x��0.05)ʱ��������Ʒһ�ο���ƽ������ԼΪ0.2 ��m����ͼ2(a)~(c)��ʾ����Щ��ϸ������������Ҫ�����ڸ�����ĥ-��е��ѧ�������[12]����ѡ650 ���е����ȴ��������������������Ƚϴ�(x��0.10)ʱ�����Ų���������������Ʒһ�ο���ƽ������������������ƣ���ͼ2(d)��2(e)��ʾ�����������������MgO���Ӽ������ã����������Ŀ����ͱȽϴ�ıȱ�����������������������Ƚϴ��������ս�[17]�����⣬Ҳ�������ս�������Բ�������ĵ�ȱ�������ԭ�ӵ�����ɢ������ʹ�ս��������[17]����������ͬ��е��ѧ������µõ���ǰ�����У���������MgO���Ӽ������������ӣ���ʣ�������������ϴ���ս���̲����ĵ�ȱ�ݽ϶࣬�������ս�������Խ�࣬ʹ�ڲ�����Ʒ�����ս�����Ĵ��������Ƶ�ʾ�Խ�࣬���²�����Ʒ��һ�ο���ƽ������������ͼ2(d)��2(e)�ɿ���������������ϴ�ͬʱ���в���С����������ͼ2(b)��2(c)���Ĵ������С������

ͼ2 �ϳ�LiFe1�C xMgxPO4��Ʒ��SEM��
Fig.2 SEM images of synthesized LiFe1�Cx- MgxPO4 samples: (a) x = 0; (b) x = 0.01;(c) x = 0.05; (d) x = 0.10; (e) x = 0.20
ͼ3��ʾΪLiFe0.99Mg0.01PO4��ƷMgԪ�طֲ����Ա�ͼ3(b)��ͼ3(a)�����Կ���MgԪ����LiFe0.99- Mg0.01PO4��Ʒ���Ǿ��ȷֲ��ģ�˵���øɷ�������ĥþ����һ�����෴Ӧ�ܺϳ�þԭ�ӷֲ����ȵ���������������ϡ�

ͼ3 LiFe0.99Mg0.01PO4��Ʒ��SEM��ò��MgԪ�طֲ�
Fig.3 SEM image(a) and Mg element distribution mapping for LiFe0.99Mg0.01PO4 sample
`2.3 LiFe1-xMgxPO4��Ʒ�ĵ绯ѧ����
ͼ4��ʾΪLiFe1-xMgxPO4(x = 0��0.01��0.05��0.10��0.20)��Ʒ������0.1C(14 mA/g)�״�ѭ����ŵ����ߡ���ͼ���ܿ����������ӱ�������Ʒ���зdz�ƽ�ȵ�3.5 V���ƽ̨��3.4 V�ŵ�ƽ̨��Ϊ�������ʯ�������������ת����̣���LiFe1-xMgxPO4(x = 0��0.01��0.05��0.10��0.20)���״ηŵ������ֱ�Ϊ144.6��150.8��136.4��132.2��121.1 mA?h/g���������о�ǰ�ڱ�����125.6 mA?h/g�״ηŵ������ͳ�ŵ�ƽ̨[10]����Щ���Ƶĵ绯ѧ���ܿ��ܹ��ڸɷ�������ĥ-��е��ѧ����յ�ʹ�ã������Ʊ���ϸ�����͵�һ�����ʯ��������ﮣ���ͼ1��ͼ2��ʾ�����⣬��δ���Ӳ�����Ʒ��ȣ���Mg������x = 0.01ʱ��������Ʒ�ķŵ��������˵�����ӹ�����ڲ�����Ʒ�����ķ��ӡ���������Mg2+ȡ��LiFePO4��Fe2+Խ�࣬��λĦ��LiFe1-xMgxPO4�����в���绯ѧ��Ӧ��Fe2+��Խ�٣�����Ҳ��Խ�٣���θ���Padhi��[2]ָ��������﮳�ŵ������﮴���LiFePO4|FePO4������ƣ��ھ���������﮵�������Ͽ����ߴ���һ��������Ҫ�����أ����Դ�SEM������(ͼ2)���ɲ��ӹ��������һ�ο���ƽ����������Ҳ�����ڲ���������������ķ��ӡ�
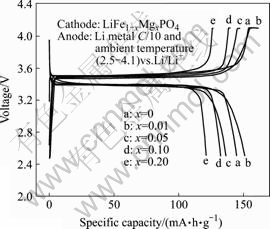
ͼ4 ����ʱ0.1C������LiFe1-xMgxPO4��Ʒ���״�ѭ����ŵ�����
Fig.4 Charge/discharge profiles in first cycle for LiFe1-x- MgxPO4 samples at ambient temperature and 0.1C rate
ͼ5��ʾΪ�ϳɵ�LiFe1-xMgxPO4(x = 0��0.01��0.05��0.10��0.20)��Ʒ�����²�ͬ����ѭ���������ߡ���0.1C�ͱ����·ŵ磬�����ӱ�������Ʒѭ�����ܶ��ȽϺã���20��ѭ�������������ʷֱ�Ϊ97.6%��97.7%��97.4%��97.9%��98.5 %�������ڱ��о�ǰ�ڱ����Ľ��[10]��˵����ϸ�����ĥ-��е��ѧ�����Mg����������﮵��Ʊ��ܵõ��߷ŵ��������ȶ���ѭ������������1C�߱��ʷŵ��£�δ������Ʒ�ķŵ�����Ϊ123.6 mA?h/g����0.1C��������85.5%��10��ѭ��������������Ϊ99.1%������һ����෨�ϳɵĴ����������������(20 �棬�ŵ�����ܶ�Ϊ0.5 mA/cm2���ŵ�����Ϊ116 mA?h/g��10��ѭ��������������ԼΪ97%)[18]���Ҫ�ã�˵��������ĥ-��е��ѧ������������Ʊ�������﮵���Ч�ԡ���������x = 0.01����x = 0.10ʱ��������Ʒ1C�ŵ�������129.9����108.6 mA?h/g����ռ0.1C������86.2���� 82.2 %��10��ѭ�������������ʴ�99.5����95.3 %��˵�����ӹ���Ҳ�����ڲ�����Ʒ�������ܵķ��ӡ�����ܹ��ڲ��ӹ��������һ�ο���ƽ����������;�������ļ�С(���1���У�x = 0.01����VֵΪ0.290 7 nm3��x = 0.20����VֵΪ0.288 9 nm3)��ʹ���Ӵ���·���������;����϶�ļ��٣����²����в�����ӵ��������Ͳ�ı������ܡ�
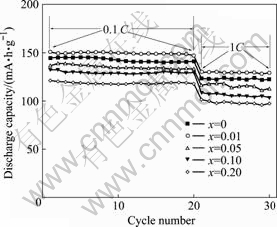
ͼ5 LiFe1-xMgxPO4��Ʒ�����²�ͬ����ѭ������
Fig.5 Cycling performance of LiFe1-xMgxPO4 samples at ambient temperature under various rates
���LiFe0.99Mg0.01PO4���ϵĵ絼��Ϊ10-3~10-4 S/cm���봿�������(Լ10-9~10-10 S/cm)[6]��ȵ絼�������6����������
��������þ���Ӹ�����������������ϵĵ絼�ʣ�������[10]��������ϸ���͡�����Mg����ȡ��Feλ��������LiFePO4�Ĵ�λȱ�ݣ��Բ��ϵĵ絼�ʵ�����а��������Mg2+�İ뾶(0.066 nm)С��Fe2+�İ뾶(0.074 nm)������Mg������仯����(���1���У�δ���ӵ�VֵΪ0.290 6 nm3��������x = 0.01��VֵΪ0.290 7 nm3)��Ȼʹ�����еĿ�϶���ӣ��Ӷ�Ϊ���Ӽ����ӵ��˶��ṩ�����ͨ����ʹ���ϵĵ絼����ߡ�
3 ����
1) ��Mg���������е�ʱ�����Ʊ��������ʯ�ṹ��LiFe1-xMgxPO4(0��x��0.10)�������ϡ�
2) ��������a��b���������V���Ų����������Ӷ���С��
3) ��Mg������(0��x��0.05)�Ƚϵ͵�ʱ��ʹ�ø÷����Ʊ�����ϸ�Ŀ���������Mg������(x��0.10)�����ʱ���������������Ʒ�����ij���
4) �绯ѧ���ܼ�ⷢ�֣���ƷLiFe0.99Mg0.01PO4�ĵ绯ѧ������ѣ�����0.1C�����³�ŵ����״ηŵ�����Ϊ150.8 mA?h/g��20��ѭ��������������Ϊ97.7 %����ʹ��1C�߱��ʷŵ��£�Ҳ��129.9 mA?h/g��������10��ѭ��������������˥������Ϊ������Mg���������ڲ�����Ʒ�����ͱ������ܵķ��ӡ�
REFERENCES
[1] CHEN J M, TSAI C L, YAO C Y, SHEU S P, SHIH H C. Experimental design method applied to Li/LiCoO2 rechargeable cells[J]. Mater Chem and Phys, 1997, 51: 190-194.
[2] PADHI A K, NANJUNDASWAMY K S, GOODENOUGH J B. Phospho-olivines as positive-electrode materials for rechargeable lithium batteries[J]. J Electrochem Soc, 1997, 144(4): 1188-1194.
[3] YANG S, SONG Y, ZAVALIJ P Y, WHITTINGHAM M S. Reactivity, stability and electrochemical behavior of lithium iron phosphates[J]. Electrochem Commun, 2002, 4: 239-144.
[4] CROCE F, EPIFANIO A D, HASSOUN J, DEPTULA A, OLCZAC T. A novel concept for the synthesis of an improved LiFePO4 lithium battery cathode[J]. Electrochem Solid-State Lett, 2002, 5(3): A47-A50.
[5] ������, ������, ������. ��Һ���ϳ�LiFePO4/C�������ϼ���绯ѧ����[J]. ����ѧѧ��, 2006, 22(9): 1610-1614.
XU Zhi-hui, LAI Qiong-yu, JI Xiao-yang. Microemulsion synthesis and electrochemical properties of LiFePO4/C cathode materials[J]. Chinese J Inorg Chem, 2006, 22(9): 1610-1614.
[6] CHUNG S Y, BLOKING J T, CHIANG Y M. Electronically conductive phospho-olivines as lithium storage electrodes[J]. Nat Mater, 2002, 1: 123-128.
[7] WANG G X, BEWLAY S, NEEDHAM S A, LIU H K, LIU R S. Synthesis and characterization of LiFePO4 and LiTi0.01Fe0.99PO4 cathode materials[J]. J Electrochem Soc A, 2006, 153(1): A25-A31.
[8] YANG J, XU J J. Synthesis and characterization of carbon- coated lithium transition metal phosphates LiMPO4 (M = Fe, Mn, Co, Ni) prepared via a nonaqueous sol-gel route[J]. J Electrochem Soc, 2006, 153(4): A716-A723.
[9] ARNOLD G, GARCHE J, HEMMER R, STR?BELE S, VOGLER C, WOHLFAHRT-MEHRENS M. Fine-particle lithium iron phosphate LiFePO4 synthesized by a new low-cost aqueous precipitation technique[J]. J Power Sources, 2003, 119/121: 247-251.
[10] �� ��, ���º�, ���ı�, ��־��. LiFe1-xMgxPO4����ӵ���������ϵĵ绯ѧ����[J]. ���ϴ�ѧѧ��: ��Ȼ��ѧ��, 2006, 37(6): 1094-1097.
ZHANG Bao, LI Xin-hai, LUO Wen-bin, WANG Zhi-xing. Electrochemical properties of LiFe1-xMgxPO4 for cathode materials of lithium ion batteries[J]. J Cent South Univ : Science and Technology, 2006, 37(6): 1094-1097.
[11] FRANGER S, CRAS F L, BOURBON C, ROUAULT H. Comparison between different LiFePO4 synthesis routes and their influence on its physico-chemical properties[J]. J Power Sources, 2003, 119/121: 252-257.
[12] KWON S J, KIM C W, JEONG W T, LEE K S. Synthesis and electrochemical properties of olivine LiFePO4 as a cathode material prepared by mechanical alloying[J]. J Power Sources, 2004, 137: 93-99.
[13] FANG H S, WANG Z X, YIN Z L, LI X H, GUO H J, PENG W J. Effect of ball milling and electrolyte on properties of high-voltage LiNi0.5Mn1.5O4 spinel[J]. Trans Nonferrous Met Soc China, 2005, 15(6): 1429-1432.
[14] FANG H S, WANG Z X, LI X H, GUO H J, PENG W J. Exploration of high capacity LiNi0.5Mn1.5O4 synthesized by solid-state reaction[J]. J Power Sources, 2006, 153: 174-176.
[15] ANDERSSON A S, KALSKA B, H?GGSTR?M L, THOMAS J O. Lithium extraction/insertion in LiFePO4: an X-ray diffraction and M?ssbauer spectroscopy study[J]. Solid State Ionics, 2000, 130: 41-52.
[16] ANDERSSON A S, THOMAS J O. The source of first-cycle capacity loss in LiFePO4[J]. J Power Sources, 2001, 97/98: 498-502.
[17] ������. ��ĩ�ս�����[M]. ����: ұ��ҵ������, 2007: 11-19.
GUO Shi-ju. Theory of powder sintering[M]. Beijing: Metallurgical Industry Press, 2007: 11-19.
[18] TAKAHASHI M, TOBISHIMA S, TAKEI K, SAKURAI Y. Characterization of LiFePO4 as the cathode material for rechargeable lithium batteries[J]. J Power Sources, 2001, 97/98: 508-511.
������Ŀ�������ص�����о���չ�ƻ�������Ŀ(2007CB613607)
�ո����ڣ�2007-09-30�������ڣ�2007-03-24
ͨѶ���ߣ����Ľܣ������ڣ���ʿ���绰��0731-8836633��E-mail: lixu_1103@163.com
(�༭ �°���)