���±�ţ�1004-0609(2014)02-0506-05
ͭ����ѡ��Cu(��)��Ni(��)���Ӷ�����ʯ�Ļ����
�� ��1, 2�����ǻ�1���ﴫҢ3��������2
(1. ������ѧ ��Դ����ľ����ѧԺ������ 110819��
2. ���ɹſƼ���ѧ ��ҵ����ѧԺ����ͷ 014010��
3. ������ұ�о���Ժ������ 100044)
ժ Ҫ��ͨ�������︡ѡ��Zeta��λ���ԡ��������������Һ��ѧ����������о�Cu(��)��Ni(��)���Ӷ�����ʯ��ѡ�Ļ�����������������ҺpH��6.5ʱ��ͭ������ˮ��Һ�е��������Ϊ������ͭ������������ͭ��������������ʯ���棬���ԭ�����Ӧ���Ӷ������ʯ��ѡ����ҺpH��8ʱ����������ˮ��Һ���������Ϊ��������������������������ʯ����ʹ����������������Cu2+��������pHֵ��Χ�ڣ�ͭ������ˮ��Һ����Ҫ��Cu2+��Ni2+��ʽ���ڣ�������ʯ��ѡû�л���á�
�ؼ��ʣ�ͭ����ѡ���������ʯ
��ͼ����ţ�TD951 �� �� ���ױ�־�룺A
Activation mechanism of serpentine by Cu(��) and Ni(��) ions in copper-nickel sulfide ore flotation
CAO Zhao1, 2, ZHANG Ya-hui1, SUN Chuan-yao3, CAO Yong-dan2
(1. College of Resources and Civil Engineering, Northeastern University, Shenyang 110819, China;
2. School of Mining Engineering, Inter Mongolia University of Science and Technology, Baotou 014010, China;
3. Beijing General Research Institute of Mining and Metallurgy, Beijing 100044, China)
Abstract: The activation mechanism of serpentine by Cu2+ and Ni2+ in copper-nickel sulfide ore floatation was investigated with pure mineral flotation tests, Zeta potential measurement, IR spectrum measurement and solution chemistry analysis. The results show that copper hydroxide Cu(OH)2 is the main component in cupric solution as pH��6.5, which will cover up serpentine and react with xanthate, activating the flotation of serpentine. And similarly, the nickel hydroxide Ni(OH)2 is the main component in nickelous solution at pH��8, which will be adsorbed onto serpentine and make it activated, and the activation of Ni2+ is weaker the that of Cu2+. While in acidic pH range, metal ions of Cu2+ and Ni2+ are the main species in solution, which can not activate the flotation of serpentine.
Key words: copper-nickel sulfide ore; flotation; activation; serpentine
ͭ����ѡ������MgO��ʯ���ﳤ������һֱ��ѡ��ļ������⣬��ʯ����ҪMgO��ʯ����������ʯ����ʯ������ʯ��[1]���о�������ͭ����ѡ��MgO��ʯ������Ҫ������3�ַ�ʽ���븡ѡ����1) MgO��ʯ��������ͭ�����������巽ʽ���뾫��2) ���ڿ�����ʯ�ָ������ÿ������桢ճ������ˮ���ż��ӷ�ʽ���뾫��[2-4]��3) ��þ��״�����ο���(�绬ʯ)���ھ���������Ȼ�ɸ��Զ����븡ѡ����[5-6]��
FORNASIERO��[7]��MALYSIAK��[8]�о�����MgO��ʯ�������ܿ���Cu2+��Ni2+����ܱ���ҩ�����ϸ�������������Ҷ�������ϼ�������ϴ����ȥ������ʯ����ʯ����ʯ����ʯ�������������ӵĻ����[9-13]��
��������ͨ�������︡ѡ��Zeta��λ���ԡ�������ײ��Ժ���Һ��ѧ����ȷ������о�����ѡ��Cu2+��Ni2+�������Ӷ�����ʯ��ʯ����Ļ���ã�Ϊ��һ���о�ͭ����ѡ��MgO��ʯ�������Ƽ��ṩ���ۼ�����������
1 ʵ��
1.1 �������Լ�
����ʯ������ȡ��ɽ�����ԣ��������ѡ���ô���ĥĥϸ���õ�37~74 ��m��������Ʒ���ڴ����︡ѡ���顣
���������ᡢ�������ơ�CuSO4��5H2O��NiSO4��6H2O��Ϊ�������������ƻ�ҩΪ��ҵ����������ˮΪһ������ˮ��
1.2 �����
1.2.1 �����︡ѡ����
�����︡ѡ�������40 mL XFG �Ҳ�ʽ��ѡ����ÿ�γ�ȡ����ʯ������2 g�����ڸ�ѡ���ڣ�����һ��Ũ�ȸ�ѡҩ��(�Ե����������ռ������ݼ�˳������)��ÿ�μ�ҩ�����5 min����pHֵ��ѡ�ֹ�����5 min�������ڲ�Ʒ����ĭ��Ʒ��ɡ��������������ʡ�
1.2.2 Zeta�����
������ʯ������ϸĥ��������2 ��m��ȡһ�������Ƴ�Ũ��Ϊ0.6 g/L����Һ����������������������Malvern Zetasizer Nano ZS90��������������ʯZeta��λ��ÿ���3�κ�ȡƽ��ֵ��
1.2.3 ���������
��ȡ������2 ��m������ʯ������2 g������������������pHֵ������10-4 mol/L��Cu2+��100 mg/L�Ķ���ҩ����ֽ�����ô���������������������ϲ���Һ��Ȼ��������ˮ���ϴ�ӿ����Һ�������Ȼ���ɣ�����Nicolet FTIR-670 ����Ҷ�任��������ǽ��к�����ײ��ԡ�
1.2.4 ��Һ��ѧ�����������
ʹ��IUPAC SC-database���ݿ⼰SCDbase Species.exe��Һ��ѧ�������������㲢���Ƴ�Cu2+��Ni2+��Һ��������֣���OriginPro 8.0������ͼ��
2 ���������
2.1 �����︡ѡ
�ڶ�����ҩ����Ϊ1.2��10-4 mol/L���ɴ�������Ϊ15 mg/Lʱ�����첻ͬCu2+Ũ����pHֵ������ʯ��ѡ��Ӱ�죬�����ͼ1��ʾ����ͼ1���Կ�������Һ����Cu2+��pHֵ��5~11��Χ��ʱ������ʯ�����ʾ�����10%����Һ�д��ڲ�ͬŨ��Cu2+ʱ������ʯ����������pHֵ���߶�������pH=9���Ҵﵽ���ֵ��֮����pHֵ�������С��
��ͬpHֵ�²�ͬCu2+Ũ�ȶ�����ʯ��ѡӰ�������Cu2+Ũ��Ϊ5��10-4 mol/Lʱ������ʯ��ѡ��������ߣ�Cu2+Ũ��������1��10-3 mol/L����ʯ�����ʷ����½��������Cu2+Ũ��Ϊ5��10-4 mol/Lʱ����ʯ�����ѱ��ǻ�ͭ����ﱥ����������Һ�й���Cu2+���ǻ�ͭ������ӻ�������Ļ�ҩ����ɻ������½���������Cu2+Ũ�ȼ�������pHֵ�����£�Cu2+������ʯ��ѡ��������á�
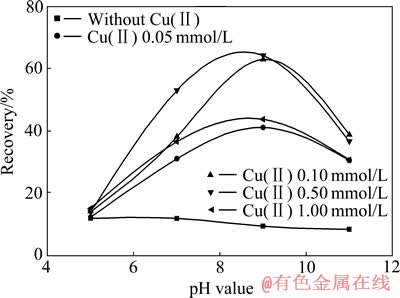
ͼ1 pHֵ��Cu2+Ũ�ȶ�����ʯ�����ʵ�Ӱ��
Fig. 1 Effects of pH value and Cu2+ concentration on recovery of serpentine
ͼ2��ʾΪ��ͬNi2+Ũ����pHֵ������ʯ��ѡӰ��(������ҩ����1.2��10-4 mol/L���ɴ���15 mg/L)����ͼ2�ɼ�����Һ��Ni2+Ũ��Ϊ5��10-4 mol/Lʱ������ʯ��������pH=9���Ҵﵽ���ֵ������Ni2+��һ��Ũ�ȼ�������pHֵ�����¶�����ʯ��һ���Ļ���ã�����������Cu2+������
2.2 Zeta��λ���Է���

ͼ2 pHֵ��Ni2+Ũ�ȶ�����ʯ������Ӱ��
Fig. 2 Effects of pH value and Ni2+ concentration on recovery of serpentine
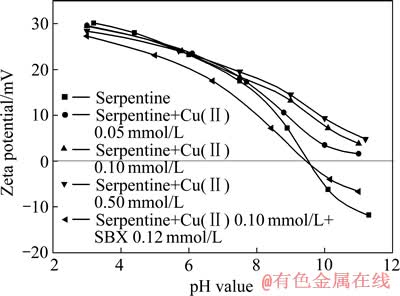
ͼ3 pHֵ��Cu2+Ũ�ȶ�����ʯZeta��λ��Ӱ��
Fig. 3 Effects of pH value and Cu2+ concentration on Zeta potential of serpentine
���첻ͬCu2+Ũ�ȶ�����ʯZeta��λ��Ӱ�죬�����ͼ3��ʾ����ͼ3�ɼ�����Һ��û��Cu2+���� ʱ������ʯZeta��λ��pHֵ�������С������pHֵΪ9.4����Һ�м���Cu2+ʱ��pH��6.5������ʯZeta��λû�б仯������Cu2+������ʯ�����������٣�pH��6.5������ʯZeta��λ���ƣ���Cu2+Ũ��Խ������ʯZeta��λ���Ʒ���Խ����Cu2+��ͭ���ǻ�������������ڿ�����棬��������ʯ����Zeta��λ�����붡����ҩ��ԭ���������ʯ����������ͭ���ӷ�Ӧ���ɻ�ԭ��ͭ���Ӷ�����Cu2+������ɣ���������ʯ����Zeta��λ��
ͼ4��ʾΪ��ͬNi2+Ũ�ȶ�����ʯZeta��λ��Ӱ�졣��ͼ4�ɼ�����Һ�д���Ni2+ʱ��pH��8������ʯZeta��λû�б仯������Ni2+������ʯ�����������٣�pH��8������ʯZeta��λ���ƣ���Ni2+Ũ��Խ������ʯZeta��λ���Ʒ���Խ����Ni2+ �������ǻ�������������ڿ�����棬��������ʯ����Zeta��λ�����붡����ҩ��ԭ���������ʯ���������������ӷ�Ӧ���ɻ�ԭ�������Ӷ���������ʯ����Zeta��λ��
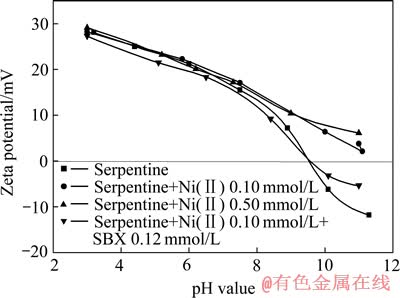
ͼ4 pHֵ��Ni2+Ũ�ȶ�����ʯZeta��λ��Ӱ��
Fig. 4 Effect of pH value and Ni2+ concentration on Zeta potential of serpentine
2.3 ���������

ͼ5 ����ʯ�붡��ҩ����ǰ��ĺ������
Fig. 5 Contrast infrared spectra of adsorbed onto serpentine
Ϊ���о�����ʯ��Cu2+�ǰ���붡��ҩ����������������˺���������������ͼ5��ʾ����ͼ5�ɼ�������aΪ�����ƻ�ҩ�ĺ�����ף�1 178.5��1 155.4 cm-1��ΪC��O��C�����Գ������壬1 104.8 cm-1��ΪC��O��C���Գ������壬1 071.5 cm-1��ΪC=S��������[14-16]������bΪ��ԭ��ͭ�ĺ�����ף�1 145.7 cm-1��ΪC��O��C�����Գ������壬1 110.3 cm-1��ΪC��O��C���Գ������壬1 020.8 cm-1��ΪC=S�������壻����cΪ����ʯ��Cu2+���ú��붡��ҩ��Ӧ�ĺ�����ף��ɼ�����ҩ������ʯ����ͭ��Ӧ�����˻�ҩ��C��O��C��������(����1 125.2��1 085.3 cm-1��)��C=S��������(����1 042.6 cm-1��)����������ʯ����������ͭ���������ԭ�����Ӧ���ɻ�ԭ��ͭ������dΪ����ʯ�ĺ�����ף�����eΪ����ʯ�붡��ҩ��Ӧ��ĺ�����ף�������a��b��c��d�Աȣ�����eֻ������ʯ��Ӧ���շ壬û�г��ֶ���ҩ����ԭ��ͭ�������ŵ����շ壬��������ҩû��������ʯ��������������������ʯ����ֱ�ӷ�Ӧ��
2.4 Cu(��)��Ni(��)ˮ��Һ��������ּ������
��Һ��Cu2+Ũ��Ϊ10-4 mol/L�������Cu2+ˮ��Һ��������ֲַ���ͼ6��ʾ����ͼ6�ɼ�����ҺpH��6.5ʱ����Һ����Ҫ���ΪCu2+�������︡ѡ��Zeta��λ���Ա�������ҺpH��6.5ʱ��Cu2+����������ʯ�������������Զ�����ʯ��ѡ����ã�Ҳ����ı�����ʯ����Zeta��λ����ҺpH��6.5ʱ����Һ���������Ϊ������ͭ����(Cu(OH)2)��������ͭ��������������ʯ���棬����Һ�л�ԭ�����Ӧ���Ӷ������ʯ��ѡ��
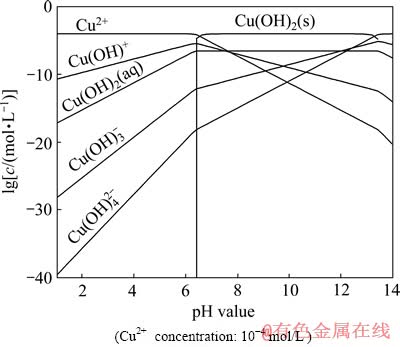
ͼ6 Cu2+��Һ��ϵlg c��pHͼ
Fig. 6 lg c��pH diagram of Cu2+ solution system
��Һ��Ni2+Ũ��Ϊ10-4 mol/L�������Ni2+ˮ��Һ��������ֲַ���ͼ7��ʾ����ͼ7�ɼ�����ҺpH��8ʱ����Һ����Ҫ���ΪNi2+�������︡ѡ��Zeta��λ���Ա�����pH��8ʱ��Ni2+����������ʯ�������������Զ�����ʯ��ѡû�л���ã�Ҳ����ı�����ʯ����Zeta��λ����ҺpH��8ʱ����Һ���������Ϊ������������(Ni(OH)2)�������︡ѡ��Zeta��λ���Ա�����pH��8ʱ������������������������ʯ���棬�Ӷ�������ʯ��ѡ����á�
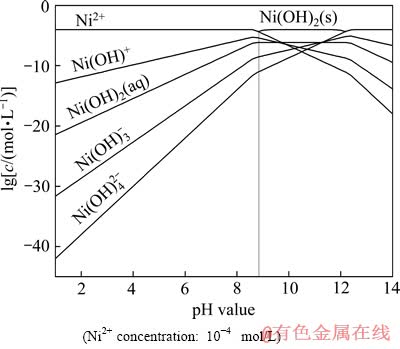
ͼ7 Ni2+��Һ��ϵlg c �� pHͼ
Fig. 7 lg c �� pH diagram of Ni2+ (Ni2+ concentration: 10-4 mol/L)
3 ����
1) �����︡ѡ��������ҩ�����ռ�ʱ��Cu2+��Ni2+�ֱ�����ҺpH��6.5��pH��8ʱ������ʯ��ѡ���л���ã���Cu2+������ʯ�Ļ��������Ni2+������ʯ�Ļ������
2) Zeta��λ���Ա�����Cu2+����ҺpH��6.5ʱ������ʯZeta��λ��Ӱ�죬����ҺpH��6.5ʱ����������ʯ����Zeta��λ������ҺpH��6.5ʱ��Cu2+����Һ��Ҫ���Ϊ������ͭ����������������ʯ����ʹ����Ni2+����ҺpH��8ʱ������ʯZeta��λ��Ӱ�죬����ҺpH��8ʱ��ʹ����ʯ����Zeta��λ���ơ�����ҺpH��8ʱ��Ni2+����Һ��Ҫ���Ϊ������������������������ʯ���棬�Ӷ������ʯ��ѡ��������pHֵ��Χ�ڣ�ͭ������ˮ��Һ����Ҫ��Cu2+��Ni2+��ʽ���ڣ�������ʯ��ѡû�л���á�
3) �������������������ҺpH=9ʱ����ʯ��Cu2+���ú�(�������Ϊ������ͭ����)�����붡��ҩ��Ӧ�ĺ�������г����˻�ҩ��C��O��C��������(��Զ���ҩ����1 125.2��1 085.3 cm-1��)��C=S��������(����1 042.6 cm-1��)����������������ʯ�����ͭ���������ԭ�����Ӧ���ɻ�ԭ��ͭ���Ӷ���������ʯ����Ļ��
REFERENCES
[1] ���ǻ�, �Ϸ���, �ﴫҢ. ͭ����ѡ������MgO��ʯ��������;��̽��[J]. ��ұ, 2012, 21(2): 1-5.
ZHANG Ya-hui, MENG Fan-dong, SUN Chuan-yao. Analysis of effective approaches for depressing MgO-containing gangue minerals in copper-nickel sulfide ore floatation[J]. Mining & Metallurgy, 2012, 21(2): 1-5.
[2] �� ��, ������, ¬����. ��ƫ����������ͭ����ѡ�еķ�ɢ����[J]. �й���ɫ����ѧ��, 2012, 22(6): 1763-1769.
LONG Tao, FENG Qi-ming, LU Yi-ping. Dispersive mechanism of sodium hexametaphosphate on flotation of copper-nickel sulphide[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(6): 1763-1769.
[3] EDWARDS C R, KIPKIE W B, AGAR G E. The effect of slime coatings of the serpentine minerals, chrysotile and lizardite, on pentlandite flotation[J]. International Journal of Mineral Processing, 1980, 7(1): 47-50.
[4] �� ��, ���ı�. ��ϸ��ͭ����ѡ������ʯ����ʯ���︡ѡ��Ϊ�о�[J]. �й���ҵ, 2008, 17(2): 47-50.
TANG Min, ZHANG Wen-bin. A study on floatability of serpentine in ultra-fine copper-nickel sulfide[J]. China Mining Magazine, 2008, 17(2): 47-50.
[5] BEATTIE D A, HUYNH L, KAGGWA G B N, RALSTON J. The effect of polysaccharides and polyacrylamides on the depression of talc and the flotation of sulphide minerals[J]. Minerals Engineering, 2006, 19(6/8): 596-608.
[6] ¬˸ʮ. ��ʯ�ľ��廯ѧ�о���������ɫ������ѡ���еĸ�ѡ��״��ʵ��[J]. ��ұ, 2010, 19(3): 8-11.
LU Shuo-shi. Research on crystal chemistry of talc and review and application of talc flotation in minerals processing of nonferrous sulphide ores[J]. Mining & Metallurgy, 2010, 19(3): 8-11.
[7] FORNASIERO D, RALSTON J. Cu(��) and Ni(��) activation in the flotation of quartz, lizardite and chlorite[J]. International Journal of Mineral Processing, 2005, 76(1): 75-81.
[8] MALYSIAK V, SHACKLETON N J, O��CONNOR C T. An investigation into the floatability of a pentlandite�Cpyroxene system[J]. International Journal of Mineral Processing, 2004, 74(1/4): 251-262.
[9] MALYSIAK V, O��CONNOR C T, RALSTON J, GERSON A R, COETZER L P, BRADSHAW D J. Pentlandite-feldspar interaction and its effect on separation by flotation[J]. International Journal of Mineral Processing, 2002, 66(1/4): 89-106.
[10] BREMMELL E, FORNASIERO D, RALSTON J. Pentlandite�C lizardite interactions and implications for their separation by flotation[J]. Colloids and Surfaces A, 2005, 252(2/3): 207-212.
[11] SHACKLETON N J, MALYSIAK V, O��CONNOR C T. The use of amine complexes in managing inadvertent activation of pyroxene in a pentlandite-pyroxene flotation system[J]. Minerals Engineering, 2003, 16(9): 849-856.
[12] KELEBEK S, TUKEL C. The effect of sodium metabisulfite and triethylenetetramine system on pentlandite�Cpyrrhotite separation[J]. International Journal of Mineral Processing, 1999, 57(2): 135-152.
[13] SUI C, FINCH J A, XU Z. Effect of diethylenetriamine on xanthate interaction with Pb-contaminated Pyrite[J]. Minerals Engineering, 1998, 11(7): 639-649.
[14] WANG Xiang-huai. Interfacial electrochemistry of pyrite oxidation and flotation ��. FTIR studies of xanthate adsorption on pyrite surfaces in neutral pH solutions[J]. Journal of Colloid and Interface Science, 1995, 171(2): 413-428.
[15] HU Yue-hua, SUN Wei, WANG Dian-zuo. Electrochemistry of flotation of sulphide minerals[M]. Beijing: Tsinghua University Press, 2009: 99-102.
[16] ZHANG Ya-hui, CAO Zhao, SUN Chuan-yao, CAO Yong-dan. FTIR studies of xanthate adsorption on chalcopyrite, pentlandite and pyrite surfaces[J]. Journal of Molecular Structure, 2013, 1048(9): 434-440.
(�༭ ��ѧ��)
������Ŀ��������Ȼ��ѧ����������Ŀ( 51174154)�����ɹſƼ���ѧ���»���������Ŀ(2012NCL012��2012NCL029)
�ո����ڣ�2013-04-07�������ڣ�2013-07-24
ͨ�����ߣ����ǻԣ����ڣ���ʿ���绰��13504009158��E-mail: zhangyahui@mail.neu.edu.cn