莲子蛋白酶解的扩散-反应动力学
蔡联辉,曾虹燕,蔡西玲,刘学英,谭奕哲
(湘潭大学 化工学院,湖南 湘潭,411105)
摘要:为了探索莲子蛋白质的酶水解动力学特性,于温度为55 ℃和pH为5.0的条件下,用木瓜蛋白酶酶解莲子蛋白研究酶解莲子蛋白的拟态条件下的米氏常数Km,构建考虑底物抑制和无抑制等影响因素下的扩散-反应动力学模型。研究结果表明:酶和底物在反应体系中的扩散影响酶解反应;当底物初始质量浓度高于13.63 g/L时,反应底物对酶解产生抑制作用;建立的数学模型能够合理地描述和解释莲子蛋白降解的动力学过程,为确定酶解反应的各种参数提供依据。
关键词:莲子蛋白;木瓜蛋白酶;酶解;动力学
中图分类号:TS201.2 文献标志码:A 文章编号:1672-7207(2013)05-1775-06
Diffusion-reaction kinetics for enzymatic hydrolysis of Lotus Seed Protein
CAI Lianhui, ZENG Hongyan, CAI Xiling, LIU Xueying, TAN Yizhe
(School of Chemical Engineering, Xiangtan University, Xiangtan 411105, China)
Abstract: The enzymatic hydrolysis of lotus seed protein by papain was carried out with pH-stat method at pH 5.0 and 55 ℃ to study the enzymatic hydrolysis kinetic characterization in lotus seed processing. The Michaelis constant Km was investigated under the mimesis of papain hydrolysis using lotus seed protein as a substrate. The diffusion-reaction kinetic model was established under the conditions of substrate inhibition and no-inhibition. The results show that the diffusion of enzyme and substrate in the reaction system affects the enzyme reaction velocity. The substrate inhibites the papain activity when the initial concentration is above 13.63 g/L. The model can simulate the enzymatic hydrolysis of lotus seed protein, and it provides theoretical reference to the determination of the parameters of enzymatic hydrolysis process.
Key words: lotus seed protein; papain; enzymatic hydrolysis; kinetic
莲子为睡莲科植物莲的种子,营养丰富,富含蛋白质,且莲子蛋白是氨基酸平衡较理想的优质植物蛋白[1]。酶水解可改变蛋白质的空间结构,蛋白质通过酶水解可制备营养价值更高和功能性质更好的蛋白多肽等产品[2-3]。目前,莲子蛋白的研究多停留在提取工艺和组成方面,很少见对莲子蛋白酶水解及其水解动力学的研究。根据酶水解原理及酶促动力学理论,蛋白酶解是一个复杂的反应过程,酶解分为底物分子扩散到酶上和酶剪切底物分子,其反应速率与底物的扩散速率直接相关, 强运动阻力会制约底物分子的扩散运动,进而影响反应的速度,对酶解反应动力学产生影响[4-7]。目前,人们蛋白酶解体系中扩散现象的研究较少,有关构建蛋白酶解反应动力学模型的实验设计往往仅以考察“反应”这单因素,而忽略了底物大分子扩散作用对反应动力学的影响。要全面描述蛋白酶解历程反应行为,有必要引入扩散因素,对其动力学进一步完善。在此,本文作者以莲子蛋白为底物,考察其在木瓜蛋白酶作用下的反应-扩散动力学行为,分析扩散现象对酶解反应的影响,研究木瓜蛋白酶过程的扩散-反应动力学特性,建立相应的水解扩散-反应动力学模型,以便为莲子蛋白酶解反应器的设计和莲子蛋白的开发应用提供依据。
1 材料与方法
1.1 主要材料
主要材料为:木瓜蛋白酶,食品级,80万U/g,北京酶制剂厂生产;空心白莲,湖南宏兴隆湘莲食品有限公司生产,于37 ℃干燥,制成莲子粉(粒径为0.150 mm)。所有化学试剂均为分析纯。
1.2 莲子蛋白提取及酶水解
莲子粉用0.1 mol/L的NaCl于45 ℃的恒温水浴锅中提取1 h,提取液以转速为4 000 r/min离心分离15 min,用0.5 mol/L的HCl 调上清液pH至4.2得莲子蛋白液。
在一定酶质量浓度下于55 ℃水浴酶解特定质量浓度的莲子蛋白液,在水解过程中不断滴加0.1 mol/L NaOH溶液以稳定反应体系pH至5.0。定时取样,样品于90 ℃下灭酶15 min,酸沉未水解蛋白,于转速为4 000 r/min时离心分离15 min,得蛋白多肽的上清液,测定水解度。
1.3 蛋白质含量的测定
参照GB 5497―85,采用凯式定氮法测量蛋白质的含量(仪器为UV9100分光光度计,日立公司制造)。
1.4 水解度的测定
取一定底物质量浓度为ρ0(单位为g/L)的蛋白水解液于100 mL烧杯中,加入60 mL去CO2蒸馏水,滴加0.1 mol/L NaOH液调其pH至8. 2。加入20 mL质量分数为37%的中性甲醛液,搅拌10 min,滴定 NaOH液至pH为9.2,NaOH液消耗的体积为V2。空白试验测得NaOH液消耗体积为V1(单位为L),则蛋白水解度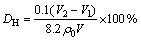 ;水解速率
;水解速率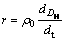 。
。
2 结果与讨论
2.1 底物浓度对水解度的影响
在酶质量浓度为0.5 g/L的条件下,考察不同蛋白浓度对酶解反应的影响,结果见图1。从图1可知:在水解时间相同时,随着底物质量浓度从4.68 g/L增加到27.26 g/L,水解度下降。这可能是随着底物质量浓度的升高,反应体系黏度逐渐增大,底物蛋白分子和木瓜蛋白酶扩散速度不断减小,降低了底物与酶分子的碰撞概率,从而使水解度DH逐渐降低;另一方面,也可能是集聚于酶活性部位的底物蛋白增多,抑制了水解反应,从而使水解度DH不断降低。
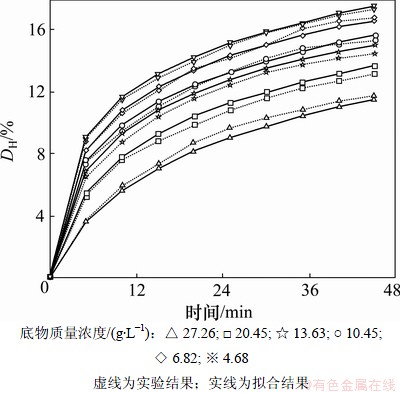
图1 底物质量浓度不同时的水解时程曲线
Fig.1 Time-course curves of protein hydrolysis at different substrate concentrations
2.2 初始酶质量浓度对水解度的影响
在蛋白底物质量浓度为13.63 g/L的条件下,考虑不同初始酶质量浓度对水解度的影响,结果见图2。底物的水解度取决于酶的质量浓度。从图2可知:水解度随着水解时间的延长而趋向稳定, 初始酶质量浓度不同时, 平衡水解度不同, 平衡水解度随初始酶质量浓度的提高而提高。
2.3 水解速率与底物质量浓度
假设木瓜蛋白酶恒温控制水解动力学遵循内切酶限制水解动力学历程,据米氏方程,当反应体系酶用量与底物质量浓度一致时, 则在同一反应条件下反应速率应相同。反应速度r与底物质量浓度ρ0的关系见图3。由图3可知:不同的蛋白底物质量浓度的酶促反应速率有较大差异;当ρ0<13.63 g/L时,随底物质量浓度的增大,反应速率加快;当ρ0>13.63 g/L时,随底物质量浓度的增大,酶解速率逐渐下降。这说明当ρ0超过13.63 g/L时,底物对木瓜蛋白酶水解莲子蛋白有抑制作用。这可能是由于底物和酶分子形成了不具催化反应活性不能分解为产物的死端复合物[8],使酶解反应的速度降低;若底物质量浓度过高,则其反应液黏度增高,底物扩散到酶分子活性中心的阻力增大,其扩散速率变小,存在底物的扩散限制效应,特别在酶催化活性高时,这种扩散限制效更为明显,从而使酶解反应的速度降低。
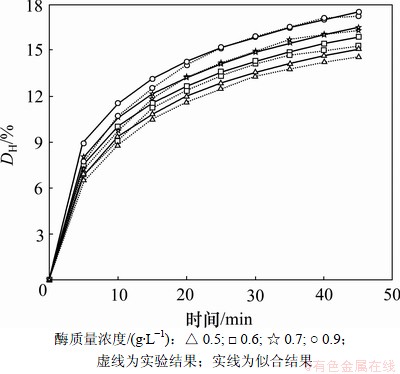
图2 不同酶质量浓度时的水解时程曲线
Fig.2 Time-course curve of protein hydrolysis at different enzyme mass concentrations
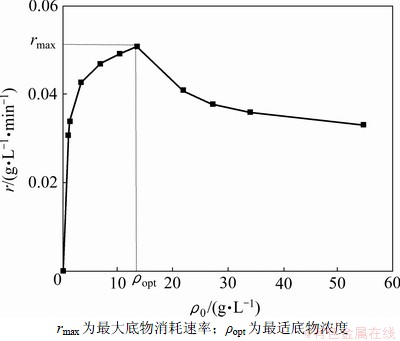
图3 反应速度r与底物质量浓度ρ0的关系
Fig.3 Relationship between reaction rate and substrate concentration
根据反应速度r与底物浓度ρ0的关系,利用双倒数L-B作图法(见图4),可求得米氏常数为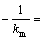
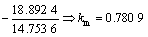 ,最大反应速度rmax=0.052 93g/(L・min)。可见km 很小,有利于底物的转化。在水相酶解莲子蛋白过程中,莲子蛋白酶解程度的控制至关重要。蛋白质适度水解,可使得蛋白质具有较好的功能特性,有利于加工利用。在蛋白的水解过程中,有必要建立酶解速率的扩散-反应动力学模型,推断模型中的扩散-反应常数和底物常数。
,最大反应速度rmax=0.052 93g/(L・min)。可见km 很小,有利于底物的转化。在水相酶解莲子蛋白过程中,莲子蛋白酶解程度的控制至关重要。蛋白质适度水解,可使得蛋白质具有较好的功能特性,有利于加工利用。在蛋白的水解过程中,有必要建立酶解速率的扩散-反应动力学模型,推断模型中的扩散-反应常数和底物常数。
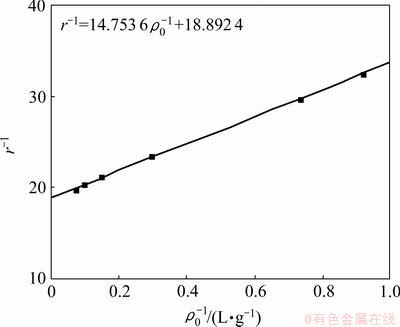
图4 酶解反应的L-B图
Fig.4 Lineweaver-Burk plot for enzymolysis
2.4 扩散-反应动力学模型
木瓜蛋白酶为专一性酶,根据中间产物理论,酶促反应可按下列两步进行,即
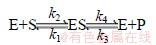
式中:E为木瓜蛋白酶;S为底物;P为产物;k1,k2,k3和k4为速度常数。由于E+P形成ES的速度极慢,故k4可忽略不计。其反应速率决定于不可逆步骤,即
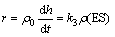 (1)
(1)
式中:k3为酶失活常数。t为反应时间;h为蛋白水解度;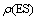 为酶与底物结合物的质量浓度。
为酶与底物结合物的质量浓度。
考虑到蛋白酶在酶解过程中失活,其失活机制可简述为
E+ES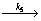 EA+Ei+P
EA+Ei+P
式中:k5为酶失活常数。其失活速率方程为
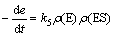 (2)
(2)
其中: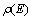 为酶的质量浓度。若存在底物的抑制,则酶解反应简述为
为酶的质量浓度。若存在底物的抑制,则酶解反应简述为
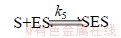
考虑蛋白质单底物水解、蛋白酶失活和底物抑制因素,酶水解反应达到平衡时,水解度h与水解时间t有如下关系[9]:
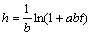 (3)
(3)
其中:a和b为动力学参数,当存在底物抑制时, ,
,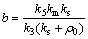 ;当无底物抑制时,
;当无底物抑制时,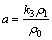 (其中,
(其中,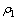 为酶质量浓度;ks为底物抑制常数),
为酶质量浓度;ks为底物抑制常数),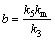 。
。
由于动力学方程式(3)未考虑底物和酶分子在反应体系中的扩散因素,也就是将酶水解的反应时间tr等同于整体反应时间t,当反应体系中底物和酶分子的扩散作用不可忽略时,必须对动力学方程(3)进行修正。莲子蛋白的酶解时间由底物和酶分子扩散并相互接触的时间td和酶水解底物的反应时间tr 构成[10],即反应时间tr=t-td。此时,式(1)转化为
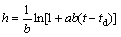 (4)
(4)
底物扩散系数与浓度存在指数函数关系[11-13]。同时,随酶解反应的进行,体系中底物和酶分子扩散并相互接触的时间td也随之增加,故td是酶解时间的函数。因此,td的表达式可设为
 (5)
(5)
式中:kf为指前因子;w0为底物的质量分数。
将式(3)代入式(2) , 可得:
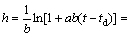
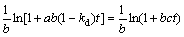 (6)
(6)
其中:km为米氏常数;ks为底物常数;k3为酶催化反应常数;kd为扩散速率。当存在底物抑制时,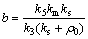 ,
,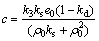 ;当无底物抑制时,
;当无底物抑制时,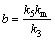 ,
,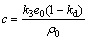 。
。
2.5 扩散-反应动力学模型参数的确定
2.5.1 ρ0和ρ1对参数b和c的影响
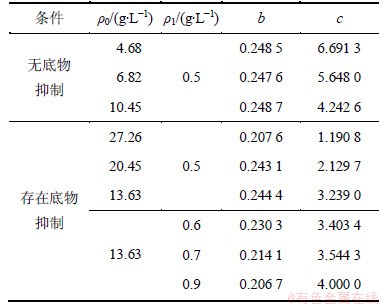
在温度为55 ℃、pH为5.0、底物质量浓度为4.68~27.26 g/L和酶起始质量浓度为0.5~0.9 g/L的条件下,根据方程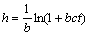 ,对不同底物质量浓度(图1)和不同初始酶质量浓度(图2)试验中的蛋白水解度DH对时间t的关系进行非线性回归运算, 可得该方程(6)中的动力学参数a 和b,见表1。从表1可知:参数b和c随ρ0增大而降低;c随ρ1增大而增加,而b随ρ1增大而减小。
,对不同底物质量浓度(图1)和不同初始酶质量浓度(图2)试验中的蛋白水解度DH对时间t的关系进行非线性回归运算, 可得该方程(6)中的动力学参数a 和b,见表1。从表1可知:参数b和c随ρ0增大而降低;c随ρ1增大而增加,而b随ρ1增大而减小。
2.5.2 扩散-反应动力学的ks,kd及k3
当存在底物抑制 (底物质量浓度ρ0为13.63~27.26 g/L) 时,根据参数b和c的表达形式,以b-1-ρ0及cρ0(bρ1)-1-e-0.1ρ0作图,结果分别见图5(a)和5(b)。利用线性回归方法求出b-1-ρ0的关系式:
b-1=0.018 89ρ0+3.740 0(相关系数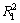 =0.984 3)
=0.984 3)
cρ0(bρ1)-1-e-0.10ρ0的关系式为
cρ0(bρ1)-1=595.392 5-957.838 6e-0.1ρ0(相关系数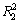 =-0.951 2)
=-0.951 2)
由b的表达式及图5(a)可得:
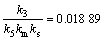 ,
,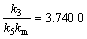 (7)
(7)
由b和c的表达式及图5(b)可得:
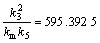 ,
,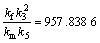 (8)
(8)
由式(7)和(8)解方程求得:k3=159.195 9 g/L;ks=197.988 4 g/L;kd=1.608 8e-0.1ρ0 g/(L・min)。
表1 莲子蛋白酶解动力学参数b和c
Table 1 Kinetic parameters b and c for hydrolysis of lotus seed protein
当无底物抑制(底物浓度ρ0为4.68~13.63 g/L)时,由表1可知:动力学参数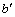 在不同的初始底物质量浓度下,其值相差很小,趋于常数0.248 3。因此,在恒温水解反应中,
在不同的初始底物质量浓度下,其值相差很小,趋于常数0.248 3。因此,在恒温水解反应中,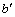 可以看作是常数, 取其平均值。根据参数b和c的表达形式,以
可以看作是常数, 取其平均值。根据参数b和c的表达形式,以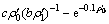 作图,结果见图5(b)。利用线性回归方法求出
作图,结果见图5(b)。利用线性回归方法求出
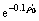 的关系式
的关系式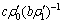 =493.695 1-378.467 3・
=493.695 1-378.467 3・ 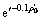 ,相关系数
,相关系数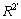 =-0.991 4。由
=-0.991 4。由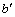 和
和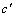 的表达式及图5(b)可得:
的表达式及图5(b)可得: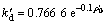 g/(L・min)。
g/(L・min)。
当存在底物抑制时,将实验数据代入拟合方程(6),其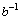 与ρ0以及cρ0(bρ1)-1与
与ρ0以及cρ0(bρ1)-1与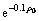 的比值具有很好的线性关系(见图5(a)和(b)),其拟合系数R2的绝对值均大于0.950 0,表明在底物质量浓度ρ0为13.63~27.26 g/L时,木瓜蛋白酶酶解莲子蛋白动力学过程较好地吻合方程(6),证明了扩散-反应模型的有效性;ks和k3相近,为同一数量级,说明底物抑制较易发生。故在酶解过程中,要控制好底物的质量浓度,避免出现底物抑制。由动力学常数计算的最适底物质量浓度(
的比值具有很好的线性关系(见图5(a)和(b)),其拟合系数R2的绝对值均大于0.950 0,表明在底物质量浓度ρ0为13.63~27.26 g/L时,木瓜蛋白酶酶解莲子蛋白动力学过程较好地吻合方程(6),证明了扩散-反应模型的有效性;ks和k3相近,为同一数量级,说明底物抑制较易发生。故在酶解过程中,要控制好底物的质量浓度,避免出现底物抑制。由动力学常数计算的最适底物质量浓度(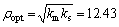 g/L)与实验数据所得rmax的最适底物质量浓度(见图3,ρopt=13.63 g/L)接近,说明本文所建扩散-反应动力学模型 (方程(6))较合理。当无底物抑制时,
g/L)与实验数据所得rmax的最适底物质量浓度(见图3,ρopt=13.63 g/L)接近,说明本文所建扩散-反应动力学模型 (方程(6))较合理。当无底物抑制时,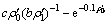 的
的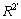 为-0.991 4,良好的线性关系证明了该扩散-反应模型的有效性。
为-0.991 4,良好的线性关系证明了该扩散-反应模型的有效性。
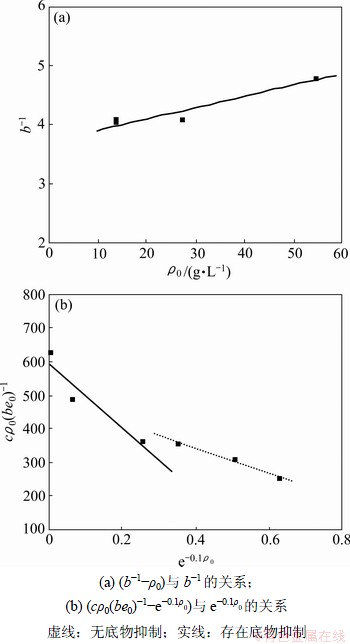
图5 酶解反应动力学参数计算
Fig.5 Determination of kinetic constants
由图5以及b与c的表达式可求得酶解的扩散-反应动力学模型为

2.6 扩散对酶解反应速率的影响
酶对底物进行催化反应时,底物必须从主体溶液传递到酶内部的催化活性中心处。这种物质传递过程包括分子扩散和对流扩散,其扩散过程的速率在某些情况下可能会对反应速率产生限制作用,特别是由于生物物质在液体中的扩散速率很小,当酶的催化活性很高时,这种扩散限制效应会相当明显。定义一个无因次数群M为最大反应速率/最大扩散速率之比。当M<<1时,酶最大催化反应速率要大大慢于底物的扩散速率,此时该反应过程为反应动力学控制;当M>>1时,底物的最大扩散速率要大大慢于酶催化反应速率,此时该反应过程为传质扩散控制。
在4.68≤ρ0<13.63 g/L时,无底物抑制;当底物质量浓度由4.68 g/L逐渐增大到10.45 g/L时,扩散速率kd由0.626 3 g/(L・min)逐渐变小到0.351 7 g/(L・min),M由0.110 3逐渐增大到0.196 3;当13.63≤ρ0≤27.26 g/L时,底物质量浓度由13.63 g/L逐渐增大到27.26 g/L时,扩散速率kd由0.411 7 g/(L・min)逐渐变小到0.105 3 g/(L・min),M由0.128 6逐渐增大到0.502 7。
当底物质量浓度由4.68 g/L逐渐增大到27.26 g/L时,M由0.110 3逐渐增大到0.502 7,扩散速率kd由0.626 3 g/(L・min)逐渐减小到0.105 3 g/(L・min),说明随底物质量浓度的增大,传质扩散对水解反应的影响逐渐增大。在本文实验底物浓度(4.68~27.26 g/L)范围内,并未出现M>>1和M<<1这2种极端情况,说明所研究的底物质量浓度范围内的酶反应速率是由反应动力学和传质扩散混合控制的,其扩散因素是不能忽略的。目前,大多酶解反应动力学研究并未考虑扩散因素,要更准确和全面地拟合及预测酶解过程变化,建立扩散-反应动力学模型可能更接近实际情况。
2.7 动力学模型拟合
根据酶解扩散-反应动力学模型的计算结果与实际试验结果进行对比,可以验证理论的动力学模型对实际实验结果的吻合程度,验证动力学模型的实际应用意义。
在pH为 5.0,温度为55 ℃,底物质量浓度为4.68~27.26 g/L和酶起始质量浓度为0.5~0.9 g/L的试验条件下,根据试验得出的水解度结果与其对应的动力学模型的计算结果进行比较,结果见图1和图2。从图1和图2 可见:除个别点外,其余平均相对误差均小于5%。可见:所建立的扩散-反应动力学模型能更准确地预测一定范围内不同底物的质量浓度和酶质量浓度,达到指定水解度所需反应时间或不同时刻对应的水解度,满足莲子蛋白水解度变化规律和特点,具有一定的通用性,这对莲子蛋白的降解和莲子蛋白肽的生产具有一定的参考价值。
3 结论
(1) 用木瓜蛋白酶解莲子蛋白动力学过程在考虑扩散因素对反应动力学影响的基础上,经过一系列假设和简化,建立了木瓜蛋白酶解莲子蛋白的扩散-反应动力学模型。木瓜蛋白酶酶解莲子蛋白在初始底物浓度4.68≤ρ0≤13.63 g/L时,符合无底物抑制扩散-反应动力学模型;在13.63 g/L≤ρ0≤27.26时,符合底物抑制扩散-反应动力学模型。
(2) 基于对不同实验条件下水解曲线的分析,提出同时考虑蛋白质单底物酶解、底物抑制作用和扩散的反应机理模型,构建木瓜蛋白酶酶解莲子蛋白的扩散-反应动力学方程:

由该动力学模型所得结果与实际实验结果基本吻合,实验拟合相对误差小于5%。酶反应速率由反应动力学和传质扩散混合控制,所提出的扩散-反应动力学模型能够合理地描述和解释酶法降解的过程,有助于认识莲子蛋白酶法降解机理,对莲子蛋白肽的生产也具有指导作用。
参考文献:
[1] 蔡联辉, 曾虹燕, 王亚举, 等. 莲子蛋白质的氨基酸组成及其营养评价[J]. 营养学报, 2010, 32(5): 503-506.
CAI Lianhui, ZENG Hongyan, WANG Yaju, et al. The amino acid contents of lotus seed protein and its nutritional evaluation[J]. Acta Nutrimenta Sinica, 2010, 32(5): 503-506.
[2] 管骁, 姚惠源, 张鸣镝. 燕麦麸分离蛋白的酶解对其功能性质的影响[J]. 农业工程学报, 2006, 22(11): 217-222.
GUAN Xiao, YAO Huiyuan, ZHANG Mingdi. Effects of enzymatic hydrolysis on the functional properties of oat bran protein isolates[J]. Transactions of the CSAE, 2006, 22(11): 217-222.
[3] 吴海文, 王强, 马铁铮. 不同制备方法对花生蛋白功能性质的影响[J]. 农业工程学报, 2009, 25(4): 304-308.
WU Haiwen, WANG Qiang, MA Tiezheng. Effects of preparation methods on functional properties of peanut protein[J]. Transactions of the CSAE, 2009, 25(4): 304-308.
[4] 袁素霞, 苏荣欣, 齐崴, 等. 魔芋葡甘聚糖酶解历程反应-扩散动力学[J]. 化工学报, 2008, 59(8): 2079-2082.
YUAN Suxia, SU Rongxin, QI Wei, et al. Reaction-diffusion kinetics for enzymatic hydrolysis of konjak glucomannan[J]. Journal of Chemical Industry and Engineering, 2008, 59(8): 2079-2082.
[5] 陈诵英, 陈平, 李永旺, 等. 催化反应动力学[M]. 北京: 化学工业出版社, 2007: 52-53.
CHEN Songying, CHEN Ping, LI Yongwang, et al. Catalyse activity and kinetics[M]. Beijing: Chemical Industry Press, 2007: 52-53.
[6] 赵学庄. 化学反应动力学原理[M]. 北京: 高等教育出版社, 1984: 154-159.
ZHAO Xuezhuang. Kinetics theory of chemical reaction[M]. Beijing: Higher Education Press, 1984: 154-159.
[7] 彭志英. 食品酶学导论[M]. 北京: 中国轻工业出版社, 2002: 155.
PENG Zhiying. Introductory theory of food enzymology[M]. Beijing: China Light Industry Press, 2002: 155.
[8] 梅乐和, 岑沛霖. 现代酶工程学[M]. 北京: 化学工业出版社, 2006: 43-58.
MEI Lehe, CEN Peilin. Enzyme engineering[M]. Beijing: Chemical Industry Press, 2006: 43-58.
[9] 齐崴, 何志敏, 何明霞. 蛋白质酶促水解反应机理与动力学模型[J]. 天津大学学报, 2005, 38(9): 768-773.
QI Wei, HE Zhimin, HE Mingxia. Mechanism and kinetic model of enzymatic hydrolysis of protein[J]. Journal of Tianjin University, 2005, 38(9): 768-773.
[10] Cheng Y, Prud’homme R K. Enzymatic degradation of guar and substituted guar galactomannans[J]. Biomacromolecules, 2000, 1(4): 782-788.
[11] Phillies G D J. The hydrodynamic scaling model for polymer self-diffusion[J]. Journal of Physical Chemistry, 1989, 93: 5029.
[12] Russo P S, Bu Z. Diffusion of dextran in aqueous (hydroxypropyl) cellulose[J]. Macromolecules, 1994, 27(5): 1187-1194.
[13] Cheng Y, Prud’homme R K, Thomas J L. Diffusion of mesoscopic probes in aqueous polymer solutions measured by fluorescence recovery after photobleaching[J]. Macromolecules, 2002, 35(21): 8111-8121.
(编辑 陈灿华)
收稿日期:2012-04-20;修回日期:2012-06-25
基金项目:国家重大科技专项(2009ZX07212-001-03);教育部大学生创新实验计划项目(101053021)
通信作者:曾虹燕(1963-),女,河南洛阳人,教授,博士生导师,从事食品及催化剂研究;电话:0731-58298175;E-mail: hyzeng@xtu.edu.cn