由电导率测定VO2+在Nafion 1135阳离子交换膜中扩散系数
桑商斌, 黄可龙, 刘素琴, 李晓刚, 王 显
(中南大学 化学化工学院, 长沙 410083)
摘 要: 研究通过电导率测定钒离子VO2+在Nafion 1135离子交换膜中的扩散系数的方法。 采用交流阻抗技术测定含不同浓度VO2+的0.1mol/L硫酸电解质溶液在有无膜时的阻抗值, 采用有膜时的阻抗减去无膜时阻抗值得到了不同条件下的膜阻抗。 结果表明: 阻抗大小与电极距离成正比, 有膜与无膜时分别测定的阻抗与电极距离的关系曲线近似呈平行线, 与电解液组成无关; 膜阻抗随着溶液中VO2+浓度的增加而增加。 根据基于Nernst-Planck扩散对流方程的二元离子在交换膜中扩散系数与电导率的关系方程计算了钒离子VO2+在Nafion 1135离子交换膜中的扩散系数为4.5×10-12 m2/s。
关键词: 钒离子(Ⅳ); 离子交换膜; 扩散系数; 电导率; 膜阻抗 中图分类号: TQ028.8
文献标识码: A
Determination of diffusion coefficient of VO2+ in Nafion 1135 cation exchange membrane by electrical conductivity measurement
SANG Shang-bin, HUANG Ke-long, LIU Su-qin,LI Xiao-gang, WANG Xian
(School of Chemistry and Chemical Engineering,Central South University, Changsha 410083, China)
Abstract: The diffusion coefficient determination of VO2+ in Nafion 1135 membrane by electrical conductivity measurement was studied. The resistances of the electrolyte with different VO2+ concentrations in 0.1mol/L vitriol solution and the solution with Nafion 1135 cation exchange membrane were measured by AC impedance technique. The membrane resistance was obtained by the difference of the resistances with and without membrane. The results show that the curves representing the relation of the membrane-solution and solution resistances with the inter-electrode distance are parallel straight lines, whatever the composition of the solution is. The membrane resistance grows with increasing VO2+ concentration. The calculated diffusion coefficient of VO2+ in Nafion 1135 cation exchange membrane is 4.5×1012 m2/s by the relation of diffusion coefficient and conductivity in bi-ionic system based on the Nernst-Plank diffusion-convection equation.
Key words: vanadium ion(Ⅳ); ion exchange membrane; diffusion coefficient; conductivity; membrane resistance
全钒液流电池是一种优秀的新型储能系统, 有着广泛的用途: 可用于通讯、 电动汽车、 潜艇等, 还可作为边远地区的储能、 发电系统进行电网调峰[1-3]。 全钒液流电池中, 正负半电池电解液中不同价态的钒离子相互扩散, 交叉污染所引起的自放电是电池能量损失的主要原因[4-7]。 因此研究离子交换膜中钒离子扩散系数对电池性能的评估及开发新型隔膜材料具有重要意义。 Wiedemann等[8-10]采用Maxwell-Stefan方程等计算膜中不同价态的钒离子在3种阳离子交换膜Neasepta CMX、 Neasepta CMS(Tokuyama Soda 公司) 和Selemion CMV(Asahi Glass 公司)的扩散系数, 需要测定自扩散条件下离子浓度与时间的关系曲线, 测试周期长, 计算处理较为繁琐。 文献[11]根据Nernst-Plank 扩散对流方程导出了电荷数为1的两种离子在膜中的电导率K与离子扩散系数D的关系, 采用交流阻抗技术, 高频条件下得到的1∶1型阴离子Cl-和NO-3离子在膜中的电导率K, 计算了Cl-和NO-3离子扩散系数。
本文作者根据Nernst-Plank 扩散对流方程推导出任意价态的二元离子在离子交换膜中扩散系数的计算通式。 采用交流阻抗的方法测定Nafion 1135膜在0.05mol硫酸介质以及含不同硫酸氧钒的0.05mol硫酸溶液中的电导率K, 计算VO2+在膜中的扩散系数D(VO2+)。
1 理论
根据Nernst-Planck 扩散对流方程:

在测量膜电导率时, 膜表面浓度极化层可以通过搅拌消除, 因此浓度梯度为零, 压力由于保持不变, 因此压力差也为零。 这样, 对只有两种离子1和2的情况, Nernst-/Planck 方程可以写为

无电流条件下:
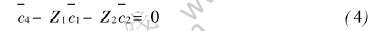
J1+J2=0(5)
式中 为膜内固定离子化基团的浓度;
为膜内固定离子化基团的浓度;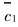 和
和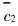 为离子1和2 在膜内的浓度。 假定只有在稀溶液中有效的经典Nernst-Einstein关系方程, 仍然可以应用于膜内溶液[12], 则有
为离子1和2 在膜内的浓度。 假定只有在稀溶液中有效的经典Nernst-Einstein关系方程, 仍然可以应用于膜内溶液[12], 则有

根据定义, 电导率K可以写为
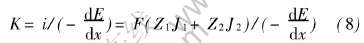
对流方程可以写为[11]
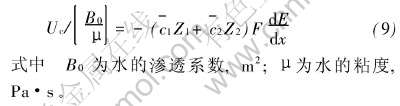
根据式(2)、 (3)、 (6)、 (8)和(9)得:

测定膜阻抗时, 膜两侧的溶液浓度和液面高度一致, 对流项很小, 可以忽略不计(B0≈0)[13], 因此有
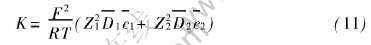
式(11)就是任意二元离子在离子交换膜中扩散系数与电导率K的关系通式。 通过测定电导率K和其中容易测定的离子扩散系数, 就可以计算出另外一种离子的扩散系数。
这里令1代表H+ , 2代表VO2+, 则有, Z1=1, Z2=2, 此时有
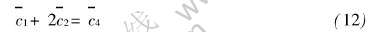
令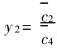 , 结合式(11), 可以得到
, 结合式(11), 可以得到

2 实验
2.1 仪器及药品
硫酸(AR, 湖南师范大学试剂厂), 硫酸氧钒(VOSO4)(攀枝花钢铁研究院提供), ZrOCl2(AR, 湖南师范大学试剂厂), 磷酸(AR, 湖南师范大学试剂厂)。 原子吸收光谱(AA-670, 日本岛津), 电化学工作站(CHI 660B, 上海辰华仪器公司)。 Nafion 1135膜(杜邦公司)。
2.2 实验步骤
2.2.1 膜中固定离子交换基团浓度的测定
按照下面的公式分别计算膜中固定交换离子基团浓度[7]:

2.2.2 电导率的测定
1) 膜的预处理。 先用去离子水冲洗3次, 后用0.5mol/L的硫酸在80℃下煮1h, 然后再用去离子水洗涤3次。 预处理后的膜放在待测电解液中浸泡过夜至离子交换平衡。
2) 将面积约为3cm×3cm 膜夹在两个用有机玻璃制作的半电解槽中间, 电解槽中间隔板上留有长2.2cm×2.2cm的半开口, 采用有机硅橡胶垫密封, 通过固定件将两半电池压紧。 将一对面积为2cm×2cm 的铂电极分别正对地固定在游标卡尺的两个外径测量爪上, 调节游标卡尺两外径测量爪间距, 可以准确地测量出两电极间距, 精度为0.01mm。
3) 调节游标卡尺位置使铂电极正对膜, 固定后采用电化学工作站(CHI660B, 上海辰华仪器公司)分别测定0.05mol/L的硫酸中的无膜和有膜时的交流阻抗。 测定时对电解液进行搅拌。 测定频率范围为1~105 Hz, 电压振幅为5mV。
4) 配制c(VO2+)∶c(H+)为0.016∶0.1, 0.013∶0.1, 0.009∶0.1和0.005∶0.1(mol/L)的硫酸氧钒的流酸溶液, 测定无膜和有膜时的阻抗大小。
膜电导率的计算公式如下:

膜电阻的计算公式如下:

2.2.3 膜中钒离子摩尔分数的测定
将膜在含有硫酸氧钒的硫酸电解液中浸泡过夜后, 用去离子水轻轻冲洗膜表面数次, 然后将膜于200mL的1.0mol/L的硫酸中浸泡12h, 后将膜取出并用去离子水洗涤3次, 一并将洗涤液和硫酸转入到500mL的容量瓶中, 再次将膜于200mL的1.0mol/L的硫酸中浸泡12h, 后将膜取出并用去离子水洗涤3次, 一并将洗涤液和硫酸转入到500mL的容量瓶中, 并在室温下定容, 然后用原子吸收光谱测定溶液中的钒离子浓度n(VO2+), 计算膜中钒离子的摩尔分数x(VO2+)。

3 结果与讨论
3.1 膜中固定离子交换基团浓度
已知Nafion 1135膜的离子交换容量为[13]: cs=0.909×10-3 mol/g, ρ1=2g/cm3, ρ2=1g/cm3, 实验测定m1=0.160g, m2=0.018g。 根据式(14)计算得Nafion 膜的 =1.484×103 mol/m3。
=1.484×103 mol/m3。
3.2 阻抗和电导率
在0.05mol/L的硫酸中, 分别在无膜和有膜时测定的交流阻抗结果如图1所示。 保持氢离子浓度c(H+)不变, 在含有不同浓度硫酸氧钒的硫酸溶液中, 测定的结果见图2。 可以看出测定的膜阻抗值与电极间距离具有较好的线性关系。 拟合后的方程分别标在图中。

图1 0.05mol/L硫酸中阻抗R与电极距离d的关系
Fig.1 Relations between electrode distance d and membrane resistance R in 0.05mol/L vitriol solution
Nafion 1135膜的厚度d=0.089mm, 膜的面积S=4.84×10-4 m2, 根据式(1)、 (2)可以计算出膜电导率K的值, 结果见表1。
3.3 膜中VO2+离子摩尔分数及离子扩散系数
在不同浓度溶液中平衡后, Nafion 1135膜中VO2+摩尔分数x(VO2+)与VO2+浓度的关系见图3。 采用Origin7.0软件进行拟合, 得到了溶液浓度c(VO2+)与膜内VO2+摩尔分数x(VO2+)之间的关系方程, 如图3 所示。
根据式(13), 离子交换膜电导率K与膜内钒离子VO2+ 摩尔分数x(VO2+)关系应为直线, 将K ―x(VO2+)作图并拟合得到图 4所示的拟合方程, 因此有

表1 Nafion 1135膜在不同溶液中的阻抗和电导率
Table 1 Resistance and conductivity of Nafion 1135 membrane in different solutions


图2 硫酸氧钒的硫酸溶液中阻抗与电极距离的关系
Fig.2 Relations between electrode distance and resistance in vanadium (Ⅳ) sulfate vitriol solution

图3 溶液中VO2浓度c(VO2+)与膜中x(VO2+)摩尔分数的关系
Fig.3 Relation between VO2+ concentration c(VO2+) in solution and mole fraction x(VO2+) in membrane
根据式(18)可以计算得到d[TX-](H+)=1.13×10-10 m2/s, 这个结果与文献[14, 15]报道的Nafion系列膜Nafion 117中氢离子扩散系数D[TX-](H+)=5×10-10 m2/s比较接近。 根据式(19)计算得到D(VO2+)=4.5×10-12 m2/s, 与Wiedemann等[4]测定的VO2+在CMV和CMX膜中的扩散系数(分别为11.5×10-13 m2/s和11.9×10-13 m2/s)相比, 为同一数量级。
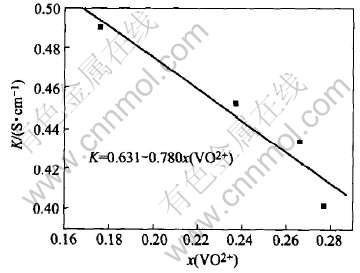
图4 VO2+在膜中的电导率K与摩尔分数x(VO2+)的关系
Fig.4 Relation between VO2+ conductivity K and mole fraction x(VO2+) in membrane
4 结论
根据Nernst-Planck扩散对流方程可以推导出二元体系中离子在交换膜中扩散系数D与电导率K的关系方程。 采用交流阻抗技术分别测定了有膜与无膜时的阻抗。 阻抗大小与溶液组成和电极距离有关。 有膜与无膜时测定的阻抗与电极距离的关系曲线近似呈平行线。 膜阻抗随着溶液中VO2+浓度的增加而增加。 相应地, 膜电导率K随着溶液中H+浓度的增加而增加。 根据推导的扩散系数D与电导率K的关系方程, 拟合可以得到VO2+离子在Nafion 1135膜中的扩散系数D(VO2+)为4.5×10-12 m2/s。
REFERENCES
[1]Fang B, Wei Y, Arai T, et al. Development of a novel redox flow battery for electricity storage system[J]. J of Appl Electrochem, 2003, 33: 197-203.
[2]Hwang G J, Ohya H. Preparation of cation exchange membrane as a separator for the all vanadium redox flow battery[J]. J Membr Sci, 1996, 120: 55-67.
[3]Mohammadi T, Skyllas-Kazacos M. Evaluation of the chemical stability of some membranes in vanadium solution[J]. J Appl Electrochem, 1997, 27: 153-158.
[4]Mohammadi T, Skyllas-Kazacos M. Preparation of sulfonated composite membrane for vanadium redox flow battery applications[J]. J Membr Sci, 1995, 107: 35-42.
[5]Mohammadi T, Skyllas-Kazacos M. Characterization of novel composite membrane for redox flow battery applications[J]. Journal of Membrane Science, 1995, 98: 77-87.
[6]Mohammadi T, Skyllas-Kazacos M. Use of polyelectrolyte for incorporation of ion-exchange groups in composite membranes for vanadium redox flow battery applications[J]. J Power Sources, 1995, 56: 91-96.
[7]Luo X L, Lu Z Z, Xi J Y, et al. Influences of permeation of vanadium ions through PVDF-g-PSSA membranes on performances of vanadium redox flow batteries[J]. J Phys Chem B, 2005, 109: 20310-20314.
[8]Wiedemann E, Heint Z A, Lichtenthaler R N. Sorption isotherms of vanadium with H3O+ ions in cation exchange membranes[J]. J Membr Sci, 1998, 141: 207-213.
[9]Wiedemann E, Heintz A, Lichtenthaler R N. Transport properties of vanadium ions in cation exchange membranes: Determination of diffusion coefficients using a dialysis cell[J]. J Membr Sci, 1998, 141: 215-221.
[10]Heintz A, Wiedemann E, Ziegler J. Ion exchange diffusion in electromembranes and its description using the Maxwell-Stefan formalism[J]. J Membr Sci, 1997, 137: 121-132.
[11]Nwal Amang D, Alexandrova S, Schaetzel P. The determination of diffusion coefficients of counter ion in an ion exchange membrane using electrical conductivity measurement[J]. Electrochimica Acta, 2003, 48: 2563-2569.
[12]Pourcelly G, Sestat P, Chapotot A, et al. Self diffusion and conductivity in Nafion membrane in contact with NaCl+CaCl2 solution[J]. J Membra Sci, 1996, 110: 69-78.
[13]Shaetzel P, Favre E, Auclair B, et al. Mass-transfer through ion exchange membranes: comparison between the diffusion and the diffusion-convection Stefan-Maxwell equations[J]. Electrochim Acta, 1997, 42: 2475.
[14]Stenina I A, Sistat P, Rebrov A I, et al. Ion mobility in Nafion-117 membranes[J]. Desalination, 2004, 170: 49-57.
[15]Li T, Wlaschin A, Balbuena B P. Theoretical studies of proton transfer in water and model polymer electrolyte systems[J]. Ind Eng Chem Res, 2001, 40: 4789-4800.
(编辑陈爱华)
收稿日期: 2005-10-14; 修订日期: 2006-03-06
通讯作者: 桑商斌, 副教授; 电话: 0731-8836618; E-mail: sangsb@126.com