文章编号:1004-0609(2015)-07-1911-09
锂离子导体包覆镍锰酸锂正极材料的制备及其电化学性能
熊利芝,刘文萍,吴玉先,何则强
(吉首大学 生物资源与环境科学学院,吉首 416000)
摘 要:采用原位包覆法制备表面包覆Li1.3Al0.3Ti1.7(PO4)3(LATP)的LiNi0.5Mn1.5O4(LNMO),即LNMO@LATP正极材料。采用X-射线衍射(XRD)、扫描电镜(SEM)、透射电镜(TEM)及电化学测试等手段对其物相结构、表面形貌及电化学性能进行研究。结果表明:LATP 以无定型态紧密包覆于LiNi0.5Mn1.5O4的表面,包覆层厚度约为5 nm。由于LATP包覆层具有保护电极材料表面和提高锂离子导电的双重作用,减少了电极过程的副反应,降低了电化学极化,提供了更多的锂离子扩散通道,导致LNMO@LATP具有比LNMO更稳定的循环性能和更好的倍率性能,特别是在高温的情况下。室温下在0.2C放电时,LNMO@LATP和LNMO的首次放电容量分别为141.5和142.6 mA・h/g,经80次循环后,二者放电容量保持率分别达到99.2%和98.0%;而在10.0C放电时,LNMO@LATP和LNMO的首次放电容量分别为93.5和70.6 mA・h/g,经80次循环后,二者放电容量保持率分别达到66.1%和49.5%。当循环温度提高到55 ℃时,LNMO@ LATP和LNMO在0.2C循环80次后的放电容量保持率分别为95.5%和79.2%;而在10.0C放电循环80次后,放电容量保持率分别为88.0%和51.0%。
关键词:LiNi0.5Mn1.5O4;Li1.3Al0.3Ti1.7(PO4)3;高电压正极;表面包覆;电化学性能
中图分类号:TM 912.9 文献标志码:A
Preparation and electrochemical properties of lithium nickel manganese oxide cathode materials coating with lithium ion conductor
XIONG Li-zhi, LIU Wen-ping, WU Yu-xian, HE Ze-qiang
(College of Biology and Environmental Science, Jishou University, Jishou 416000, China)
Abstract: LiNi0.5Mn1.5O4 (LNMO) cathode materials coated with lithium ion conductor Li1.3Al0.3Ti1.7(PO4)3 (LATP), namely LNMO@LATP cathode, was prepared by in situ coating method. X-ray diffraction(XRD),scanning electron microscopy (SEM), transmission electron microscopy (TEM) and electrochemical measurements were used to evaluate the properties of the cathodes. The results show that the coating of LATP does not change the structure of LNMO, and the LATP is attached tightly on the surface of LNMO in amorphous form. The coating layer of LATP is about 5 nm. Due to the dual roles of protecting the surface of LNMO and improving of lithium ion conductivity of LATP, LNMO@LATP cathode can reduce the side reaction between the electrolyte and LNMO, decrease the electrochemical polarization and provide more lithium ion diffusion channels in cycling, which leads to that LNMO@LATP cathode exhibits more enhanced cycling performance and better rate capability than the uncoated LNMO, especially at high temperature. The initial discharge capacities of LNMO@LATP and LNMO are 141.5 and 142.6 mA・h/g, respectively, 99.2% and 98.0% of their initial discharge capacity can be kept up after cycling at 0.2C for 80 times at room temperature. Under the discharge conditions of cycling at 10C for 80 times, the initial discharge capacities of LNMO@LATP and LNMO are 93.5 and 70.6 mA・h/g with a capacity retention rate of 66.1% and 49.5%, respectively. When cycled at 55 ℃ for 80 times, the capacity retention rates of LNMO@LATP and LNMO are 95.5% and 79.2% at 0.2C rate, and 88.0% and 51.0% ar 10.0C rate, respectively.
Key words: LiNi0.5Mn1.5O4;Li1.3Al0.3Ti1.7(PO4)3; high voltage cathode; surface coating; electrochemical property
由于具有良好的热稳定性和电化学性能,高电压正极材料LiNi0.5Mn1.5O4(LNMO)成为目前锂离子电池正极材料研究的热点[1-3],并逐步应用到锂电池体系中。日本、韩国、美国、法国、以色列等国家的一些公司已经在开始尝试LNMO材料的商品化开发问题,但目前市场上LNMO材料还没有实质意义上的正式生产。这主要是由于LNMO还面临两个问题:1) NiⅡ/NiⅣ 电对的电位在常用电解质体系的分解电压以上,LNMO容易在循环过程中与电解质溶液发生作用导致化学不稳定性;2) 由于在制备过程中氧缺失,生成LixNi1-xO或NiO等杂相,很难得到单相的LNMO,导致材料的循环性能恶化。解决第二个问题,主要依靠改进制备方法[4-5]和体相掺杂等手段[6-7]。而解决第一个问题,一方面在于研究能耐受高电压的电解液体系,如研制能在高电压下使用的氟基电解液[3];另一方面,通常采用表面包覆的方法。
大量研究报道已经表明,在LNMO表面包覆一层稳定的保护层,可避免或减少正极材料与电解液的直接接触,减少电解液的分解,有效提高材料的化学稳定性[8-9]。通常用作保护层的物质包括一些金属氧化物、磷酸盐或者导电单质[8-18],如ZnO、ZrO2、SiO2、Bi2O3和BiOF、SnO2、Li3PO4、Li4P2O7、ZnAl2O4 以及金属或非金属单质Au、Zn、Ag、C等。文献[17]中报道的表面修饰方法都能在一定程度上改善LNMO的循环稳定性,但这些方法通常在牺牲了部分正极材料的比容量的同时,堵塞了锂离子的扩散通道,既不利于材料高比容量的发挥,又无益材料高倍率性能的提升。如何在尽可能保持正极材料比容量的前提下,在LNMO表面包覆一层允许锂离子畅通的保护层,是一个值得深入探讨的问题。近年来,对快离子导体的研究十分火热,但快离子导体用于锂离子电池正极材料的表面修饰还不多[19-23]。
锂离子导体Li1.3Al0.3Ti1.7(PO4)3(LATP)作为一种固体电解质在薄膜型锂离子电池中已经得到广泛关注[24-26]。吴显明等[26]研究表明,LATP锂离子电导率可以达到10-4数量级以上[26]。本文作者曾采用湿化学法制备了表面包覆LATP的LiMn2O4正极材料,发现LATP包覆可以显著提高LiMn2O4的循环性能[19-20]。因此,如果将LATP包覆到LNMO表面,一方面由于LATP的高锂离子导电性,可望大大增加锂离子在电极材料中的扩散通道;另一方面将可以起到保护电极颗粒不被电解质溶液在循环过程中产生的HF腐蚀、缓解锰的溶解的作用[12-13, 15, 27]。本文作者采用原位包覆方式在LNMO表面包覆一层锂离子导体LATP,研究LATP包覆对LNMO循环稳定性和高倍率性能的影响规律。
1 实验
1.1 LNMO@ LATP的制备
将按照化学计量比准确称取的Li(CH3COO)・2H2O固体粉末0.133 g和Al(NO3)3・9H2O固体粉末0.325 g均匀混合后加入50 mL乙二醇甲醚液体中,待完全溶解后在强烈搅拌下缓慢加入按照文献[10]制备的LNMO固体粉末9.5 g,然后在强烈搅拌下向此悬浊液中依次加入PO(OC4H9)3 固体粉末0.349 g和Ti(OC4H9)4液体0.444 g,继续搅拌至近干后,置于120 ℃烘箱中干燥2 h,最后在马弗炉中600 ℃煅烧120 min,自然冷却,得到表面包覆LATP的LNMO粉末,记为LNMO@ LATP。
1.2 样品的表征
采用X-射线衍射(D/Max-2500型,Rigaku公司生产)研究样品的物相与结构;采用扫描电镜(JSM-5600LV型,JEOL公司生产)进行表面形貌观察和粒度估算。采用透射电镜(Tecnai G220型,FEI公司生产)分析样品的包覆层。
1.3 电化学性能测试
将粘结剂聚偏氟乙烯、导电剂乙炔黑和样品粉末按照质量比为1:1:8依次溶解在溶剂N-甲基吡咯烷酮中形成混合浆料,并均匀涂在铝箔上,形成厚度约为100 μm的涂层作为正极片。将涂好的正极片裁剪成面积为1 cm2的工作电极后,在60 ℃下真空干燥12 h备用。以金属锂箔为对电极,以1.0 mol/L LiPF6的碳酸乙酯/碳酸二甲酯(体积比为1:1)溶液为电解液,在充满氩气的手套箱中装配成2025型扣式模拟电池,陈化6 h后进行电化学测试。模拟电池的电化学测试在深圳新威公司生产的BTS高精度电池检测系统上完成,测试电压范围为3.4~4.9 V,测试温度为室温(如无特别说明,所有电化学测试的电流倍率均为0.2C(1C=140 mA・h/g))。
2 结果与讨论
2.1 样品的物相结构和表面形貌
图1所示为LNMO和LNMO@ LATP的XRD谱。从图1可以看到,在LATP包覆前后,LNMO的衍射峰位置没有变化,表明包覆没有改变LNMO的结构;但由于包覆LATP,衍射峰强度较包覆前有所减弱。从LNMO@LATP的XRD谱上没有发现LATP的衍射峰,可能是由于其在包覆样品中含量较少或者由于热处理温度较低,从而导致其结晶较差而以无定型态存在的缘故。
采用EDX 测试技术来确定材料所包含的元素(见图2)。在包覆样品中,发现了Ti、Al、P等元素成分呈一定比例存在,而在未包覆样品中,除了Li、Ni、Mn等元素外没有发现其它元素。EDS检测结果表明, Ti、Al、P的摩尔比为3:16.8:29.6,与LATP中的Ti、Al、P的理论物质的摩尔比(3:17:30)十分接近,说明在包覆样品表面确实存在一层无定形的LATP。
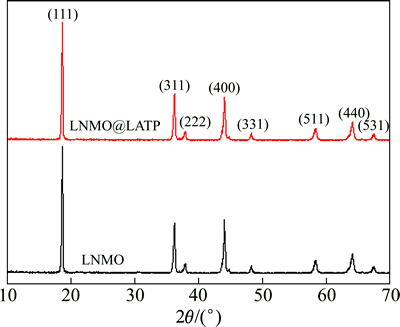
图1 LNMO和LNMO@LATP的XRD谱
Fig. 1 XRD patterns of LNMO and LNMO@LATP
图3(a)和(b)所示为LNMO和LNMO@ LATP的SEM像,图3(c)和(d)所示为LNMO和LNMO@LATP的TEM像。从图3(a)和(b)可以看到,包覆前后样品的颗粒大小基本没变化,包覆前LNMO颗粒的分散性较好,而包覆后由于LNMO@ LATP颗粒团聚现象明显,这可能是LNMO颗粒在二次烧结过程中与包覆于其表面的LATP颗粒相互连接成较大的样品颗粒或者包覆不完全有关。从图3(c)和(d)可以看到,包覆前LNMO样品表面光滑,而包覆后LNMO颗粒表面被一层平均厚度约为5 nm的LATP紧紧包裹。LATP包覆层的存在将可以有效地阻止电极颗粒LNMO与电解质溶液的直接接触,从而缓解电极中Mn的溶解,同时,高的锂离子导电特性将提供锂离子从电解质溶液向LNMO电极表面传输的通道,加快锂离子在电极中的扩散速率,最终改善LNMO材料的电化学性能。
2.2 LNMO@ LATP的电化学性能
图4所示为LNMO和LNMO@ LATP的首次充放电曲线。从图4可以发现,包覆前后样品具有十分相似的充放电曲线,表明包覆并没有改变材料的充放电机理,这与XRD分析得到的结论相一致。包覆后样品LNMO@LATP在4.0和4.7 V左右分别出现了对应Mn3+/Mn4+电对和Ni2+/Ni4+电对的放电平台。从图4还可以发现,包覆后样品的充电平台较未包覆样品的稍高,而放电平台却比后者稍低,这与用LATP包覆LiMn2O4的情况结果一致[19],可能是由于在LNMO表面包覆电子导电性差的LATP后,导致材料的欧姆极化增大的缘故[17]。比较包覆前后样品的放电曲线可知,二者的放电容量分别为142.6和141.5 mA・h/g,相差较小,说明表面包覆LATP没有影响LNMO的容量发挥。从5 V平台(4.3~4.9 V)占总放电容量的比例来看,包覆前后样品分别为87.5%和90.1%,表明包覆后样品电极中Mn的溶解减弱,高电压放电稳定性增强[28-30]。
图5所示为室温下LNMO和LNMO@LATP在0.2C下放电时的循环性能曲线。经80次循环后,LNMO和LNMO@ LATP的放电容量分别保持在139.8和140.3 mA・h/g,容量保持率分别达到98.0%和99.2%。结果表明:在较低的电流倍率下,包覆前后样品的循环稳定性都较好,但经LATP包覆的样品循环性能更优秀,这可能与LNMO@LATP中包覆层LATP的高锂离子导电性有关[21]。
为了验证LATP包覆对LNMO循环稳定性的改善效果,对不同倍率下LNMO和LNMO@ LATP的循环性能进行了研究。图6所示为室温下不同电流倍率下LNMO和LNMO@LATP的循环性能。从图6可知,当电流倍率较小(如0.2C和0.5C)时,包覆前后样品的循环性能差异较小;而电流倍率较大(如5.0C和10.0C)时,包覆后样品的循环性能明显优于未包覆样品的。这可能是由于电流倍率较小时,锂离子浓度较小,只需要较少的扩散通道即可满足锂离子从电解质溶液向电极内部进行迁移,两种电极材料的电化学极化相当。随着电流倍率的增大,锂离子浓度也增大,锂离子扩散所需要的通道也相应增多,这时由于LATP包覆可以大大增加LNMO@LATP的锂离子扩散通道,包覆样品的锂离子扩散不会受阻,因而产生的电化学极化较小,材料的倍率性能好;而未包覆材料因为只有较少的锂离子扩散通道,产生锂离子在电极表面大量“堆积”的现象,形成较大的电化学极化,因而未包覆样品的倍率性能较差。研究结果表明:依次在0.2、0.5和1.0C倍率下循环20次后,包覆前后样品再在5.0C倍率放电时,首次放电容量分别为96.1和108.5 mA・h/g;而经5.0C倍率下循环20次后,容量保持率达到0.2C初始放电容量的67.4%和76.7%;依次在0.2C、0.5C、1.0C和5.0C倍率下循环20次后,包覆前后样品再在10.0C放电时,首次放电容量分别为70.6和93.5mA・h/g,而经10.0C倍率下循环20次后,容量保持率达到0.2C初始放电容量的49.5%和66.1%。由此可见,LATP的包覆大大增加了LNMO的锂离子扩散通道,降低了电极的电化学极化作用,最终显著地改善了材料的倍率性能。

图2 LNMO@LATP中各元素的EDX扫描
Fig. 2 EDX mapping of different elements in LNMO@LATP

图3 LNMO和LNMO@LATP的SEM像和TEM像
Fig. 3 SEM images of LNMO (a) and LNMO@LATP (b) and TEM images of LNMO (c) and LNMO@LATP (d)
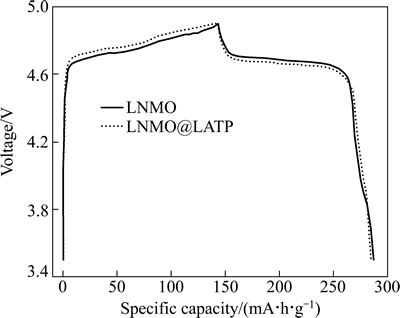
图4 LNMO和LNMO@LATP的首次充放电曲线
Fig. 4 Initial charge-discharge curves of LNMO and LNMO@LATP
图7所示为LNMO和LNMO@LATP经5次循环后Li+的扩散系数与充电电压的关系。由图7包覆前后两样品都在电压为4.7V时具有最大的锂离子扩散系数,分别为1.58×10-9和3.35×10-9 cm2/s,与文献[31]报道的结果(10-8~10-11 cm2/s)一致。导电LATP包覆后,在LNMO@ LATP中锂离子的扩散系数比在LNMO中的高,说明包覆层LATP的高锂离子导电性加速了锂离子在电极颗粒之间的传导,从而促进了电极过程的电子传输,改善了材料的电化学性能[32]。
为了证明LATP包覆层对LNMO的保护作用,包覆前后样品在55 ℃的循环性能进行了研究。图8所示为55 ℃下LNMO和LNMO@LATP在0.2C时的循环性能。
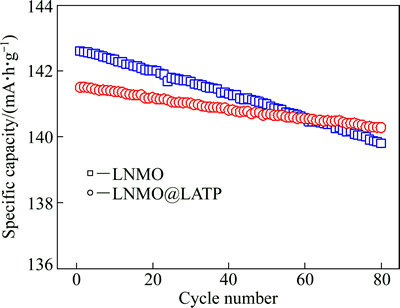
图5 室温下LNMO和LNMO@LATP在0.2C时的循环性能
Fig. 5 Cycling performance of LNMO and LNMO@LATP at 0.2C and room temperature
比较图5和8可知,将测试温度从室温提高到55 ℃以后,包覆前后样品的首次放电容量分别从142.6和141.5 mA・h/g降低到141.8和141.1 mA・h/g,这是由于升高温度加大了电池的极化所致。在0.2C下55 ℃循环80次后,包覆前后样品的放电容量分别为112.3和134.7 mA・h/g,容量保持率分别为79.2%和95.5%,均低于室温下的测定值。结果表明:即使在55 ℃进行循环,LNMO@ LATP依然保持了优良的容量保持率,而未包覆的LNMO容量衰减相对严重得多。对于高温下循环过程中LNMO的容量衰减,除了Mn的溶解加速等因素外,一个主要的原因在于充电过程电极材料中的Ni2+被氧化成Ni4+后,强氧化性的Ni4+容易与电解质溶液在电极表面进行反应产生钝化膜,导致电极中起电化学反应的活性物质减少而引起容量衰减。而这种副反应会随着温度的升高而加剧[11]。而氧化还原电对Ni2+/Ni3+ 和 Ni3+/ Ni4+在LNMO电极充放电循环过程中具有催化电解质分解的作用,会促进电解质在电极/电解质溶液界面上的分解[32-34]。CHONG等[15]研究认为,包覆在LNMO表面的Li4P2O7就如一种高效的固体电解质或准SEI膜,起到保护LNMO与电解质界面不被破坏的作用。当LNMO的表面包覆LATP后(见图3),一方面,致密的包覆层发挥了类似Li4P2O7保护电极界面的作用[15],有效地阻止了充电态电极与电解质溶液之间的副反应;另一方面,从图3可知,LNMO@ LATP颗粒依靠其表面的LATP颗粒相互联在一起,降低了电极颗粒的比表面积,自然也减少了副反应在电极表面发生的可能。两方面的结果都充分显示了LATP对LNMO的保护功能,从而保证了电极具有良好的高温循环性能。
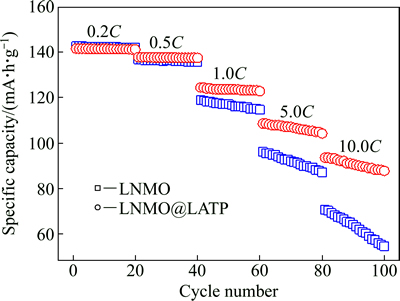
图6 室温下不同电流倍率下LNMO和LNMO@LATP的循环性能
Fig. 6 Cycling performance of LNMO and LNMO@LATP at various current rates and room temperature
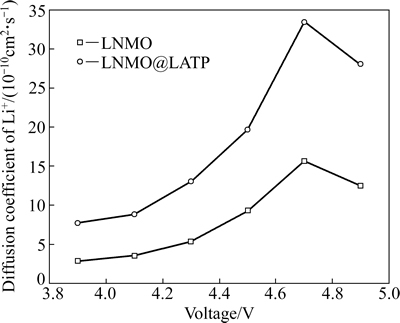
图7 LNMO和LNMO@LATP电极经5次循环后测定的Li+扩散系数与充电电压的关系
Fig. 7 Relationship between Li+ diffusion coefficient of LNMO and LNMO@LATP and charging voltage after cycling 5 times
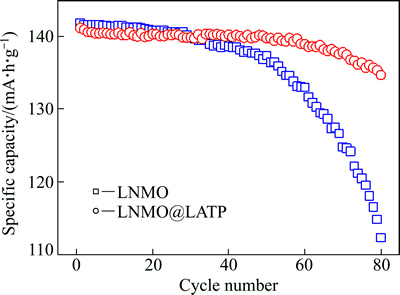
图8 55 ℃下LNMO和LNMO@LATP在0.2C时的循环性能
Fig. 8 Cycling performance of LNMO and LNMO@LATP at 0.2C and 55 ℃
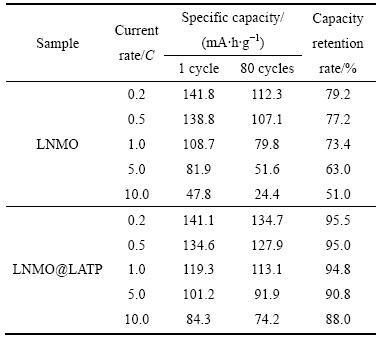
表1所列为不同电流倍率下包覆前后样品在55 ℃的循环性能数据。从表1可以看到,随着电流倍率的增大,由于电极过程的极化作用增加,两样品的放电容量都降低。但是,LNMO@ LATP容量衰减的幅度较LNMO的显著降低,放电倍率从0.2C增加到10.0C,LNMO和LNMO@ LATP的容量保持率分别从79.2%和95.5%下降到51.0%和88.0%。在5.0C和10.0C放电时,LNMO经80次循环后的容量保持率分别为63.0%和51.0%,而在同样的条件下LNMO@LATP经80次循环后的容量保持率分别为90.8%和88.0%。LNMO@LATP高倍率性能的提升应该归因于包覆层中LATP对LNMO的保护作用。
表1 55 ℃不同电流倍率下LNMO和LNMO@LATP的循环性能
Table 1 Cycling performances of LNMO and LNMO@LATP at various current rates and 55 ℃
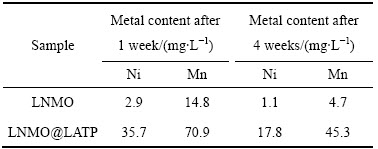
为了证明LATP包覆对LNMO表面的保护作用,将Li/LNMO电池和Li/LNMO@LATP电池完全充满电后浸泡于55 ℃的新鲜电解质溶液中,每隔一定时间采用原子吸收光谱法测量电解质溶液中Ni和Mn的含量,其结果如表2所示。研究结果表明:在浸泡1周后,浸泡LNMO电极的电解质溶液中Ni、Mn的含量分别是2.9和14.8 mg/L,而浸泡LNMO@LATP的电解质溶液中Ni、Mn的含量相对较小,分别为1.1和4.7 mg/L。随着浸泡时间的延长,浸泡两电极的电解质溶液中Ni、Mn的含量都增加,经浸泡4周后,LNMO@LATP的电解质溶液中Ni、Mn的含量分别为17.8和45.3 mg/L,而浸泡LNMO的电解质溶液中Ni、Mn的含量分别达到35.7和70.9 mg/L。实验结果充分说明:LATP的包覆减少了LNMO中活性金属Ni和Mn的溶解损失,LATP起到了保护活性材料表面、减少电解质溶液侵蚀的作用。
表2 不同电极在55 ℃新鲜电解质溶液中浸泡4周后测定的Ni和Mn含量
Table 2 Ni and Mn contents of different cathodes after soaked in new electrolyte for 4 weeks at 55 ℃
3 结论
1) LATP以无定型态紧密包覆在LNMO表面,没有改变LNMO的结构,包覆层厚度约为5 nm。
2) LATP包覆层具有双重作用:一方面,作为LNMO表面的保护层,减少电极材料与电解质溶液的副反应,降低循环过程极化作用;另一方面,由于LATP的高锂离子导电性,大大增加了锂离子从电解质溶液向电极传输时的扩散通道。双重作用的存在导致LNMO@LATP比LNMO具有更稳定的循环性能和更好的倍率性能,高温时效果尤为显著。
3) 室温下在0.2C放电时,LNMO@LATP和LNMO的首次放电容量分别为141.5和142.6 mA・h/g,经80次循环后,二者容量保持率分别达到99.2%和98.0%。而在10.0C放电时,LNMO@LATP和LNMO的首次放电容量分别为93.5和70.6 mA・h/g,经80次循环后,二者容量保持率分别达到66.1%和49.5%。当循环温度提高到55 ℃时,LNMO@ LATP和LNMO在0.2C循环80次后,容量保持率分别为95.5%和79.2%;在10.0C放电循环80次后,容量保持率分别为88.0%和51.0%。
REFERENCES
[1] BRAUN P V, CHO J, PIKUL J H, KING W P, ZHANG H. High power rechargeable batteries[J]. Current Opinion in Solid State and Materials Science, 2012, 16(4): 186-198.
[2] ZHANG X, CHENG F, YANG J, CHEN J. LiNi0.5Mn1.5O4 porous nanorods as high-rate and long-life cathodes for Li-ion batteries[J]. Nano Letters, 2013, 13(6): 2822-2825.
[3] WANG S J,LI P, SHAO L Y, WU K Q, LIN X T, SHUI M, LONG N B, WANG D J,SHU J. Preparation of spinel LiNi0.5Mn1.5O4 and Cr-doped LiNi0.5Mn1.5O4 cathode materials by tartaric acid assisted sol-gel method[J]. Ceramics International, 2015, 41(1): 1347-1353.
[4] WU Bo-rong, REN Yong-huan, MU Dao-bin, LIU Xiao-jiang, WU Feng. Modified electrochemical performance of high potential cathode using a sand-like carbonate electrolyte[J]. Electrochimica Acta, 2014, 143: 324-330.
[5] 何则强, 熊利芝, 吴显明, 刘文萍, 陈 上, 黄可龙. 流变相法制备LiNi0.5Mn1.5O4锂离子电池正极材料及其电化学性质[J]. 无机化学学报, 2007, 23(5): 872-874.
HE Ze-qiang, XIONG Li-zhi, WU Xian-ming, LIU Wen-ping, CHEN Shang, HUANG Ke-long. Preparation and electrochemical characterization of LiNi0.5Mn1.5O4 positive electrode for lithium ion batteries by rheological method[J]. Chinese Journal of Inorganic Chemistry, 2007, 23(5): 872-874.
[6] YI Ting-feng, XIE Ying, YE Ming-fu, JIANG Li-juan, ZHU Rong-sun, ZHU Yan-rong. Recent developments in the doping of LiNi0.5Mn1.5O4 cathode material for 5 V lithium-ion batteries[J]. Ionics, 2011, 17(5): 383-389.
[7] 熊利芝, 刘文萍, 吴玉先, 滕 瑶, 王家坚, 何则强. 钇掺杂量对LiNi0.5-0.5zMn1.5-0.5zYzO4电化学性能的影响[J]. 中国有色金属学报, 2014, 24(12): 3066-3073.
XIONG Li-zhi, LIU Wen-ping, WU Yu-xian, TENG Yao, WANG Jia-jian, HE Ze-qiang. Effects of Y content on electrochemical performances of LiNi0.5-0.5zMn1.5-0.5zYzO4[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(12): 3066-3073.
[8] FAN Y, WANG J, TANG Z. Effects of the nanostructured SiO2 coating on the performance of LiNi0.5Mn1.5O4 cathode materials for high-voltage Li-ion batteries[J]. Electrochim Acta, 2007, 52(11): 3870-3875.
[9] HUANG Y Y, ZENG X L, ZHOU C, WU P, TONG D G. Electrochemical performance and thermal stability of GaF3-coated LiNi0.5Mn1.5O4 as 5 V cathode materials for lithium ion batteries[J]. Journal of Materials Science, 2013, 48(2): 625-635.
[10] 何则强, 熊利芝, 梁 凯, 李菊香. 碳包覆对LiNi0.5Mn1.5O4电化学性能的影响[J]. 精细化工, 2009, 26(12): 1145-1148.
HE Ze-qiang, XIONG Li-zhi, LIANG Kai, LI Ju-xiang. Effect of C-coating on electrochemical performances of LiNi0.5Mn1.5O4[J]. Fine Chemicals, 2009, 26(12): 1145-1148.
[11] WU H M, BELHAROUAK I, ABOUIMRANE A, SUN Y K, AMINE K.Surface modification of LiNi0.5Mn1.5O4 by ZrP2O7 and ZrO2 for lithium-ion batteries[J]. Journal of Power Sources, 2010, 195(9): 2909-2913.
[12] KANG H B, MYUNG S T, AMINEC K, LEE S M, SUN Y K. Improved electrochemical properties of BiOF-coated 5V spinel Li[Ni0.5Mn1.5]O4 for rechargeable lithium batteries[J]. Journal of Power Sources, 2010, 195(7): 2023-2028.
[13] NOGUCHI T, YAMAZAKI I, NUMATA T, MASATO S. Effect of Bi oxide surface treatment on 5V spinel LiNi0.5Mn1.5-xTixO4[J]. Journal of Power Sources, 2007, 174(2): 359-365.
[14] ZHU Yan-rong, YI Ting-feng, ZHU Rong-sun, ZHOU An-na. Increased cycling stability of Li4Ti5O12-coated LiMn1.5Ni0.5O4 as cathode material for lithium-ion batteries[J]. Ceramics International, 2013, 39(3): 3087-3094.
[15] CHONG Jin, XUN Shi-di, SONG Xiang-yun, LIU Gao, BATTAGLIA V S. Surface stabilized LiNi0.5Mn1.5O4 cathode materials with high-rate capability and long cycle life for lithium ion batteries[J]. Nano Energy, 2013, 2(2): 283-293.
[16] LEE Y, MUN J, KIM D W, LEE J K, CHOI W. Surface modification of LiNi0.5Mn1.5O4cathodes with ZnAl2O4 by a sol-gel method for lithium ion batteries[J]. Electrochimica Acta, 2004, 115: 326-331.
[17] LIU D,TROTTIER J, CHAREST P, FR?CHETTE J, GUERFI A, MAUGER A, JULIEN C M, ZAGHIB K. Effect of nano LiFePO4 coating on LiMn1.5Ni0.5O4 5V cathode for lithium ion batteries[J]. Journal of Power Sources, 2012, 204: 127-132.
[18] XIONG Li-zhi, LIU Wen-ping, WU Yu-xian, HE Ze-qiang. Synthesis and characterization of LiNi0.49Mn1.49Y0.02O4@Ag by electroless plating technique[J]. Applied Surface Science, 2015, 328(15): 531-535
[19] WU Xian-ming, LI Run-xiu, CHEN Shang, HE Ze-qiang. Synthesis and characterization of Li1.3Al0.3Ti1.7(PO4)3-coated LiMn2O4 by wet chemical route[J]. Rare Metals, 2009, 28(2): 122-126.
[20] 吴显明, 谭 磊, 李 明, 余一平, 肖卓炳. 固体电解质包覆LiMn2O4正极材料的合成及表征[J]. 精细化工, 2011, 28(2): 116-119.
WU Xian-ming, TAN Lei, LI Ming, YU Yi-ping, XIAO Zhuo-bing. Synthesis and characterization of Li1.3Al0.3Ti1.7(PO4)3- coated LiMn2O4[J]. Fine Chemicals, 2011, 28(2): 116-119.
[21] 张晓萍, 郭华军, 李新海, 王志兴, 彭文杰, 伍 凌. 快离子导体Li3V2(PO4)3包覆LiFePO4的结构和性能[J]. 高等学校化学学报, 2012, 33(2): 236-242.
ZHANG Xiao-ping, GUO Hua-jun, LI Xin-hai, WANG Zhi-xing, PENG Wen-jie, WU Ling. Structure and electrochemical performance of LiFePO4 cathode with coating super iron conductor Li3V2(PO4)3[J]. Chemical Journal of Chinese Universities, 2012, 33(2): 236-242.
[22] YI Xin, WANG Xian-you, JU Bo-wei, SHU Hong-bo, WEN Wei-cheng, YU Rui-zhi, WANG Di, YANG Xiu-kang. Effective enhancement of electrochemical performance for spherical spinel LiMn2O4 via Li ion conductive Li2ZrO3 coating[J]. Electrochimica Acta, 2014, 134: 143-149.
[23] LIN Ying-bin, YANG Yan-min, YU Rui-bing, LAI Heng, HUANG Zhi-gao. Enhanced electrochemical performances of LiNi0.5Mn1.5O4 by surface modification with superconducting YBa2Cu3O7[J]. Journal of Power Sources, 2014, 259: 188-194.
[24] 吴显明. 锂离子电池材料LiMn2O4及Li1.3Al0.3Ti1.7(PO4)3 粉末与薄膜的合成及性质研究[D]. 长沙: 中南大学: 2003.
WU Xian-ming. Studies on the powder and thin-film Materials of LiMn2O4 and Li1.3Al0.3Ti1.7(PO4)3 for lithium-ion batteries[D]. Changsha: Central South University, 2003.
[25] 刘玉龙, 张 鸿, 薛 丹, 崔 彬, 李志成. Li1.3Al0.3Ti1.7(PO4)3基锂离子导电材料的制备与表征[J]. 中国有色金属学报, 2012, 22(1): 144-149.
LIU Yu-long, ZHANG Hong, XUE Dan, CUI Bin, LI Zhi-cheng. Fabrication and characterization of Li1.3Al0.3Ti1.7(PO4)3 based Li-ion conductive materials[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(1): 144-149.
[26] 吴显明, 刘金练, 李润秀, 陈 上. Li3PO4助熔剂添加对Li1.3Al0.3Ti1.7(PO4)3性质的影响[J]. 精细化工, 2011, 28(6): 573-577.
WU Xian-ming, LIU Jin-lian, LI Run-xiu, CHEN Shang. Influence of Li3PO4 addition on the properties of lithium ion-conductive electrolyte Li1.3Al0.3Ti1.7(PO4)3[J]. Fine Chemicals, 2011, 28(6): 573-577.
[27] LIU J, MANTHIRAM A. Understanding the improvement in the electrochemical properties of surface modified 5 V LiMn1.42Ni0.42Co0.16O4 spinel cathodes in lithium-ion cells[J]. Chemistry of Materials, 2009, 21(8): 1695-1707.
[28] JUN L, MANTHIRAM A. Understanding the improved electrochemical performances of Fe-substituted 5V spinel cathode LiNi0.5Mn1.5O4[J]. Journal of Physical Chemistry C, 2009, 113 (33): 15073-15079.
[29] HWANG B J, WU Y W, VENKATESWARLU M, CHENG M Y, SANTHANAM R. Influence of synthesis conditions on electrochemical properties of high-voltage Li1.02Ni0.5Mn1.5O4 spinel cathode material[J]. Journal of Power Sources, 2009, 193(2): 828-833.
[30] ARUNKUMAR T A, MANTHIRAM A. Influence of chromium doping on the electrochemical performance of the 5 V spinel cathode LiNi0.5Mn1.5O4[J]. Electrochimica Acta, 2005, 50(28): 5568-5572.
[31] SEYYEDHOSSEINZADEH H, MAHBOUBI F, AZADMEHR A. Diffusion mechanism of lithium ions in LiNi0.5Mn1.5O4[J]. Electrochimica Acta, 2013, 108: 867-875.
[32] CAO G. Nanostructures and nanomaterials[M]. Singapore: World Science Publishing, 2004.
[33] YANG L, MARKMAITREE T, LUCHT B L. Inorganic additives for passivation of high voltage cathode materials[J]. Journal of Power Sources, 2011, 196(4): 2251-2254.
[34] DALAVI S, XU M Q, KNIGHT B, LUCHT B L. Effect of added LiBOB on high voltage (LiNi0.5Mn1.5O4) spinel cathodes[J]. Electrochemical and Solid State Letters, 2012, 15(2): 28-31.
(编辑 王 超)
基金项目:国家自然科学基金资助项目(51364009,51262008,51472107);湖南省自然科学基金资助项目(12JJ2005);湖南省科技计划重点项目(2012GK2017);湖南省重点学科建设项目(JSU0713);湖南省高校科技创新团队支持计划“环境能源材料与武陵山区矿产资源精深加工”项目
收稿日期:2014-09-22;修订日期:2015-04-22
通信作者:何则强,教授,博士;电话:13787930478;E-mail:csuhzq@163.com