

硫酸镁改性铝基吸附剂脱氟的工艺及机理
孙成余1, 2,杨坤1,施哲1,张利波1,罗永光2
(1. 昆明理工大学 冶金与能源工程学院,云南 昆明,650093;
2. 云南驰宏锌锗股份有限公司,云南 曲靖,655011)
摘要:针对目前吸附剂工业效果差、制备成本高和吸附效果不稳定等现状,采用浸渍法制备硫酸镁改性铝基吸附剂。在分析吸附剂特性的基础上,研究不同吸附剂用量、吸附时间、吸附温度和溶液pH条件下的吸氟量和脱氟率,明确脱氟工艺优化条件,并进一步揭示改性铝基催化剂的脱氟机理。研究结果表明:硫酸镁改性铝基吸附剂主要活性吸附组分为AlOOH和MgAl2O4,以层状氢氧化物成形,具有物相和结构优势;当吸附剂添加量为15 g/L,溶液初始pH为5,吸附温度为70 ℃,吸附时间为2.5 h时,吸氟量为4.49 mg/g,脱氟率为50.70%;硫酸镁改性铝基吸附剂吸附工业硫酸锌溶中氟离子过程符合Langmuir吸附等温方程和准二级动力学模型,是一种优势吸附过程。
关键词:改性铝基吸附剂;工业硫酸锌溶液;脱氟;吸附条件;吸附机理
中图分类号:TF814.4 文献标志码:A 开放科学(资源服务)标识码(OSID)
文章编号:1672-7207(2021)06-2032-08
Defluorination technology and mechanism of magnesium sulfate modified aluminum-based adsorbent
SUN Chengyu1, 2,YANG Kun1,SHI Zhe1,ZHANG Libo1,LUO Yongguang2
(1. Faculty of Metallurgical and Energy Engineering, Kunming University of Science and Technology, Kunming 650093, China;
2. Yunnan Chihong Zn&Ge Co. Ltd., Qujing 655011, China)
Abstract: In view of the current situation of poor industrial effect, high preparation cost and unstable adsorption effect of adsorbent, the impregnation method was adopted to prepare magnesium sulfate modified aluminum-based adsorbent. On the basis of analyzing the characteristics of adsorbent, fluorine absorption and defluorination rate under the conditions of different adsorbent dosage, adsorption time, adsorption temperature and solution pH were studied, the optimization conditions of defluorination process were clarified, and the mechanism of defluorination was further revealed. The results show that the main active adsorption components of the magnesium sulfate modified aluminum-based adsorbent are AlOOH and MgAl2O4, which are formed as layered hydroxides, with advantages in phase and structure. Under the conditions of addition of adsorbent of 15 g/L, initial pH of solution of 5, adsorption temperature of 70 ℃, and adsorption time of 2.5 h, the fluorine absorption and defluorination rate are 4.49 mg/g and 50.70%, respectively. The adsorption process of magnesium sulfate modified aluminum-based adsorbent to dissolve fluoride ions in industrial zinc sulfate conforms to Langmuir adsorption isotherm equation and quasi-second-order kinetic model, which is an advantageous adsorption process.
Key words: modified aluminum-based adsorbent; industrial zinc sulfate solution; defluorination; adsorption conditions; adsorption mechanism
世界上约80%的金属锌是采用焙烧-浸出-净化-电积的工艺进行生产[1]。由于近几年锌矿石品位下降,锌二次资源用量加大,进一步加剧了硫酸锌溶液中氟离子的积累。当氟离子质量浓度过大时,会引起析出的锌与阴极铝板黏结,导致锌片难以剥离,加大工人劳动强度,降低生产效率[2]。工业生产硫酸锌溶液中的氟离子质量浓度一般需要控制在50 mg/L以下[3]。研究成熟的硫酸锌溶液脱氟方法主要包括石灰乳沉淀法[4]、铝盐絮凝沉淀法[5]和萃取法[6]等,但存在脱氟效果差、锌损失量大、操作条件苛刻和流程长等不足,阻碍其在工业生产中的推广应用。
近年来,吸附脱氟法以其吸附效果好、吸附剂可再生和流程短易操作等独特优势,逐渐引起广泛关注。目前研究较热的吸附剂包括生物质类吸附剂[7]、泥土类吸附剂[8]、天然矿物沸石[9]、骨炭[10]和铝盐吸附剂[11-12],尤其是聚合铝盐吸附剂,具有吸附和絮凝双重作用,除氟能力高、再生过程损耗低,已成为应用最广泛的除氟剂,在氧化铝中添加镁盐和锰盐,能将废水中的氟去除98%以上[13-14]。由此可知,将聚合铝盐吸附剂用于硫酸锌溶液脱氟前景巨大。刘争伟等[15]采用Al,Ca复合除氟剂对加氟硫酸锌模拟溶液中的氟离子进行脱除,最佳条件下,氟离子的脱除率可以达到96%;FANG等[16]研究了焙烧改性氢氧化铝在模拟加氟硫酸锌溶液中的脱氟效果,其最大吸附容量可以达到3.68 mg/g;TIAN等[17]制备一种层状的铝基复合物吸附剂,研究其在工业硫酸锌溶液中的除氟效果,最大吸附容量可达5.62 mg/g。尽管效果较好,聚合铝盐吸附剂脱除硫酸锌溶液氟离子的研究仍尚未成熟,且上述脱氟剂制备成本较高,吸附效果不稳定。
针对目前聚合铝盐吸附剂制备成本高和吸附效果不稳定等缺陷,本文作者提出一种硫酸镁改性氢氧化铝制备的铝基吸附剂,研究工艺参数对工业硫酸锌溶液中氟离子的脱除效果的影响及脱氟机理,确定合理的脱氟工艺,查明F-在硫酸镁改性铝基吸附剂的吸附分离机制。
1 实验
1.1 催化剂制备
硫酸镁改性铝基吸附剂的制备采用浸渍法,将氢氧化铝浸泡于0.05 mol/L硫酸镁溶液中,浸泡温度为40 ℃,浸泡液固比为8:1,达到平衡后取出在室温下陈化20 h,干燥后于350 ℃下焙烧2 h,即得吸附剂。利用本方法制备吸附剂,其吸附活性组分仅分布在氢氧化铝表面,利用率高,用量少,成本低。
1.2 吸附实验及设备
将一定量的硫酸镁改性铝基吸附剂投加到工业硫酸锌溶液中,利用H2SO4溶液调节溶液pH,控制反应时间和温度,以140 r/min的振荡速度进行混合吸附反应,测定不同吸附剂用量、吸附时间、吸附温度和溶液pH等条件下硫酸镁改性铝基吸附剂对氟离子的吸氟量和脱氟率。
实验所用工业硫酸锌溶液来自国内某锌冶炼厂,溶液中Zn2+质量浓度为119 g/L,Mn2+质量浓度为4.6 g/L,F-质量浓度为116 mg/L,Cl-质量浓度为0.57 g/L,属于高F-硫酸锌溶液。
实验样品物相组成分析采用荷兰帕纳科公司的X′PERT3 POWDER型X射线衍射分析仪,检测角度为10°~80°,检测速率为4(°)/min。组成物相形貌及赋存状态分析采用荷兰飞纳高分辨率台式扫描电镜Phenom ProX (SEM-EDAX)。
1.3 氟离子的检测方法
实验中采用氟离子计(F-1,南京科技分析仪器有限公司)测量溶液中的氟离子,计算吸附反应后溶液中氟离子浓度。氟离子的脱除率(脱氟率)与吸附剂吸附容量(吸氟量)通过下式计算[13],
 (1)
(1)
 (2)
(2)
式中:A为氟离子脱除率,%;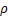 0为工业硫酸锌溶液中初始氟离子质量浓度,mg/L;
0为工业硫酸锌溶液中初始氟离子质量浓度,mg/L;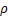 e为吸附平衡时工业硫酸锌溶液中氟离子质量浓度,mg/L;qe为吸附平衡时吸附剂的吸附容量,mg/g;V为溶液体积,L;m为吸附剂的质量,g。
e为吸附平衡时工业硫酸锌溶液中氟离子质量浓度,mg/L;qe为吸附平衡时吸附剂的吸附容量,mg/g;V为溶液体积,L;m为吸附剂的质量,g。
2 改性铝基吸附剂的特性
2.1 物相分析
实验制备所得硫酸镁改性铝基吸附剂的主要物相如图1所示。从图1可见:吸附剂主要由Al(OH)3,AlOOH,MgAl2O4,MgAl2(OH)8和Mg0.338Al2.408O4组成。其中,Al(OH)3为吸附基体,而其他成分均为硫酸镁改性焙烧后的产物。羟基氧化铝(AlOOH)为无定形态,对F离子的吸附性能要远高于晶体态的氧化物,镁铝尖晶石(MgAl2O4,MgAl2(OH)8和Mg0.338Al2.408O4)某些表面裸露的“―O―Mg―”结构能充当吸附活性中心,与“―O―Al―”结构相比,“―O―Mg―”中Mg2+具有更强的正点性质,对于硫酸镁溶液中负电性的F-具有更强选择性吸附作用[17-18],因此,本文利用硫酸镁改性铝基吸附剂脱除氟是可行的。
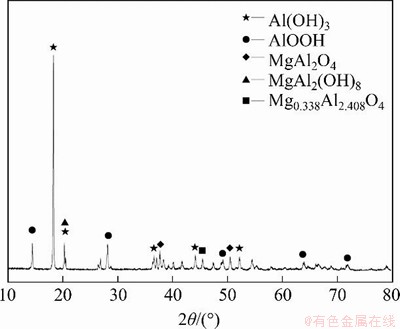
图1 硫酸镁改性后铝基吸附剂的XRD图
Fig. 1 XRD pattern of modified aluminum-based adsorbent
2.2 微观结构
针对硫酸镁改性铝基吸附剂分析形貌和物相组分赋存状态,改性后铝基吸附剂的SEM图如图2所示。

图2 改性后铝基吸附剂的SEM图
Fig. 2 SEM images of modified aluminum-based adsorbent
从图2可见:浸渍法制备得到的吸附剂主要为层状堆叠结构,即吸附剂以层状氢氧化物成型。层状氢氧化物被认为具有优良的阴离子交换性能,可作有害阴离子吸附剂。本文制备的吸附剂具有结构优势。
图3所示为改性后铝基吸附剂的面扫图。从图3可见:吸附剂基体上附着较均匀的元素Mg,且与元素Al和元素O共生,证明镁铝尖晶石(MgAl2O4,MgAl2(OH)8和Mg0.338Al2.408O4)的存在,Al元素部分与元素Mg和元素O共存,部分仅与元素O共生,证明存在Al(OH)3和AlOOH相,SEM面扫描结果与XRD分析结果吻合。

图3 改性后铝基吸附剂的面扫图
Fig. 3 Surface scan images of modified aluminum-based adsorbent
3 硫酸锌溶液的脱氟工艺
在硫酸锌溶液的脱氟工艺中,主要研究吸附剂用量、吸附时间、吸附温度和溶液pH这4个因素对氟离子脱除的影响,图4所示为工艺因素对氟离子脱除的影响。
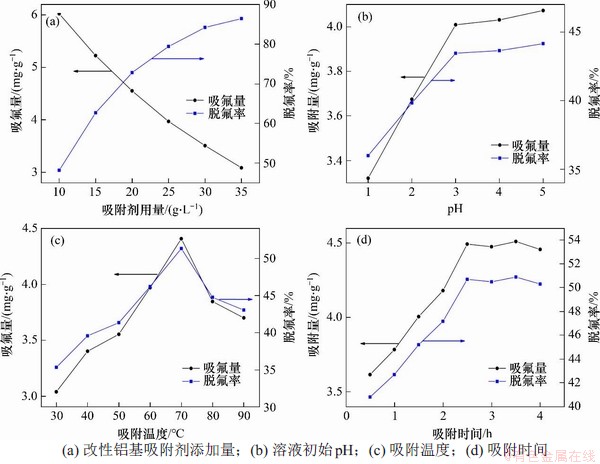
图4 工艺因素对氟离子脱除的影响
Fig. 4 Effect of process factors on defluorination of solution
研究改性铝基吸附剂添加量的影响时,控制温度为40 ℃,时间为2 h,pH为5.0。由图4(a)可见:改性铝基吸附剂的脱氟率随着吸附剂用量增加而提高,且提高趋势逐渐变缓,当吸附剂用量从10 g/L增加至35 g/L时,其脱氟率从48.18%增加至86.44%。而吸附剂的吸氟量随着吸附剂用量增加而降低,且降低趋势减弱,当改性铝基吸附剂加入量为10 g/L时,氟离子的吸氟量为6.02 mg/g,随着吸附剂用量增加至35 g/L时,吸附剂的吸氟量降低至3.09 mg/g。综合考虑吸氟量和脱氟率,选取15 g/L作为最佳实验加入量,工业硫酸锌溶液中氟离子剩余质量分数为41.61 mg/g,已经达到国家限制标准,此时吸氟量为5.226 mg/g,脱氟率为62.7%。
在15 g/L吸附剂条件下,考察溶液初始pH对氟离子脱除的影响,如图4(b)所示。由图4(b)可见:脱氟率和吸氟量都随着溶液初始pH增大而提高,当pH为1~3时,脱氟率和吸氟量都呈线性增加。当pH为1时,吸氟量仅为3.32 mg/g,此时脱氟率为35.99%;当pH为3时,吸氟量上升至4.01 mg/g,脱氟率增加至43.45%;当pH增大到3~5时,脱氟率和吸氟量提高的趋势逐渐变缓;pH为5时,吸氟量为4.07 mg/g,脱氟率为44.15%。为了达到最大脱氟效果,选取pH为5作为最佳初始pH,此时工业硫酸锌溶液不会产生氢氧化锌沉淀,有利于锌的回收率。
在溶液初始pH 5.0条件下,考察吸附温度对氟离子脱除的影响,如图4(c)所示。由图4(c)可见:吸附温度对于硫酸锌溶液氟离子脱除影响明显,脱氟率和吸氟量均随着吸附温度上升出现了先提高后降低的趋势。当吸附温度为30~70 ℃时,吸氟量与脱氟率随着吸附温度上升而提高。当吸附温度为30 ℃时,吸氟量仅为3.04 mg/g,脱氟率为35.35%;当吸附温度达到70 ℃时,吸氟量和脱氟率均达到最大值,最大吸氟量为4.41 mg/g,最大脱氟率为51.33%;当吸附温度超过70 ℃,吸氟量和脱氟率开始降低,这主要是由于温度升高,改性铝基吸附剂表面逐渐变得致密,结合氟的能力下降,同时水中游离态的OH-越多,会与F-发生竞争;当吸附温度为90 ℃时,吸氟量下降到3.70 mg/g,脱氟率下降到43.05%。因此,选取70 ℃为最佳吸附温度。
在吸附温度70 ℃条件下,考察吸附时间对氟离子脱除的影响,如图4(d)所示。由图4(d)可见:脱氟率和吸氟量随着吸附时间延长出现先提高后变缓的趋势。当吸附时间从0.5 h增加至2.5 h时,吸氟量与脱氟率随着吸附时间延长逐渐提高,脱氟率从40.8%增加至50.7%,吸氟量从3.615 mg/g增加至4.493 mg/g。而当吸附时间大于2.5 h时,整个吸附过程趋于稳定,吸氟量与脱氟率几乎不再变化。因此,确定最佳吸附时间为2.5 h。
综上硫酸锌溶液的脱氟工艺,当吸附温度为70 ℃,吸附剂用量为15 g/L,吸附时间为2.5 h,溶液初始pH为5.0时,改性铝基吸附剂对氟离子的吸附效果达到最佳,吸氟量为4.493 mg/g,脱氟率为50.7%。
4 硫酸锌溶液的脱氟机理
利用吸附动力学和吸附等温线研究改性铝基吸附剂对工业硫酸锌溶液中氟离子的脱除机理,以查明氟离子的迁移规律,F-与改性铝基吸附剂之间的动态相互作用,及F-在硫酸锌溶液与改性铝基吸附剂之间的平衡分配。
4.1 吸附动力学
目前,分析溶液中离子的动力学过程主要采用准一级吸附模型[19]和准二级吸附模型[20]。
1) 准一级吸附动力学方程:
 (3)
(3)
式中:qt为改性铝基吸附剂在t时刻的吸氟量,mg/g;t为改性铝基吸附剂的吸附时间,h;K1为准一级吸附动力学吸附速率常数,h-1。
2) 准二级吸附动力学方程:
 (4)
(4)
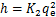 (5)
(5)
式中:K2为准二级吸附速率常数,g・mg-1・h-1;h为初始吸附速率,mg・g-1・h-1。
分别利用准一级、准二级吸附动力学方程对不同温度下吸附数据进行拟合,拟合结果如图5所示。
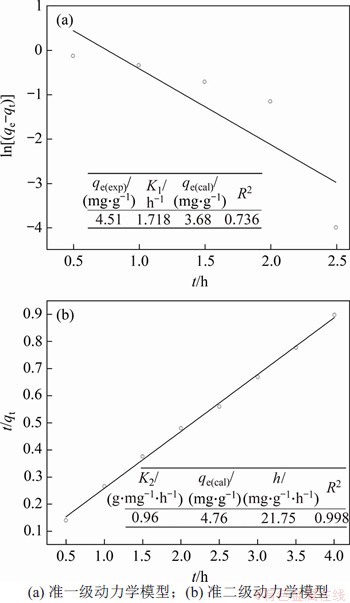
图5 改性铝基吸附剂吸附动力学模型
Fig. 5 Adsorption kinetic models of modified aluminum-based adsorbent
从图5可见:准二级动力学模型对吸附数据的拟合程度更高,准一级动力学拟合的相关系数(R2)仅为0.736,计算所得平衡吸附量qe(cal)远低于实验值4.41 mg/L,而准二级动力学拟合线性相关性很好,计算平衡吸附量(qe(cal))与实验值十分接近。说明准二级动力学模型包含的吸附过程,能够更准确地反映F-与改性铝基吸附剂之间的动态相互作用,改性铝基吸附剂的初始吸附速率h为21.75 mg・g-1・h-1,在t时刻的吸氟量为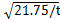 。
。
4.2 吸附等温线
用于描述吸附剂吸附氟离子的等温线模型主要包括Langmuir和Freundlich这2种吸附等温线模型[21],其相关线性方程如下。
1) Langmuir吸附等温线模型为:
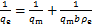 (6)
(6)
 (7)
(7)
式中:qm为改性铝基吸附剂饱和吸氟量,mg/g;b为Langmuir吸附平衡常数,mg/L。RL为分离常数。
2) Freundlich吸附等温线模型为
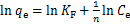 (8)
(8)
式中:KF为与吸氟量有关的Freundlich经验常数,mg/g;n为与吸附强度有关的Freundlich经验常数。
分别利用Langmuir和Freundlich这2种吸附等温线模型对不同温度下吸附数据进行拟合,拟合结果见图6。
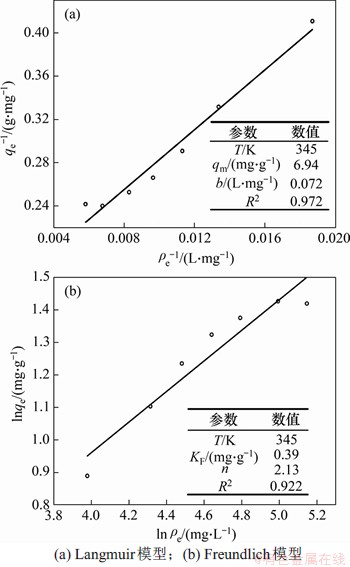
图6 改性铝基吸附剂吸附等温线模型拟合图
Fig. 6 Fitting plots of modified isotherm models of modified aluminum-based adsorbent
从图6可见:实验数据采用Langmuir和Freundlich吸附等温线模型拟合的相关系数(R2)分别为0.972和0.922,Langmuir吸附等温线模型数据拟合程度更高。由此说明,改性铝基吸附剂对工业硫酸锌溶液中氟离子的吸附更适合采用Langmuir吸附等温线模型来描述,其吸附以单层吸附模式为主[22]。且在Langmuir吸附等温线模型中,吸氟量饱和值(qm)为6.94 mg/g,接近实际最大吸附量6.02 mg/g;同时得到在不同氟离子浓度下的无量纲分离常数RL均处于0~1之间(见表1),说明吸附过程为优势吸附,即F-在硫酸锌溶液与改性铝基吸附剂之间更趋向于改性铝基吸附剂[23]。
表1 改性铝基吸附剂在不同氟离子质量浓度工业硫酸锌溶液中的分离常数RL
Table 1 Values of separation constant RL of modified aluminum-based adsorbent in industrial zinc sulfate solution with different fluoride ion mass concentrations

5 结论
1) 实验制备所得硫酸镁改性铝基吸附剂的物相包括AlOOH,MgAl2O4,MgAl2(OH)8和Mg0.338Al2.408O4,以层状氢氧化物为主,具有物相和结构优势。
2) 将硫酸镁改性铝基吸附剂应用于工业硫酸锌溶液中氟离子脱除,其最佳脱氟条件如下:吸附剂添加量为15 g/L,溶液初始pH为5,吸附温度为70 ℃,吸附时间为2.5 h。其效果如下:吸氟量为4.493 mg/g,脱氟率为50.7%。
3) 准二级吸附动力学方程更为准确的反应F-与改性铝基吸附剂之间的动态相互作用,改性铝基吸附剂的初始吸附速率h为21.75 mg・g-1・h-1。用Langmuir模型可以较好地描述F-在硫酸锌溶液与改性铝基吸附剂之间的平衡分配,吸附过程为优势吸附。
参考文献:
[1] YANG Kai, LI Yifan, ZHAO Zejun, et al. Amorphous porous layered-Al2O3 derived from AlFu MOFs as an adsorbent for removing fluorine ions in industrial ZnSO4 solution[J]. Chemical Engineering Research and Design, 2020, 153: 562-571.
[2] WU Xuelian, LIU Zhongqing, LIU Xu. The effects of additives on the electrowinning of zinc from sulphate solutions with high fluoride concentration[J]. Hydrometallurgy, 2014, 141: 31-35.
[3] LAI Yanqing, YANG Kai, YANG Chao, et al. Thermodynamics and kinetics of fluoride removal from simulated zinc sulfate solution by La(III)-modified zeolite[J]. Transactions of Nonferrous Metals Society of China, 2018, 28(4): 783-793.
[4] 谢维新. 湿法炼锌中电解锌溶液除氟的研究[J]. 广西民族学院学报(自然科学版), 1996, 2(2): 28-32.
XIE Weixin. Study on the removal of F- from electrolytic Zinc Solution used for zinc-making in wet method[J]. Journal of Guangxi University for Nationalities(Natural Science Edition), 1996, 2(2): 28-32.
[5] 卢建杭, 刘维屏, 郑巍. 铝盐混凝去除氟离子的作用机理探讨[J]. 环境科学学报, 2000, 20(6): 709-713.
LU Jianhang, LIU Weiping, ZHENG Wei. The removal mechanisms of fluoride ion by aluminum salt coagulant[J]. Acta Scientiae Circumstantiae, 2000, 20(6): 709-713.
[6] 王志斌, 韦国龙, 余坦, 等. 一种萃取脱除氟、氯的湿法炼锌方法: 中国, CN102732722A[P]. 2012-10-17.
WANG Zhibin, WEI Guolong, YU Tan, et al. A method for wet zinc metallurgy using extraction to remove fluorine and chlorine: China, CN102732722A[P]. 2012-10-17.
[7] 陶庭先. 茶叶质铁对氟离子的吸附性能[J]. 安徽机电学院学报, 1998, 13(2): 33-36.
TAO Tingxian. On the adsorption properties of fluorion on tea-Fe(Ⅲ)[J]. Journal of Anhui Institute of Mechanical and Electrical Engineering, 1998, 13(2): 33-36.
[8] 王鲁敏, 殷军港, 邓昌亮, 等. 褐煤型吸附剂对氟离子的吸附[J]. 烟台大学学报(自然科学与工程版), 2003, 16(4): 293-297.
WANG Lumin, YIN Jungang, DENG Changliang, et al. Study of adsorption for F-ion on adsorbernt lignite[J]. Journal of Yantai University(Natural Science and Engineering Edition), 2003, 16(4): 293-297.
[9] ONYANGO M S, KOJIMA Y, AOYI O, et al. Adsorption equilibrium modeling and solution chemistry dependence of fluoride removal from water by trivalent-cation-exchanged zeolite F-9[J]. Journal of Colloid and Interface Science, 2004, 279(2): 341-350.
[10] SUNDARAM C S, VISWANATHAN N, MEENAKSHI S. Defluoridation chemistry of synthetic hydroxyapatite at nano scale: Equilibrium and kinetic studies[J]. Journal of Hazardous Materials, 2008, 155(1/2): 206-215.
[11] TANG Yulin, GUAN Xiaohong, SU Tingzhi, et al. Fluoride adsorption onto activated alumina: modeling the effects of pH and some competing ions[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2009, 337(1/2/3): 33-38.
[12] MALIYEKKAL S M, SHUKLA S, PHILIP L, et al. Enhanced fluoride removal from drinking water by magnesia-amended activated alumina granules[J]. Chemical Engineering Journal, 2008, 140(1/2/3): 183-192.
[13] TRIPATHY S S, BERSILLON J L, GOPAL K. Removal of fluoride from drinking water by adsorption onto alum-impregnated activated alumina[J]. Separation and Purification Technology, 2006, 50(3): 310-317.
[14] TRIPATHY S S, RAICHUR A M. Abatement of fluoride from water using manganese dioxide-coated activated alumina[J]. Journal of Hazardous Materials, 2008, 153(3): 1043-1051.
[15] 刘争伟, 于枭影, 钟晓聪, 等. 含Al、Ca复合除氟剂在含氟硫酸锌溶液中的除氟性能[J]. 中国有色金属学报, 2016, 26(5): 1151-1157.
LIU Zhengwei, YU Xiaoying, ZHONG Xiaocong, et al. Performance of Ca, Al-containning composite defluoridation agent in zinc sulfate solution[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(5): 1151-1157.
[16] FANG Zhao, XUE Ning, LI Linbo, et al. Performance and mechanism for de-fluorination by modified aluminum hydroxide in zinc sulfate solution[J]. Journal of Nanoscience and Nanotechnology, 2016, 16(12): 12470-12475.
[17] TIAN Zhongliang, GUO Weichang, ZHANG Zhijian, et al. Removal of fluorine ions from industrial zinc sulfate solution by a layered aluminum-based composite[J]. Hydrometallurgy, 2017, 171: 222-227.
[18] LU Xiaojun, XU Zhenming, LI Jie, et al. Investigation of fluorine adsorption on nitrogen doped MgAl2O4 surface by first-principles[J]. Applied Surface Science, 2016, 376: 97-104.
[19] XIANG Wei, ZHANG Gaoke, ZHANG Yalei, et al. Synthesis and characterization of cotton-like Ca-Al-La composite as an adsorbent for fluoride removal[J]. Chemical Engineering Journal, 2014, 250: 423-430.
[20] KUMAR K V, PORKODI K. Modelling the solid-liquid adsorption processes using artificial neural networks trained by pseudo second order kinetics[J]. Chemical Engineering Journal, 2009, 148(1): 20-25.
[21] POINERN G E J, GHOSH M K, NG Y J, et al. Defluoridation behavior of nanostructured hydroxyapatite synthesized through an ultrasonic and microwave combined technique[J]. Journal of Hazardous Materials, 2011, 185(1): 29-37.
[22] WANG Jian, KANG Dongjuan, YU Xiaolin, et al. Synthesis and characterization of Mg-Fe-La trimetal composite as an adsorbent for fluoride removal[J]. Chemical Engineering Journal, 2015, 264: 506-513.
[23] WANG Yu, CHEN Ningping, WEI Wei, et al. Enhanced adsorption of fluoride from aqueous solution onto nanosized hydroxyapatite by low-molecular-weight organic acids[J]. Desalination, 2011, 276(1/2/3): 161-168.
(编辑 秦明阳)
收稿日期: 2020 -06 -30; 修回日期: 2020 -09 -10
基金项目(Foundation item):污酸酸泥的外场定向除杂与回用关键技术及示范(2019YFC1904204);2018年高层次人才平台建设项目(KKKP201852032) (Project(2019YFC1904204) supported by Key Technology and Demonstration of Field-Oriented Decontamination and Reuse of Sour Acid/Sludge; Project(KKKP201852032) supported by 2018 High-level Talent Platform Construction Program)
通信作者:施哲,教授,从事冶金反应工程学研究;E-mail: truepsyche@sina.com
DOI: 10.11817/j.issn.1672-7207.2021.06.033
引用格式:孙成余, 杨坤, 施哲, 等. 硫酸镁改性铝基吸附剂脱氟的工艺及机理[J]. 中南大学学报(自然科学版), 2021, 52(6): 2032-2039.
Citation:SUN Chengyu, YANG Kun, SHI Zhe, et al. Defluorination technology and mechanism of magnesium sulfate modified aluminum-based adsorbent[J]. Journal of Central South University(Science and Technology), 2021, 52(6): 2032-2039.