文章编号:1004-0609(2013)11-3225-07
中度嗜热微生物作用下黄铜矿表面改性
王 军1, 2,赵红波1, 2,李思奇1, 2,杨 勰1, 2,杨聪仁1, 2,覃文庆1, 2,邱冠周1, 2
(1. 中南大学 资源加工与生物工程学院, 长沙 410083;
2. 中南大学 生物冶金教育部重点实验室,长沙410083)
摘 要:通过分析黄铜矿表面接触角、Zeta电位和表面形貌变化,研究嗜热硫氧化硫杆菌(Sulfobacillus thermosulfidooxidans,S.t菌)和氧化亚铁钩端螺旋菌(Leptospirillum ferrooxidans,L.f菌)对黄铜矿表面性质的影响。结果表明,细菌培养基(9K培养基)对黄铜矿表面性质无明显影响,接触角稳定在黄铜矿表面接触角48°左右。两种细菌对黄铜矿表面性质影响规律相似,采用细菌摇瓶浸出时,振动条件下,矿物表面的亲水性随浸出过程逐渐增强;而在静置细菌浸出过程中,浸出初期黄铜矿表面疏水性变强,之后随浸出时间的延长黄铜矿表面的亲水性增强,推测可能是由于浸出前期黄铜矿表面生成疏水硫化物和元素硫,后期被进一步氧化分解。不同细菌作用后,黄铜矿的等电点接近细菌的等电点,说明两种细菌均能有效地吸附在黄铜矿表面。通过原子力显微镜(AFM)观察发现,黄铜矿经细菌浸出后,表面不同程度地被腐蚀,并且随着浸出时间的延长,表面腐蚀程度加剧,其中S.t菌对黄铜矿的腐蚀作用较L.f菌更强。
关键词:黄铜矿;中度嗜热微生物;表面性质
中图分类号:TF18 文献标志码:A
Surface modification of chalcopyrite in presence of moderately thermophilic bacteria
WANG Jun1, 2, ZHAO Hong-bo1, 2, LI Si-qi1, 2, YANG Xie3, YANG Cong-ren1, 2, QIN Wen-qing1, 2, QIU Guan-zhou1, 2
(1. School of Minerals Processing and Bioengineering, Central South University, Changsha 410083, China;
2. Key Laboratory of Biometallurgy, Ministry of Education, Central South University, Changsha 410083, China)
Abstract:The effects of Sulfobacillus thermosulfidooxidans and Leptospirillum ferrooxidans on the surface properties of chalcopyrite were investigated by analyzing the contact angle, Zeta-potential and surface morphology changes. The results show that the culture medium (9K medium) has no distinct effect on the chalcopyrite surface properties, the contact angles keep at about 48°. The hydrophilcity of chalcopyrite surface increases during bioleaching in shake flask under vibration condition, while in bioleaching under stationary condition, the surface hydrophobicity of chalcopyrite increases in the initial stage as the formation of hydrophobic substances like elemental sulphur and secondary Cu-Fe-S intermediate species, and then decreases as further oxidation. The isoelectric point of chalcopyrite in the presence of bacterium shifts towards the bacteria’s isoelectric point correspondingly, indicating that bacteria adsorb on the surface of chalcopyrite effectively. The erosion degree of chalcopyrite surface increases with bioleaching through observing atomic force microscope (AFM) images, and the corrosion rate in the presence of Sulfobacillus thermosulfidooxidans is higher than that in the presence of Leptospirillum ferrooxidans.
Key words: chalcopyrite; moderately thermophilic bacteria; surface properties
微生物冶金因其具有流程短、设备简单和环境友好等技术优势,在湿法冶金领域已获得广泛关注[1-3]。吸附是微生物与矿物作用的第一步,部分研究发现不同生长条件下的微生物具有不同的表面性质,对矿物表面表现出不同的吸附能力,从而具有不同的浸矿活性,DEVASIA等[4]认为细菌吸附到矿物表面不仅仅改变了细菌的生物化学性质,同时也改变了浸矿体系中的界面性质。LOOSDRECHT等[5]认为细菌表面性质中决定吸附的主要是表面疏水性和动电位。顾帼华等[6]通过对原子力显微镜表面进行表征及摇瓶浸出试验考察不同能源(Fe2+、单质硫和黄铜矿)培养的氧化亚铁硫杆菌 (A.f菌)对黄铜矿表面性质的影响及其与黄铜矿浸出的关系,结果表明,驯化的A.f菌在矿表面的附着能力更强,并显著改变黄铜矿表面性质。由于细菌对硫化物的吸附及氧化是在矿物的表面发生的,因此矿物的表面性质,包括表面元素分布、表面电性、缺陷、表面能和表面的不均匀性等,对细菌在矿物表面的吸附及氧化过程具有重要影响[7-9]。
众多研究表明,细菌在矿物表面的吸附可以极大地改变矿物表面性质,而选矿过程(如浮选和絮凝)主要取决于矿物表面性质,故通过生物处理实现对其矿物之间的有效分离具有重要意义。许多研究者利用细菌选择性地在黄铁矿表面或煤表面富集,通过改变黄铁矿的亲水性或煤的疏水性,增大欲分离矿物间可浮性的差异,从而强化后续分选作业。ATKINS等[10-11]采用黄铁矿粉驯化500 h的T.f菌在2%矿浆浓度条件下,对某高硫煤进行了2 min的细菌改性,然后常规浮选分离,结果表明,在有菌条件下,黄铁矿抑制效果增加一倍。CAPES等[12]将高硫煤浆在pH>5时用T.f菌处理改性后用油团絮凝法分离,结果可脱出90%黄铁矿。WATLING[7]发现矿物吸附A. ferrooxidans 菌后,矿物表面亲水性或疏水性发生变化,其可浮性发生变化。OHMURA等[13]选用多粘芽胞杆菌和氧化亚铁硫杆菌来改变黄铜矿和黄铁矿的表面性质特性,改变其浮选,使得从黄铁矿中优先浮选黄铜矿成为可能。
综上所述,开展微生物在矿物表面的吸附研究具有重要意义,有关微生物与矿物作用后表面性质变化的报道己经很多,主要是用它改变黄铁矿表面性质,从而达到硫化矿生物浮选和絮凝,但关于中度嗜热微生物对黄铜矿表面性质影响及铁氧化菌和硫氧化菌对黄铜矿表面性质改变效果区别的研究工作鲜有报道。
因此,本文作者选用两种重要的浸矿细菌,即高温(≥45 ℃)培养的嗜热硫氧化硫杆菌(Sulfobacillus thermosulfidooxidans,S.t菌)和中温(35 ℃)培养的氧化亚铁钩端螺旋菌(Leptospirillum ferrooxidans,L.f菌),分别考察其对黄铜矿表面性质的影响,着重研究这两种细菌浸出前后黄铜矿表面接触角、动电位和表面腐蚀形貌的变化。
1 实验
1.1 实验材料和仪器
纯黄铜矿取自广东梅州,经过磨矿、干式筛分之后,取粒径小于0.074 mm 矿粒,再经玛瑙研磨至粒径小于5 μm,用于Zeta电位测定。挑选结晶良好的块状黄铜矿进行切割、打磨、抛光,用于接触角测定和原子力显微镜(AFM)测试。试验选用嗜热硫氧化硫杆菌(Sulfobacillus thermosulfidooxidans,S.t菌)和嗜铁钩端螺旋菌(Leptospirillum ferrooxidans,L.f菌),均取自中南大学生物冶金教育部重点实验室。
HZQ-C培养箱(哈尔滨东联电子技术有限公司生产)用于细菌的培养,用Usk-Ⅱ型不锈钢电热蒸馏水器(上海三申医疗器械有限公司生产)自制蒸馏水,YX280A型手提式不锈钢蒸汽消毒器(上海三申医疗器械有限公司生产)用于仪器灭菌,PHSJ-4A型pH计(上海精密仪器有限公司生产)测试矿浆酸度,用JJC-1型接触角测定仪(长春市第五光学仪器有限公司生产)测量接触角,用TDL5-A-5型台式离心机(上海安亭科学仪器厂生产)离心细菌集合体,用Coulter Dels44osx型 Zeta电位测定仪(美国贝克曼库尔特公司生产)测试动电位,用diMultiMode V型原子力显微镜观察黄铜矿表面形貌。
1.2 实验方法
1.2.1 细菌培养
原始菌株用9K培养基培养,pH调节为2.0,9K培养基成分如下:3 g/L (NH4)2SO4,0.1 g/L KCl,0.5 g/L K2HPO4,0.5 g/L MgSO4・7H2O,0.01 g/L Ca(NO3)2,整个实验过程均采用现制备的蒸馏水。S.t菌培养加入 10 g/L硫粉作为能源物质,L.f菌培养加入44.7 g/L FeSO4・7H2O作为能源物质。培养基在灭菌锅中采用0.1 MPa、121 ℃条件灭菌20 min,细菌接种量均为5%,细菌培养均在摇床中进行,转速为170 r/min,温度分别为45和35 ℃。
1.2.2 接触角测定
测量接触角时,用微量进样器(2.0 mL)将蒸馏水在距待测固体表面约3 mm处垂直滴加在待测固体表面,形成座滴,快速测量,读取6次接触角值,计算平均值作为接触角值。
1.2.3 Zeta电位的测定
将0.1 g黄铜矿粉分别加入到离子强度I=0.01 mol/L和I=0.001 mol/L的NaCl溶液中,调节pH值,搅拌5 min后,放入洗净的样品槽,将样品槽放入电位测定仪中, 测定黄铜矿的Zeta电位;将0.1 g矿粉加入到细菌浓度为2×108 c/mL-1、pH值为2.0的NaCl溶液中,搅拌60 min后,离心法分离出矿粒,控制矿浆浓度为1 g/L, 在离子强度I=0.01 mol/L的NaCl溶液中进行细菌作用后矿物Zeta电位的测定;同理,在离子强度I=0.01 mol/L的NaCl溶液中加入细菌(L.f和S.t)悬液,细菌浓度为2×108 cell/mL,调节pH值,测定不同pH值条件下细菌的Zeta电位。测试中用HCl和NaOH溶液调节pH值,每个样品测量3次,取其平均值。
1.2.4 原子力显微镜(AFM)形貌
采用美国Veeco公司生产的diMultiMode V型原子力显微镜进行试验。其微悬臂由氮化硅(Si3N4)制成,弹性系数为0.16 N/m,最大扫描范围为125 μm×125 μm,扫描频率为0.5 Hz,采用接触式(Contact mode)连续扫描。9K培养基接种细菌浓度为2×108 cell/mL的菌液,接种量为10%,黄铜矿置于菌液中,不同时间后取出,蒸馏水反复冲洗后,自然晾干,用于观察矿物表面腐蚀形貌。
2 结果与讨论
2.1 原子力显微镜(AFM)形貌
图1 所示为微生物浸出前的黄铜矿表面形貌,可见黄铜矿表面基本平整光滑。图2(a)和图2(b)所示分别为S.t菌浸出黄铜矿 2 h 和 2 d 后矿物表面的三维图。由图2可见,S.t菌浸出2 h 后的黄铜矿表面,相对于浸出前,更为粗糙,有很明显的腐蚀现象;而细菌浸出 2 d 后的黄铜矿表面,较浸出 2 h 的黄铜矿表面更为粗糙,表面腐蚀现象明显加重。
图3(a)和图3(b)所示分别为L.f菌浸出2 d和5 d后黄铜矿的表面形貌。可见L.f菌浸出2 d后的黄铜矿表面较为粗糙,具有明显的腐蚀现象;L.f菌浸出5 d后的黄铜矿表面比只浸出2 d后的表面更加粗糙,腐蚀明显加重。对比两种细菌浸出黄铜矿2 d的AFM像可知,S.t菌作用下的黄铜矿浸出2 d后的表面腐蚀程度较L.f菌更为严重,由此可知,在微生物浸出前期,S.t菌对黄铜矿表面的氧化/腐蚀作用较L.f菌的更强。
2.2 接触角测定
表1和2所列分别为S.t菌和L.f菌的接触角数据。从表中可以看出,S.t菌的接触角为14.5°左右,L.f菌的接触角为9.5°左右,均具有较强亲水性,主要由于细菌细胞表面上分布着许多膜蛋白,并含有―OH、―COOH、―SH、―NH2等极性基团,从而使细菌表面亲水。L.f菌亲水性较S.t菌的更强,主要由于其蛋白质含量更高。
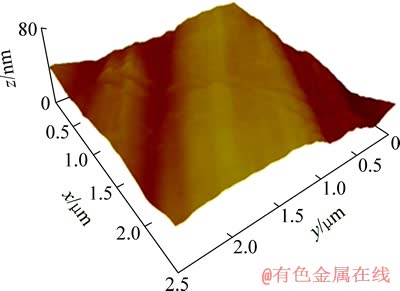
图1 细菌作用前黄铜矿表面三维图
Fig. 1 3D image of polished chalcopyrite surface before treatment by bacteria
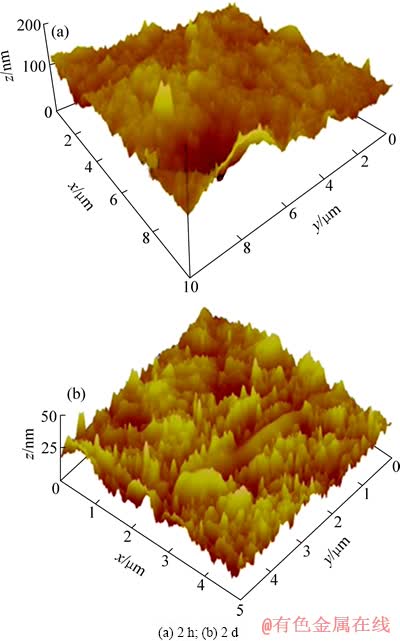
图2 S.t菌作用不同时间后黄铜矿表面的三维图
Fig. 2 3D images of chalcopyrite surface treated by S.t bacteria for different times
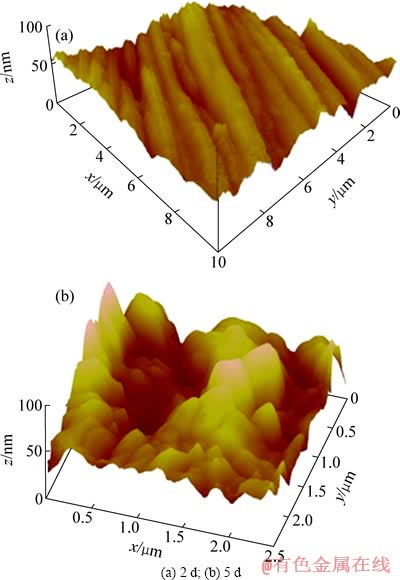
图3 L.f 菌作用不同时间后黄铜矿表面的三维图
Fig. 3 3D images of chalcopyrite surface treated by L.f for different times
表1 S.t菌的接触角
Table 1 Contact angle of S.t bacteria

表2 L.f菌的接触角
Table 2 Contact angle of L.f bacteria

图4所示为黄铜矿的磨光片在室温条件下,9K培养基(pH=2.0)浸出后接触角变化。可以看出,随着浸出时间增加,黄铜矿磨光片的接触角基本上没有变化,由此可知,所选培养基对黄铜矿表面润湿性无明显影响。
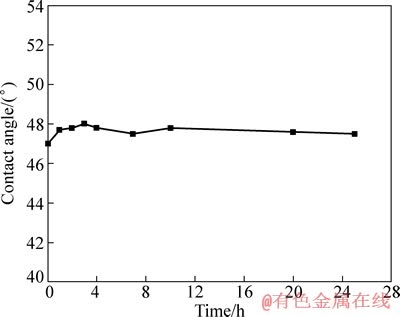
图4 黄铜矿在酸性9 K培养基中浸出后接触角的变化
Fig. 4 Variation of contact angle of chalcopyrite treated by acid 9 K culture medium
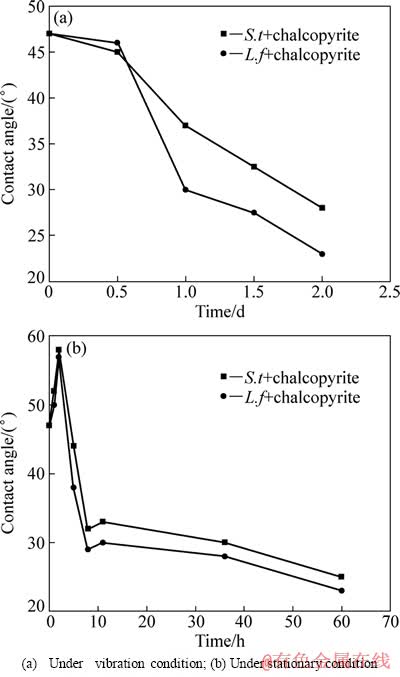
图5 振动浸出和静置浸出条件下黄铜矿表面接触角的变化
Fig. 5 Variation of contact angle of chalcopyrite treated by bacteria under different conditions
图5(a)所示为振动条件下黄铜矿被S.t菌和L.f 菌浸出后接触角的变化。随着浸出时间增加,黄铜矿表面的接触角持续变小,亲水性持续增强;图5(b)所示为黄铜矿在静置、室温条件下被S.t菌和L.f菌浸出后接触角的变化,浸出前2 h,黄铜矿表面接触角增大,疏水性增强。随后表面接触角减小,亲水性增强。对于黄铜矿微生物浸出过程,大量研究表明,主要存在以下化学反应[1, 14-16]:
CuFeS2+2H++1/2O2→CuS+Fe2++H2O+S0 (1)
CuFeS2→Cu2++Fe3++Cun-1Fen-1S2n+5e (2)
Fe2++H++1/4O2→Fe3++1/2H2O (3)
CuS+Fe3++4H2O→Fe2++Cu2++8H++S0 (4)
S0+4H2O→SO42-+8H+ (5)
2CuFeS2+8.5O2+H2SO4→2CuSO4+Fe2(SO4)3+H2O (6)
因此,推测在静置浸出过程初阶段,由于传质过程速率较慢,黄铜矿表面因疏水铜硫化合物和元素硫的产生,导致矿物表面疏水性增强,以直接作用为主,如反应(1)和(2)所示;随着浸出反应的进行,疏水铜硫化合物和元素硫被继续氧化为亲水的硫酸盐,从而导致矿物表面亲水性逐渐增强,如反应(4)和(5)所示。而振动条件下浸出,由于传质过程速率较快,从而加强了黄铜矿溶解的动力学过程,表面产生疏水铜硫化合物和元素硫被较快氧化,反应如(6)所示,由此可知,振动可以促进黄铜矿在微生物作用条件下的溶解。
2.3 Zeta电位测定
在离子强度I=0.01 mol/L 和I=0.001 mol/L 的NaCl溶液中测定不同pH值条件下黄铜矿的Zeta电位,结果如图6(a)所示。黄铜矿的Zeta电位随着pH值的增大而变得更负,离子强度I=0.01 mol/L 时黄铜矿的Zeta 电位较离子强度 I=0.001 mol/L 时黄铜矿的Zeta电位明显负移。根据古依-切普曼-斯特恩(GCS)双电层模型[17-18],在离子强度较低的情况下,斯特恩电位可以等同于动电位,分散层可以等效为平行板电容,则斯特恩电位ψ(即Zeta电位)的表达式可简化为: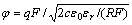 ,c为电解质浓度,q为表面电荷密度,由上式可知,随着电解质浓度增大,溶液离子强度增大,Zeta电位因分散层被压缩而变小。
,c为电解质浓度,q为表面电荷密度,由上式可知,随着电解质浓度增大,溶液离子强度增大,Zeta电位因分散层被压缩而变小。
在离子强度I=0.01 mol/L 的NaCl溶液中测定不同pH值条件下细菌的Zeta电位,结果如图6(b)所示,S.t菌的等电点在pH=3.1处,L.f菌的等电点在pH=6.0处,两种细菌的Zeta电位值均随着pH值的增大而负移,L.f菌较S.t菌具有更高的动电位和等电点的原因主要是其EPS和蛋白质含量更高。
分别以S.t菌和L.f菌浸出黄铜矿,并对比分析黄铜矿Zeta电位的变化,结果如图7所示。可见,S.t菌和L.f菌单独浸出黄铜矿时,随着浸出过程进行,黄铜矿动电位曲线逐渐接近对应浸矿细菌的,等电点也靠近对应浸矿细菌等电点。说明S.t菌和L.f菌单独浸出黄铜矿时,能有效吸附于黄铜矿表面。
采用S.t菌和L.f菌的混合菌浸出黄铜矿,Zeta电位测试结果如图8所示。可见,混合菌作用下黄铜矿动电位曲线和等电点正好介于两种细菌之间,说明两种细菌均能同时有效吸附于黄铜矿表面。不同细菌作用后黄铜矿表现出不同的电动行为,表明不同的细菌对黄铜矿表面性质的改变能力是不同的,吸附能力也是不同的。
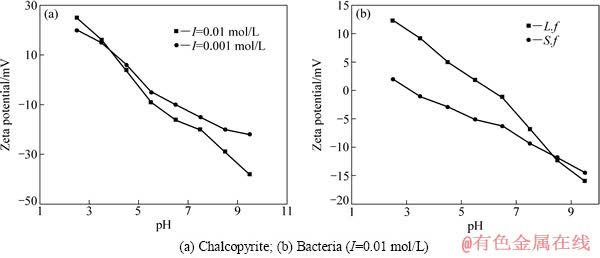
图6 黄铜矿和细菌的Zeta电位
Fig. 6 Zeta potential of chalcopyrite and bacteria
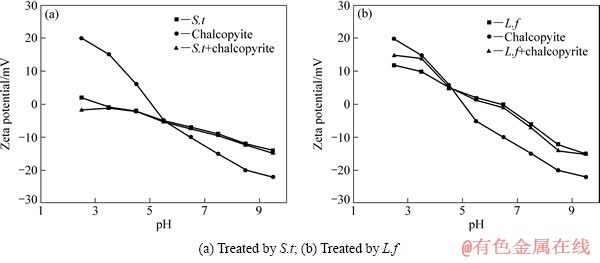
图7 S.t菌和L.f菌作用后黄铜矿的Zeta电位(I=0.01 mol/L)
Fig. 7 Zeta potential of chalcopyrite after treated by S.t and L.f (I=0.01 mol/L)
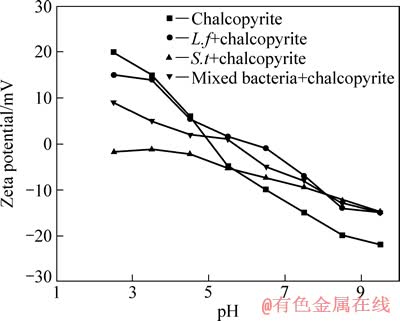
图8 不同细菌作用后黄铜矿的Zeta电位(I=0.01 mol/L)
Fig. 8 Zeta potential of chalcopyrite after treated by different bacteria (I=0.01 mol/L)
3 结论
1) S.t和L.f菌两种浸矿细菌的接触角均很小,亲水性较强, L.f菌由于具有更高蛋白质含量,亲水性更强。细菌浸出初期,以直接作用为主,振动利于加快黄铜矿的溶解。
2) L.f菌较S.t菌具有更高等电点,可能是由于含有更多的EPS和蛋白质,细菌的吸附使黄铜矿的等电点朝细菌的等电点方向偏移,表明两种细菌在黄铜矿表面发生了特效吸附,改变了原来黄铜矿的双电层结构;混合菌作用下动电位和等电点正好介于两种细菌之间,说明两种细菌均能同时有效吸附于黄铜矿表面。
3) 黄铜铜矿浸出初期,S.t菌较L.f菌具有更强的氧化/腐蚀能力。
REFERENCES
[1] 白 静, 温建康, 黄松涛, 武 彪, 姚国成. 不同成矿条件下黄铜矿微生物浸出研究概况[J]. 稀有金属, 2012, 36(4): 644-650.
BAI Jing, WEN Jian-kang, HUANG Song-tao, WU Biao, YAO Guo-cheng. Review on bioleaching of chalcopyrite with different mineralization[J]. Chinese Journal of Rare Metals, 2012, 36(4): 644-650.
[2] 尹升华, 吴爱祥, 王洪江, 韩 斌. 微生物浸出低品位矿石技术现状与发展趋势[J]. 矿业研究与开发, 2010, 30(1): 46-49.
YIN Sheng-hua, WU Ai-xiang, WANG Hong-jiang, HAN Bin. Current status and present situation and developing trend of low grade ore bioleaching technology[J]. Mining Research and Development, 2010, 30(1): 46-49.
[3] BRIERLEY J A, BRIERLEY C L. Present and future commercial applications of biohydrometallurgy[J]. Hydrometallurgy, 2001, 59(2): 233-239.
[4] DEVASIA P, NATARAJAN K A, SATHYANARAYANA D N, RAO G R. Surface chemistry of Thiobacillus ferrooxidans relevant to adhesion on mineral surfaces[J]. Applied and Environmental Microbiology, 1993, 59(12): 4051-4055.
[5] van LOOSDRECHT M C, LYKLEMA J, NORDE W, SCHRAA G, ZEHNDER A J. Electrophoretic mobility and hydrophobicity as a measured to predict the initial steps of bacterial adhesion[J]. Applied and Environmental Microbiology, 1987, 53(8): 1898-1901.
[6] 顾帼华, 陈明莲, 苏丽君, 李建华, 胡岳华, 邱冠周. 氧化亚铁硫杆菌对黄铜矿表面性质及其浸出的影响[J]. 中南大学学报: 自然科学版, 2010, 41(3): 807-812.
GU Guo-hua, CHEN Ming-lian, SU Li-jun, LI Jian-hua, HU Yue-hua, QIU Guan-zhou. Effects of Acidithiobacillus ferrooxidans on surface properties of chalcopyrite and bioleaching[J]. Journal of Central South University: Science and Technology, 2010, 41(3): 807-812.
[7] WATLING H R. The bioleaching of sulphide minerals with emphasis on copper sulphides―A review[J]. Hydrometallurgy, 2006, 84(1): 81-108.
[8] JIA Chun-yun, WEI De-zhou, LIU Wen-gang, HAN Cong, GAO Shu-ling, WANG Yu-juan. Selective adsorption of bacteria on sulfide minerals surface[J]. Transactions of Nonferrous Metals Society of China, 2008, 18(5): 1247-1252.
[9] ANDREWS G F. The selective adsorption of thiobacilli to dislocation sites on pyrite surfaces[J]. Biotechnology and Bioengineering, 1988, 31(4): 378-381.
[10] ATKINS A S, BRIDGWOOD E W, DAVIS A J, POOLEY F D. A study of the suppression of pyritic sulphur in coal froth flotation by Thiobacillus ferrooxidans[J]. Coal Perparation, 1987, 5(1/2): 1-13.
[11] TOWNSLEY C C, ATKINS A S, DAVIS A J. Suppression of pyritic sulphur during flotation tests using the bacterium Thiobacillus ferrooxidans[J]. Biotechnology and Bioengineering, 1987, 30(1): 1-8.
[12] BUTLER B J, KEMPTON A G, COLEMAN R D, CAPES C E. The effect of particle size and pH on the removal of pyrite from coal by conditioning with bacteria followed by oil agglomeration[J]. Hydrometallurgy, 1986, 15(3): 325-336.
[13] OHMURA N, KITAMURA K, SAIKI H. Mechanism of microbial flotation using Thiobacillus ferrooxidans for pyrite suppression[J]. Biotechnology and Bioengineering, 1993, 41(6): 671-676.
[14] DORADO A D, SOLE M, LAO C, ALFONSO P, GAMISANS X. Effect of pH and Fe (III) ions on chalcopyrite bioleaching by an adapted consortium from biogas sweetening[J]. Minerals Engineering, 2012, 39: 36-38.
[15] WANG Yu-guang, SU Li-jun, ZHANG Li-juan, ZENG Wei-min, WU Jun-zi, WAN Li-li, QIU Guan-zhou, CHEN Xin-hua, ZHOU Hong-bo. Bioleaching of chalcopyrite by defined mixed moderately thermophilic consortium including a marine acidophilic halotolerant bacterium[J]. Bioresource Technology, 2012, 121: 348-354.
[16] XIA Le-xian, URIBE P, LIU Xin-xing, YU Chu, CHAI Li-yuan, LIU Jian-she, QIU Wen-qing, QIU Guan-zhou. Comparison of chalcopyrite bioleaching after different microbial enrichment in shake flasks[J]. World Journal of Microbiology and Biotechnology, 2013, 29(2): 275-280.
[17] 王淀佐, 邱冠周, 胡岳华. 资源加工学[M]. 北京: 科学出版社, 2005.
WANG Dian-zuo, QIU Guan-zhou, HU Yue-hua. Minerals Processing[M]. Beijing: Science Press, 2005.
[18] HENDERSON D, BODA D. Insights from theory and simulation on the electrical double layer[J]. Phys Chem Chem Phys, 2009, 20(11): 3822-3830.
(编辑 龙怀中)
基金项目:国家自然科学基金面上项目(51374248);教育部新世纪人才计划项目(NCET-13-0595);国家高技术研究发展计划项目(2012AA061501);国家重点基础研究发展计划项目(2010CB630905);高等学校博士学科点专项科研基金资助项目(20120162120010)
收稿日期:2013-04-10;修订日期:2013-07-15
通信作者:王 军,副教授,博士;电话:0731-88876557;E-mail:wjwq2000@126.com.