网络首发时间: 2018-02-06 17:48
稀有金属 2018,42(06),650-656 DOI:10.13373/j.cnki.cjrm.xy17050036
La0.9Rb0.1Co1-xFexO3-δ钙钛矿催化剂上NOx辅助碳烟燃烧性能的研究
车祥 汪炜 商周 王丽 郭耘 卢冠忠
华东理工大学工业催化研究所
摘 要:
通过柠檬酸溶胶凝胶法制备了La0.9Rb0.1Co1-xFexO3-δ (x=0.1~0.8) 系列钙钛矿催化剂。通过X射线衍射 (XRD) 、氢气程序升温还原 (H2-TPR) 、NOx程序升温脱附 (NOx-TPD) 及X射线光电子能谱 (XPS) 考察了Fe含量变化对催化剂结构、NOx辅助碳烟燃烧反应活性、催化剂氧化还原活性、催化剂表面Fe和Co的化学状态以及NOx储存能力的影响。结果表明:所制备的催化剂均保持钙钛矿结构, Co与Fe的共掺杂改变了B位金属的化学状态, 催化剂表面存在Co2+和更高价态的Fe物种。相比纯LaCoO3和LaFeO3, La0.9Rb0.1Co1-xFexO3-δ (x=0.1~0.8) 催化剂碳烟燃烧的特征温度T50分别下降约30和70℃, 碳烟燃烧的速度也随之加快。同时, 在NOx辅助碳烟燃烧过程中, NO氧化所生成的NO2可与碳烟反应生成N2, 其中La0.9Rb0.1Co0.6Fe0.4O3-δ催化剂具有最高的NOx消除能力, 在381℃时达到36.4%。
关键词:
钙钛矿;LaRbCoFeO;NO辅助碳烟燃烧;NO储存;
中图分类号: TQ426
作者简介:车祥 (1991-) , 男, 新疆克拉玛依人, 硕士研究生, 研究方向:环境催化;E-mail:bullet630@163.com;;王丽, 副教授;电话:021-64253703;E-mail:wangli@ecust.edu.cn;
收稿日期:2017-05-18
基金:国家科技部863计划项目 (2015AA034603);国家自然科学基金项目 (21333003) 资助;
Catalytic Performances of La0.9Rb0.1Co1-xFexO3-δ Perovskite-Type Catalysts for NOx-Assisted Sootcombustion
Che Xiang Wang Wei Shang Zhou Wang Li Guo Yun Lu Guanzhong
Research Institute of Industrial Catalysis, East China University of Science and Technology
Abstract:
A series of La0.9Rb0.1Co1-xFexO3-δ (x = 0. 1 ~ 0. 8) perovskite-type catalysts were prepared via citric acid sol-gel method.X-ray diffraction (XRD) , hydrogen temperature programmed reduction (H2-TPR) , NOx temperature programmed desorption (NOxTPD) and X-ray photoelectron spectroscopy (XPS) were used to investigate the effects of doping Fe on the structures, activities for NOx-assisted sootcombustion, surface properties of catalysts. The results showed that the prepared samples showed perovskite structure, and co-doping of Fe and Co could modify the chemical states of B sites and produce Co2+ and high valence Fe specieson the surface. Compared with pure LaCoO3 and LaFeO3, the T50 of soot combustion on La0.9Rb0.1Co1-xFexO3-δ (x = 0. 1 ~ 0. 8) catalysts decreased by 30 and 70 ℃, respectively, and the combustion rate of soot was also promoted. Meanwhile, the NO2 formed by the oxidation of NO could react with soot to produce N2 during the process of NOxassisted soot combustion. Among them, La0.9Rb0.1Co0.6Fe0.4O3-δ behaved the highest removal efficiency of NOx, reaching 36. 4% at 381 ℃.
Keyword:
perovskite; La0.9Rb0.1Co1-xFexO3-δ; NOx-assisted sootcombustion; NOx storage;
Received: 2017-05-18
柴油机以低油耗、高效率、动力强的优点, 近年来在很多领域得到了广泛的应用, 但其尾气是城市环境中NOx的主要来源之一[1,2,3]。1989年, Yoshida等[4]首次提出, 在催化型颗粒捕集器 (catalyzed diesel particulate filter, CDPF) 上捕集颗粒物 (particulate matter, PM) , 并在NOx/O2条件下利用NOx作为氧化剂除去PM, 生成无害的N2和CO2。目前, 针对PM在NOx气氛下进行消除的催化剂开发主要集中在过渡金属氧化物[5], Ce O2固溶体材料[6,7], 钙钛矿[8,9]及尖晶石型[10]复合氧化物等材料上。其中, 钙钛矿催化剂具有良好的应用前景, 对钙钛矿A位和B位进行掺杂可有效提高催化剂对于NOx-碳烟反应的活性。本文试图考察Co与Fe同时存在于钙钛矿B位的掺杂钙钛矿催化剂对于NOx辅助的碳烟燃烧反应性能。
利用溶胶凝胶法制备了La0.9Rb0.1Co1-x FexO3-δ (x=0.1~0.8) 系列催化剂, 对其催化NOx辅助碳烟燃烧的活性进行了考察, 并利用X射线衍射 (XRD) 、氢气程序升温还原 (H2-TPR) 、NOx程序升温脱附 (NOx-TPD) 及X射线光电子能谱 (XPS) 对催化剂进行了表征。
1 实验
1.1 催化剂制备
按所需化学计量比称取硝酸镧、硝酸铷、硝酸钴、硝酸铁, 及一定量柠檬酸, 溶于去离子水, 超声震荡5 min, 得到澄清溶液。所加入柠檬酸的摩尔量为总阳离子量的1.2倍。溶液在80℃水浴中持续加热搅拌, 首先得到牛奶状不透明溶胶, 然后随着水分蒸发变为半透明粘稠凝胶状物质。随后120℃过夜, 再将所得蓬松海绵状固体研碎后转移至马弗炉, 400℃焙烧2 h, 除去有机络合剂及硝酸盐, 再继续750℃焙烧4 h, 得到催化剂。本文催化剂命名规则如下:只写出各元素首字母, 用数字表示Fe掺杂量。如La0.9Rb0.1Co0.9Fe0.1O3简写为LRCF0.1。其余以此类推。La Co O3记为LC, La Fe O3记为LF。
1.2 催化剂活性评价
活性评价在石英固定床反应器中进行。原料气通过质量流量器控制流量进入混气罐, 混合均匀后经过内径6 mm的固定床石英管反应器的催化剂床层, 催化剂与碳烟、石英砂颗粒 (245~350μm) 拌匀。反应气氛为500×10-6NO+8%O2/Ar, 气体体积流量为200 ml・min-1。反应开始前, 催化剂先在反应气氛中100℃吸附30 min。以5℃・min-1速率从100℃升温至650℃, 碳烟消耗殆尽后反应结束。床层温度由插入石英管反应器的K型热电偶记录并储存。反应产物CO, CO2气体由浙江福立GC9790气相色谱分析, 气体经由Porapak Q色谱柱分离后进入甲烷转化炉, 再以氢火焰离子化检测器 (FID) 检测。NO, NO2和NOx浓度用Thermofisher 42i-HL NO-NO2-NOx分析仪检测。
催化剂用量为90 mg, 碳烟用量为10 mg。碳烟与催化剂采取紧密接触, 即催化剂与碳烟用药匙混合3 min后, 在玛瑙研钵中研磨5 min。
通过比较温度-碳烟转化率曲线的特征温度, 即T10, T50及T90来代表样品的碳烟燃烧活性, 下标数字代表碳烟转化为CO2的百分比。将T10和T90作为反应起始及结束的标志, 并计算二者间的温度差ΔT作为碳烟燃烧速度的参考指标。主要以T50评价催化剂活性的高低。另外计算了催化剂催化NOx消除反应的活性, 以NOx最大转化率 (ηmax.) 表示, 定义如下:

式中[NOx]in代表反应开始时反应气氛中NOx浓度, [NOx]min表示出口气体最小NOx浓度。
1.3 催化剂表征
XRD图谱在Bruker D8 Focus型X射线粉末衍射仪上获得。使用Cu Kα射线, λ=1.54056 nm, X光管工作条件为40 k V, 40 m A, 扫描范围10°~80°, 扫描步长0.02°, 扫描速度6 (°) ・min-1。晶相及物种通过MDI Jade 5.0软件中JCPDS卡片进行确定。催化剂的晶粒尺寸通过Scherer公式进行计算:

用XPS测定催化剂样品的表面组成, 使用Thermo ESCALAB 250型电子能谱仪测定。所用射线激发源为单色Al Kα, 能量1486.6 e V, 功率150 W, X射线束斑500μm, 能量分析器固定透过能为30 e V。数据经过校正, 用作参考的污染碳C 1s主峰结合能定为284.8 e V。
H2-TPR实验采用商用程序升温还原仪。称取100 mg样品放入U型石英管, 连接管路后通入气体流量为40 ml・min-1的5%H2/N2混合气, 待基线平稳后, 从50℃升温至800℃, 升温速率10℃・min-1。采用热导检测器 (TCD) 记录升温过程中氢气浓度变化, 得到温度-TCD信号曲线。
NOx-TPD实验在活性评价装置上进行。称量90 mg催化剂放入直管式石英管, 通入200 ml・min-1的500×10-6NO+8%O2/Ar在350℃保持30 min至吸附饱和。随后在相同气氛下降温至50℃, 再将气体切换为200 ml・min-1的Ar气, 吹扫30 min。最后以10℃・min-1的速率从当前温度升温至600℃。反应出口气体NO, NO2和NOx浓度使用NO-NO2-NOx分析仪检测并记录。
2 结果与讨论
2.1 催化剂的NOx辅助碳烟燃烧性能
表1列出了各催化剂NOx气氛下的碳烟燃烧反应性能。由表1可见, LC催化剂的碳烟燃烧性能高于LF催化剂, T50分别为372和419℃。A位掺杂Rb, B位为不同比例Fe和Co的催化剂, 其活性均优于LC和LF催化剂, 同时发现Fe含量的变化对催化剂起燃温度的影响并不显著, 各掺杂催化剂的T10均在300℃附近, T50分布在340~360℃范围, ΔT在75~85℃之间。其中LRCF0.3催化剂的碳烟燃烧活性最高, 碳烟燃烧的T10和T50最低, 分别为289和342℃。同时, 掺杂提高了催化剂上的碳烟燃烧速度, 即ΔT减小。在A位Rb掺杂量不变的情况下, B位Fe掺杂量合适时 (x=0.3~0.6) , 掺杂催化剂上碳烟燃烧的ΔT相比LC和LF分别降低了30~40℃。
2.2 XRD表征
La0.9Rb0.1Co1-xFexO3-δ (LRCFx, x=0.1~0.8) 的XRD谱图见图1 (a) 。各样品上都未检测到Rb物种的峰, 可认为Rb进入了钙钛矿的晶格。催化剂取代后依旧能够保持菱形钙钛矿结构, 且衍射峰均处于La Co O3 (JPCDS 48-0123) 以及La Fe O3 (JPCDS 37-1493) 之间, 并随B位Fe含量的升高, 逐渐向La Fe O3形式变化。如图1 (b) 的局部放大谱图及表2所示, Fe掺杂量的增加使得主衍射峰2θ向低角度偏移, 在x≤0.5时, 在2θ=36.882°处可检测到立方相尖晶石结构的Co3O4的特征峰, 且Co3O4衍射峰的强度随Fe掺杂量的升高而逐渐减弱。
表1 La0.9Rb0.1Co1-xFexO3-δ系列催化剂NOx辅助碳烟燃烧活性Table 1Catalytic performance of La0.9Rb0.1Co1-xFexO3-δcatalysts for NOx-assisted soot combustion 下载原图
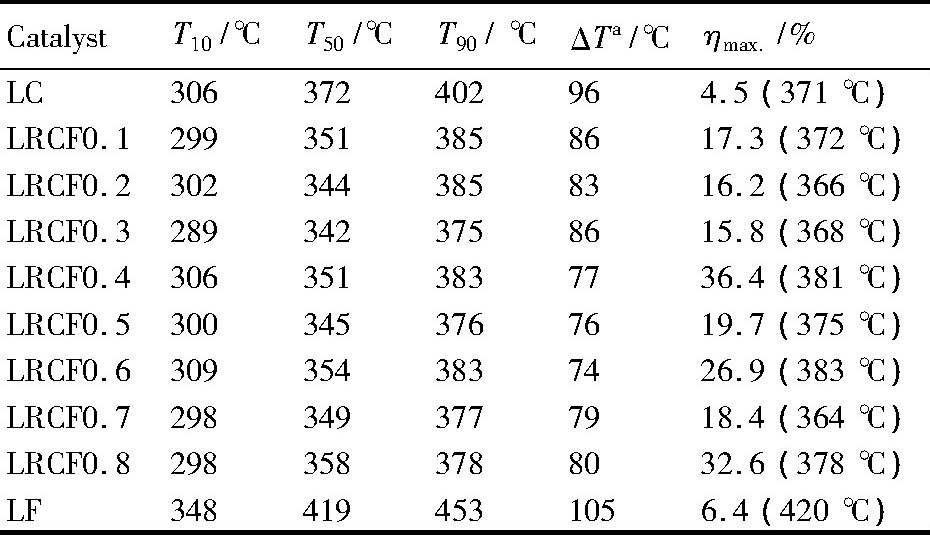
表1 La0.9Rb0.1Co1-xFexO3-δ系列催化剂NOx辅助碳烟燃烧活性Table 1Catalytic performance of La0.9Rb0.1Co1-xFexO3-δcatalysts for NOx-assisted soot combustion
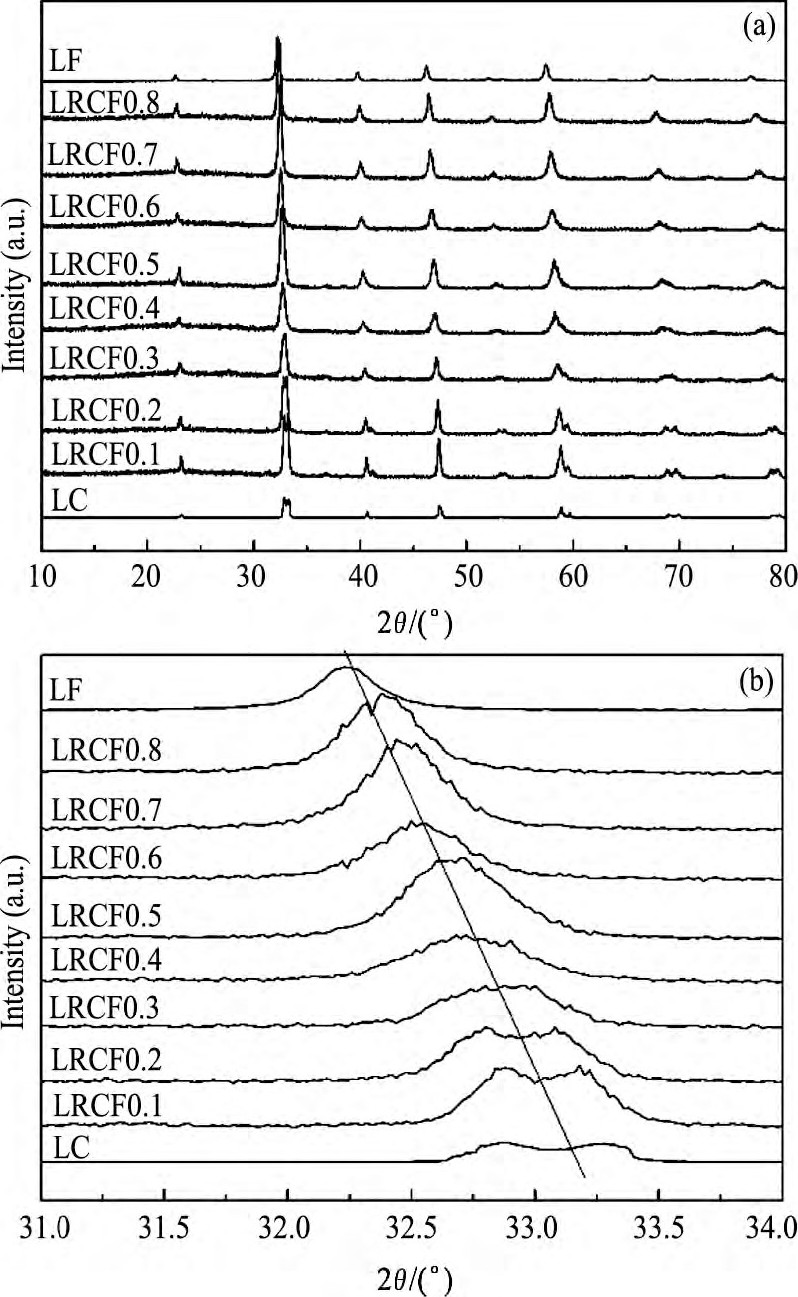
图1 La0.9Rb0.1Co1-xFexO3-δ (x=0.1~0.8) 催化剂的XRD谱图Fig.1XRD patterns of La0.9Rb0.1Co1-xFexO3-δ (x=0.1~0.8) catalysts
(a) Full spectrum; (b) Enlarged spectrum
表2 衍射峰位置及晶粒尺寸Table 2 Peak positions and grain sizes of La0.9Rb0.1Co1-x FexO3-δ (x=0.1~0.8) catalysts 下载原图
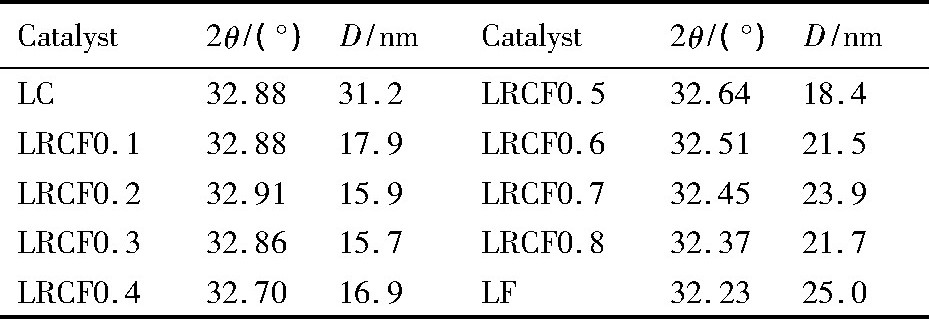
表2 衍射峰位置及晶粒尺寸Table 2 Peak positions and grain sizes of La0.9Rb0.1Co1-x FexO3-δ (x=0.1~0.8) catalysts
同时, 随着Fe含量增加, 衍射峰的强度先减弱, 再增加, 说明当Fe的掺杂较低时, 降低了LaCo O3的结晶度, 但随着Fe含量的升高, 其晶相逐渐向La Fe O3转变, 催化剂的结晶度随之逐渐升高。根据Scherer公式所得到的平均催化剂晶粒尺寸随Fe含量的变化呈“倒火山型”变化, 当Fe含量较低时, 晶粒尺寸随Fe含量的增大逐渐收缩, LRCF0.3具有最小的晶粒尺寸。继续增大Fe含量, 催化剂的晶粒尺寸逐渐增大。
2.3 H2-TPR表征
图2给出了催化剂H2-TPR表征结果。在LC上主要出现两个还原峰, 出现在454和612℃, 分别对应于Co3+到Co2+的还原, 以及Co2+到Co0的还原过程[11]。LF催化剂也分别在360和450℃检测到两个还原峰, 前者可归因于Fe4+/Fe3+到Fe2+的还原, 后者为Fe2+到Fe0的还原过程[12]。随B位Fe含量增加, 催化剂的TPR曲线表现出由LC向LF变化的趋势。当Fe掺杂量在x=0.3~0.5时, 高温段的还原峰减弱, 并在530~580℃处出现宽化的还原峰, 表明此处发生了Co-Fe的共还原, 还原峰向低温偏移。结合表1中的数据, 发现催化剂碳烟燃烧的活性与与TPR结果并不直接对应, 如LF催化剂的还原峰温度显著低于LC催化剂, 但其活性却明显低于LC催化剂。这可能是由两方面原因造成的: (1) 与K的作用类似, 碱金属Rb的引入可促进反应过程中催化剂与碳烟的接触[9,11], 从而使得掺杂催化剂具有更佳的碳烟燃烧效果。 (2) 从表1中看出, 掺杂催化剂的ΔT要远小于LF和LC。结合XRD和H2-TPR结果, 认为Co, Fe共掺杂时, 不仅使得晶体结构发生了变化, 相应地增加了结构缺陷;而且TPR中出现了CoFe共还原物种, 说明二者间的相互作用使其化学状态发生了变化。这两方面因素的共同作用使得催化剂吸附、活化氧的速度得到提高, 从而提高了碳烟燃烧反应速度。
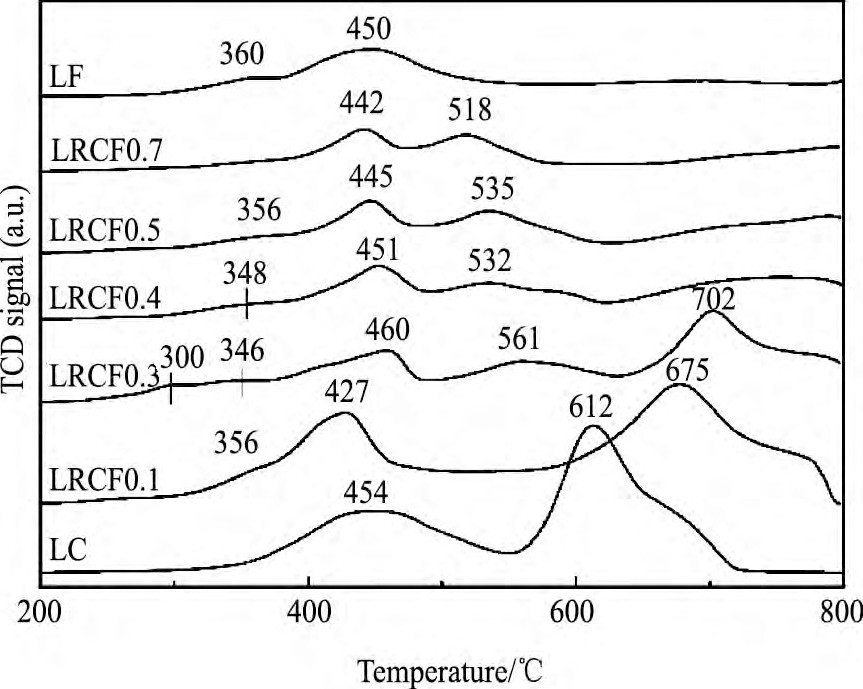
图2 La0.9Rb0.1Co1-xFexO3-δ催化剂H2-TPR谱图Fig.2 H2-TPR profiles of La0.9Rb0.1Co1-xFexO3-δcatalysts
2.4 XPS表征
掺杂催化剂和纯LC的XPS表征结果列于图3和表3中。
各样品的Co 2p XPS谱图见图3 (a) 。纯LC的Co 2p3/2结合能为779.5 e V, LRCF系列催化剂的结合能位于779.7e V左右。由于Co3+与Co2+结合能十分接近, 仅凭Co 2p3/2的结合能很难准确判断Co的价态, 于是参考2p自旋轨道分裂能 (ΔE) 进行分析。据文献报道, CO2O3的ΔE为15.0 e V[13], Co3O4的ΔE为15.2 e V[14]。由表3可知, 纯LC的自旋轨道分裂能为15.0 e V, 主要归属于Co3+, 这符合其钙钛矿结构的要求。Co, Fe共掺杂样品中, 在790.0 e V左右的伴峰证明了Co3+的存在, 但Co离子分裂轨道能有所升高, 为15.2 e V左右, 说明掺杂样品中Co可能主要以+2和+3混合价态存在。这可能是由于Fe的电负性低于Co, 当Fe引入后, O更倾向与从Fe处得电子, 从而使部分Fe物种的化学价态升高, 部分Co以Co2+形式存在, 以维持钙钛矿结构的电中性。表3中列出的Fe 2p3/2的结合能随Co含量的增加而有所升高也证实了这一点。结合图2中H2-TPR的结果, 可认为Fe, Co共掺杂导致了二者的化学状态发生了变化, 从而表现出共还原的行为。
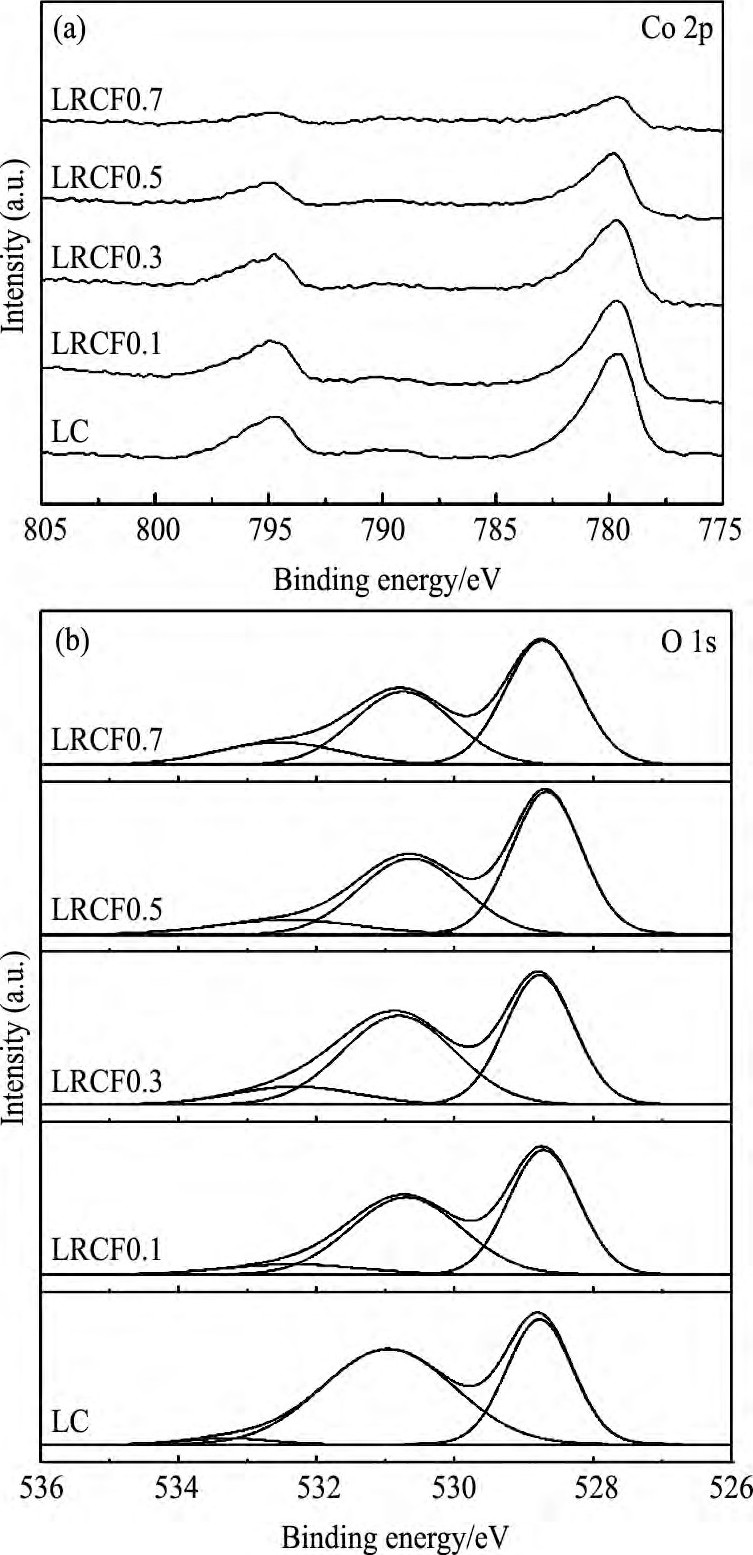
图3 La0.9Rb0.1Co1-xFexO3-δ (x=0.1, 0.3, 0.5, 0.7) 催化剂Co 2p及O 1s图谱Fig.3 XPS spectra for Co 2p (a) and O 1s (b) of La0.9Rb0.1Co1-xFexO3-δ (x=0.1, 0.3, 0.5, 0.7) catalysts
表3 XPS统计数据Table 3 Statistics of XPS survey (e V) 下载原图
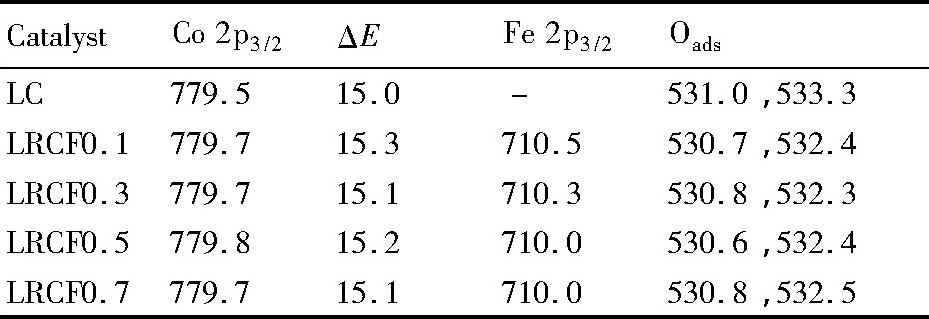
表3 XPS统计数据Table 3 Statistics of XPS survey (e V)
图3 (b) 列出了不同催化剂上的O 1s XPS谱图。由图3可见, 氧物种主要有3个峰:在低结合能, 约528.7 e V处的O 1s峰归属于晶格氧Olat (O2-) [15], 530.7 e V左右的峰主要是吸附在氧空穴中的化学吸附氧Oads (O-及过氧物种 (O22-) , 羟基 (OH-) 等[16,17]) , 高结合能532.4 e V处较弱的宽峰则主要归属于一些表面的弱化学吸附氧如碳酸根 (CO32-) 等[18]。在所有掺杂催化剂之中, LRCF0.3具有最高的Oads/Olat比例。结合表1结果, LRCF0.3催化剂的碳烟燃烧的T10最低。因此, 较高含量的吸附氧可能有利于碳烟燃烧反应的进行。
2.5 NOx-TPD表征
从表1中数据还可观察到掺杂催化剂具有一定的NOx消除能力, 其中LRCF0.4在381℃时具有最大的NOx转化率, 达到36.4%。
NOx浓度显著下降也可能是由于NOx在催化剂上发生吸附和储存所致, 因此, 利用NOx-TPD研究了催化剂储放NOx的能力, 列于图4及表4中。各催化剂在300~600℃处出现明显的NO脱附, 在150~300℃时检测到NO2的脱附, 且NO2的脱附量显著低于NO。据NOx-TPD结果计算的NOx储存能力 (NSC) 计算结果见表4。从中可以看出, 催化剂的NSC随着Fe含量的升高, 呈“火山型”趋势变化, 其中, LRCF0.4催化剂的NSC最大, 可达到411.1μmol・g-1, 这与其具有最高的NOx消除活性相对应。一般认为, 较高的NSC意味着在催化剂表面有更多的硝酸盐或亚硝酸盐物种, 而该 (亚) 硝酸盐物种可在一定的温度范围内与碳烟进行反应, 从而在提高碳烟燃烧性能的同时, 也可促进NOx的消除。对比表1可发现, 整体表现为催化剂的NSC越高, NOx消除性能也越高, 但二者之间并不存在直接的对应关系, 这说明NOx在催化剂上的消除并不仅取决于NOx的吸附与储存。因此进一步分析了LRCF0.4催化剂上反应过程中NO2, NOx浓度及CO2产率之间的关系, 结果见图5。从中可以看出, 当反应温度达到300℃时, 碳烟开始起燃, 且随着反应温度的升高, 碳烟燃烧速率快速增加, 所生成的CO2也随之迅速增多。与此同时, NOx的浓度出现了明显的降低。对于NO氧化而言, 所生成NO2的浓度随温度的升高而逐渐增大至最高, 随后受热力学限制, NO2的浓度逐渐降低。但图5中的结果表明, 在碳烟燃烧的温度区间, 即300~380℃的范围内, NO2的浓度却随着温度的升高逐渐下降。因此, 认为NO氧化生成的NO2与碳烟反应, 是导致NOx浓度降低的主要原因。同时, 利用红外分析了尾气中可能副产物N2O的浓度, 发现N2O的浓度最高时不超过3×10-6, 可忽略不计。因此, 认为在反应过程中NOx浓度的降低是NO2与碳烟反应生成N2所致。
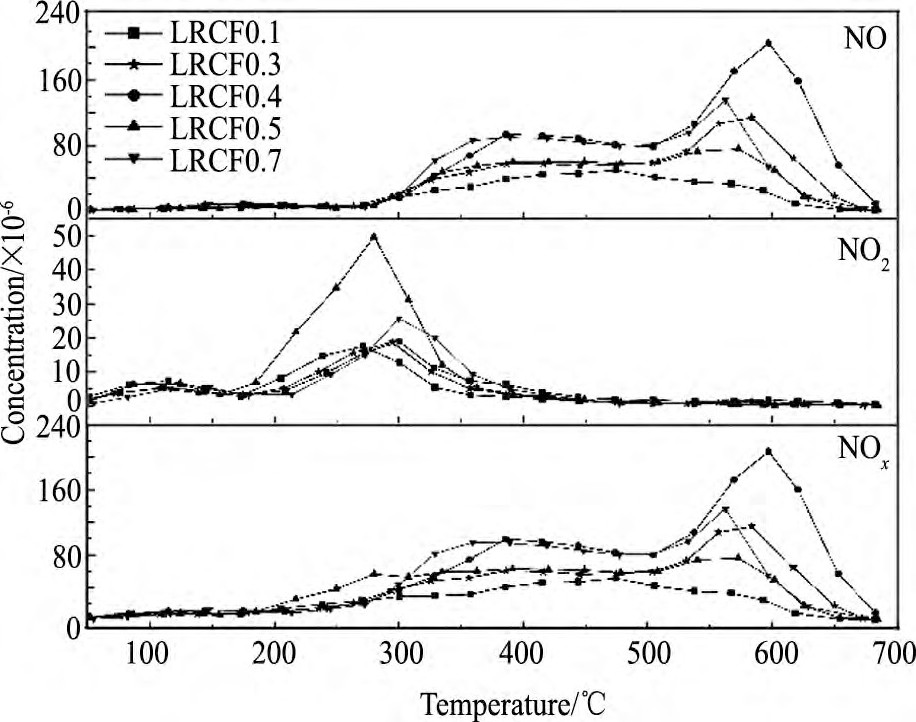
图4 LRCF系列催化剂NOx-TPD谱图Fig.4 NOx-TPD profiles of LRCF catalysts
表4 La0.9Rb0.1Co1-xFexO3-δ催化剂的NOx储存能力Table 4 NOxstorage capacity (NSC) of La0.9Rb0.1Co1-x FexO3-δcatalysts (μmol・g-1) 下载原图
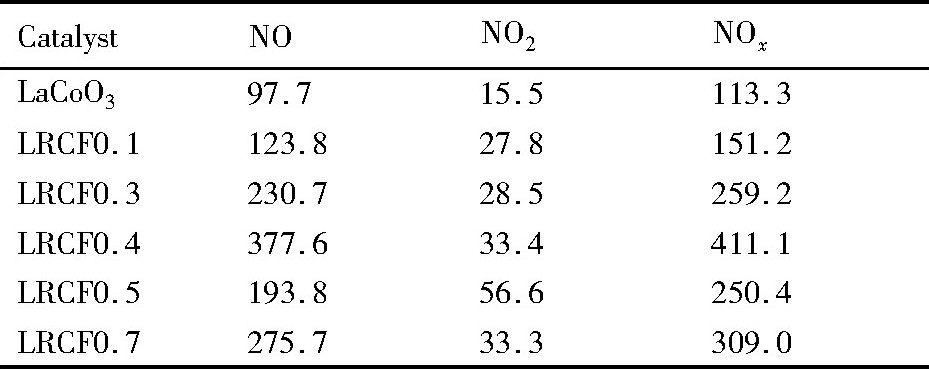
表4 La0.9Rb0.1Co1-xFexO3-δ催化剂的NOx储存能力Table 4 NOxstorage capacity (NSC) of La0.9Rb0.1Co1-x FexO3-δcatalysts (μmol・g-1)
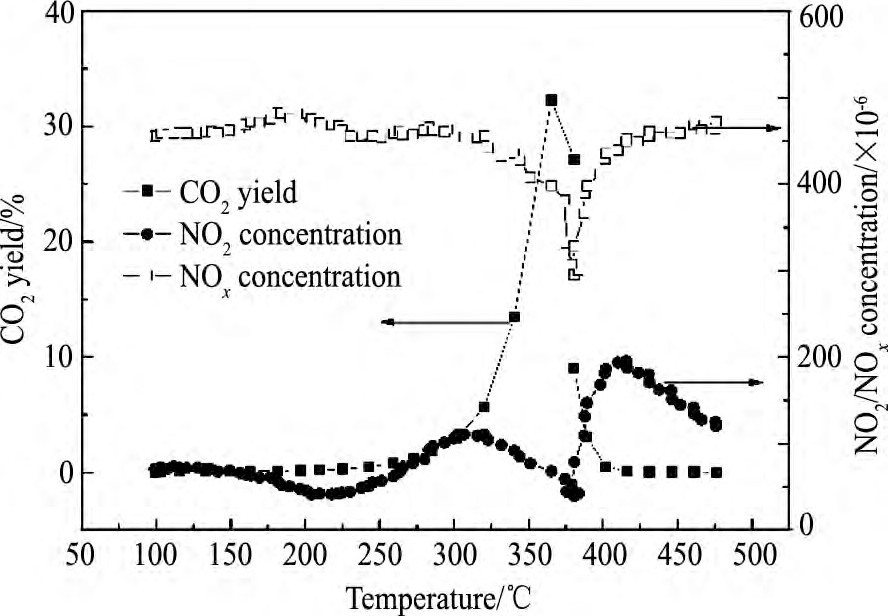
图5 LRCF0.4催化剂反应过程中CO2产率和NOx, NO2浓度随温度的变化曲线Fig.5 Profiles of CO2yield and NOx, NO2concentrations over LRCF0.4 catalyst during soot oxidation
由于碳烟燃烧殆尽, 但反应温度超过380℃后, CO2产率快速降低, NOx浓度也逐渐回复到原先水平。
3 结论
利用溶胶凝胶法制备了La0.9Rb0.1Co1-xFexO3-δ (x=0.1~0.8) 系列催化剂, 对其催化NOx辅助碳烟燃烧性能进行了考察, 并对催化剂结构进行了表征, 得到结论如下:
1.所制备的催化剂均为钙钛矿结构, 掺杂元素可进入钙钛矿的晶格, 并随Fe含量的增加, 其结构从La Co O3逐渐过渡到La Fe O3晶型, 结晶度先减弱再增强。
2.对于La0.9Rb0.1Co1-xFexO3-δ (x=0.1~0.8) 系列催化剂, Rb的引入可改善催化剂与碳烟之间的接触状况, 同时Co, Fe共掺杂还改变了Co, Fe的化学状态, 并产生了更多的结构缺陷, 加快了氧的吸附活化, 从而使其表现出较纯La Co O3和La Fe O3更高的碳烟活性和燃烧速度。
3.在NOx辅助碳烟燃烧过程中, NOx的消除能力除了与催化剂上NOx储存能力相关外, 还取决于NO氧化所生成的NO2与碳烟之间的反应。产物分析结果表明, 所生成的NO2可与碳烟反应生成N2, 其中LRCF0.4催化剂具有最高的NOx消除能力, 在381℃时达到36.4%。
参考文献
[1] Liu F D, Shan W P, Pan D W, Li T Y, He H.Selective catalytic reduction of NOxby NH3for heavy-duty diesel vehicles[J].Chinese Journal of Catalysis, 2014, 35 (9) :1438.
[2] Granger P, Parvulescu V I.Catalytic NOxabatement systems for mobile sources:from three-way to lean Burn after-treatment technologies[J].Chemical Reviews, 2011, 111:3155.
[3] Liu Z M, Woo S I.Recent advances in catalytic DeNOxscience and technology[J].Catalysis Reviews:Science and Engineering, 2006, 48 (1) :43.
[4] Yoshida K, Makino S, Sumiya S, Muramatsu G.Simultaneous reduction of NOxand particulate emissions from diesel engine exhaust[R].Society of Automotive Engineers, 1989, 892046.
[5] Nejar N, García-Cortés J M, Salinas-Martínez de Lecea C, Illán-Gómez M J.Bimetallic catalysts for the simultaneous removal of NOxand soot from diesel engine exhaust:a preliminary study using intrinsic catalysts[J].Catalysis Communications.2005, 6 (4) :263.
[6] Matarrese R, Morandi S, Castoldi L, Villa P, Lietti L.Removal of NOxand soot over Ce/Zr/K/Me (Me=Fe, Pt, Ru, Au) oxide catalysts[J].Applied Catalysis B:Environmental, 2017, 201:318.
[7] Atribak I, Suchbasanez I, Buenolopez A, Garcia A.Comparison of the catalytic activity of MO2 (M=Ti, Zr, Ce) for soot oxidation under NOx/O2[J].Journal of Catalysis, 2007, 250 (1) :75.
[8] Teraoka Y, Nakano K, Shangguan W F, Kagawa S.Simultaneous catalytic removal of nitrogen oxides and diesel soot particulate over perovskite-related oxides[J].Catalysis Today, 1996, 27 (1) :107.
[9] Bin F, Song C, LüG, Song J, Gong C, Huang Q.La1-xKxCo O3and La Co1-yFeyO3perovskite oxides:preparation, characterization, and catalytic performance in the simultaneous removal of NOxand diesel soot[J].Industrial&Engineering Chemistry Research, 2011, 50 (11) :6660.
[10] Fino D, Russo N, Saracco G, Specchia V.Catalytic removal of NOxand diesel soot over nanostructured spinel-type oxides[J].Journal of Catalysis, 2006, 242 (1) :38.
[11] Fang S, Wang L, Sun Z, Feng N, Shen C, Lin P, Wan H, Guan G.Catalytic removal of diesel soot particulates over K and Mg substituted La1-xKxCo1-yMgyO3perovskite oxides[J].Catalysis Communications, 2014, 49:15.
[12] Wei Y C, Zhao Z, Jiao J Q, Liu J, Duan A J, Jiang G Y.Facile synthesis of three-dimensionally ordered macroporous La Fe O3-supported gold nanoparticle catalysts with high catalytic activity and stability for soot combustion[J].Catalysis Today, 2015, 245:37.
[13] Ichimura K, Inoue Y, Yasumori I.Hydrogenation and hydrogenolysis of hydrocarbons on perovskite oxides[J].Catalysis Reviews, 1992, 34 (4) :301.
[14] Cesar D V, Perez C A, Schmal M, Salim V M M.Quantitative XPS analysis of silica-supported Cu-Co oxides[J].Applied Surface Science, 2000, 157 (3) :159.
[15] Imamura M, Massubayashi N, Shimada H.Catalytically active oxygen species in La1-xSrxCo O3-δstudied by XPS and XAFS spectroscopy[J].Journal of Physical Chemistry B, 2000, 104 (31) :7348.
[16] Wang H, Zhao Z, Liang P, Xu C, Duan A, Jiang G, Xu J, Liu J.Highly active La1-xKxCo O3perovskitetype complex oxide catalysts for the simultaneous removal of diesel soot and nitrogen oxides under loose contact conditions[J].Catalysis Letters, 2008, 124 (1-2) :91.
[17] O'Connell M, Norman A, Huttermann C.Catalytic oxidation over lanthanum-transition metal perovskite materials[J].Catalysis Today, 1999, 47 (1) :123.
[18] Zou G C, Yao X, Wang S J, Chen M X, Shangguan W F.The synergistic effect in Co-Ce oxides for catalytic oxidation of diesel soot[J].Catalysis Science&Technology, 2015, 5 (2) :1084.