�ȼ���ά���ƶ�ϸ�����Լ���������ܵ�Ӱ��
��Դ�ڿ���ϡ�н���2018���11��
�������ߣ����� �½��� ���
����ҳ�룺1199 - 1209
�ؼ��ʣ��ȼ���ά����;����ѱ��;ʵʱӫ�ⶨ��PCR����;��������;
ժ Ҫ���ȼ���ά���ƣ�CMC-Na����Ϊһ������ճ���,�ڵ�Ʒλ��ʯ����ѽ�������DZ�ڵ�Ӧ�ü�ֵ����Ϊǰ���о�����,��Ҫ������CMC-Na��ϸ���������Լ���������ܵ�Ӱ�졣���ȿ�����CMC-NaŨ�ȣ�0��10 g��L-1����ϸ����������5%��30%������ʼpHֵ��1. 2��2. 4�����¶ȣ�15��45�棩��Fe2+Ũ�ȣ�3��9 g��L-1�������ض�ϸ���������Ե�Ӱ��;ͨ����ѱ������,ʹϸ��������CMC-NaŨ�ȴ�4 g��L-1�ﵽ��10 g��L-1������,����ʵʱӫ�ⶨ��PCR����������CMC-NaŨ��Ϊ0��10 g��L-1�ľ�Һ������ϸ����Ⱥ�ṹ����,���������Һ�о�����Acidithiobacillus sp.,Leptopirillum sp.,Ferroplasma sp. 3��ϸ��,����Acidithiobacillus sp.��Ϊ���ƾ���;���ͨ����������L9��34��������CMC-NaŨ�ȣ�2��10 g��L-1����ϸ����������10%��30%������ʼp Hֵ��1. 2��2. 4������Ũ�ȣ�2%��5%�������ضԵ�Ʒλ��ʯ�������ʱ�����ʵ�Ӱ��,�ó�������Ӱ�������˳��Ϊ:CMC-NaŨ��>ϸ��������>��ʼp Hֵ>��Ũ�ȡ�
������ʱ��: 2017-03-07 17:42
ϡ�н��� 2018,42(11),1199-1209 DOI:10.13373/j.cnki.cjrm.XY16090022
���� �½��� ���
������ɫ�����о���Ժ����ұ����ҹ���ʵ����
�ȼ���ά���� (CMC-Na) ��Ϊһ������ճ���, �ڵ�Ʒλ��ʯ����ѽ�������DZ�ڵ�Ӧ�ü�ֵ����Ϊǰ���о�����, ��Ҫ������CMC-Na��ϸ���������Լ���������ܵ�Ӱ�졣���ȿ�����CMC-NaŨ�� (0��10 g��L-1) ��ϸ�������� (5%��30%) ����ʼpHֵ (1. 2��2. 4) ���¶� (15��45��) ��Fe2+Ũ�� (3��9 g��L-1) �����ض�ϸ���������Ե�Ӱ��;ͨ����ѱ������, ʹϸ��������CMC-NaŨ�ȴ�4 g��L-1�ﵽ��10 g��L-1������, ����ʵʱӫ�ⶨ��PCR����������CMC-NaŨ��Ϊ0��10 g��L-1�ľ�Һ������ϸ����Ⱥ�ṹ����, ���������Һ�о�����Acidithiobacillus sp., Leptopirillum sp., Ferroplasma sp. 3��ϸ��, ����Acidithiobacillus sp.��Ϊ���ƾ���;���ͨ����������L9 (34) ������CMC-NaŨ�� (2��10 g��L-1) ��ϸ�������� (10%��30%) ����ʼp Hֵ (1. 2��2. 4) ����Ũ�� (2%��5%) �����ضԵ�Ʒλ��ʯ�������ʱ�����ʵ�Ӱ��, �ó�������Ӱ�������˳��Ϊ:CMC-NaŨ��>ϸ��������>��ʼp Hֵ>��Ũ�ȡ�
�ȼ���ά����;����ѱ��;ʵʱӫ�ⶨ��PCR����;��������;
��ͼ����ţ� TF18
����飺���� (1990-) , ��, ������ˮ��, ˶ʿ�о���, �о�����:����ұ��;E-mail:1056853111@qq.com;;*�½���, ���ڼ�������ʦ;�绰:010-82241313;E-mail:kang3412@126.com;
�ո����ڣ�2016-09-18
����������Ȼ��ѧ������Ŀ (51574036) ����;
Luo Yi Wen Jiankang Wu Biao
National Engineering Laboratory of Biohydrometallurgy, General Research Institute for Nonferrous Metals, Beijing
Abstract��
As an agglomeration binder, sodium carboxymethyl cellulose ( CMC-Na) has a potential application prospect in the lowgrade oreheap bioleaching process. The effect of CMC-Na on the oxidation activity and leaching properties of bacteria were mainly studied. Firstly, the affecting parameters, such as CMC-Na concentration ( 0 �� 10 g��L-1) , inoculation amount of bacteria ( 5%�� 30%) , initial p H value ( 1. 2 �� 2. 4) , reaction temperature ( 15 �� 45 ��) and Fe2 +concentration ( 3 �� 9 g��L-1) were systemically investigated. Through a gradual domestication of bacteria, itsresistant for CMC-Na concentration was improved obviously from 4 to 10 g��L-1.And then, the real-time fluorescence quantitative PCR technology was employed to identify the community structure of cultured bacterial solution with CMC-Na 0 �� 10 g��L-1. The analysis results demonstrated that the main compositions of bacteria in these solutions were Acidithiobacillus sp., Leptopirillum sp. and Ferroplasma sp. and the Acidithiobacillus sp. was the dominant bacteria. Finally, the influence of CMC-Na concentration ( 2 �� 10 g��L-1) , inoculation amount of bacteria ( 10%�� 30%) , initial p H value ( 1. 2 �� 2. 4) and pulp density ( 2% �� 5%) on the leaching rate of low-grade ore bioleaching were investigated by orthogonal test L9 ( 34) , and the experimental results revealed that the rank of influence factors was: CMC-Na concentration > inoculation amount of bacteria > initial p H value > pulp density.
Keyword��
sodium carboxymethyl cellulose; domestication; FQ-PCR; orthogonal experiment;
Received�� 2016-09-18
���Ÿ�Ʒλ���״�����ʯ��Դ�IJ��ϼ���, ͬʱ�����Դ����ƶ�������Լ�����ѹ�����վ���
��ʯ�ڿ��ɺ���������в��ɱ������������ķۿ��ۿ�Ŀ�ʯʵ�ʶѽ�������, ��������ʱ���ڴ�ϸ��������ƫ����������ʱ�����ϸ�������������Һ����Ǩ�ƶ�����ѡ�Ca, Mg, Al�ȼ������������ᷴӦ���¿�ѽṸ����������Һ��ͨ��ͨ��, ���յ��¿�ѱ����ˮ���γɹ���, �ѽ����Բ��Լ��м۽����Ľ����ʵ�
ѡ����ʵ�ճ��������������ɹ��Ĺؼ�����֮һ, ѡ���ճ���Ӧ����
�ȼ���ά���� (CMC-Na) ���ж��ص�ճ���ԡ������ԡ������Ժ�ˮ�ֱ����Ե�����, ���㷺Ӧ����ʳƷ��ҽҩ����ױƷ��Ϳ�ϡ����ᡢ��֯��ʯ�ͺ���ֽ����ҵ
1ʵ��
1.1����
ʵ�����õ�ͭ����Դ���½�ij��, ��ʯͨ�����顢ĥϸ��-74��m�����ں��������顣��ѧ������֪�ÿ�ʯ��Cu 0.77%, Fe 5.10%, S0.22%, CuΪ��Ҫ�м����, ��������û�л������õļ�ֵ��������ͭ���������, ��������ÿ�ʯ����ͭ�����ͭ����ռ�ı����ֱ�Ϊ65.97%, 31.43%��
ʵ�����õľ���ȡ�Ա�����ɫ�����о���Ժ����ұ����ҹ���ʵ����ijͭ���� (30��5) ������������Ľ���Һ��������������9 K������, ������������ (g��L-1) : (NH4) 2SO4, 3.0;K2HPO4, 0.5;KCl, 0.1;MgSO4��7H2O, 0.5;Ca (NO3) 2��2H2O, 0.01;FeSO4��7H2O, 44.22;����ˮ1000 ml��
ʵ�������ȼ���ά���� (CMC-Na) Ϊ��ɫ��ĩ״, ��ṹʽ��ͼ1��ʾ, ���Կ���, CMC-Na���ӽṹ�к��д����ļ��Ի���-OH��-COONa��
1.2����
1.2.1 CMC-Na��ϸ���������Ե�Ӱ��
������250 ml��ƿ�н���, ����CMC-NaŨ�ȡ���ʼpHֵ�����������¶ȡ�Fe2+Ũ�ȶ�ϸ���������Ե�Ӱ��, ����ָ��Ϊϸ����9 K��������Fe2+��������, Fe2+��������= (CFe2��+-CFe2��+) /CFe2��+��100%, CFe2��+, CFe2��+ΪFe2+��ʼ������Ũ�ȡ�
ͼ1 CMC-Na�ĽṹʽFig.1 Structural formula of CMC-Na
1.2.2 CMC-Na��ϸ������ͭ�����ʵ�Ӱ��
������250 ml��ƿ�н���, ҡ���¶�30�桢ת��150 r��min-1, ����10 d��������������L9 (34) , ��Ҫ����CMC-NaŨ�ȡ���ʼpHֵ������������Ũ�ȶ�ϸ������ʱͭ�����ʵ�Ӱ�졣
1.3����������
1.3.1 pHֵ��������ԭ��λ (ORP, oxidation reduction potential) �IJⶨ��������p Hֵ����Thermo Orion 3-Star��pH�ƽ��в���, ����1��1������Һ�����������ij�ʼpHֵ;������ԭ��λ����SUNTEX PC-350�͵�λ�ƽ��вⶨ��
1.3.2����Һ��Fe2+Ũ�ȵIJⶨFe2+Ũ�Ȳ����ظ���صζ����ⶨ, ����Ϊȡ1 ml�ı���Һ, ����10 ml�������� (�����Ϊ����������ȥ����ˮ=15��15��30) , ����3~4����������Ϊ0.5%�Ķ�������������Ϊָʾ��, ʹ�õζ���T=1.0���ظ������Һ���еζ�, ��Һ��ɫ����ɫ��Ϊ��ɫ, ��30 s�ڲ���ɫ, �����ظ������Һ����������������Һ�е�Fe2+��Ũ�ȡ�
1.3.3ϸ����Ⱥ�ṹ�ķ���ϸ������һ��ʱ���, ȡ����Һ200 ml���䶳ʽ�������Ļ���ת��11000 r��min-1������10 min, Ȼ����ȥ����ˮϴ��, ��ת��11000 r��min-1������5 min, ϴ��2~3�κ�, ��������Һ, ���ռ��ľ�����Powersoil�LDNA Isolation kit�Լ�����ȡDNA, Ȼ�����ʵʱӫ�ⶨ��PCR��������ϸ������Ⱥ�ṹ��
2���������
2.1ϸ���Ļ��ת������������
ʵ�����õľ���ȡ��ijͭ���� (30��5) ������������Ľ���Һ, �Խ���Һ�е�ϸ�����л��ת������3�Ρ��������������ں��������顣ϸ���ڻ��ת�ӡ���������������ÿ��ⶨ����Һ��pHֵ��ORP��Fe2+��������, �����ͼ2~4��ʾ��
��ͼ2���Կ���, ϸ���ڻ��������������, ORP��������ʱ����ӳ�һֱ���ߡ���ͼ3 (a) �п��Կ���, ϸ��3��ת������ʱpHֵ��ʱ������Ӿ����������Ӻ��½�������, ��������pHֵ����������ϸ�������������е�Fe2+Ϊ��Դ��������, ��Fe2+����ΪFe3+, �ù�����������H+, ����һ��ʱ���p Hֵ�½��������γɵ�Fe3+ˮ����������˻Ƽ���������, �ͷų�H+����ͼ3 (b) ���Կ���, ϸ��3��ת������ʱORP����ʱ������Ӷ�һֱ����, ORP����ת�Ӵ�������������Խ�졣��ͼ3 (c) �п��Կ���, ϸ��3��ת������ʱFe2+������������ʱ������Ӷ�����, ֱ��Fe2+����ȫ����������ת�Ӵ���������, ϸ����ȫ����Fe2+�����ʱ��Խ��, ��1��ת������ʱ, ϸ����ȫ����Fe2+��Ҫ100 h, ��2��ת������ʱ, ϸ����ȫ����Fe2+��Ҫ72 h, ��3��ת������ʱ, ϸ����ȫ����Fe2+��Ҫ56 h��3��ת������, ϸ��Fe2+�������Էֱ�Ϊ0.077, 0.100, 0.1317g��L-1��h-1, ����ڵ�1��ת������ʱ, ϸ��Fe2+�������Էֱ������29.87%, 71.04%����ͼ4���Կ���, ϸ��������������ORP��������ʱ����ӳ�һֱ����, ���ձ��ֽϸߵ�ORP (Լ650 m V) ��
2.2 CMC-Na��ϸ���������Ե�Ӱ������
ͼ2 ϸ���ʱp Hֵ��ORP��ʱ��ı仯����Fig.2 Curves of p H value and ORP changing with time during bacterial activation
ͼ3 ϸ��ת������������p Hֵ��ORP Fe2+��������ʱ��ı仯���� (1~3��ʾת�Ӵ���) Fig.3 Curves of p H value (a) and ORP (b) Fe2+oxided rate changing with time during bacterial transfer culture (1~3 representing transit times)
2.2.1 CMC-NaŨ�ȵ�Ӱ������
��������Ϊ������15%, �¶�30��, ת��150 r��min-1, pHֵ1.8, �ֱ����0, 2, 4, 6, 8, 10 g��L-1CMC-Na��CMC-NaŨ�ȶ�ϸ���������Ե�Ӱ����ͼ5��ʾ��
��ͼ5���Կ���, ϸ����Fe2+����������ʱ������Ӷ����ӡ���CMC-NaŨ�ȵ����Ӷ��½�������93.5 hʱCMC-NaŨ��Ϊ0, 2, 4, 6, 8, 10g��L-1ʱ, Fe2+�������ʷֱ�Ϊ59.21%, 38.37%, 33.72%, 10.47%, 10.47%, 12.79%���벻��CMC-Naʱϸ����Fe2+�������������, ��CMC-NaŨ�ȸ���4 g��L-1ʱ, ϸ����Fe2+�����������ܵ������Ե�����, ��CMC-NaŨ�ȵ���4 g��L-1ʱ, ϸ����Fe2+���������Ե��������ý�С, ���ȷ������������CMC-Na��Ũ��Ϊ4 g��L-1��
ͼ4 ��������ʱp Hֵ��ORP��ʱ��ı仯����Fig.4 Curves of p H value and ORP changing with time during bacterial expanding culture
ͼ5 CMC-NaŨ�ȶ�ϸ���������Ե�Ӱ��Fig.5Effect of CMC-Na concentration on oxidation activity of bacteria
2.2.2��ʼp Hֵ��Ӱ������
��������Ϊ������15%, �¶�30��, ҡ��ת��150 r��min-1, CMC-NaŨ��4 g��L-1, ��ʼpHֵ�ֱ�Ϊ1.2, 1.5, 1.8, 2.1, 2.4����ʼpHֵ��ϸ���������Ե�Ӱ����ͼ6��ʾ����ͼ6���Կ���, ϸ����Fe2+����������ʱ������Ӽӡ�������������ʼpHֵ�����Ӷ�����, pHֵΪ1.2��1.5ʱ, ϸ����Fe2+�������ʽϵ�, pHֵΪ1.8~2.4ʱ, ϸ����Fe2+���������Խϸ�, ��һ�����ϸ�������������������, �������õ�ϸ�������¾�Acidithiobacillus sp.Ϊ��, ����������pH��ΧΪ1.8~2.5�����ǵ�pHֵ����2ʱ, ϸ������Fe2+���ɵ�Fe3+�ᷢ��ˮ������γɻƼ���������Ӱ��ϸ��������, ��˺���������ѡ���������ij�ʼpHֵΪ1.8��
ͼ6 ��ʼp Hֵ��ϸ���������Ե�Ӱ��Fig.6 Effect of initial p H value on oxidation activity of bacteria
2.2.3ϸ����������Ӱ������
��������Ϊ��ʼpHֵ1.8, �¶�30��, ҡ��ת��150 r��min-1, CMC-NaŨ��4 g��L-1, ϸ���������ֱ�Ϊ5%, 10%, 15%, 20%, 25%, 30%��ϸ����������ϸ���������Ե�Ӱ����ͼ7��ʾ����ͼ7���Կ���, ϸ����Fe2+����������ʱ������Ӷ����ӡ����Ž����������Ӷ����ӡ�������Ϊ5%ʱFe2+�������ʵ�������������ʱFe2+�������ʡ�����96 hʱ������Ϊ5%, 10%, 15%, 20%, 25%, 30%ʱ, Fe2+�������ʷֱ�Ϊ46.51%, 80.90%, 83.90%, 89.53%, 97.70%, 98.88%, ������Ϊ25%��30%ʱ, ����Fe2+�������ʽ���1.18%������CMC-NaŨ�ȳ���һ��ֵ���ϸ���������������ý�ǿ, ������ӽ��������������ϸ����CMC-Na����������, ȷ����������ϸ���Ľ�����Ϊ25%��Ϊ���ʡ�
2.2.4�¶ȵ�Ӱ������
��������Ϊ������25%, ��ʼp Hֵ1.8, ҡ��ת��150 r��min-1, CMC-NaŨ��4 g��L-1, �¶ȷֱ�Ϊ15, 30, 45�档�¶ȶ�ϸ���������Ե�Ӱ����ͼ8��ʾ��
��ͼ8���Կ���, ϸ����Fe2+����������ʱ������Ӷ����ӡ��¶ȶ�ϸ������Fe2+���Ե�Ӱ��ϴ�, �ϸ��¶�45��ʱ, ϸ����Fe2+�������ʽϵ�;�¶�Ϊ15��30��ʱϸ����Fe2+�������ʽϸߡ�����68 hʱ, �¶�Ϊ15, 30, 45��ʱ, Fe2+�������ʷֱ�Ϊ97.67%, 98.82%, 13.95%, �¶�Ϊ30��ʱ, ϸ����Fe2+�����������, ��һ�����ϸ�������������������, �������õ�ϸ�������¾�Acidithiobacillus sp.Ϊ��, �����������¶ȷ�ΧΪ30~35�档���ȷ�����������¶�Ϊ30�档
ͼ7 ϸ����������ϸ���������Ե�Ӱ��Fig.7 Effect of bacterial inoculation amount onoxidation activ-ity of bacteria
ͼ8 �¶ȶ�ϸ���������Ե�Ӱ��Fig.8 Effect of temperature on oxidation activity of bacteria
2.2.5 Fe2+Ũ�ȵ�Ӱ������
��������Ϊ������25%, ��ʼp Hֵ1.8, �¶�30��, ҡ��ת��150 r��min-1, CMC-NaŨ��4 g��L-1, ��������Fe2+Ũ�ȷֱ�3.0, 4.5, 6.0, 7.5, 9.0 g��L-1, Fe2+Ũ�ȶ�ϸ���������Ե�Ӱ����ͼ9��ʾ��
��ͼ9���Կ���, ϸ����Fe2+����������ʱ������Ӷ����ӡ�����Fe2+Ũ�ȵ����Ӷ����ӡ�Fe2+Ũ�ȶ�ϸ������Fe2+���Ե�Ӱ���С, ����68 hʱFe2+Ũ��Ϊ3.0, 4.5, 6.0, 7.5, 9.0 g��L-1ʱ, Fe2+�������ʷֱ�Ϊ100%, 97.67%, 98.30%, 98.59%, 98.81%, Fe2+������������, ˵���������нϵ͵�Fe2+Ũ��Ҳ��������ϸ����������
2.3ϸ���Ը�Ũ��CMC-Na�����Ե�ѱ�����鼰��Ⱥ�ṹ�ķ���
ͼ9 Fe2+Ũ�ȶ�ϸ���������Ե�Ӱ��Fig.9 Effect of Fe2+concentration on oxidation activity of bac-teria
2.3.1ѱ������
ǰ��������������, ��CMC-NaŨ�ȳ���4 g��L-1ʱ, ϸ����Fe2+�����������ܵ������Ե����ơ�Ϊ�����ϸ���Ը�Ũ��CMC-Na��������, ��Ҫ���϶�ϸ������ѱ��������ϸ��ѱ�������ķ���Ϊ��ʼCMC-NaŨ��Ϊ4g��L-1, ת������3�κ�, �����CMC-Na��Ũ�Ȳ�����ת������, ֱ��CMC-Na��Ũ�ȴﵽ10g��L-1, ֹͣѱ����������������ΪװҺ��100 ml, ������25%, ��ʼp Hֵ1.8, �¶�30��, ҡ��ת��150 r��min-1, ѱ�����������в��ϸ����Fe2+����������ʱ��ı仯��ͼ10 (a) ~ (d) ��ʾ��
��ͼ10 (a) �п��Կ���, ��ʼ��4 g��L-1CMC-Naϸ��3��ת������ʱFe2+������������ʱ������Ӷ�����, ֱ��Fe2+����ȫ����������ת�Ӵ���������, ϸ����ȫ����Fe2+�����ʱ��Խ��, ��1��ת������ʱ, ϸ����ȫ����Fe2+��Ҫ72h, ��2��ת������ʱ, ϸ����ȫ����Fe2+��Ҫ67 h, ��3��ת������ʱ, ϸ����ȫ����Fe2+��Ҫ45 h��3��ת������, ϸ��Fe2+�������Էֱ�Ϊ0.1167, 0.1284, 0.1933 g��L-1��h-1, ����ڵ�1��ת������ʱ, ϸ��Fe2+�������Էֱ������10.03%, 65.64%�����CMC-Na��Ũ�Ƚ���ѱ��, ��ͼ10 (b) ���Կ���, ��CMC-Na�ĺ�������6 g��L-1ʱ, ϸ����Fe2+�����������ܵ������Ե�����, ��CMC-NaŨ�ȵ���6 g��L-1ʱ, ϸ����Fe2+���������Ե��������ý�С, ����51 hʱ, CMC-NaŨ��Ϊ4, 6, 8, 10 g��L-1, Fe2+�������ʷֱ�Ϊ85.06%, 68.24%, 11.49%, 11.24%���������CMC-Na��Ũ�Ƚ���ѱ��, ��ͼ10 (c) ���Կ���, ��CMC-Na��Ũ�ȸ���8 g��L-1ʱ, ϸ����Fe2+�����������ܵ����Ե�����, CMC-Na��Ũ�ȵ���8g��L-1ʱ, ϸ����Fe2+���������Ե��������ý�С, ����71 hʱ, CMC-NaŨ��Ϊ6, 8, 10, Fe2+�������ʷֱ�Ϊ57.95%, 47.67%, 13.95%���������CMC-Na��Ũ�Ƚ���ѱ��, ��ͼ10 (d) ���Կ���, CMC-NaŨ�ȴﵽ10 g��L-1ʱ, ϸ����Fe2+���������Ե���CMC-NaŨ��Ϊ8 g��L-1ʱϸ����Fe2+��������, ����46 hʱ, CMC-NaŨ��Ϊ8, 10 g��L-1, Fe2+�������ʷֱ�Ϊ98.85%, 97.73%, ��������1.12%���������ͨ��ѱ��������������ϸ���Ը�Ũ��CMC-Na��������, ʹϸ������CMC-Na��Ũ�ȴ�4 g��L-1�����10 g��L-1��
ͼ1 0 ϸ��ѱ��������Fe2+��������ʱ��仯����Fig.10 Curves of Fe2+oxided rate changing with time during bacterial domestication
(a) Bacterial transfer culture three times with CMC-Na concentration being 4 g��L-1 (1��3 representing transit time) ; (b) Bacterial domestication with CMC-Na concentration being 4, 6, 8, 10 g��L-1, respectively; (c) Bacterial domestication with CMC-Na concentration being 6, 8, 10 g��L-1, respectively; (d) Bacterial domestication with CMC-Na concentration being 8, 10 g��L-1, respectively
2.3.2ϸ������Ⱥ�ṹ����
���������ʵʱӫ�ⶨ��PCR������ԭʼ��Һ������4, 6, 8, 10 g��L-1CMC-Naѱ�������õ��ľ�Һ����ϸ����Ⱥ�ṹ�ķ���, ϸ��������������, ��Һ���ĺ��ռ��ľ������Լ���Powersoil�LDNA Isolation kit��ȡϸ����DNA, �ô��Լ�����ȡ��DNA���Ƚϸ�, ��ֱ�ӽ���PCR������ʵʱӫ�ⶨ��PCR��������Acidithiobacillus sp., Leptopirillum sp., Sulfobacillus sp., Ferroplasma sp.4���������������Ʒ��Ŀ�Ļ���, ��ػ���ı�������ͼ11 (a~d) ��ʾ, 4���������������Ŀ�Ļ���ʵʱӫ�ⶨ��PCR�����ͼ12 (a~d) ��ʾ��ͨ��Rotor-Gene6000 Series Software 1.7������4���������ı����߿��Լ������ƷDNA�и�Ŀ�Ļ���Ŀ�����, Ȼ��������Ӧ��ϸ��������, �����ͼ13 (a~c) ��ʾ��
ʵʱӫ�ⶨ��PCR�������, ֻ��3�����������������ɹ�, Acidithiobacillus sp., Leptopirillum sp., Ferroplasma sp.3��ϸ��, ����Acidithiobacillus sp.Ϊ��Ҫ�ľ���, ��ռ�ı����ߴ�99.81%, Leptopirillum sp.��Ferroplasma sp.������ռ�ı���֮�Ͳ���0.2%;���ֺ�4, 6, 8, 10 g��L-1CMC-Na�����ľ�Һ��Acidithiobacillus sp.��Ϊ��Ҫ�ľ���, ��ռ�ı����ֱ�Ϊ99.82%, 99.72%, 99.99%, 81.07%;��Һ�о���Leptopirillum sp.ϸ��, ��ռ�ı����ֱ�Ϊ0.08%, 0.01%, 0.01%, 17.26%;�����ں�6��10 g��L-1CMC-Na�����ľ�Һ�к��������Ĺž�Ferroplasma sp., ��ռ�ı����ֱ�Ϊ0.27%, 1.67%;��Һ�о�δ��Sulfobacillus sp., ��һ������ϸ���������Ļ����Լ�ʵ��ʱϸ��������������������صġ�Acidithiobacillus sp.���ڸ���������������������, �ܹ�����Fe2+����������������, �ܹ���pHֵ0.5~6.0���¶�15~35�淶Χ������
ͼ1 1 ʵʱӫ�ⶨ��PCR����4���������ı�����ͼFig.11 Sstandard curves of four desin primers in FQ-PCR test (CT standing for cycle threshold)
(a) Acidithiobacillus sp.; (b) Leptopirillum sp.; (c) Sulfobacillus sp.; (d) Ferroplasma sp.
ͼ1 2 ʵʱӫ�ⶨ��PCR���Fig.12 Results of FQ-PCR
(a) 0, 4 g��L-1CMC-Na; (b) 6 g��L-1CMC-Na; (c) 8 g��L-1CMC-Na; (d) 10 g��L-1CMC-Na
ͼ1 3 �������и�ϸ��:Acidithiobacillus sp., Leptopirillum sp., Ferroplasma sp.��ռ�ı���Fig.13 Percent of bacteria in medium
(a) Acidithiobacillus sp.; (b) Leptopirillum sp.; (c) Ferroplasma sp.
2.4 CMC-Na��ϸ������ʱͭ�����ʵ�Ӱ��
ǰ�������������, 9K��������CMC-NaŨ�ȳ���4 g��L-1���Ӱ��ϸ����Fe2+����������, ϸ�����Խ�Fe2+����ΪFe3+, Fe3+��Ϊ���������, ����ϸ���Ľ�������Ҳ���ܵ�Ӱ�졣��������������鿼��CMC-NaŨ�� (A) �������� (B) ����Ũ�� (C) ����ʼp Hֵ (D) 4�����ض�ϸ���������ܵ�Ӱ��, ÿ����������3��ˮƽ, ���ѡȡL9 (34) ��Ϊ�����������, ʵ�����ؼ�ˮƽ�������1��ʾ��������250 ml����ƿ�н���, ������30�桢ת��Ϊ150 r��min-1ҡ��������, ��������Ϊ10 d, ����������ⶨ����Һ��Cu2+��Ũ�Ȳ�����Һ��Cu�Ľ�����, ����������Ƽ����������2��ʾ, ��ø����������½���Һ��pHֵ��ORP��ʱ��ı仯��ͼ14 (a) ~ (b) ��ʾ����2��, K1, K2, K3�ֱ��ʾ����Ӧ�����¸�ˮƽ��Ӧ������ָ��ֵ֮��, k1, k2, k3�ֱ��ʾ����Ӧ�����¸�ˮƽ��Ӧ������ָ��ľ�ֵ, r��ʾ���صļ���, ��ӳ�˸��������õĴ�С, ��ֵԽ��, ��ζ�Ŷ�Ӧ���صIJ�ͬˮƽ������ָ������ɵIJ��ϴ�, ���ݼ���ֵ�Ĵ�С����ȷ�������ص�����˳��, ���Կ��������ض�ͭ�Ľ����ʵ�Ӱ���С˳��Ϊ:CMC-NaŨ��>������>��ʼp Hֵ>��Ũ��, ����CMC-NaŨ�ȶ�ͭ�����ʵ�Ӱ�����, һ����ǰ�������������CMC-NaŨ�ȳ���4 g��L-1ʱ, ϸ����Fe2+�����������ܵ������Ե�����, ��ϸ������Fe2+��Ϊ��Դ����, ��������ΪFe3+�ͷų����������������������뷱ֳ, Fe3+��Ϊ�������������, Fe3+�ò�����ֵIJ���, �������ӵĽ����ʱ�Ȼ���ܵ�Ӱ��, ��صĻ�ѧ����ʽ����:
��1 �����������ؼ�ˮƽ����Table 1Encoding of orthogonal experimental factors and levels ����ԭͼ

��1 �����������ؼ�ˮƽ����Table 1Encoding of orthogonal experimental factors and levels
��2 ����ʵ����Ƽ�ʵ����Table 2 Orthogonal experimental design and results ����ԭͼ
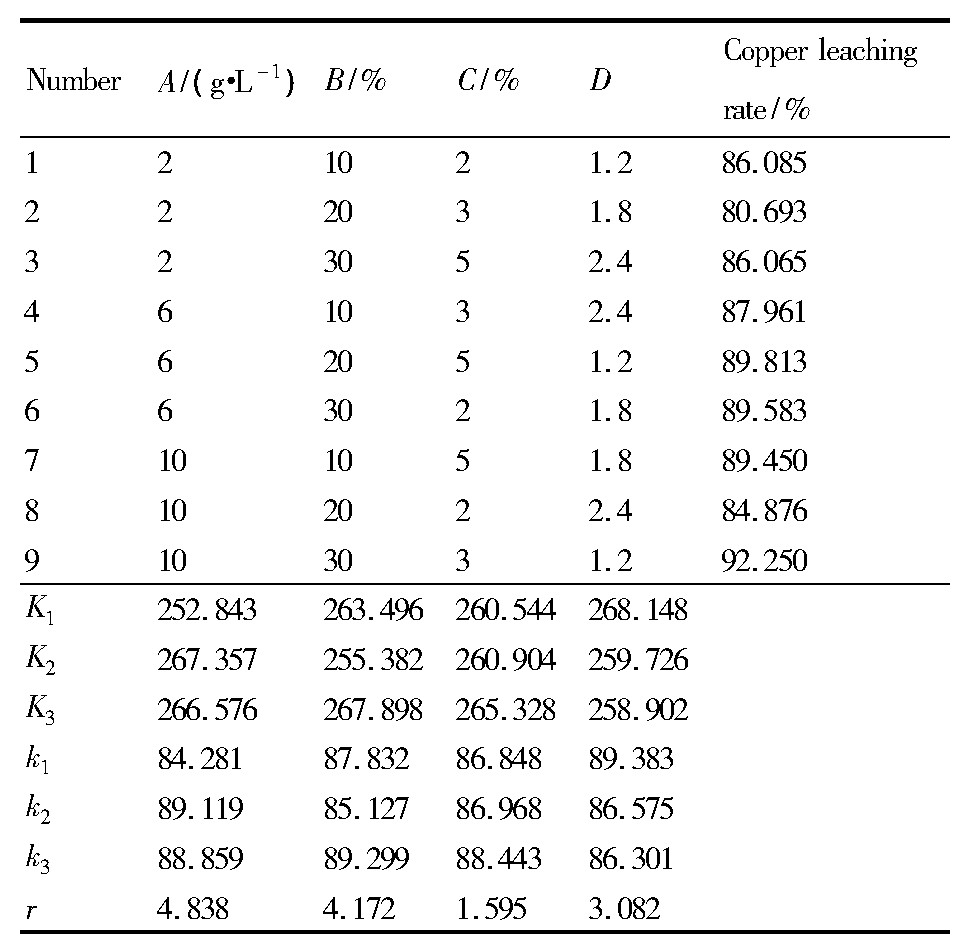
��2 ����ʵ����Ƽ�ʵ����Table 2 Orthogonal experimental design and results
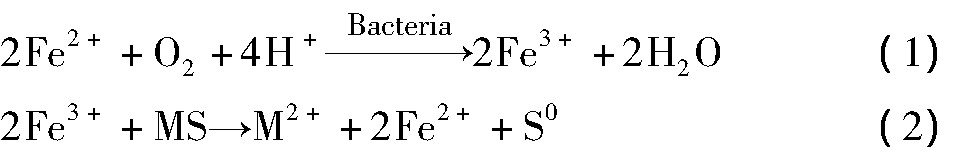
��һ����, CMC-Na�ṹ�к��д����ļ��Ի���-OH��-COONa, ������Ӳ���ԭ��, ��Ӳ����Ӳ������, ��������������, �����γ��ȶ�������, ��Fe3+����Ӳ��, Fe2+���ڽ�����, -OH, -COO-����Ӳ��, Fe3+��Fe2+����-OH, -COO-�γ������, ������Һ��Fe3+��Fe2+Ũ�ȵĽ���, ����Ӱ��ͭ��Ľ���Ч����
3����
1.ճ���CMC-Na��ϸ������Fe2+�����кܴ��Ӱ�졣�벻��CMC-Naʱϸ����Fe2+�������������, ��CMC-NaŨ�ȸ���4 g��L-1ʱ, ϸ����Fe2+�����������ܵ������Ե�����, ��CMC-NaŨ�ȵ���4 g��L-1ʱ, ϸ����Fe2+���������Ե��������ý�С��
ͼ1 4 ������������p Hֵ��ORP��ʱ��ı仯����Fig.14 Curves of p H value and ORP changing with time at different experimental condition
2.ͨ����ѱ������, ��������ϸ���Ը�Ũ��CMC-Na��������, ϸ������CMC-Na��Ũ�ȴ�4 g��L-1������10 g��L-1��
3.ͨ��ʵʱӫ�ⶨ��PCR��������ԭʼ��Һ������4, 6, 8, 10 g��L-1CMC-Na�����ľ�Һ�о�����Acidithiobacillus sp., Leptopirillum sp., Ferroplasma sp.3��ϸ��, ����Acidithiobacillus sp.��Ϊ���ƾ��֡�
4.ͨ����������L9 (34) �ó������ض�ͭ�����ʵ�Ӱ���С˳��Ϊ:CMC-NaŨ��>������>��ʼpHֵ>��Ũ��, ����CNC-NaŨ�ȶ�ͭ�����ʵ�Ӱ�����
�����

