���±�ţ�1004-0609(2014)06-1656-07
W(��)-V(��)-H 2O��ϵ�ٷ����������ѧ����
�ż���������ΰ
(���ϴ�ѧ ұ���뻷��ѧԺ����ɳ 410083)
ժ Ҫ��ͨ������ѧ�������25 ��ʱW(��)-V(��)-H2Oϵ�д��ڵ�������pH���١���Ũ�ȱ仯������ѧƽ��ͼ�����ܽ���仯���ɡ�ͨ������ѧ��������������Ѱ�ҵ��١����ڻ����Һ�д�����ʽ�ϵIJ��죬���ݴ�����ٷ�����ļ���·�ߡ����γɾۺ����ӵ�����ǿ���١���pHԼΪ8.5~9.0�������£���Һ�о��ֵķ��Ծۺ�������ʽ���ڣ�������ȫ��Ϊ�������ӣ����øò���ͨ�������ķ����ֶμ���ʵ�ֶ��ߵ���Ч���룻�����١���Ũ�Ⱦ��ϵ�ʱ����ϵ����pH�ϵ͵��������γ�VO2+���ӣ�����ʱ�ٵĴ�����ʽȫ��Ϊ�����ӣ������������������ȡ������������֬����ѡ���Եؽ�VO2+����Һ�з��롣
�ؼ��ʣ�W(��)-V(��)-H 2Oϵ���٣��������룻����ѧƽ�⣻�ٷ��Ӷ��������
��ͼ����ţ�TF801 �� �� ���ױ�־�룺A
Thermodynamic analysis for separation of tungsten and vanadium in W(��)-V(��)-H 2O system
ZHANG Jia-liang, ZHAO Zhong-wei
(School of Metallurgy and Environment, Central South University, Changsha 410083, China)
Abstract: The thermodynamic equilibrium diagrams were drawn for the distribution of species at different pH and concentrations in the W(��)-V(��)-H 2O system at 25 ��. The difference of existing forms between W and V in the mixed solution was found by the theoretical analysis, and accordingly the technical routes for separation of W and V were presented. The results show that the polymeric ability of VO43- is stronger than that of WO42-. At the pH range of 8.5-9.0, most of VO43- transform to polymeric anions, while almost all W ions still exist as the form of monomeric WO42-. This difference makes it possible that W and V can be separated efficiently by a proper method. In the solution with low concentration of W and V, VO2+ ions are formed under low pH conditions, while W ions exist as the form of anions. Consequently, VO2+ ions can be selectively separated by the cation extraction agent or exchange resin.
Key words: W(��)-V(��)-H 2O system; W; V; separation; thermodynamic equilibrium; tungstovanadate
�١���ͬ����ϡ�и��۵��������������������������ѧ���ʣ��ڹ��ú��������������������������Ҫ������[1-2]����ǰ���Ŵ�ͳ������Դ�IJ������ģ��Ӷ�����ĸ��ӿ���ԭ�ϺͶ�����Դ�л����١�����ռ�ı���������ߡ��ڿ�����Դ���棬�����ҹ����Ϻ��ݵȵز�����������оͰ����зḻ���١������м۽���[3]���ڶ�����Դ�У�����һЩ�Ͼɸֲġ��ϺϽ��Լ��ϴ������ٺͷ��ĺ������ϸ�[4]��Ȼ����Ϊ�˱�֤���ϵ�ʹ�����ܣ������ٷֱ�Ϊ�١���ұ���Ʒ�����ϸ���Ƶ�����Ԫ�ء������ҹ����ұ�GB/T 10116��2007�涨0��������鱗�Ʒ�з����������ٵ������Ȳ�����0.0010%[5]����ˣ��ٷ�����ȷ����Ϊ������Դ���ù����еĹؼ��������⡣
�����١�����������ѧ���ʽ�Ϊ���ƣ�������ʪ��ұ�������У���������Ҳ�������Ƶ���Ϊ�����Ӷ����¶��ߵķ��뼫Ϊ����[6-7]����������������ٷ�������о��������[8-11]��ͬʱ������ĿǰҲȱ���Ըû����ϵ����ѧ���ʵ������о�����ʹΪ������ķ��뷽���ڼ���·���Լ����ղ�����ѡ����Ҳ��������һ����äĿ�ԡ��ڴ˱����£��б�Ҫ���ȴ�����ѧ������ٷ������ϵ�����о���̽������Һ��ϵ��������ѧ���ʣ����ڴ�������Ϊ�ٷ��ķ����ṩ�����ļ���·�ߡ�
�١�����ˮ��Һ�еĴ�����̬ʮ�ָ��ӣ����˴��ڸ��ֵ����������⣬����Һ���ữ�Ĺ����У��������ӻ���ۺϳɸ���ͬ��������ӣ������������Ӧ�γɶ����ٷ��Ӷ�������ӡ�ͬʱ���������ӻ�������ҺŨ�ȵIJ�ͬ�������仯������Ϊ����ϵ�ĸ����ԣ���һ���̶������������Ϊֹ��������������ѧ���ʽ��б��������о��߿����˵�һ�١���ˮ��Һ��ϵ������ѧ��Ϊ������������ϵ�д���������pH��Ũ�ȱ仯������ѧƽ��ͼ[12-13]�����������о���ֻ������١�����һ��ϵ�����о����������˶���֮�������ã���û�п��������ٷ��Ӷ����������������Ӱ�졣������ʵ���ٷ������Һ�У��Ӷ�����ӵ��γ��Dz��ɱ���ģ�����������ٷ��������ż��䲻����Ӱ�죬������ݺ��ӡ�
���������ڶ����е�����ѧ���ݽ��й㷺���Ѽ���ɸѡ�����ϣ�ȫ�濼���ٷ������ϵ�д��ڵĸ��ֵ������ӡ�ͬ����������Լ��Ӷ�������ӣ���������25 ��ʱW(��)-V(��)-H 2Oϵ�д��ڵĸ�������pH���١���Ũ�ȱ仯������ѧƽ��ͼ��ͨ������ѧ����Ѱ�ҵ��١�������Һ�д�����ʽ�ϵIJ��죬���ݴ�������ٷ�������ܵļ���·�ߡ�
1 ����ѧ���ݼ�����
1.1 ����ѧ����
W(��)-V(��)-H 2Oϵ���漰��Ӧ�ķ���ʽ������ʾ��
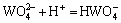 (1)
(1)
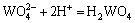 (2)
(2)
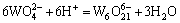 (3)
(3)
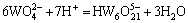 (4)
(4)
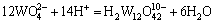 (5)
(5)
 (6)
(6)
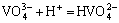 (7)
(7)
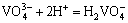 (8)
(8)
 (9)
(9)
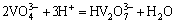 (10)
(10)
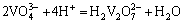 (11)
(11)
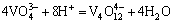 (12)
(12)
 (13)
(13)
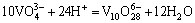 (14)
(14)
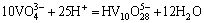 (15)
(15)
 (16)
(16)
 (17)
(17)
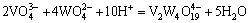 (18)
(18)
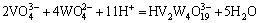 (19)
(19)
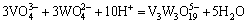 (20)
(20)
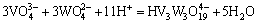 (21)
(21)
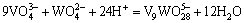 (22)
(22)
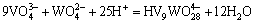 (23)
(23)
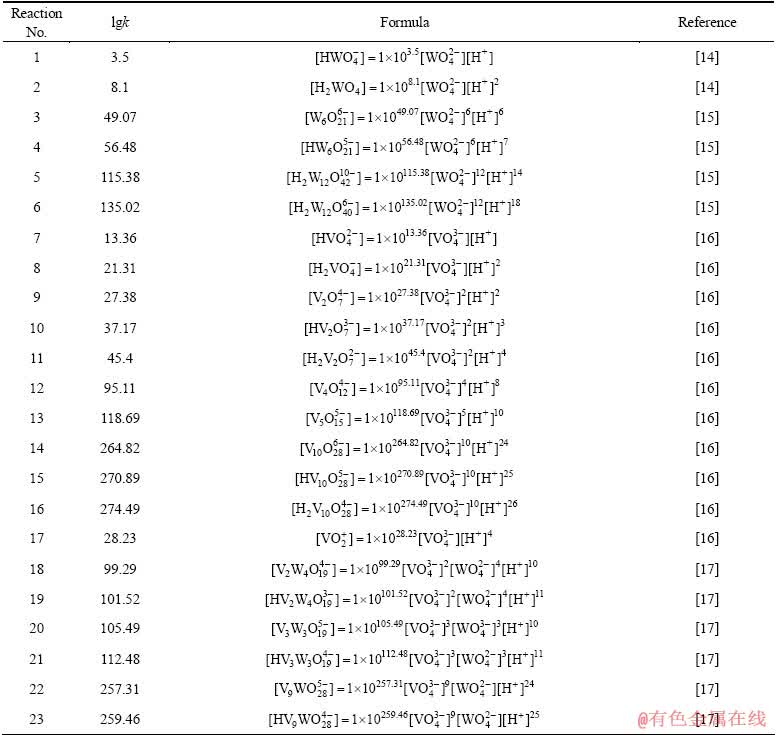
ͨ���������ף���������Ӧ������ѧ���ݽ����˹㷺���Ѽ���ɸѡ������ȷ���˸���Ӧ��ƽ�ⳣ��������ʽ�����1���С����ڸ�Ũ�ȵ������Ρ���������Һ��pH=1.0��pH=2.0�����ֱ���γ�H2WO4��V2O5�������������ӦŨ�ȵ���Һ��ϵ�У����������Ը���ϵ���γɳ�����pH���ϵķ�Χ��������ѧ��������������ȱ��������ʵĻ��ϵ�����ڼ�������о������ӵ�Ũ�ȴ����ȡ�
1.2 �������
��[W]T��[V]T�ֱ�Ϊ��Һ�������١����뷰����Ũ�ȣ���[ ]��Ϊ��Һ�и�������ֵ�Ũ�ȣ�����ͬʱƽ��������غ�ԭ������W(��)-V(��)-H 2O��ϵ������Եõ����·��̣�



 (24)
(24)
��1 �漰��Ӧ��ƽ�ⳣ��������ʽ(25 ��)
Table 1 Equilibrium constants and formulas of relevant reactions(25 ��)
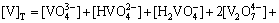
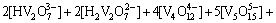
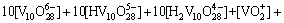

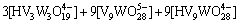 (25)
(25)
���ֱ������ϵ���١�������Ũ�ȼ���Һ��pHֵ��ͨ������ʽ(1)~(25)��⣬���ɵõ������ӵ�Ũ�ȡ��������Ӻ��١�����Ħ��Ũ�������١��ܷ�Ħ��Ũ�ȵı�ֵ��Ϊ������ռ���١��ܷ���Ħ���������ɼ�����ϵ�д��ڵ��������Ӻ����뺬����Ħ������֮�;�Ϊ1��
2 ���������
2.1 W(��)-V(��)-H 2Oϵ����ѧƽ�����
��W(��)-V(��)-H 2Oϵ�У���pHֵ0.5Ϊ������ɼ��������pHֵ����ϵ�д��ڵĸ����Ӻ��١�����Ħ��������ͼ1��ʾΪ��ͬ�١���Ũ���¸���Ҫ���ӵ�Ħ��������pH�Ĺ�ϵͼ��
����Һ��[W]T=[V]T=0.05 mol/Lʱ(��ͼ1(a))���������������pHԼΪ8.5ʱ��ʼ�ۺϣ��ۺϺ������̬������ҪΪ�Ӷ��������V2W4O194-����pHΪ3.5~7.0�ķ�Χ�ڣ�V2W4O194-���ٵ�Ħ��������90%���ϣ���pH��3.5ʱ��V2W4O194-�������ӻ�ת��ΪHV2W4O193-��������٣����ڻ����Һ�ữ�����еı仯�����Ϊ���ӡ�����ҺpHΪ10.0~12.0ʱ����Һ�еķ������Ե������ӵ�HVO42-����֮�⣬�����ڲ��־ۺϵĽ����������V2O74-�Լ�HV2O73- ����pH�����½�ʱ���������������ת��Ϊ��ԭ�������ߵ�ƫ���������V4O124-��V5O155-����pH=8.5ʱ����Һ�оۺϵķ�������ӵ�Ħ�������ӽ�95%�������pH���������Ե������Ӵ��ڵ��ٴ������ԵIJ��졣��������pH����Һ�еķ���������V2W4O194-��V9WO285-�Լ������������ӵ����ӻ���ʽ���ڡ�����ֵ��ע����ǣ�����Һ��Ƚϵ�ʱ����ϵ�л��γ�һ������VO2+�����ӣ���pH=1.0ʱ��VO2+��Ħ�������ﵽ50%���ϡ�
����Һ���������ܷ�Ũ�Ⱦ�������0.5 mol/Lʱ(��ͼ1(b))��WO42-��ʼ�ۺ��γ��Ӷ��������V2W4O194-��pH������9.0������pHΪ2.5~8.0�ķ�Χ�ڣ�V2W4O194-��Ϊ�ٵ���Ҫ������ʽ��������Һ�еķ���˵����pHΪ10.5~12.0ʱ��������Ҫ��HVO42-�ͽ����������V2O74-��HV2O73- ���ڣ�ֻ�����ڷ�Ũ�ȵ�����ʹ�ô�ʱ��ԭ�������ߵĽ��������������ϵ��ռ�����ơ�Ũ�ȵ�����ʹ��������ת��Ϊƫ��������ӵ���ʼpH������10.5����pH=9.0ʱ(��ϵ����ΪWO42-)����Һ�з���ͬ��������ӵ�Ħ�������ﵽ90%���ϡ�pH�������ͣ�����ͬ�������������ת��Ϊ�����Ӷ�������ӡ�
����ϵ������Ũ�ȸ����ܷ�Ũ��ʱ(��ͼ1(c))��WO42-��pHԼΪ9.0ʱ��ʼ�ۺϣ��γɾۺ����ӳ�����ǰ������Ũ�������¾����ڵ��Ӷ��������V2W4O194-֮�⣬������3��ͬ���������W6O216-��HW6O215-��H2W12O4210-����pH�������ͣ�������������ת��Ϊƫ���������H2W12O406-���Ӷ���� ����HV2W4O193- ���ڴ�Ũ�������£���Һ�еķ���pH=10.0ʱ����HVO42-�ͽ����������ת��Ϊƫ��������ӣ�������Ũ���ϴ������ƣ�ƫ���������ռ�����Ƶ�pH��ѹ����8.5~9.5�ķ�Χ�ڡ�����pH=9.0ʱ����ϵ�оۺϵķ�������ӵ�Ħ�������Ըߴ�75%���ϡ���pH����8.0ʱ����Һ�еķ�����ȫ�����Ӷ��������V2W4O194- ��HV2W4O193-���ڡ�
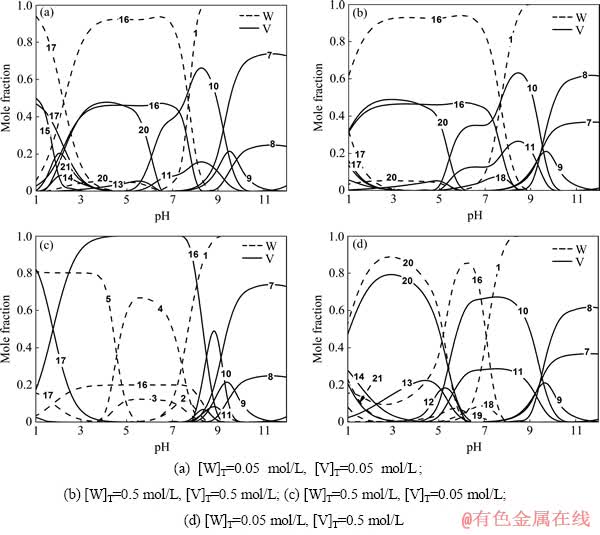
ͼ1 ��ͬ�ٷ�Ũ����W(��)-V(��)-H 2Oϵ��Ҫ�������Ӻ��١�����Ħ��������pH�Ĺ�ϵ(25 ��)
Fig. 1 Mole fraction of W and V in main ions as a function of pH at different concentrations of W[T] and V[T] in W(��)-V(��)-H 2O system (25 ��) (1��WO42-; 2��W6O216-; 3��HW6O215-; 4��H2W12O4210-; 5��H2W12O406-; 6��VO43-; 7��HVO42-; 8��V2O74-; 9��HV2O73-; 10��V4O124-; 11��V5O105-; 12��V10O286-; 13��HV10O285-; 14��H2V10O284-; 15��VO2+; 16��V2W4O194-; 17��HV2W4O193-; 18��V3W3O195-; 19��HV3W3O194-; 20��V9WO285-; 21��HV9WO284-)
������ϵ������Ũ�ȵ����ܷ�Ũ��ʱ(��ͼ1(d))������pH=8.5��ʼ�ۺϺ�����γ�V2W4O194-֮�⣬�����γ�������V3W3O195-��HV3W3O194-��֮������pH�Ľ��ͣ������Ӷ������������ת��Ϊ����ԭ�ӱȸ��ߵ�V9WO285-��HV9WO284-�����ڷ���˵��HVO42-�ͽ������������pH=10.5ʱ��ʼת��Ϊƫ��������ӣ�����7.0~9.5��pH�����ڣ�ƫ�������������ϵ�ж�ռ�ݾ��Ե����ơ���pH=8.5ʱ����ϵ�з���ͬ��������ӵ�Ħ�������ӽ�100%����pH��7.0�����½�ʱ����ϵ�������γɴ�����V9WO285-�Լ�һ������ʮ��ͬ���������(V10O286-��HV10O285-��HV10O284-)��
2.2 �ٷ�����·�ߵ����
����Ԫ�ط���Ĺؼ������ҵ�Ԫ��֮�������ϵIJ��죬֮���ٽ����ں����ķ����ֶμ���ʵ�ֶ��ߵ���Ч���롣��֮ǰ�������ģ���W(��)-V(��)-H 2O��ϵ�д������ӵ����Ϳɷ�Ϊ��������(�˴���VO2+Ҳ��������)��ͬ����������Լ��Ӷ�������ӡ���W(��)-V(��)-H 2O��ϵ����3�����͵����ӷֱ���ͣ��õ���ͬ�ٷ�Ũ���¸��������Ӻ��١�����Ħ��������pH�仯������ͼ����ͼ2��ʾ����ͼ2�п��Կ��������������Ӿۺϵ���ʼpH��Ҫ����Һ�е���Ũ���йأ���[W]T=0.5 mol/L���ۺϵ���ʼpHΪ9.0������[W]T=0.05 mol/Lʱ����ʼpH��Ϊ8.5���ۺ�֮����˸��ٵͷ���ϵ�⣬������Һ��ϵ���پ����Ӷ����������ʽ���ڣ�����W[T]=0.5 mol/L��V[T]=0.05 mol/L�ĸ��ٵͷ���Һ�У��������ɺ���Ħ������Ϊ20%���ҵ��Ӷ��������֮�⡣���⣬80%�ĺ���������Ϊ�ٵ�ͬ��������ӣ���������Ħ����������ֵ��pH��6.5�ķ�Χ�ڼ������ֲ��䣬����Ҫ����Ϊ��ʱ��Һ�еķ�����ȫ�����١���Ħ����Ϊ2���Ӷ�������Ӵ��ڡ�
������Һ�еķ���˵����pH=12.0ʱ�����ֵķ����Ծۺϵ�ͬ��������Ӵ���(��ҪΪ���۵Ľ����������)���ҷ�Ũ��Խ�ߣ��ۺ����ӵ�Ħ������Խ��������ữ�Ĺ����У����˷����ӽ�һ��ת��Ϊͬ��������ӡ��ܵ���˵����[W]T=0.5 mol/Lʱ������ͬ��������ӵ�Ħ��������pH=9.0ʱ�ﵽ�����[W]T=0.05 mol/Lʱ������pH=8.5ʱ�ﵽ�����ǡ��Ҳ������Ӧ��Һ���ٿ�ʼ�γɾۺ����ӵ�pHֵ���ڸ�pH�����£���Һ�о��ֵķ��Ծۺ�������ʽ���ڣ�������ȫ���Ե������Ӵ��ڣ��ɼ���ʱ�������ڴ�����ʽ�ϴ����Ų��죬ͬʱ��Ҳ�������γɾۺ����ӵ�����ǿ���ٵġ�
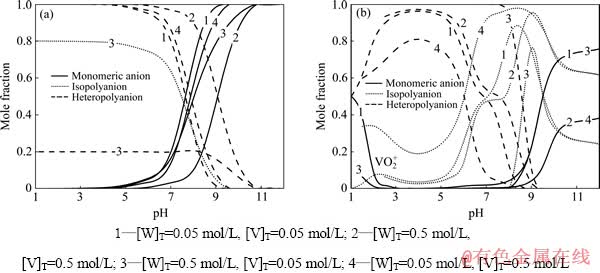
ͼ2 ��ͬ�ٷ�Ũ����W(��)-V(��)-H 2Oϵ�е������ӡ�ͬ��������ӡ��Ӷ������Ӻ��١�����Ħ��������pH�ı仯(25 ��)
Fig. 2 Mole fractions of W(a) and V(b) in monomeric anions, isopolyanions, heteropolyanions as function of pH at different concentrations of [W]T and [V]T in W(��)-V(��)-H2O system (25 ��)
����������pHʱ����Һ�з���ͬ��������ӵ�Ħ���������ͣ��Ӷ�������ӵ�Ħ�������������ߡ���pHΪ2.5~6.5�ķ�Χ�ڣ���Һ���д������ٷ��Ӷ���������γɣ�������ٷ��ķ�����Ȼ�Ǽ��䲻���ġ���ˣ��ڲ��ƻ���ϵ���Ӷ����ǰ���£���pH���������������ٷ�����Ч����ġ�������Һ���ٷ�Ũ�Ⱦ��ϵ͵�����£���ϵ������Ƚϵ�ʱ�γ�һ������VO2+���ӣ�����ʱ��ϵ���ٵĴ�����ʽ��ȫ��Ϊ�����ӣ���Ҳ���١�����ˮ��Һ�д�����ʽ�ϵ�����һ�����졣
�������϶�W(��)-V(��)-H 2Oϵ������ѧ�������ҵ��١����ڸ���ϵ�д�����ʽ�ϵ��������죬������Щ���죬������������ֿ��ܵ��ٷ�����ļ���·�ߣ�
1) �����ٷ��γɾۺ����������IJ���
��֮ǰ�������ģ����γɾۺ����ӵ�����ǿ���٣���pHԼΪ8.5~9.0ʱ����Һ�о��ֵķ��Ծۺ�������ʽ���ڣ�������ȫ���Ե���������ʽ���ڡ��ۺ������ڳ����ᾧ�����Լ���ijЩ���������������������Եȷ����뵥���������Žϴ�IJ��죬������ͨ����������ȡ�������ȷ�ʽ���ٷ����з��롣�Ը�����(Fe3+��Mn4+��Sn4+��)ˮ�������������������˵�������δ�ۺϵ�WO42-���ۺϷ��������(��ҪΪƫ���������V4O124-��V5O155-)��۸��ߣ��������ӵ�ˮ��������ʵ������һ�������Ե������ӽ��������������ۺϷ��������Ӧ���и�ǿ��������ͬʱ�ۺϷ�������ӵķ�ԭ��������֮����Ը�������ζ��ÿ������λ����������ķ���Ҳ��Ҫ�����ٵġ���������ԭ����Ԥ�ڲ��ø����ӵ�ˮ����������pHΪ8.5~9.0�������¿�ѡ���Ե����������Һ�еķ�������ʵ���ٷ�����Ч���롣
2) ���÷�����Һ�п��γ������ӵIJ���
����ѧ�������������١���Ũ�Ⱦ��ϵ�ʱ����Һ����pH�ϵ͵��������γ�һ������VO2+�����ӣ�����ʱ����������ȫ��Ϊ�����ӡ�������һ���죬������������ȡ������������֬����ѡ���Եؽ�VO2+����Һ�з��롣��ͬʱ��ͼ2 ��Ҳ���Կ�������pH��������ϵ������һ���ֵķ������Ӷ������������ʽ���ڣ�����Ʊ�Ҫ��ȡһ���Ĵ�ʩ�ƻ��Ӷ�������ӡ���ʱ�����ʵ�����Һ�м���һ������H2O2��EDTA����ʯ�������Լ����ٽ��Ӷ�������ӵĽ�ۣ��Ӷ������ٷ��ķ���Ч����
���˴���������������������ٷ�����ļ���·��֮�⣬����ѧ�������ɽ�һ�������������ķ������������Ż��������١�������Һ�еĴ�����ʽ��pH�ı仯��Ϊ���У�������˽��з����pHֵ�ķ�ΧҲ��Ϊ��խ�����Ҹ�pH��Χ���������١���Ũ�ȵIJ�ͬ�������ı䡣�����Ҫ�ڷ��벻ͬ����Һʱ������Һ��pH������Ӧ�ĵ������Ի�����ŵķ���Ч������ͳ��ֻ��ͨ������õ����˵ķ�������������ʵ����������Ȼ�Dz�����ʵ�ֵġ���ʱ����Ը���ϵ������ѧ��������ȫ���ֵĴ�������̽�������Է������������Ż����Ӷ�Ϊ�ٷ������ʵ���ṩ����ָ����
3 ����
1) ȫ�濼�����ٷ������ϵ�д��ڵĸ��ֵ������ӡ�ͬ����������Լ��Ӷ�������ӣ�ͨ������ѧ���㣬������25 ��ʱW(��)-V(��)-H 2Oϵ�д���������pH���ٷ�Ũ�ȱ仯������ѧƽ��ͼ�����ܽ�����仯���ɡ�
2) ���γɾۺ����ӵ�����ǿ���ٵģ���pHԼΪ8.5~9.0�������£���Һ�о��ֵķ��Ծۺ����ӵ���ʽ���ڣ�������ȫ���Ե���������ʽ���ڡ����øò��죬���ø�����ˮ�������������ȷ���Ԥ�ڿ�ʵ���ٷ�����Ч���롣
3) ����Һ���١���Ũ�Ⱦ��ϵ͵�����£���ϵ����pH�ϵ�ʱ�γ�VO2+���ӣ�����ʱ�ٵĴ�����ʽ��ȫ��Ϊ�����ӡ����ڸò��������������ȡ������������֬����ѡ���Եؽ�VO2+�ӻ����Һ�з��롣
4) ͨ��W(��)-V(��)-H 2O��ϵ������ѧ����������ٷ�����ļ���·�ߣ�ͬʱ���ɱ����ضԷ��벻ͬŨ����Һ��pH���������Ż����Ӷ�Ϊ�ٷ������ʵ���ṩ����ָ����
REFERENCES
[1] ����ΰ. ��ұ����������Ӧ��[M]. ����: �廪��ѧ������, 2013: 1-4.
ZHAO Zhong-wei. Tungsten metallurgy: Fundamentals and applications[M]. Beijing: Tsinghua University Press, 2013: 1-4.
[2] GUPTA C K, KRISHNAMURTHY N. Extractive metallurgy of vanadium[M]. Amsterdam: Elsevier Science Publishers, 1992: 2-7.
[3] ��˧��, ������, �����, ������. ������о���״����չ����[J]. �й���ҵ, 2013, 27(6): 8-12.
JIA Shuai-guang, CHEN Xing-yu, LIU Xu-heng, LI Yue-xing. Research status and development trends of Ni-Mo ore[J]. China Tungsten Industry, 2013, 27(6): 8-12.
[4] ������, ��̸��. ���ⷰұ��[M]. ����: ұ��ҵ������, 1985: 4-19.
LIAO Shi-ming, BO Tan-lun. Extractive metallurgy of vanadium[M]. Beijing: Metallurgical Industry Press, 1985: 4-19.
[5] GB/T 10116��2007. �������[S]. ����: ���������, 2007.
GB/T 10116��2007. Ammoniumparatungstate[S]. Beijing: China Standards Press, 2007.
[6] ����, ��, �� ��. ��ұ��ѧ[M]. ��ɳ: ���ϴ�ѧ������, 2010: 211-228.
LI Hong-gui, YANG Jian-gao, LI Kun. Tungsten metallurgy[M]. Changsha: Central South University Press, 2010: 211-228.
[7] ����־. ��ұ��[M]. ����: ұ��ҵ������, 2010: 65-66.
YANG Shou-zhi. Vanadium metallurgy[M]. Beijing: Metallurgical Industry Press, 2010: 65-66.
[8] �� ��, ���Ȩ. ���ӽ��������븻����������Һ�еķ�[J]. ϡ�н�����Ӳ�ʺϽ�, 2006, 34(3): 5-7.
SONG Fu, ZHU Bin-quan. Extraction of vanadium from sodium tungstate by ion exchange[J]. Rare Metals and Cemented Carbides, 2006, 34(3): 5-7.
[9] �� ��, ������, �ν���. �ӷ������ٽ�����Ʒ�л����ٺͷ�[J]. ��ұ, 2002, 11(1): 50-54.
LUO Lin, TOYOHISA F, OSAMU S. Recovery of tungsten and vanadium from tungsten scrap[J]. Mining & Metallurgy, 2002, 11(1): 50-54.
[10] LUO L, MIYAZAKI T, SHIBAYAMA A, YEN W, FUJITA T. A novel process for recovery of tungsten and vanadium from a leach solution of tungsten alloy scrap[J]. Minerals Engineering, 2003, 16(7): 665-670.
[11] LUO L, LIU K, SHIBAYAMA A, YEN W, FUJITA T, SHINDO O, KATAI A. Recovery of tungsten and vanadium from tungsten alloy scrap[J]. Hydrometallurgy, 2004, 72(1): 1-8.
[12] CRUYWAGEN J J. Protonation, oligomerization and condensation reactions of vanadate(��), molybdate(��) and tungstate(��)[J]. Advances in Inorganic Chemistry, 2000, 49: 127-182.
[13] NEKOVAR P, SCHROTTEROVA D. Extraction of V(��), Mo(��) and W(��) polynuclear species by primene JMT[J]. Chemical Engineering Journal, 2000, 79: 229-233.
[14] BAES C F, MESMER R E. The hydrolysis of cations[M]. New York: Wiley, 1976: 259.
[15] CRUYWAGEN J J, MERWE F J. Tungsten(��) equilibria: a potentiometric and calorimetric investigation[J]. Journal of the Chemical Society, Dalton Transactions, 1987(7): 1701-1705.
[16] ELVINGSON K, FRITZSCHE M, REHDER D, PETTERSON L. Speciation in vanadium bioinorganic systems. 1. A potentiometric and V-51 NMR-study of aqueous equilibria in the H+-vanadate(��)-L-alpha-alanyl-L-histidine system[J]. Acta Chemica Scandinavica, 1994, 48(11): 878-885.
[17] ANDERSSON I, HASTINGS J J, HOWARTH O W. Aqueous tungstovanadate equilibria[J]. Journal of the Chemical Society, Dalton Transactions, 1996(13): 2705-2711.
(�༭ ����)
������Ŀ��������Ȼ��ѧ�����ص���Ŀ(51334008)
�ո����ڣ�2014-01-05�������ڣ�2014-05-10
ͨ�����ߣ�����ΰ�����ڣ���ʿ���绰��0731-88830476��E-mail: zhaozw@csu.edu.cn