纳米磁性铁铝复合物的制备及其除氟性能
赵娜1, 2, 3,王云燕1, 2,杨卫春1, 2,尤翔宇1, 2,柴立元1, 2
(1. 中南大学 冶金与环境学院,湖南 长沙,410083;
2. 中南大学 国家重金属污染防治工程技术研究中心,湖南 长沙,410083;
3. 长沙有色冶金设计研究院,湖南 长沙,410011)
摘要:采用碱性共沉淀的方法制备载体纳米Fe3O4,并选用硫酸铝对其进行包覆改性制备除氟吸附剂,优化制备条件,考察制备得出的吸附剂对氟化物的去除效果,并采用透射电镜(TEM)、能谱(EDS)、X线衍射(XRD)、振动样品磁强计(VSM)等对吸附剂的性质进行表征。研究结果表明:吸附剂最优制备条件参数为Fe3O4与Al投加量摩尔比1:2,制备反应pH=5.0。最优条件下制备的除氟吸附剂即纳米磁性铁铝复合物,其比表面积为63.37 m2/g,平均粒径为15~20 nm,饱和磁化强度为15.63 A・m2/kg,零电荷点pHpzc为11.2。该吸附剂适用pH范围广,在pH为4.0~10.0范围内除氟率均在84%以上,在pH为7.0时的氟化物吸附等温线符合Langmuir等温模型,吸附容量可达48 mg/g。
关键词:氟离子;吸附;纳米磁性材料;铁铝复合物
中图分类号:TG146 文献标志码:A 文章编号:1672-7207(2014)01-0334-07
Preparation and application in fluoride removal of iron-aluminum composite magnetic nanoparticles
ZHAO Na1, 2, 3, WANG Yunyan1, 2, YANG Weichun1, 2, YOU Xiangyun1, 2, CHAI Liyuan1, 2
(1. School of Metallurgy and Environment, Central South University, Changsha 410083, China;
2. National Engineering Research Center for Pollution Control of Heavy Metal, Central South University,
Changsha 410083, China;
3. Changsha Nonferrous Metallurgy Engineering and Research Institute, Changsha 410011, China)
Abstract: The adsorbents for fluoride removal were prepared by coating magnetite nanoparticles with aluminum sulphate. The properties of the adsorbents were analyzed by transmission electron microscope (TEM), energy disperse spectroscopy (EDS), X-ray diffraction (XRD), vibrating sample magnetometer (VSM). The results show that the optimum preparation condition is as follows: molar ratio of Fe3O4 to Al being 1:2, and preparation pH being 5.0. The properties of the adsorbent prepared under the optimum condition are as follows: BET surface area being 63.37 m2/g, average particle size being 15-20 nm, pHpzc being 11.2 and saturation magnetization being 15.63 A・m2/kg. Moreover, this adsorbent can be applied in wide pH range (pH 4.0-10.0). Its removal efficiencies for fluoride can be reached above 84% with the initial fluoride concentration of 25 mg/L over the pH range 4.0-10.0. The adsorption isotherm of fluoride on Fe/Al composite magnetic nanoparticles can be well fitted with Langmuir model, and the maximum adsorption capacity of fluoride is 48 mg/g.
Key words: fluoride ions; adsorption; magnetic nanoparticles; iron-aluminum composite
氟广泛存在于自然水体中,适量的氟能防止龋齿的发生,但长期饮用高氟水,可导致氟斑牙和氟骨症。轻则引起牙齿变质,重则造成骨质硬化或骨质疏松,骨骼变形,甚至瘫痪[1]。在我国,大多数省市自治区都存在不同程度的地方性氟中毒,全国饮用水型地方氟病分布面积约220万km2,据统计,目前我国有7000多万人饮用高氟水[2]。我国生活饮用水卫生标准规定氟质量浓度不得超过1.0 mg/L[3]。目前针对含氟水的处理方法主要有吸附法和膜分离技术等[4-5]。吸附法凭借其成本低、效果好、操作简单、可塑性强等优势越来越受到人们的关注。其中以铝盐类吸附剂[6-7]和稀土元素[8-10]除氟的研究报道较多。研究表明:铝盐对F-具有较好的亲和力,或通过静电吸引与F-形成Al(OH)3-xFx将其吸附在表面,或通过键合形成Al-F络合物将F-从溶液中脱除。稀土元素具有较高的价态可提供轨道,属于硬酸;F-具有较高的电负性可提供电子,属于硬碱;根据硬酸硬碱理论[11],二者之间的键合较强。尽管如此,上述吸附剂仍存在易造成二次污染、或成本高、或固液难以分离等问题[10, 12]。近年来,纳米吸附剂的研究使得除氟技术有了更进一步的发展,纳米尺度的材料具有较高的比表面积,同时缩短了溶质的传播路径,大大提高了吸附剂的吸附容量和吸附速率[13];吸附剂本身具有的特殊磁性,使得通过外加磁场可容易的实现固液分离,克服了传统分离技术引起的滤料阻塞、吸附剂磨损、分离不彻底等问题。纳米磁性吸附剂展现出了优越的除氟性能,具有广阔的应用前景[14-16]。如Ma等[17]制备合成的磁性壳聚糖颗粒,吸附容量可达22.49 mg/g。然而,此类吸附剂对反应pH有严格要求,通常只有在pH 5~6范围内[18-20]或更低的pH环境中才具有较好的吸附效果。本文作者以纳米Fe3O4为载体,采用硫酸铝包覆改性制备除氟吸附剂,并进行制备条件参数的优化,研究吸附剂的除氟性能,其目的是制备出一种对氟吸附能力强、适用pH范围广、具有磁性易于从水体中分离的除氟吸附剂,以期为含氟水的处理提供一种新材料、新方法。
1 实验
1.1 实验材料
主要实验药剂:三氯化铁(FeCl3・6H2O)、氯化亚铁(FeCl2・4H2O)、硫酸铝(Al2(SO4)3・18H2O)和氟化钠(NaF),均为分析纯(AR),由国药集团化学试剂有限公司提供。
1.2 实验方法
1.2.1 载体Fe3O4的制备
称取FeCl3・6H2O和FeCl2・4H2O(Fe3+与Fe2+的摩尔比为1.25:1)溶于盐酸溶液,然后将溶液逐滴加入到pH=11.0的NaOH溶液中,保持恒温80 ℃,通惰性气体,并用1 mol/L NaOH调节反应溶液 pH保持在11.0左右,机械搅拌反应1.5 h(250~260 r/min)。将反应得到的悬浮液冷却至室温,用去离子水清洗,得到Fe3O4悬浮液备用。
1.2.2 除氟吸附剂的制备
以硫酸铝作为改性剂,溶于去离子水,将改性剂溶液逐滴加入到制备好的Fe3O4悬浮液中,投加的Fe3O4与Al摩尔比分别为1:0.5,1:1,1:2,1:3,1:4和1:8,充分搅拌,反应过程中温度控制在80 ℃,通惰性气体,分别调节反应溶液pH为3.0,3.5,4.0,5.0,6.0和8.0,机械搅拌反应1.5 h。将反应得到的悬浮液冷却至室温,过滤分离, 将过滤后的固体产物用去离子水、无水乙醇清洗数遍,干燥碾磨,得到吸附剂。
1.2.3 吸附剂除氟性能研究
称取吸附剂样品0.1 g放入120 mL的聚乙烯瓶中,加入100 mL初始质量浓度为25 mg/L的含F-溶液,分别调节溶液pH为2.0,3.0,4.0,5.0,6.0,7.0,8.0,9.0,10.0,11.0,11.5和12.0,在恒温水浴振荡箱中保持25 ℃振荡7 h。将吸附反应后的溶液过滤,测定溶液中F-的浓度。
将吸附剂样品0.1 g和100 mL配制好的含氟溶液放入120 mL聚乙烯小瓶,初始氟质量浓度范围为2~160 mg/L,溶液pH为7.0,在恒温水浴振荡箱中保持25 ℃振荡7 h。将吸附反应后的溶液过滤,测定溶液中F-的质量浓度。
1.2.4 样品的表征和分析方法
采用日本电子公司生产的JEM-2100型透射电子显微镜(TEM)观察样品的形貌,仪器的加速电压为200 kV;采用美国EDAX公司生产的EDS-GENESIS 60S型能谱仪(EDS)分析样品的元素组成和相对百分含量;采用美国QUANTACHRME公司生产AUTOSORBI/MONOSORB型自动比表面积分析仪测定样品的比表面积(BET);样品的晶型和组成采用日本株式会学理学公司生产的Rigaku-TTRIII型X线粉末衍射仪(XRD)进行分析,最大输出功率为18 kW,Cu靶Kα辐射,扫描范围为2θ=0°~158°;采用南京大学的HH-15振荡样品磁强计(VSE)测定样品的饱和磁化强度。利用 K-Alpha 1063型X线光电子能谱仪对样品表面元素组成进行分析,X线源为铝Kα微聚集单色器;分析器为180°双聚集半球分析器-128通道检测器;光斑直径为400 μm,真空度为0.9~1.0 kPa,分辨率为0.5 eV。
溶液中的F-质量浓度及pH分别采用上海精密科学仪器有限公司生产的pF-1型氟离子选择电极和PHS-3E型pH计测定。
2 结果与讨论
2.1 载体Fe3O4的性质表征
图1(a)所示为Fe3O4的透射电镜(TEM)图。从图1(a)可看出:样品的颗粒分布较为均匀,形状较规则,大致呈球形,平均粒径为20 nm左右。图1(b)所示为Fe3O4的能谱图(EDS),样品所含的元素主要为Fe和O。图1(c)所示为样品的X线衍射图谱,2θ为30.4°, 35.6°, 43.3°, 57.3°和62.8°为Fe3O4的特征峰;而且主峰的峰宽较窄,说明样品的晶化程度高。从图1分析可知:实验采用的碱性共沉淀法制备出的样品为纳米尺度的Fe3O4且晶化程度高可用于后续的包覆改性实验。
2.2 吸附剂制备条件参数的优化
制备反应pH和物料配比为吸附剂制备过程中的重要影响因素,因此,实验考察了这2种因素对吸附剂除氟效果的影响。图2所示为不同pH条件下(pH 3.0,3.5,4.0,5.0,6.0和8.0)制备的吸附剂对氟离子去除效果的影响。吸附反应条件为室温,初始氟质量浓度30 mg/L。由图2可知:在pH为3.0和3.5时,除氟率较低(低于40%),而在pH 4~6时,吸附剂的除氟率较高,达到80%以上,在pH 5.0左右达到最大值,接近90%;而当pH升高到8.0时,除氟率有所下降(小于60%):因此,在制备除氟吸附剂反应过程中选择pH为5.0。
图3所示为制备反应溶液pH 5.0时,不同Fe3O4与Al投加量摩尔比制备出的吸附剂的除氟率。由图3可知:随着Fe3O4与Al摩尔投加比中铝含量的增加,吸附剂的除氟率逐渐增加,并在Fe3O4与Al投加量摩尔比降低为1:2后趋于稳定,除氟率接近88%。这可能是由于Al3+对F-有较强的亲合力,随着铝盐投加量的增加,F-的去除效率也相应增加。但随着载体Fe3O4被完全包覆后,即使增加铝盐的含量,除氟率也无明显增加。图4所示为不同Fe3O4与Al摩尔投加比吸附剂的磁化曲线,由图4可见:载体Fe3O4的饱和磁化强度为47.64 A・m2/kg,随着铝盐投加量的增加,样品的饱和磁化强度呈递减趋势。

图1 Fe3O4的透射电镜图、能谱图和X线衍射图
Fig. 1 TEM, EDS and XRD images of Fe3O4

图2 吸附剂制备反应pH对除氟率的影响
Fig. 2 Effect of preparation pH on fluoride removal efficiency
由图3和图4可知:当Fe3O4与Al投加量摩尔比为1:2时,吸附剂的除氟率达到87%,同时饱和磁化强度为15.63 A・m2/kg,可在外加磁场下实现固液分离[17]。随着Fe3O4与Al投加量摩尔比中铝含量的进一步增加,吸附剂的除氟率并没有显著提高,而饱和磁化强度下降较多,不利于后续的固液分离。综合考虑除氟效率、磁性能及药剂用量,确定吸附剂制备的最优条件参数为:Fe3O4与Al投加量摩尔比1:2,制备反应中pH=5.0。
图5所示为不同物料配比吸附剂的比表面积与除氟率对应图(1~7号样品Fe3O4与Al投加量摩尔比分别为1:0,1:0.5,1:1,1:2,1:3,1:4和1:8)。由图5可见:包覆改性前后,样品的比表面积无太大变化,基本保持在62~78 m2/g之间,且无规律可循;此外,样品的比表面积与除氟率亦无明显规律,因此推断:F-的去除并不是简单的附着在吸附剂表面,而是与吸附剂的表面活性位点有关,可能是静电吸附,也可能是形成表面络合物而被去除,抑或是二者共同作用的结果。

图3 物料比对除氟率的影响
Fig. 3 Effect of molar ratio of Fe3O4 to Al on fluoride removal efficiency

图4 不同物料配比吸附剂的磁化曲线
Fig. 4 VSM magnetization curves of adsorbents with different molar ratios of Fe3O4 to Al
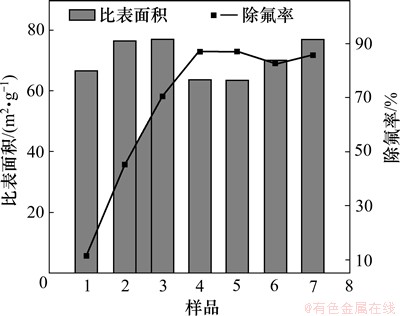
图5 不同物料配比吸附剂的比表面积和除氟率对应图(1~7号样品Fe3O4与Al摩尔比分别为1:0,1:0.5,1:1,1:2,1:3,1:4和1:8)
Fig. 5 Specific surface area and fluoride removal efficiency of adsorbents with different molar ratios of Fe3O4 to Al
2.3 纳米磁性铁铝复合物的性质表征
采用Al2(SO4)3・18H2O作为改性剂,制备反应pH 5.0,Fe3O4与Al投加量摩尔比1:2制得的吸附剂即纳米磁性铁铝复合物,比表面积为63.37 m2/g,饱和磁化强度为15.63 A・m2/kg。图1(a)所示的透射电镜图谱显示:该吸附剂为纳米颗粒呈不规则团聚,平均粒径为15~20 nm,与载体Fe3O4的粒径相近。图6(a)所示为吸附剂X线衍射图,图谱中只显示Fe3O4的主峰,而没有出现铝化合物的峰,说明经过包覆改性后,可能生成了一种非晶形的铝化合物。图6(b)所示为吸附剂的X线光电子能谱,谱图中Al 2p峰表明样品中的Al以三氧化二铝形态存在,且Al原子数分数较高(Al 为23.11%,而Fe为 7.48%),因此,推测改性后形成的吸附剂是一种以三氧化二铝为外壳,Fe3O4为内核的磁性纳米材料。图6(c)所示为吸附剂在不同pH条件下的Zeta电位曲线。由图6(c)可见:吸附剂的零电荷点(pHpzc)为11.2,当溶液pH等于pHpzc时,吸附剂表面所带的净电荷为零;当溶液pH<pHpzc时,吸附剂表面带正电荷;当溶液pH>pHpzc时,吸附剂表面带负电荷[11]。本研究中制备的纳米磁性铁铝复合物pHpzc高于目前报道的绝大多数除氟吸附材料[21],高pHpzc表明该吸附剂在水体环境中带正电荷,有利于带负电荷阴离子的吸附。

图6 纳米磁性铁铝复合物XRD图谱、X线光电子能谱和不同pH条件下的Zeta电位
Fig. 6 XRD pattern, X-ray photoelectron spectroscopy and Zeta potential at different pH for iron-aluminum composite magnetic nanoparticles
2.4 铁铝复合物磁性颗粒的除氟性能
2.4.1 pH的影响
pH对吸附剂除氟率起着重要的作用。图7所示为不同pH条件下,纳米磁性铁铝复合物对氟化物的去除率。由图7可看出:当溶液的pH为4.0~10.0时,除氟效果较好,在酸性(pH<4.0)和碱性(pH>10.0)条件下,除氟率显著下降。由图6可知:纳米磁性铁铝复合物的pHpzc为11.2,在pH为4.0~10.0时,吸附剂表面带正电荷,可以通过静电吸引吸附溶液中的带负电的氟离子;当pH小于4.0时,吸附剂表面带正电荷,但此时溶液中的多数氟化物以电中性HF分子的形式存在,因此除氟率下降;当pH大于10.0时,吸附剂表面的正电荷逐渐减少并开始带有大量的负电荷,与溶液中的F-产生静电排斥,故除氟率下降。由此可见,氟离子是通过静电吸引作用从溶液中转移至吸附剂表面而被去除的。

图7 pH对除氟率的影响
Fig. 7 Effect of pH on fluoride removal efficiency
2.4.2 氟离子的吸附等温线
在常温,pH 7.0条件下,纳米磁性铁铝复合物对氟化物的吸附等温线如图8所示。采用Langmuir和Freundlich 2种模型进行吸附等温线的拟合。2种吸附等温方程描述如下。
Langmuir:  (1)
(1)
Freundlich:  (2)
(2)
其中: 为平衡时溶液中F-的质量浓度,mg/L;qe为平衡时单位吸附剂吸附F-的质量,mg/g;Qmax为吸附剂的最大吸附容量,mg/g;Kl为与吸附能有关的Langmuir常数,L/mg;Kf和1/n分别为与吸附容量、吸附强度有关的Freundlich常数,mg1-(1/n)・L1/n・g-1。2种模型拟合的参数见表1。
为平衡时溶液中F-的质量浓度,mg/L;qe为平衡时单位吸附剂吸附F-的质量,mg/g;Qmax为吸附剂的最大吸附容量,mg/g;Kl为与吸附能有关的Langmuir常数,L/mg;Kf和1/n分别为与吸附容量、吸附强度有关的Freundlich常数,mg1-(1/n)・L1/n・g-1。2种模型拟合的参数见表1。
实验数据与Langmuir吸附等温线模型拟合较好(相关系数R2>0.96)。由图8可见:随着初始F-质量浓度的增加,吸附剂对F-的吸附量逐渐增加;但随着初始F-浓度的不断增加,吸附量的增加幅度越来越小,并趋于平缓,说明F-的吸附与吸附剂表面有限的活性位点有关,随着表面活性位点被逐渐占据,F-的吸附量也趋于饱和。在常温,pH=7.0条件下,纳米磁性铁铝复合物对F-的最大吸附容量约为48 mg/g,高于目前国内外大多数报道的除氟吸附剂材料[17-20]。
表1 Langmuir和Freundlich吸附模型对氟化合物吸附等温线的拟合参数
Table 1 Parameters of Langmuir and Freundlich adsorption models to fluoride adsorption isotherm
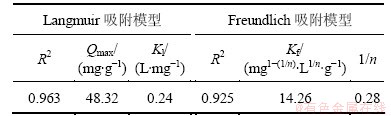

图8 纳米磁性铁铝复合物对氟离子的吸附等温线
Fig. 8 Adsorption isotherm of fluoride on iron-aluminum composite magnetic nanoparticles
3 结论
(1) 采用碱性共沉淀的方法制备了载体纳米Fe3O4,并选用硫酸铝对其进行包覆改性制备除氟吸附剂,吸附剂最优制备条件参数为Fe3O4与Al投加量摩尔比1:2,制备反应pH 5.0。最优条件下制备的除氟吸附剂即纳米磁性铁铝复合物,其比表面积为63.37 m2/g,平均粒径15~20 nm,零电荷点pHpzc为11.2,饱和磁化强度为15.63 emu/g,可通过外加磁场进行固液分离。
(2) 氟离子是通过静电吸引作用从溶液中转移至吸附剂表面而被去除的,由于纳米磁性铁铝复合物的零电荷点(pHpzc=11.2)远高于其他已报道过的吸附剂的零电荷点,因此该吸附剂适用pH范围广,在pH=4.0~10.0范围内除氟率均在84%以上。
(3) 纳米磁性铁铝复合物对F-的吸附等温线符合Langmuir吸附等温模型,在常温,pH=7.0的条件下,纳米磁性铁铝复合物对F-的最大吸附容量约为48 mg/g。
参考文献:
[1] Ortize-Peter D, Redriguez-Martinez M, Martinez F, et al. Fluoride-induced disruption of reproductive hormones in men[J]. Environmental Research, 2003, 93(1): 20-30.
[2] 刘宁. 充分关注水质, 科学保障饮水安全[J]. 中国水利, 2006(3): 5-9.
LIU Ning. Attention on water quality adequately and ensuring drinking water safety scientifically[J]. China Water, 2006(3): 5-9.
[3] GB 5749―2006, 生活饮用水卫生标准[S].
GB 5749―2006, Standards for drinking water quality[S].
[4] 汪清, 李伟英. 纳滤膜和低压反渗透膜去除水中氟的对比研究[J]. 给水排水, 2009, 35: 17-20.
WANG Qing, LI Weiying. Comparative study on fluoride removal by NF and RO[J]. Water & Wastewater Engineering, 2009, 35: 17-20.
[5] 朱迪瑞, 陈男, 和树庄, 等. 铁氧化物陶瓷颗粒除氟效果及吸附特性研究[J]. 环境科学与技术, 2011, 34(6): 71-75.
ZHU Dirui, CHEN Nan, HE Shuzhuang, et al. Effect of fluoride removal by iron oxide ceramic materials[J]. Environmental Science & Technology, 2011, 34(6): 71-75.
[6] Rozic L, Novakavic T, Petrovic S, et al. The sorption and crystallographic characteristics of aluminum activated in a reactor for pneumatic transport[J]. Journal of Serbian Chemical Society, 2006, 71(11): 1237-1246.
[7] Tripathy S S, Bersillon J L, Gopal K. Removal of fluoride from drinking water by adsorption onto alum-impregnated activated alumina[J]. Separation and Purification Technology, 2006, 50(3): 310-317.
[8] Zhou Y M, Yu C X, Shan Y. Adsorption of fluoride from aqueous solution on La3+-impregnated cross-linked gelatin[J]. Separation and Purification Technology, 2004, 36(2): 89-94.
[9] Liao X P, Shi B. Adsorption of fluoride on zirconium(Ⅳ)- impregnated collagen fiber[J]. Environmental Science and Technology, 2005, 39(12): 4628-4632.
[10] Wu X M, Zhang Y, Dou X M, et al. Fluoride removal performance of a novel Fe-Al-Ce trimetal oxide adsorbent[J]. Chemosphere, 2007, 69(11): 1759-1764.
[11] Tchomgui-Kamga E, Alonzo V, Nanseu-Njiki C P, et al. Preparation and characterization of charcoals that contain dispersed aluminum oxide as oxide as adsorbents for removal of fluoride from drinking water[J]. Carbon, 2010, 48(2): 333-343.
[12] Turner B D, Binning P, Stipp S L S. Fluoride removal by calcite: evidence for fluoride precipitation and surface adsorption[J]. Environmental Science and Technology, 2005, 39(24): 9561-9568.
[13] ZHAO Xiaoli, SHI Yali, CAI Yaqi, et al. Cetyltrimethylammonium bromide-coated magnetic nano- particles for the pre-concentration of phenolic compounds from environmental water sample[J]. Environmental Science and Technology, 2008, 42(4): 178-184.
[14] Yantasee W, Warner C L, Sangvanich T, et al. Removal of heavy metals from aqueous systems with thiol functionalized superparamagnetic nanoparticles[J]. Environmental Science and Technology, 2007, 41(14): 5114-5119.
[15] ZHAO Xiaoli, SHI Yali, Wang T, et al. Preparation of silica-magnetite nanoparticle mixed hemimicelle sorbents for extraction of several typical phenolic compounds from environmental water sample[J]. Journal of Chromatography A, 2008, 1188(2): 140-147.
[16] Bhaumik M, Leswifi T Y, Maity A, et al. Removal of fluoride from aqueous solution by polypyrrole/Fe3O4 magnetic nanocomposite[J]. Journal of Hazardous Materials, 2011, 186(1): 150-159.
[17] Ma W, Ya F Q, Han M, et al. Characteristic of equilibrium, kinetics studies for adsorption of fluoride on magnetic-chitosan particle[J]. Journal of Hazardous Materials, 2007, 143(1/2): 296-302.
[18] LI Yanhui, WANG Shuguang, CAO Anyuan, et al. Adsorption of fluoride from water by amorphous alumina supported on carbon nanotubes[J]. Chemical Physics Letters, 2001, 350(5/6): 412-416.
[19] Dey S, Goswami S, Ghosh U C. Hydrous ferric oxide (HFO)―A scavenger for fluoride from contaminated water[J]. Water Air Soil Pollution, 2004, 158(1): 311-323.
[20] Ma Z Y, Guan Y P, Liu H Z. Synthesis and characterization of micron-sized monodisperse superparamagnetic polymer particles with amono groups[J]. Journal of Polymer Science Part A: Polymer Chemistry, 2005, 43(15): 3444-3439.
[21] Bhatnagar A, Kumar E,  M. Fluoride removal from water by adsorption: A review[J]. Chemical Engineering Journal, 2011, 171: 811-840.
M. Fluoride removal from water by adsorption: A review[J]. Chemical Engineering Journal, 2011, 171: 811-840.
(编辑 杨幼平)
收稿日期:2012-12-07;修回日期:2013-03-17
基金项目:国家自然科学基金资助项目(51304252);国家“十二五”科技支撑计划项目(2012BAC12B04);湖南有色金属研究基金资助项目(2011年);国家公益性(环保)行业科研项目(2011467062)
通信作者:杨卫春(1982-),女,湖南湘乡人,博士,副教授,从事废水废渣治理研究;电话:0731-88830875;E-mail: yang220222000@yahoo.com.cn