网络首发时间: 2015-04-07 09:26
稀有金属 2014,38(06),1134-1140 DOI:10.13373/j.cnki.cjrm.2014.06.031
钒渣无焙烧加压酸浸过程研究
余彬 孙朝晖 张廷安 鲜勇 牟望重 唐红建
攀枝花钢铁集团研究院有限公司钒钛资源综合利用国家重点实验室
东北大学材料与冶金学院多金属共生矿生态化利用教育部重点实验室
摘 要:
针对现有产业化钒渣“焙烧-浸出”提钒工艺冶金废弃物多的现状, 采用钒渣“无焙烧-加压酸浸”工艺进行了试验研究, 考察了浸出温度、液固比、浸出时间、初酸浓度及搅拌速率对转炉钒渣中钒、钛、铁浸出率的影响, 绘制了高温 (150℃) 条件下V-Fe-H2O系E-p H图, 并分析了钒渣矿物中各组分在该条件下与H2SO4反应的可能性、有价金属转入溶液的理论限度和生成物的稳定状态。150℃V-Fe-H2O系高温Ep H图结果表明:150℃时, 在H2O及Fe2+的稳定区范围内, 钒铁尖晶石 (Fe O・V2O3) 能够在p H<1.5的强酸条件下分解, 可溶性钒离子主要以VO2+的形式在体系中充分浸出;通过无焙烧-加压酸浸试验, 得到粒度-0.075~+0.055 mm钒渣的最优酸浸工艺参数为:浸出温度130℃、浸出时间90 min、初酸浓度200 g・L-1、液固比10∶1、搅拌速率500 r・min-1。结果表明:在最优工艺条件下, 通过无焙烧-酸浸能够使钒渣中的钒浸出率达96.93%, 铁浸出率为92.33%, 钛浸出率为15.95%, 并在渣中富集。
关键词:
钒渣;无焙烧;加压酸浸;浸出率;
中图分类号: TF803.21
作者简介:余彬 (1987-) , 男, 四川内江人, 硕士研究生, 工程师, 研究方向:钒钛资源综合利用、冶金工程;E-mail:robinyjgc@si-na.com;;鲜勇, 高级工程师;电话:13882307083;E-mail:cdxianyong@163.com;
收稿日期:2014-08-03
基金:国家科技部重点基础研究发展计划项目 (2012CB724202) 资助;
Non-Roasting Pressure Acid-Leaching Process of Vanadium Slag
Yu Bin Sun Zhaohui Zhang Tingan Xian Yong Mu Wangzhong Tang Hongjian
State Key Laboratory of Vanadium and Titanium Resources Comprehensive Utilization, Panzhihua Iron and Steel Group Research Institute Company
Ministry of Education Key Laboratory of Ecological Utilization of Multi-Metal Intergrowth Ores, School of Materials and Metallurgy, Northeastern University
Abstract:
As the roasting-leaching process produced large amounts of metallurgical wastes, “non-roasting acid leaching”process for vanadium slag was studied experimentally. The leaching temperature, the ratio of liquid to solid, the leaching time, the initial acid concentration and the stirring speed were tested to measure the leaching rates of V, Ti and Fe of vanadium slag. The possibility of reactions between components and H2SO4, the theoretical limits of valuable metal transferred into the solution and the steady state of products were analyzed using E-p H diagram of V-Fe-H2 O system under high temperature conditions. The results showed that Fe O・V2O3could be leached out in the form of VO2 +when p H < 1. 5 in the stable area of H2 O and Fe2 +, and the optimum process parameters for obtaining vanadium slag with particle size of- 0. 075 ~+ 0. 055 mm were: leaching temperature of 130 ℃, liquid to solid ratio of 10∶1, leaching time of 90 min, initial acid concentration of 200 g・L- 1, and stirring speed of 500 r・min- 1. As a result, the leaching rates in non-roasting acid leaching process were 96. 63%, 92. 33% and 15. 95% for V, Fe and Ti, respectively, with Ti enriched in the leaching residue.
Keyword:
vanadium slag; non-roasting; pressure acid-leaching; leaching rate;
Received: 2014-08-03
钒具有重要的战略价值, 因其熔点高, 无磁性, 韧性好, 同时作为合金添加剂具有超强的晶粒细化和沉淀强化作用, 被广泛应用于含钒中间合金, 含钒全液流电磁和含钒航空航天材料的生产[1,2,3]。世界上已探明的钒资源主要以正三价氧化物和类质同相与其他金属共生的形式存在于不同含钒矿物中, 其中有98%为钒钛磁铁矿。钒钛磁铁矿经转炉半钢提钒所得的转炉钒渣中钒含量达到5%~15%, 是世界上提钒的主要原料[4]。
目前, 以钒渣为原料的提钒工艺主要采用焙烧-浸出的方式, 通过强化氧化、焙烧等手段破坏钒铁尖晶石的致密结构, 使渣中的钒转化为水溶性或酸溶性的含钒酸盐[5,6,7]。但是传统的焙烧-浸出过程中, 焙烧工艺段需要使用沸腾炉或回转窑等设备, 工艺流程长, 物料消耗量大, 焙烧过程易产生有害有毒气体, 同时在钒渣资源综合利用方面还存在缺陷。随着全球对环境保护和提高资源有效利用的重视, 以及湿法冶金强化浸出技术的快速发展, 无焙烧浸出技术逐渐成熟。本文通过无焙烧-加压酸浸工艺, 取消焙烧过程, 直接采用高温硫酸浸出, 考察转炉钒渣的可浸性, 并获取最优工艺参数, 为工业化生产提供设计依据。
电位-p H图 (E-p H图) 是研究湿法冶金过程重要的热力学依据[8,9]。通过E-p H图可以判断钒渣矿物中各组分与溶剂反应的可能性, V, Ti, Fe等金属转入溶液的理论限度, 以及生成物的稳定状态, 初步确定浸出条件, 为获得经济有效的浸出效果提供理论指导。
1 实验
1.1 原料
转炉钒渣:取自攀枝花钢铁集团钒业公司转炉半钢冶炼所得钒渣, 采用X射线荧光 (XRF) 光谱定性分析结合化学全分析的方法得到其化学成分, 见表1。98%H2SO4, 分析纯。
1.2 设备
KCFD2-10型酸式加压反应釜;KE型变频行星式高能球磨机;BPG-9200BH型高温真空干燥箱;2XZ-1型旋片式真空泵;DV215CD型电子天平;PW3040/60型X射线衍射仪 (XRD) ;带能谱分析的SSX-550型扫描电镜 (SEM-EDX) 。
表1 钒渣的化学成分 (%, 质量分数) Table 1Chemical compositions of vanadium slag (%, mass fraction) 下载原图
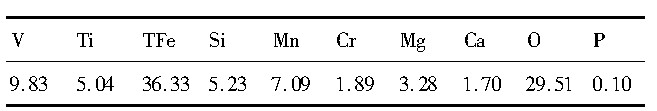
表1 钒渣的化学成分 (%, 质量分数) Table 1Chemical compositions of vanadium slag (%, mass fraction)
1.3 内容与方法
150℃V-Fe-H2O系E-p H图的绘制:分析V-Fe-H2O三元系中所有可能存在的化学反应, 通过理论推导得到高温条件下各反应化学ET和p HT数学表达式, 借助热力学数据手册查出相关物质的标准热力学数据, 最后利用绘图软件绘制得到150℃条件下E-p H图。
无焙烧-酸浸试验研究:将转炉钒渣破碎, 球磨到粒度为-0.075~+0.055 mm, 每次取样50 g, 与稀释到一定浓度的稀H2SO4一同加入酸式加压反应釜中, 并密封。混合后于设定的浸出温度, 液固比, 浸出时间, 初酸浓度, 搅拌速率条件下进行浸出。浸出结束后待混合浆料冷却至室温, 对其进行固液分离, 并洗涤残渣, 获得酸浸液和富钛渣。本文采用全谱直读发射光谱仪 (ICP) 所测酸浸液离子浓度结果计算浸出率。

式中ηi为ICP测浸出率, %;ci为ICP测离子浓度 (稀释1000倍) , 10-6;Vi为浸出液体积, ml;m矿为加入的钒渣原矿质量, g;wi为原矿中元素含量, %。
2 结果与讨论
2.1 高温V-Fe-H2O系E-p H图的绘制
湿法冶金过程中化学反应可以用式 (2) 来表示[10]:
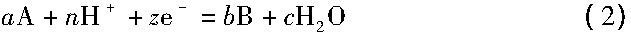
式中A和B分别是无焙烧浸出过程可能发生反应的钒、铁及其化合物。
根据反应有无H+或e-参加, 不同温度条件下氧化还原反应体系的ET及溶解-沉淀反应的p HT计算公式分别为式 (3) , (4) 和 (5) [11]:
(1) 有e-参加, 无H+参加,

(2) 有H+参加, 无e-参加,

(3) 有H+参加, 有e-参加,
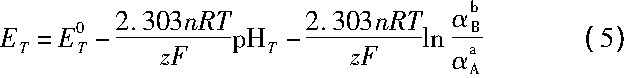
式中z为无焙烧浸出过程化学反应转移的电子数目, F为法拉第常数, αA和αB分别为氧化态A和还原态B的活度。
随着温度的升高, 反应的ET (不同温度T条件下, 反应的还原电位) 和p HT (不同温度T条件下, 反应的p H值) 较常温E298和p H298将发生显著迁移[12]。高温条件下ET0 (温度T时, 反应的标准还原电位) , p HT0 (温度T时, 反应的标准p H值) 与常温 (298 K) 条件下E0298, p H0298存在如下规律:
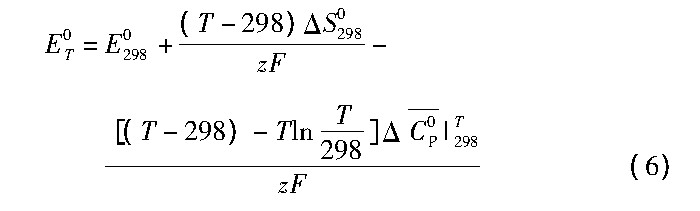
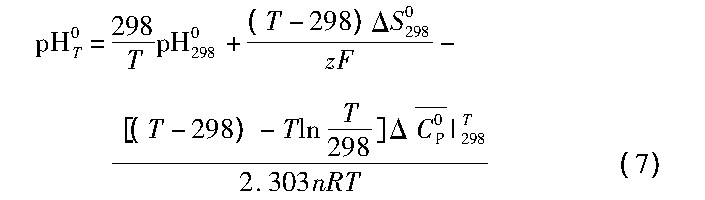
式中ΔS0298为298 K时反应的标准摩尔熵;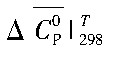 为298~T K的反应标准平均热容。
为298~T K的反应标准平均热容。
对于平均热容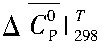 的计算通常分为两种方法: (1) 适用于熔渣体系的中性物质平均热容法; (2) 适用于水溶液离子平均热容法。因此本研究采用离子平均热容法。根据Cobble提出的“离子熵对应原理”, 对于某类型的离子, 温度T和298 K条件下的偏摩尔绝对熵
的计算通常分为两种方法: (1) 适用于熔渣体系的中性物质平均热容法; (2) 适用于水溶液离子平均热容法。因此本研究采用离子平均热容法。根据Cobble提出的“离子熵对应原理”, 对于某类型的离子, 温度T和298 K条件下的偏摩尔绝对熵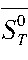 (i, 绝对) 和
(i, 绝对) 和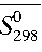 (i, 绝对) 之间存在着直线关系[13], 如式 (8) 所示:
(i, 绝对) 之间存在着直线关系[13], 如式 (8) 所示:
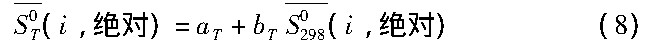
式中aT, bT为给定温度下的常数值, 只与选择的标准态、溶剂、温度以及离子类型有关, 而与个别离子性质无关。
从离子熵计算平均热容的方法及平均热容的定义分别有式:

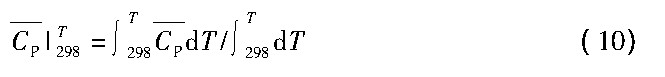
近似处理得到如下公式:
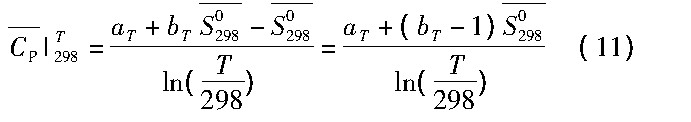
表2列出了150℃时4种离子类型的aT和bT值[10]。利用相关热力学数据[13,14,15], 将其带入式 (11) 可求得150℃的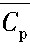 值, 利用式 (6) , (7) , 即可求得E0423, p H0423。最后得到各类型反应E423和p H423的数学表达式。为简化计算, 计算过程中取Fe O・V2O3-H2O系水溶液中各离子的活度系数为1.0、离子浓度0.1 mol・L-1。所得150℃条件下Fe O・V2O3-H2O系E-p H图如图1所示。由图1可知, 在H2O的稳定区范围内, 钒铁尖晶石 (Fe O・V2O3) 在弱酸及中性、弱碱性条件下均稳定存在。而在一定氧化还原电位条件下, 当p H<1.5或p H>14.0时, Fe O・V2O3开始分解, 使得钒渣中的钒浸出进入液相, 说明在强酸或强碱条件下转炉钒渣分解具有可行性。针对酸性体系, 当p H<1.5时, 含钒矿物中钒以V3+, VO2+和VO2+3种水溶性离子形式浸出, 而在H2O的稳定区内, 则主要以VO2+形式存在。此外, 对于“无焙烧-酸浸”工艺, 浸出氧化还原电位在1.0~1.5 V时, 可溶性VO2+稳定区全部包含在Fe3+的稳定区范围内;浸出电位0~1.0 V时, VO2+的稳定区全部包含在Fe2+的稳定区范围内, 表明转炉钒渣酸浸过程在浸出可溶性钒离子的同时, 一定伴随有铁的浸出。这也从热力学的角度表明, 试图通过改变浸出体系温度、硫酸浓度等因素来控制氧化还原电位和p H值, 以保证钒渣中钒被充分浸出的同时铁不浸出, 从而达到钒、铁分离是不可行的。浸出液还需要进一步净化来生产高纯度的钒制品。
值, 利用式 (6) , (7) , 即可求得E0423, p H0423。最后得到各类型反应E423和p H423的数学表达式。为简化计算, 计算过程中取Fe O・V2O3-H2O系水溶液中各离子的活度系数为1.0、离子浓度0.1 mol・L-1。所得150℃条件下Fe O・V2O3-H2O系E-p H图如图1所示。由图1可知, 在H2O的稳定区范围内, 钒铁尖晶石 (Fe O・V2O3) 在弱酸及中性、弱碱性条件下均稳定存在。而在一定氧化还原电位条件下, 当p H<1.5或p H>14.0时, Fe O・V2O3开始分解, 使得钒渣中的钒浸出进入液相, 说明在强酸或强碱条件下转炉钒渣分解具有可行性。针对酸性体系, 当p H<1.5时, 含钒矿物中钒以V3+, VO2+和VO2+3种水溶性离子形式浸出, 而在H2O的稳定区内, 则主要以VO2+形式存在。此外, 对于“无焙烧-酸浸”工艺, 浸出氧化还原电位在1.0~1.5 V时, 可溶性VO2+稳定区全部包含在Fe3+的稳定区范围内;浸出电位0~1.0 V时, VO2+的稳定区全部包含在Fe2+的稳定区范围内, 表明转炉钒渣酸浸过程在浸出可溶性钒离子的同时, 一定伴随有铁的浸出。这也从热力学的角度表明, 试图通过改变浸出体系温度、硫酸浓度等因素来控制氧化还原电位和p H值, 以保证钒渣中钒被充分浸出的同时铁不浸出, 从而达到钒、铁分离是不可行的。浸出液还需要进一步净化来生产高纯度的钒制品。
表2 4种离子类型在150℃时的aT和bT值 (标准态H+ (aq) 的熵为27.20 J・mol-1・K-1) Table 2 aTand bTvalues of four ionic types at 150℃ (En-tropy of standard H+ (aq) =27.20 J・mol-1・K-1) 下载原图
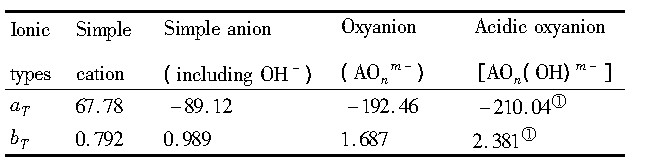
(1) :Working out values at lower temperature
表2 4种离子类型在150℃时的aT和bT值 (标准态H+ (aq) 的熵为27.20 J・mol-1・K-1) Table 2 aTand bTvalues of four ionic types at 150℃ (En-tropy of standard H+ (aq) =27.20 J・mol-1・K-1)
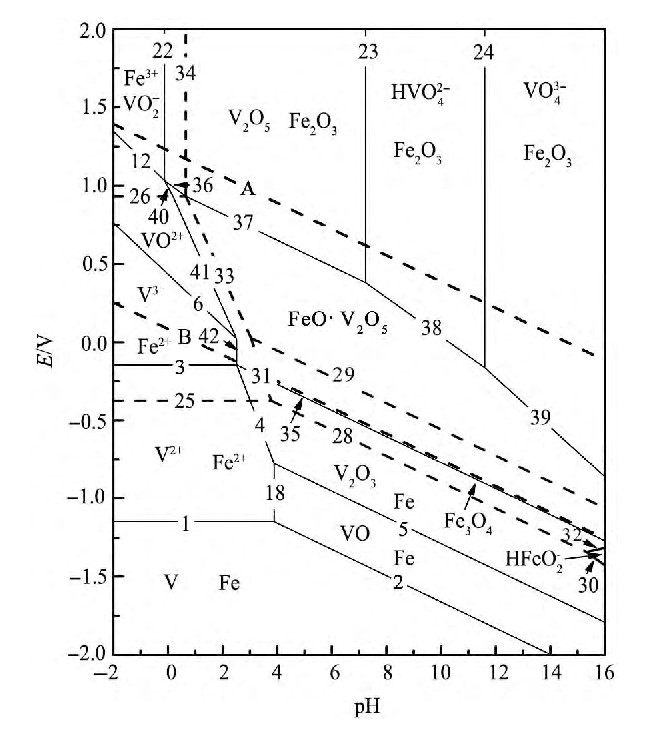
图1 150℃Fe O・V2O3-H2O系E-p H图Fig.1 E-p H diagram of Fe O・V2O3-H2O system at 150℃
2.2 浸出温度对浸出率的影响
在液固比20∶1、浸出时间120 min、搅拌速率500 r・min-1、初酸浓度200 g・L-1、钒渣粒度-0.075~+0.055 mm的条件下, 不同浸出温度试验结果如图2所示。
由图2可知, 随着温度从100增加到130℃, V, Ti, Fe浸出率分别从88.97%, 15.95%, 87.86%增加到98.06%, 17.85%, 93.75%。当温度提高到130℃以后, V浸出率增长趋于稳定, Ti浸出率继续提高到19.53%。Ti浸出速度有较大提高, 继续升高温度对浸出液的净化分离将有很大的副作用, 因此最优酸浸温度选择为130℃。
2.3 液固比对浸出率的影响
在浸出温度130℃、浸出时间120 min、搅拌速率500 r・min-1、初酸浓度200 g・L-1、钒渣粒度-0.075~+0.055 mm的条件下, 不同液固比试验结果如图3所示。
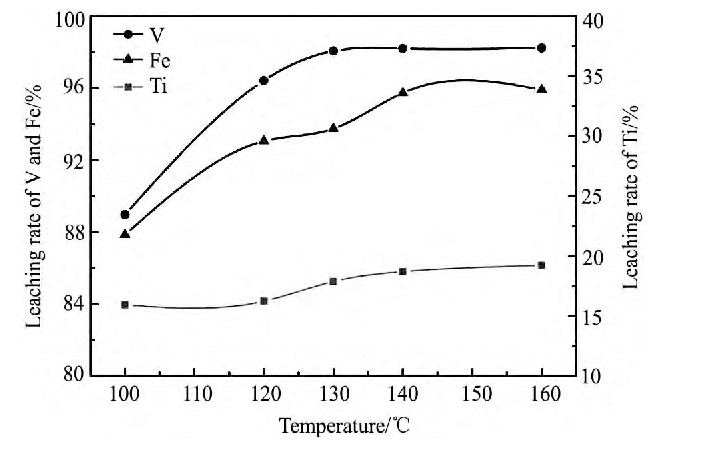
图2 浸出温度对V, Ti, Fe浸出率的影响Fig.2 Effect of leaching temperature on leaching rates of V, Ti and Fe
由图3可知, 随着浸出过程液固比由5∶1增加到10∶1, V, Ti, Fe浸出率分别由85.83%, 9.38%, 90.87%提高到97.01%, 16.31%, 92.47%。随着液固比进一步增加到20∶1, 实验结果趋于稳定, V, Ti, Fe浸出率分别为97.76%, 17.88%, 93.75%。液固比的增加会使物料流量增大, 降低酸浸液离子浓度, 不利于钒的提取。因此液固比控制在10∶1。
2.4 浸出时间对浸出率的影响
在浸出温度130℃、液固比10∶1、搅拌速率500 r・min-1、初酸浓度200 g・L-1、钒渣粒度-0.075~+0.055 mm的条件下, 考察了不同浸出时间对浸出率的影响, 结果如图4所示。

图3 液固比对V, Ti, Fe浸出率的影响Fig.3 Effect of liquid to solid ratio on leaching rates of V, Ti and Fe
由图4可知, 随着浸出时间由30增加到90min, V, Ti, Fe浸出率分别由79.32%, 12.76%, 83.29%增加到96.93%, 15.95%, 92.33%;浸出时间进一步增加到150 min, V, Fe浸出率趋于稳定;Ti浸出率增加到17.06%。说明90 min以后, 钒铁尖晶石已基本分解完全, 而含钛物相的浸出则继续进行。继续浸出导致酸浸液成分复杂, 不利于钒的分离提取, 因此反应时间应该控制在90 min。
2.5 初酸浓度对浸出率的影响
在浸出温度130℃、浸出时间90 min、液固比10∶1、搅拌速率500r・min-1、钒渣粒度-0.075~+0.055 mm的条件下, 考察不同初酸浓度对浸出率的影响, 结果如图5所示。
由图5可知, 随着初酸浓度由125提高到200g・L-1, V, Ti, Fe浸出率分别由87.67%, 6.47%, 85.34%提高到96.63%, 15.95%, 92.33%。随着初酸浓度进一步提高, V浸出率增长趋于稳定, 为97.22%, Ti, Fe浸出率分别增加到18.73%和93.46%。最优初酸浓度选择为200 g・L-1。
2.6 搅拌速率对浸出率的影响
在浸出温度130℃、浸出时间90 min、液固比10∶1、初酸浓度200 g・L-1、钒渣粒度-0.075~+0.055 mm的条件下, 考察不同搅拌速率对浸出率的影响, 结果如图6所示。
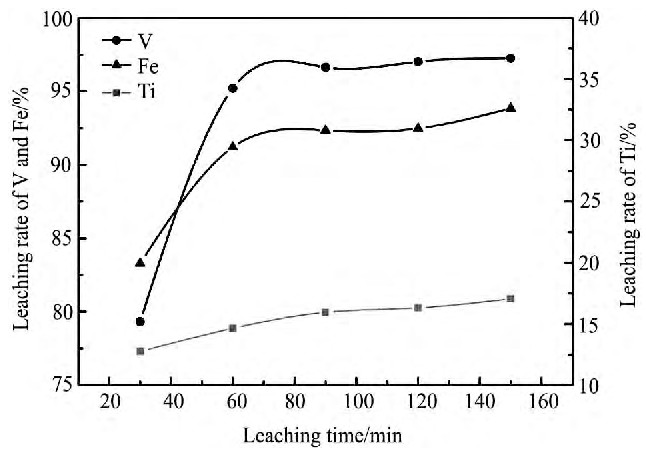
图4 浸出时间对V, Ti, Fe浸出率的影响Fig.4Effect of leaching time on leaching rates of V, Ti and Fe
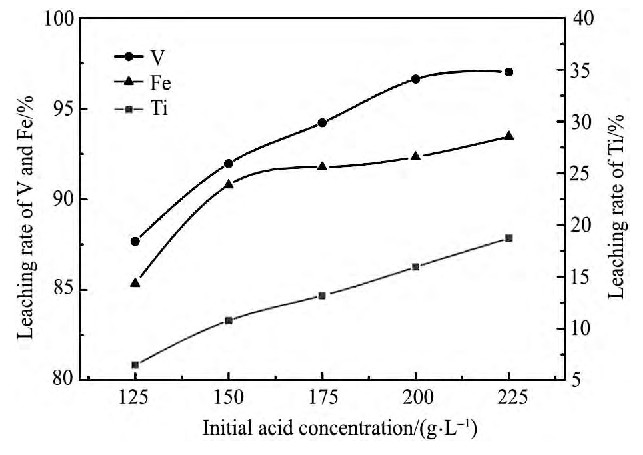
图5 初酸浓度对V, Ti, Fe浸出率的影响Fig.5Effect of initial acid concentration on leaching rates of V, Ti and Fe
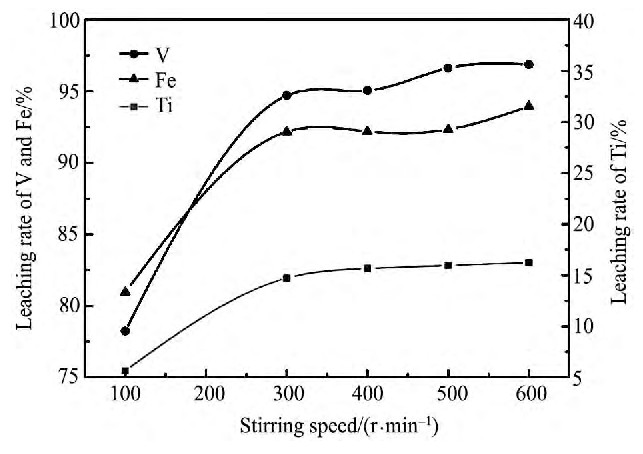
图6 搅拌速率对V, Ti, Fe浸出率的影响Fig.6Effect of stirring speed on leaching rates of V, Ti and Fe
由图6可知, 当搅拌速率从100提高到300r・min-1时, V, Ti, Fe浸出率增加明显, 继续提高搅拌速率, 三者的浸出率缓慢增加, 当搅拌速率达500 r・min-1时, 三者浸出率分别达96.93%, 15.95%, 92.33%, 继续提高搅拌速率, 对V浸出率的提高作用不大。因此最佳搅拌速率选择为500r・min-1。
2.7 钒渣与浸出渣物相及表观形貌
采用XRD, SEM-EDX对钒渣及最优酸浸渣物相组成, 化学成分及表观形貌进行分析表征, 结果见图7。由图7可知, 钒渣中物相有 (Mn, Fe) 2 (V, Cr) 2O4, Fe2VO4, (Fe, Mn) 2Si O4, Fe2Ti O2及Si O2;酸浸渣中物相为钛氧化物 (Ti O2, Ti2O3) 和Si O2, 同时含有微量未被破坏的钛铁尖晶石相。经过高温酸浸过程, 钒渣中主要含钒物相 (Mn, Fe) 2 (V, Cr) 2O4的衍射峰几乎全部消失, 酸浸渣中未能检测到V的存在, 表明钒渣的浸出效果较好。对比钒渣和酸浸渣表观形貌可知, 钒渣结构致密, 表面较为平整, 密度较大;酸浸渣结构疏松, 不平整, 呈蜂窝状。分析认为, 在浸出条件充分地情况下, 由于致密的钒铁尖晶石相逐渐溶解破坏, 随着渣中V及Fe的浸出, 原本平整致密的钒渣转变为疏松絮状物。与V-Fe-H2O三元系E-p H分析结果和试验结果有较好的吻合度。
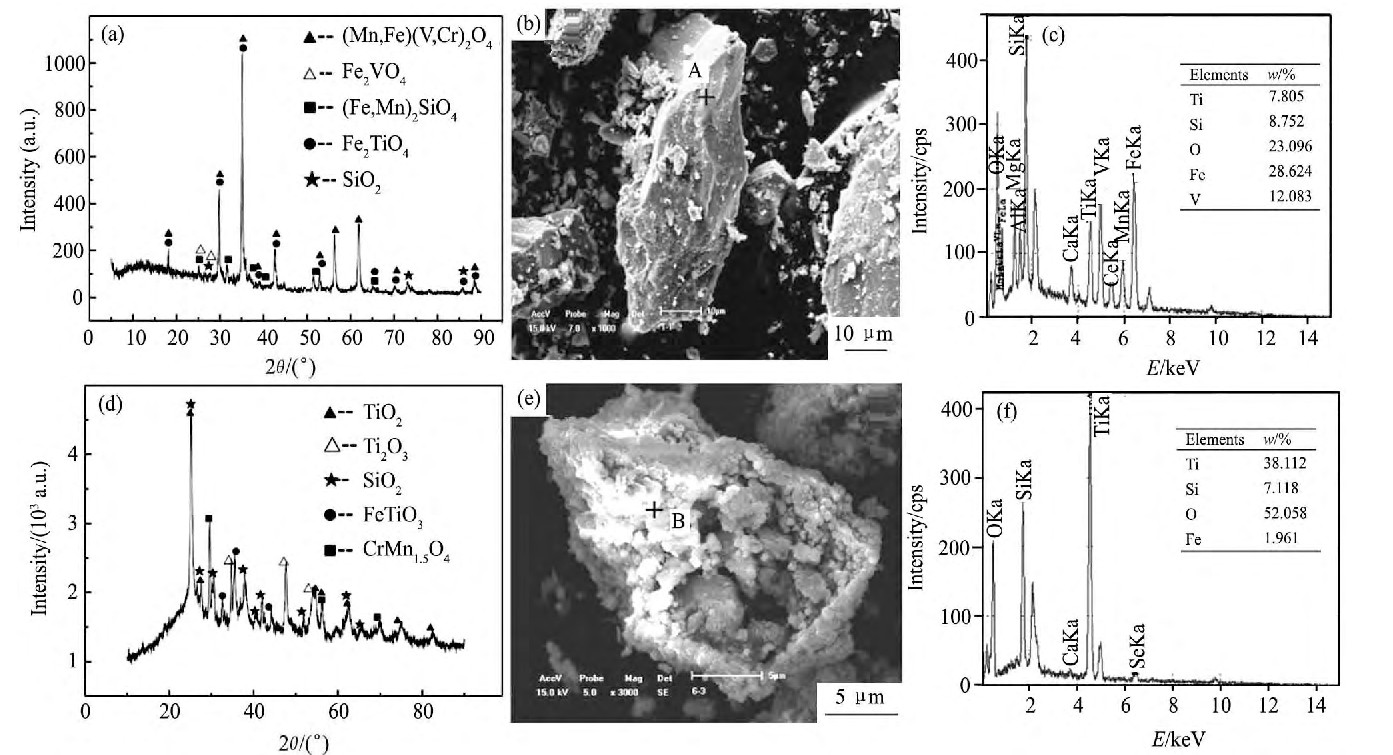
图7 钒渣和酸浸渣XRD, SEM图谱及EDX能谱分析Fig.7 XRD, SEM and EDX results of vanadium slag and residue
(a) XRD pattern of vanadium slag; (b) SEM image of vanadium slag; (c) EDX spectrum at Point A in b; (d) XRD pattern of residue; (e) SEM image of residue; (f) EDX spectrum at Point B in e
3 结论
1.高温V-Fe-H2O系E-p H图结果表明:150℃时, 在H2O的稳定区范围内, 钒铁尖晶石 (Fe O・V2O3) 能够在p H<1.5的强酸条件下主要以VO2+的形式充分浸出。
2.V, Fe浸出稳定区间重合度高, 浸钒工艺条件下, 渣中铁元素也将大量浸出, 酸浸液需要进一步进行V, Fe分离。
3.粒度-0.075~+0.055 mm钒渣无焙烧浸出的最优工艺条件为:浸出温度130℃、浸出时间90 min、初酸浓度200 g・L-1、液固比10∶1、搅拌速率500 r・min-1。
4.最优工艺条件下, V, Fe浸出率分别为96.93%和92.33%, 而Ti浸出率为15.95%, 主要以钛氧化物 (Ti O2, Ti2O3) 形式富集于酸浸渣中。
参考文献
[1] Sun Z H.Analysis on new vanadium technologies and prospects of vanadium industry[J].Iron Steel Vanadium Titanium, 2012, 33 (1) :1. (孙朝晖.钒新技术及钒产业发展前景分析[J].钢铁钒钛, 2012, 33 (1) :1.)
[2] Moskalyk P, Alfantazi M.Processing of vanadium:a review[J].Mineral Engineering, 2003, 16 (9) :3.
[3] Zhou J Z.Development of vanadium industrial in China[A].International Conference of Vanadium[C].Guilin, 1999.34. (周家棕.中国钒工业的发展[A].钒国际会议[C].桂林, 1999.34.)
[4] Zhang G B, Zhang Y M, Huang J.Raffinate recycling utilization of vanadium extraction from stone coal[J].Chinese Journal of Rare Metals, 2013, 37 (6) :952. (张国斌, 张一敏, 黄晶.石煤提钒萃余液的循环利用研究[J].稀有金属, 2013, 37 (6) :952.)
[5] Cai J Q, Ba L.Several new techniques for extracting vanadium from stone coal[J].Conservation and Utilization of Mineral Resources, 1993, 5 (3) :30. (蔡晋强, 巴陵.石煤提钒的几种新工艺[J].矿产保护与利用, 1993, 5 (3) :30.)
[6] Zhang Z H, Wang Y H.A new process of vanadium extraction from silica based vanadium ore by oxidation roasting with calcium compounds[J].Chemistry World, 2000, 41 (6) :1. (张中豪, 王彦恒.硅质钒矿氧化钙化焙烧提钒新工艺[J].化学世界, 2000, 41 (6) :1.)
[7] Zou X Y, Peng Q J, Ouyang Y Z.Research on the roasting process with calcium compounds for silica based vanadium ore[J].The Chinese Journal of Process Engineering, 2001, 51 (2) :291. (邹晓勇, 彭清静, 欧阳玉祝.高硅低钙钒矿的钙化焙烧过程[J].过程工程报, 2001, 51 (2) :291.)
[8] Ma R J.Hydrometallurgical Principle[M].Beijing:Metallurgical Industry Press, 2007.324. (马荣骏.湿法冶金原理[M].北京:冶金工业出版社, 2007.324.)
[9] Rohrmann B.Vanadium in South Africa[J].Journal of the South African Institute of Mining and Metallurgy, 1985, 85 (5) :39.
[10] Tian Y W, Zhai X J, Liu K R.Short Course of Metallurgical Physical Chemistry[M].Beijing:Chemical Industry Press, 2007.225. (田彦文, 翟秀静, 刘奎仁.冶金物理化学简明教程[M].北京:化学工业出版社, 2007.225.)
[11] Post K, Robins R.Thermodynamic diagrams for the vanadium-water system at 298.15 K[J].Electrochimica Acta, 1976, 21 (6) :401.
[12] Mu W Z, Zhang T A, Dou Z H.New progress of extraction vanadium by hydrometallurgical technology[A].National Nonferrous Metals Industry Proceedings Excellent Essay Contest[C].Beijing:The Nonferrous Metals Society of China, 2011.43. (牟望重, 张廷安, 豆志河.钒渣湿法提钒技术新进展[A].全国有色行业论文大赛优秀论文集[C].北京:中国有色金属学会, 2011.43.)
[13] Larson J.Thermochemistry of vanadium in aqueous solutions[J].Journal of Chemical Engineering Data, 1995, 40 (6) :52.
[14] Yang X W.Handbook of Thermodynamic Data in Aqueous Solutions at High Temperature[M].Beijing:Metallurgical Industry Press, 1983.523. (杨显万.高温水溶液热力学数据计算手册[M].北京:冶金工业出版社, 1983.523.)
[15] Zhang T A, Mu W Z, Dou Z H.Potential-pH diagrams for V-Fe-H2O system during oxygen pressure acid leaching of vanadium-bearing converter slags[J].Chinese Journal of Nonferrous Metals, 2011, 21 (11) :2936. (张廷安, 牟望重, 豆志河.转炉钒渣氧压酸浸过程V-Fe-H2O系的电位-pH图[J].中国有色金属学报, 2011, 21 (11) :2936.)