���Ƚ���̿���ƽ�̿�ӻ���Ӧ����ѧ
����־1, 2��������1��������1
(1. ֣�ݴ�ѧ ��������ԴѧԺ������ ֣�ݣ�450001��
2. ���Ͻ���ѧԺ ��ѧϵ������ ֣�ݣ�450046)
ժҪ�����б��Ƚ���̿���ƽ�̿�ӻ���Ӧ����ѧʵ�飬��δ��Ӧ������ģ�ͱ�������ѧʵ�����ݣ��������Ƚ���̿���ƽ�̿�ӻ���Ӧ����ѧģ�ͣ�ȷ��ģ�Ͳ���������������ѧģ�ͣ���������ƽ�̿�ӻ���Ӧ�����е��������ɢ������g/�Ʀǡ��������ɢ������D/�ƦǺ���Խ��淴Ӧ������C/�Ʀǡ��о������������Arrhenius���̵õ����Ƚ���̿���ƽ�̿�ӻ���Ӧ�Ļ��Ea=217.0 kJ/mol����Ч��ɢ���ED=162.9 kJ/mol�������ڿհ�̿�ӻ���Ӧ�Ļ��Ea=142.0 kJ/mol����Ч��ɢ���ED=96.30 kJ/mol�����Ƚ�̿���ƽ�̿�ӻ���Ӧ��ʼ����Ҫ�ܽ��滯ѧ��Ӧ������ɢӰ�죬���ŷ�Ӧ���У��ӻ���Ӧ������ɢ�����滯ѧ��Ӧ������ɢͬʱӰ�죻�ڽϵ��¶��£���̿�ӻ���Ӧ��Ҫ�ܽ��滯ѧ��Ӧ���ƣ��淴Ӧ�¶����ߣ����滯ѧ��Ӧ������������½���
�ؼ��ʣ���̿�����Ƚ�̿�������ӻ���Ӧ��ģ�ͣ�����ѧ
��ͼ����ţ�TQ520��TF526.1 ���ױ�־�룺A ���±�ţ�1672-7207(2013)06-2583-08
Kinetics of inhibition reaction to coke deterioration by Benzene pyrolysis carbons
ZHANG Zezhi1, 2, WANG Liucheng1, WANG Fuan1
(1. School of Chemical and Energy Engineering, Zhengzhou University, Zhengzhou 450001, China;
2. Department of Chemistry, Henan Institute of Education, Zhengzhou 450046, China)
Abstract: The kinetics data of inhibition reaction to coke deterioration by benzene pyrolysis carbons were obtained to establish the models of the reaction and to determine model parameters using unreacted shrinking reaction core model. According to the kinetics models, the relative resistances of external diffusion ��g/�Ʀ�, the relative resistances of internal diffusion ��D/�Ʀ�, and the relative resistance of surface chemical reaction ��C/�Ʀ�, were calculated. The results show that based on Arrhenius equation, the activation energy Ea=217.0 kJ/mol and the effective diffusion activation energy ED=162.9 kJ/mol of the inhibition reaction of coke samples infiltrated by benzene pyrolysis carbons are both higher than those of the blank coke samples, Ea=142.0 kJ/mol and ED=96.30 kJ/mol, respectively. The inhibition reaction to deterioration is mainly affected by surface chemical reaction and external diffusion at the beginning of the reaction and then by internal diffusion, external diffusion and surface chemical reaction simultaneously. In addition, the inhibition reaction to deterioration is affected by the surface chemical reaction at the lower reaction temperatures, and then ��C/�Ʀ� decreases with the increase of the reaction temperatures.
Key words: coke; benzene pyrolysis carbons; inhibition reaction to deterioration; model; kinetics
��̿�Ǹ�����ҵ��Ϊ��Ҫ��ԭ�ϣ���������Դ����ԭ������̼����¯�����Ǽ����á����Ÿ�¯�ݻ�����ú�ȵ�����̿�ĹǼ������Ե���Ϊ��Ҫ����̿�ڸ�¯�������ܵ�CO2�Ȼ�ѧ��ʴ�����ӻ���Ӧ����ɽ�̿�����ӻ���ǿ���½����Ǽ����ü������谭��¯ұ��˳�������ӽ��ȣ����˷���Դ�����������������ŷţ���ˣ������ƽ�̿�ӻ��������о��϶�[1-4]����¯ұ�������н�̿��CO2�������ӻ���Ӧ������-�̷Ǿ��෴Ӧ���䷴Ӧ����ѧ�о��Ƿ�Ӧ����̽�֡������ӻ������з�����Ӧ����ơ���ҵ�������Ż�����Ҫ������������ѧ�ߴӲ�ͬ�ǶȺ������������������ѧ��Ӧģ�͡�Poterson���ģ�͡����ҡ������ˡ�ģ�͡���ɢ-�������Ͽ���ģ�͡�δ��Ӧ������ģ�͵ȸ�¯ұ�������н�̿�ӻ���Ӧ����ѧģ��[5-10]���������ƽ�̿�ӻ���Ӧ����ѧ���о����١���������ּ��ǰ���о�[11]�����Ͻ��б��Ƚ���̿���ƽ�̿�ӻ���Ӧ����ѧʵ�飬��������ѧģ�ͣ�ȷ������ѧ�������Ա�Ϊ���Ƚ���̿���ƽ�̿�ӻ�������ҵ���ṩ�ο���
1 ʵ��
1.1 ���Ϻ�����
�����У���̿�����ּ��Ž�������������(����������99.5%)�������л�ѧ�Լ���������������̼(���ȣ�99. 999%)��֣�ݿ�����������˾����������(���ȣ�99. 999%)��֣�ݿ�����������˾������
�����У�NOVA4200e�ȱ��������϶�ȷ����ǣ�QUANTACHROME��˾���죻���ط�����TGA/SDTA851e��METTLER-TOLEDO��˾���졣
1.2 ʵ�鷽��
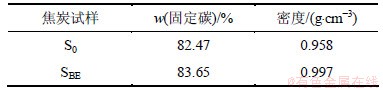
����̿�Ƴ�����Ϊ(10��1) mm �Ľ����ɸ��ɺ��ã�������[11]������ʵ�鷽�������������Ƚ�̿�������ڽ�̿�����Ƶ����ƽ�̿�ӻ���Ӧ����ѧʵ��������SBE������SBE����Ϊ�ԱȵĿհ�̿����S0�Ĺ̶�̼���ܶ�(��)�Ȼ�����������1��
��ѹ�£��������ط����Dzⶨ������һ����Ӧ�¶Ⱥͷ�Ӧʱ���µ��ӻ���Ӧ��x��ȷ����һ������m0�Ľ�̿�����������ط������У���ͨ��ߴ��������������÷�Ӧ�¶ȷֱ�Ϊ1 223��1 323��1 423��1 523 K�������ﵽ�趨�¶��ȶ��رյ���ͨ��CO2���壬��������Ϊ50 mL/min��ÿ5 min��ȡ1����������������ʽ���������ӻ���Ӧ��x��
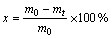 (1)
(1)
ʽ�У�m0Ϊ��̿������ʼ������g��mtΪtʱ�̽�̿����������g��
��1 ��̿������������
Table 1 Parameters of coke samples
2 ���������
2.1 ���Ƚ���̿���ƽ�̿�ӻ���Ӧ����ѧʵ����
ʵ���ò�ͬ��Ӧ�¶�T����ͬ��Ӧʱ��t�±��Ƚ���̿���ƽ�̿�ӻ���Ӧ��x(��ͼ1)��Ϊ�˱Ƚϣ�����ͬ���������δ�����Ƚ�̿�������Ľ�̿����S0����ͬ�����µ��ӻ���Ӧ�ʣ���ͼ1��
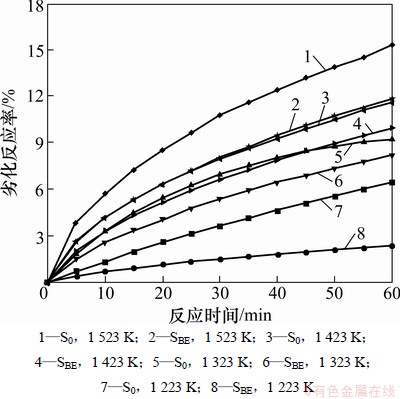
ͼ1 ��ͬ��Ӧ�¶��½�̿�����ӻ���Ӧ���淴Ӧʱ��ı仯
Fig. 1 Variations in deterioration reaction rates of coke samples with reaction time at different temperatures
2.2 ���ƽ�̿�ӻ���Ӧ����ѧģ��
���Ƚ���̿���ƽ�̿�ӻ���Ӧ��Ҫ�ǹ��役̿������CO2��ķǾ��෴ӦΪ
C(s)+CO2(g)=2CO(g)
�ڷ�Ӧ�����У�����CO2����役̿������ɢ�γ�����߽�㣬CO2�������ڹ����������C���н��淴Ӧ��������̬CO�ͽ����ɵĹ������㣬��������CO�����뿪�������������ɢ��CO2�ܹ�ͨ���ù���������ɢ��δ��Ӧ�˱��棬����巴Ӧ��C������ѧ��Ӧ�����淴Ӧ�Ľ��У����巴Ӧ��ĺ�������С��ֱ����ȫ��ʧ����ͼ2��ʾ��
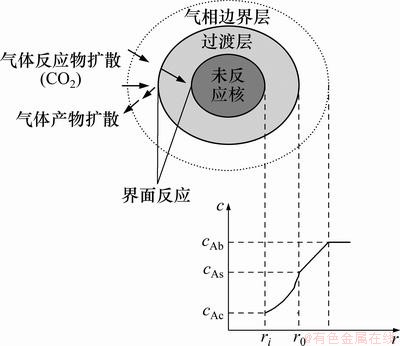
ͼ2 δ��Ӧ������ģ��ʾ��ͼ
Fig. 2 Schematic diagram of unreacted shrinking reaction core model
��Ȼ������һ����������ɢ������ɢ�����������淴Ӧ���Ѹ���һϵ�л�Ԫ��Ӧ�����̷Ǿ��ิ�ӷ�Ӧ[12-13]���Դ˸��ӷ�Ӧ�����IJ�������[13]��δ��Ӧ������ģ�ͽ��б�����
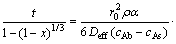
 (2)
(2)
ʽ�У�xΪ��̿�ӻ���Ӧ�ʣ�%��tΪ�ӻ���Ӧʱ�䣬min��r0Ϊ������ʼ�����뾶��m����Ϊ�����ܶȣ�g/cm3����Ϊ������״ϵ����DeffΪ��Ч��ɢϵ����m2/s��ksΪ��Ӧ���ʳ�����m/s��cAb��cAs�ֱ�ΪCO2������߽��Ũ�Ⱥ����������ƽ��Ũ�ȣ�mol/m3��
���Ƚ���̿���ƽ�̿�ӻ���Ӧ�ﵽ����̬ʱ����һ����Ӧ�¶��¶��ڸ�����������r0���ѣ�Deff��ks������cAs����Ϊ��ֵ���뷴Ӧʱ���ء�cAb���뷴Ӧʱ���йأ����ڱ��о�������Χ�ڿ���Ϊ��ֵ����ˣ�ʽ(2)�У���
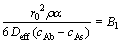 (3)
(3)
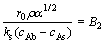 (4)
(4)
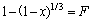 (5)
(5)
ʽ�У�B1��B2�ֱ�Ϊʽ(3)��(4)����ij�����FΪ���ȡ���ʽ(2)�ɸ�дΪ
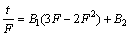 (6)
(6)
��ͼ1�б��Ƚ���̿���ƽ�̿�ӻ���Ӧ����ѧʵ�����ݣ���ʽ(6)��t/F��3F�C2F2��ͼ����ͼ3��
��ͼ3������t/F��3F�C2F2֮�������ֱ�߹�ϵ���������Ƚ���̿���ƽ�̿�ӻ���Ӧ����ѧʵ��������ʽ(6)��ϡ���ˣ����Ƚ���̿���ƽ�̿�ӻ���Ӧ����ѧ����δ��Ӧ������ģ����������õĿհ�̿�ӻ���Ӧ����ѧʵ������ͬ������δ��Ӧ������ģ�ͣ���ͼ4��ʾ��
2.3 ����ѧģ�Ͳ�����ģ�͵�ͳ�Ƽ���
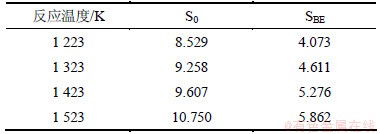
��ʽ(6)�Զ���ѧʵ����������С���˷�������÷��̲���B1��B2�����ϵ��r2����2���ɱ�2���Կ���������B1��B2�����¶����߶���С������ͬ�¶��£�SBE�����IJ���B1��B2�ֱ��������S0����Ӧ����B1��B2��
��2 ��̿�����Ķ���ѧģ�Ͳ���
Table 2 Parameters of kinetic models of coke sample of S0 and SBE, respectively
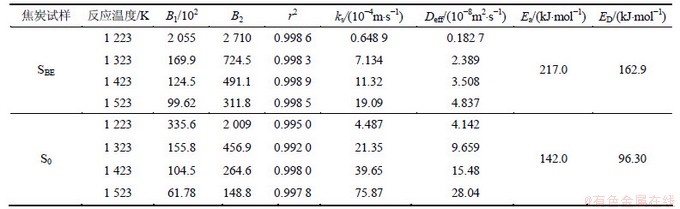
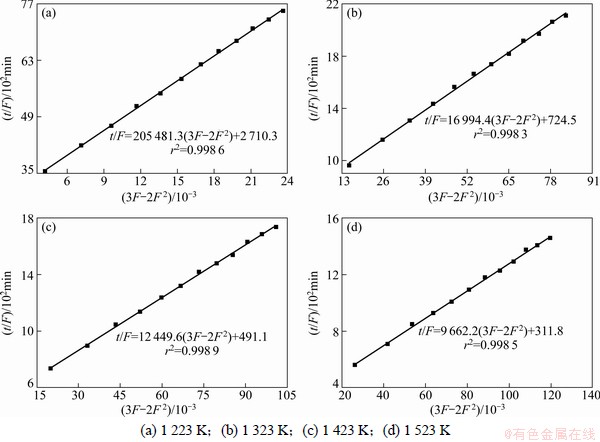
ͼ3 ��ͬ��Ӧ�¶�������SBE��t/F��(3F-2F2)�Ĺ�ϵ
Fig. 3 Relationship between t/F and (3F-2F2) of coke sample SBE at different temperatures
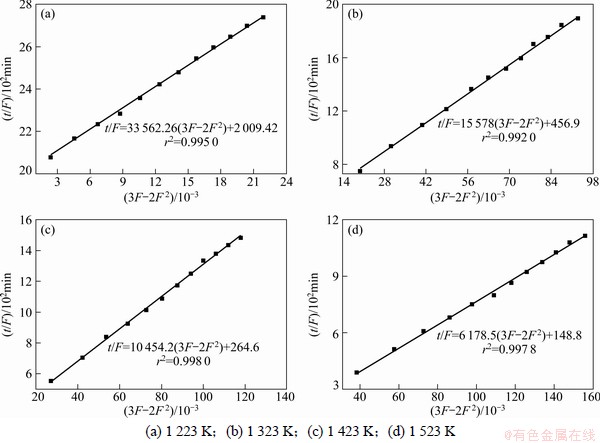
ͼ4 ��ͬ��Ӧ�¶�������S0��t/F��(3F-2F2)�Ĺ�ϵ
Fig. 4 Relationship between t/F and (3F-2F2) of coke sample S0 at different temperatures
��Ч��ɢϵ��Deff�ͷ�Ӧ���ʳ���ks�ɱ�2�в���B1��B2��ʽ(3)��(4)���㡣���������뾶r0����״ϵ�����ֱ���ʽ���㣺
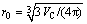 (7)
(7)
 (8)
(8)
ʽ�У�VCΪ�������������m3��S��Ϊ���������������ȵ���ı������m2��S��Ϊ���������������m2�������㣬�õ�r0=0.004 99 m����=0.892��
ʵ��������CO2Ũ��cAb����������״̬���̼��㣺
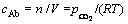 (9)
(9)
ʽ�У�nΪCO2�����ʵ�����mol��VΪ��Ӧ���������m3��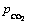 Ϊ��Ӧ������CO2ѹ����ȡ105 Pa��TΪ��Ӧ������ѧ�¶ȣ�K��RΪĦ�����峣����ȡ8.314 J/(mol��K)����Ӧƽ��ʱCO2��Ũ�������ƽ�̿�ӻ���Ӧ��Ҫ����ʽ�Ļ�ѧƽ�ⳣ������������ѧ[14]���淽�����㡣
Ϊ��Ӧ������CO2ѹ����ȡ105 Pa��TΪ��Ӧ������ѧ�¶ȣ�K��RΪĦ�����峣����ȡ8.314 J/(mol��K)����Ӧƽ��ʱCO2��Ũ�������ƽ�̿�ӻ���Ӧ��Ҫ����ʽ�Ļ�ѧƽ�ⳣ������������ѧ[14]���淽�����㡣
�ɴ˼���õ���ͬ��Ӧ�¶�����Ч��ɢϵ��Deff�ͷ�Ӧ���ʳ���ks������2���ɱ�2���Կ��������ڱ��Ƚ�̿�������Ľ�̿����SBE������Ч��ɢϵ��Deff�ͷ�Ӧ���ʳ���ks������С��ͬ���¿հ�����S0����Ӧֵ���ҷ�Ӧ���ʳ���ks ����Ч��ɢϵ��Deff���¶����߳����������ơ�
������Ӧ�¶��µķ�Ӧ���ʳ���ks����Ч��ɢϵ��Deff�ֱ�Arrhenius������ʽ(10)��ʽ(11)������ϣ���õķ�Ӧ���Ea����Ч��ɢ���ED����2���ӱ�2���Կ���������SBE�ķ�Ӧ���Ea����Ч��ɢ���ED����������S0����Ӧֵ��˵�����Ƚ���̿�ܹ��谭��������̿��CO2�ӻ���Ӧ�����ƽ�̿��̬����[1, 11]��
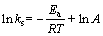 (10)
(10)
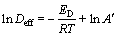 (11)
(11)
��������ͳ�Ƶķ���������ģ�ͽ��м��飬��3�г��˱��Ƚ���̿���ƽ�̿�ӻ���Ӧ��x��ģ�ͼ���ֵxC��ʵ��ֵx�Ƚϵ�F���鼰���ϵ��r2��F����ʽ����[15-16]��
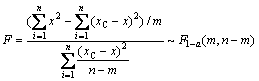 (12)
(12)
��ͳ����ѧ�о�[17-18]��Ϊ����ģ�����ϵ��r2����0.9ʱ����ѧ�����ǿɿ��ģ���F����10Faʱ�����ö���ѧ�����Ǹ߶������ġ��ӱ�3���Կ�����ʵ���¶������ö���ѧ���̵�r2������0.900 0��F�����10F0.05��˵������ѧ�����ǿɿ��ģ����и߶������ԡ�
��3 ����ѧģ�͵�ͳ�Ƽ���
Table 3 Statistical tests of kinetic models
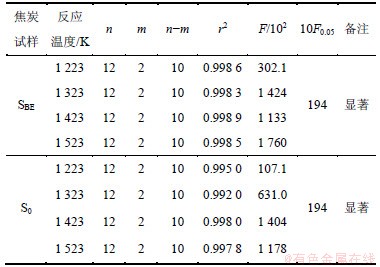
���˷�Ӧ����ѧģ�Ͳ������Ϳ��Լ�����һ��Ӧ�¶���һ��Ӧʱ���µķ�Ӧ�ʡ��о�������4���¶���96��ʵ������ģ�ͼ���ֵ��ʵ��ֵ��Ƚϵ���ƽ��������Ϊ2.1%��˵������ģ���ܽϺõط�ӳ���Ƚ���̿���ƽ�̿�ӻ���Ӧ���ԣ�Ϊ��Ӧ����ơ������Ż��ͷ�Ӧ����̽���ṩ���ݡ�
2.4 ���ƽ�̿�ӻ���Ӧ�����и����������������
���ƽ�̿�ӻ���Ӧ�����и����������������������δ��Ӧ������ģ�Ͱ����·��̼��㲻ͬ��Ӧ�¶ȡ���ͬ��Ӧʱ�������ɢ������g������ɢ������D �ͽ��淴Ӧ������C��
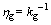 (13)
(13)
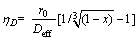 (14)
(14)
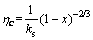 (15)
(15)
ʽ�У�r0Ϊ���������뾶��m��kgΪ����߽�㴫��ϵ����m/s��
����߽�㴫��ϵ��kg���������崫�ʹ��̣����������εĴ��������̼���[7]��
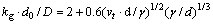 (16)
(16)
ʽ�У�d0Ϊ��������ֱ����m��vt ΪCO2 �����ڷ�Ӧ�������٣�m/s��dΪ��Ӧ�ܹܾ���m��DΪ����߽����CO2-CO������ɢϵ����m2/s����Ϊ�����˶��ȣ�m2/s��
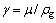 (17)
(17)
ʽ�У���Ϊ������ȣ�Pa��s����gΪ������ܶȣ�kg/m3��
���ܶȶ�����������������Wilke����[7, 11]���㣺
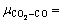
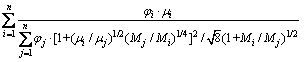 (18)
(18)
ʽ�У�M Ϊ����Ħ��������g/mol����iΪ����i�������������iΪ����i���ȡ�
����߽����CO2-CO�ķ�����ɢϵ��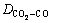 ����ʽ����[7]��
����ʽ����[7]��
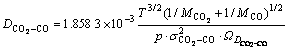 (19)
(19)
ʽ�У�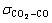 Ϊ��ײֱ����
Ϊ��ײֱ����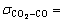
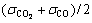 ��pΪϵͳѹ��(0.1 MPa)��
��pΪϵͳѹ��(0.1 MPa)��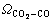 Ϊ�������¶�
Ϊ�������¶�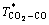 ʱCO2-CO ����������ײ���֣�
ʱCO2-CO ����������ײ���֣�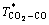 ����ʽ(20)��(21)���㡣
����ʽ(20)��(21)���㡣
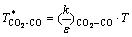 (20)
(20)
 (21)
(21)
ʽ�У�CO��CO2��Lennard-Jones������/kȡ������[19]��
����ʽ(16)~(21)���㣬�õ���ͬ��Ӧ�¶�������߽�㴫��ϵ��kg���������4��
��4 ��̿����SBE��S0�ڲ�ͬ��Ӧ�¶��µ�kg
Table 4 kg of coke samples at different temperatures 103
��ʽ(13)~(15)�ɼ��㱽�Ƚ���̿���ƽ�̿�ӻ���Ӧ�����в�ͬ��Ӧ�������������ɢ������g/�Ʀǡ��������ɢ������D/�ƦǺ���Խ��淴Ӧ������C/�Ʀ�(���СƦ�=��g+��D+��C)�������ͼ5����Ϊ�Աȣ��հ�̿����S0�ӻ���Ӧ�����и����������������ͼ6 ��ʾ��
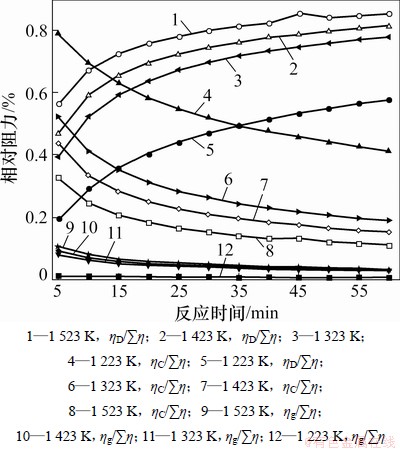
ͼ5 ��ͬ��Ӧ�¶�������SBE�����ӻ���Ӧ�����и�������������淴Ӧʱ��ı仯
Fig. 5 Variations of relative reaction resistance of various steps of sample SBE with reaction times at different temperatures in process of inhibition reaction to deterioration
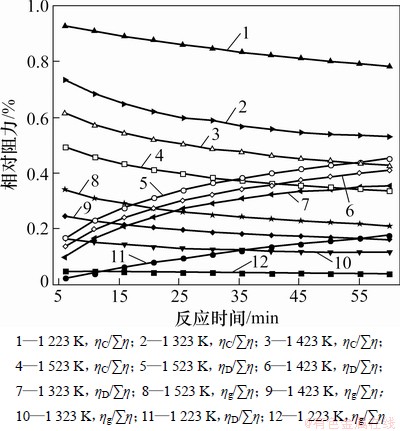
ͼ6 ��ͬ��Ӧ�¶�������S0�ӻ���Ӧ�����и�������������淴Ӧʱ��ı仯
Fig. 6 Variations of relative reaction resistance of various steps of sample S0 with reaction times at different temperatures in process of deterioration reaction
��ͼ5��ͼ6���Կ�������ʵ�������£���̿�ӻ���Ӧ����ʼ�����ڷ�Ӧ�����ϱ�����һ���̶��Ϸ�Ӧ��Ҫ�ܽ��滯ѧ��Ӧ������ɢӰ�죻���ŷ�Ӧ���У��ӻ���Ӧ������ɢ�����滯ѧ��Ӧ������ɢͬʱӰ�졣��̿�������������ṹ���ɣ����滯ѧ��Ӧ���ʽϿ죬����Ӧ������С����������ɢ����ռ���������������ߡ��ڽϵ��¶��£���̿�ӻ���Ӧ��Ҫ�ܽ��滯ѧ��Ӧ���ƣ��淴Ӧ�¶����ߣ����滯ѧ��Ӧ�����������C/�Ʀ����½���
����ͬ�ӻ���Ӧ�¶Ⱥͷ�Ӧʱ���£�����SBE�ķ�Ӧ������������ͬ����������S0�ķ�Ӧ��������˵�����Ƚ���̿�ܹ�����̿�ӻ���Ӧ����������CO2�뽹̿�����ӻ���Ӧ��
3 ����
(1) �������ط�������ʵ���ò�ͬ��Ӧ�¶ȡ���ͬ��Ӧʱ���±��Ƚ���̿���ƽ�̿�ӻ���Ӧ����ѧ���ݡ�
(2) ���Ƚ���̿���ƽ�̿�ӻ���Ӧ��һ������������ɢ�����Ѹ������淴Ӧ��һϵ�л�Ԫ��Ӧ����-�̷Ǿ��ิ�ӷ�Ӧ������ѧʵ������δ��Ӧ������ģ����ϣ������˱��Ƚ���̿���ƽ�̿�ӻ���Ӧ����ѧģ�ͣ�ȷ���˶���ѧģ�Ͳ�����ͳ�Ƽ���������������Ƚ���̿���ƽ�̿�ӻ���Ӧ����ѧģ���������Ϳ��ŵģ�����Ϊ��Ӧ����ơ������Ż��ͷ�Ӧ����̽�ֵ����ݡ�
(3) ���Ƚ���̿���ƽ�̿�ӻ���Ӧ��ܺ���Ч��ɢ��ֱܷ�Ϊ217.0��162.9 kJ/mol�����Ը��ڿհ�̿�ӻ���Ӧ���142.0 kJ/mol����Ч��ɢ���96.30 kJ/mol��
(4) ����������ѧģ�ͻ����ϼ�������Ƚ���̿���ƽ�̿�ӻ���Ӧ������ʵ�������µ��������ɢ������g/�Ʀǡ��������ɢ������D/�ƦǺ���Խ��淴Ӧ������C/�Ʀǣ��������ƽ�̿�ӻ���Ӧ����ʼ����Ҫ�ܽ��淴Ӧ������ɢӰ�죬���ŷ�Ӧ���У��ӻ���Ӧͬʱ������ɢ�����淴Ӧ������ɢӰ�졣
�ο����ף�
[1] ZHANG Zezhi, WANG Liucheng, WANG Fuan, et al. Inhibition to coke deterioration by benzene pyrolysis using response surface methodology[J]. Coke and Chemistry, 2012, 55(6): 222-230.
[2] Fernandez A M, Barriocanal C, Alvarez R. The effect of additives on coking pressure and coke quality[J]. Fuel, 2012, 95: 642-647.
[3] Bogolova V V, Sultanguzin I A, Gyulmaliev A M. Enhancing coke quality in dry slaking[J]. Coke and Chemistry, 2011, 54(10): 362-365.
[4] Koszorek A, Krzesi��ska M, Pusz S, et al. Relationship between the technical parameters of cokes produced from blends of three Polish coals of different coking ability[J]. International Journal of Coal Geology, 2009, 77(3/4): 363-371.
[5] ����, ɭɽ��. ұ��Ӧ����[M]. ��־��, лԣ�� ��. ����: ��ѧ������, 1981: 284-285.
Muchi I, Moriyama A. Reaction engineering in metallurgical[M]. CAI Zhipeng, XIE Yusheng, trans. Beijing: Science Press, 1981: 284-285.
[6] Szekely J, Aderibigbe D A. Structural changes and reactivity of conventional coke and from coke during reaction with CO-CO2 gas mixture at 1 000 ��[J]. Ironmaking and Steelmaking, 1982, 9(3): 130-135.
[7] ��ƽ, ����, ����, ��. ��̿����Ӧ����ѧ����ģ���о�[J]. ȼ�ϻ�ѧѧ��, 2006, 34(3): 280-284.
CUI Ping, ZHANG Lei, YANG Min, et al. Study on kinetics and model of coke loss reaction with CO2 in blast furnace[J]. Journal of Fuel Chemistry and Technology, 2006, 34(3): 280-284.
[8] ����, ������, �����,��. ����ѧ�����½�̿�����������Ե�ģ���о�[J]. ȼ�ϻ�ѧѧ��, 2009, 37(1): 31-35.
ZHOU Wei, LUO Yonghao, WU Guojiang, et al. Modeling the gasification characteristics of char particle under kinetics control[J]. Journal of Fuel Chemistry and Technology, 2009, 37(1): 31-35.
[9] Omori K. Blast furnace phenomena and modeling[M]. London: Elsevier Applied Science, 1987: 97-296.
[10] Shunji H, Shinji O, Jiro K, et al. Gas-solid reaction model for a shrinking spherical particle with unreacted shrinking core[J]. Chemical Engineering Science, 2005, 60(18): 4971-4980.
[11] ����־. ��̿�ӻ����Ƽ������ƹ��̻����о�[D]. ֣��: ֣�ݴ�ѧ��������ԴѧԺ, 2012: 54-81.
ZHANG Zezhi. Fundamental research on the deterioration inhibitors of coke and its inhibitory process[D]. Zhengzhou: Zhengzhou University. School of Chemical and Energy Engineering, 2012: 54-81.
[12] �쿪��, Ԭμ��. ��ѧ��Ӧ���̷���[M]. ����: �ߵȽ���������, 2002: 220-227.
ZHU Kaihong, YUAN Weikang. Chemical reaction engineering analysis[M]. Beijing: Higher Education Press, 2002: 220-227.
[13] ��Ԫ��, ������. ұ��������ѧ[M]. �Ϸ�: �Ϸʹ�ҵ��ѧ������, 2011: 293-299.
DONG Yuanchi, WANG Haichuan. Metallurgy physical chemistry[M]. Hefei: Hefei University of Technology Press, 2011: 293-299.
[14] Smith J M, van Ness H C, Abbott M M. Introduction to chemical engineering thermodynamics[M]. 7th ed. New York: McGraw-Hill, 2005: 206-237.
[15] κ�鳯, ������, ����. LB�ͽ��ܴ����ϸ��±任��Ӧ��������ѧ����ҵ���ⶨ[J]. ����ѧ��, 2008, 59(9): 2232-2240.
WEI Lingchao, WANG Fuan, LIU Yi. WGS reaction intrinsic kinetics and industrial measurement over LB energy-saving high temperature shift catalyst[J]. Journal of Chemical Industry and Engineering, 2008, 59(9): 2232-2240.
[16] κ�鳯. LB�ͽ��ܸ��±任�������̻����о�[D]. ֣��: ֣�ݴ�ѧ��������ԴѧԺ, 2009: 131.
WEI Lingchao. The engineering fundamental research of LB energy-saving high temperature shift catalyst[D]. Zhengzhou: Zhengzhou University. School of Chemical and Energy Engineering, 2009: 131.
[17] ��ɽ, �����, ��ԪԪ, ��. ����ʯȥ��ˮ���и�Ũ�������εķ�Ӧ����ѧ[J]. ���ϴ�ѧѧ��: ��Ȼ��ѧ��, 2010, 41(5): 2039-2045.
ZHONG Shan, WANG Liao, LIU Yuanyuan, et al. Kinetics of concentrated phosphate removal by calcite[J]. Journal of Central South University: Science and Technology, 2010, 41(5): 2039-2045.
[18] Haeno H, Gonen M, Davis M B. Computational modeling of pancreatic cancer reveals kinetics of metastasis suggesting optimum treatment strategies[J]. Cell, 2012, 148(1): 362-375.
[19] ������, ���Ǹ�. �������ݵ���[M]. ����: ��ѧ��ҵ������, 1995: 26-30.
WANG Fuan, JIANG Denggao. Guidance of chemical data[M]. Beijing: Chemical Industry Press, 1995: 26-30.
(�༭ ����ƽ)
�ո����ڣ�2012-07-25�������ڣ�2012-09-16
������Ŀ������ʡ�ش����Կ�����Ŀ(08110911800)
ͨ�����ߣ�������(1938-)���У����������ˣ����ڣ���ʿ����ʦ��������ɫ���̹����о����绰��0371-63888116��E-mail��fawang@zzu.edu.cn