熔体结构对钢包渣脱氧速率的影响
张志祥,闵义,王德永,姜茂发
(东北大学 材料与冶金学院,辽宁 沈阳,110004)
摘 要:采用熔渣脱氧实验、动力学分析和实验渣熔体结构分析,对熔体结构对钢包渣脱氧速率的影响进行研究。研究结果表明:初始Al2O3的质量分数和碱度(二元碱度,w(CaO)/w(SiO2))对熔渣初始脱氧速率具有重要影响;铁离子扩散是熔渣脱氧反应的控制环节;随Al2O3的质量分数的提高,熔渣聚合程度增强,黏度升高,铁离子平均扩散直径减小,铁离子扩散系数先增大后减小;随着碱度增大,熔渣聚合程度减弱,黏度降低,铁离子平均扩散直径增大,铁离子扩散系数也呈先增大后减小的趋势;铁离子扩散系数变化趋势与熔渣初始脱氧速率变化趋势相一致。为提高LF精炼过程钢包渣脱氧速率,LF(Ladle furnace)精炼前钢包渣改质的成分调整控制目标为:w(CaO)/w(SiO2)=4~5,w(Al2O3)=18%~20%。
关键词:钢包渣;脱氧;扩散直径;黏度;扩散系数
中图分类号:TF 044 文献标志码:A 文章编号:1672-7207(2011)01-0001-06
Effect of silicate melt structure on deoxidization velocity of ladle slag
ZHANG Zhi-xiang, MIN Yi, WANG De-yong, JIANG Mao-fa
(School of Materials & Metallurgy, Northeastern University, Shenyang 110004, China)
Abstract: The effect of silicate melt structure on deoxidization velocity of ladle slag was studied using the lade slag deoxidization experiment. The results show that the initial deoxidization rate is affected by the original content and basicity of Al2O3. And the diffusion of iron ions is the controlling factor of deoxidization reaction. With the increase of Al2O3 content, the polymerization degree of molten slag increases, the viscosity increases and the average diffusion diameter of iron ions decreases, thereby the diffusion coefficient of iron ions increases then decreases when exceeding a critical Al2O3 content; with the increase of basicity, the polymerization degree of molten slag decreases, the viscosity decreases and the average diffusion diameter of iron ions increases, so the diffusion coefficient of iron ions increases then decreases when basicity exceeds a critical value. The variation tendencies of initial deoxidization rate is in coincide with diffusion coefficient of iron ions. To enhance the deoxidization rate of ladle slag, the composition of ladle slag should be modified with w(CaO)/w(SiO2)=4-5, w(Al2O3)=18%-20% before LF refining.
Key words: ladle slag; deoxidization; diffusion diameter; viscosity; diffusion coefficient
在现代纯净钢冶炼尤其是管线钢等超低硫钢[1]冶炼中,LF(Landle furnace)白渣精炼功能发挥着重要作用。为实现白渣精炼功能,必须对钢包渣进行改质。钢包渣改质工艺一般包括2步:一是在出钢过程中通过加入复合精炼渣等改质剂调整钢包渣成分,改质后钢包渣依然具有较高的氧化性;二是在LF精炼过程中加入金属铝等还原剂对钢包渣脱氧。在工业生产中,由于钢包渣氧化性降低速率低,从而导致精炼效果差、精炼周期长,制约了生产效率的提高。前人的研究多集中于钢包渣改质剂的组成及其加入工艺等对钢包渣脱氧和精炼效果的作用[2-3],对钢包渣脱氧速率的研究较少。影响钢包渣脱氧速率的因素包括脱氧剂种 类、粒度、加入工艺等,另外,成分对钢包渣脱氧过程也具有重要影响。钢包渣成分变化将导致熔体结构发生变化,进而影响熔渣中离子的存在形式及扩散行为[4-7],即影响熔渣脱氧的动力学过程。本文作者根据LF精炼渣组成,针对CaO-SiO2-MgO-Al2O3-FexO渣系进行钢包渣脱氧实验研究,并基于熔体结构理论分析成分对钢包渣脱氧速率的影响。
1 实验方法
实验用钢包渣采用分析纯化学试剂配置而成,按照工业生产钢包渣的成分,MgO的质量分数保持不变,均为8%;熔渣氧化性采用Fe2O3配入量控制,质量分数为11.11%。为考察碱度(二元碱度,w(CaO)/ w(SiO2),下同)和Al2O3质量分数对脱氧速度的影响,碱度分别取3,5和7;Al2O3质量分数分别为5%,15%,20%和25%。采用工业纯铝颗粒作还原剂,考虑到烧损及SiO2的还原,加入量为完全还原Fe2O3用量的1.5倍。金属铝粒度为3~5 mm,可确保其加入熔渣后3 s内迅速熔化[8]。实验用钢包渣成分见表1。
表1 钢包渣脱氧实验结果(质量分数)
Table 1 Experimental projects of ladle slag deoxidization

实验在高温管式电阻炉内进行,实验温度均为 1 823 K。渣料用内衬厚为0.1 mm钼片的高纯MgO坩埚盛放,坩埚内径为50 mm,深度为80 mm,壁厚为2 mm。外套石墨坩埚保护,石墨坩埚内径为60 mm,高度为120 mm,壁厚为10 mm。采用直径为10 mm的除锈钢棒蘸取熔渣。主要实验步骤如下:
(1) 按比例称取150 g渣料,混合均匀后装入MgO坩埚中,放入电阻炉内升温,并通入氩气保护;
(2) 达到实验温度,恒温30 min,取原始渣样并水冷;
(3) 用石英玻璃管将金属铝粒加入熔渣并搅 拌,分别在铝粒加入后1,3,5,10和15 min取渣样并水冷;
(4) 将所取渣样磨至粒度约75 μm,磁选去除金属铁,制样后采用荧光光谱仪对其成分进行分析。
2 实验结果
图1所示为不同Al2O3初始含量和初始碱度下,还原率随时间的变化关系。还原率计算方法如下式 所示:
 (1)
(1)
式中:Rredu为还原率; 为熔渣初始全铁含量(质量分数,下同);
为熔渣初始全铁含量(质量分数,下同); 为各取样时刻熔渣全铁含量。从图1可以看出,除了Al2O3初始质量分数为5%的实验外,熔渣脱氧速度很快,加入还原剂5 min后,还原率不再增加,脱氧反应基本结束。对比图1中1 min时的还原率可以看出,在初始碱度w(CaO)/w(SiO2)为3条件下,当Al2O3初始质量分数为20%时,还原率最高,为61.75%;当Al2O3初始质量分数为5%时,还原率最低,为40.61%;而当Al2O3初始质量分数为15%和25%时,其还原率介于二者之间。在初始Al2O3质量分数为20%时,还原率随碱度的增加而降低。
为各取样时刻熔渣全铁含量。从图1可以看出,除了Al2O3初始质量分数为5%的实验外,熔渣脱氧速度很快,加入还原剂5 min后,还原率不再增加,脱氧反应基本结束。对比图1中1 min时的还原率可以看出,在初始碱度w(CaO)/w(SiO2)为3条件下,当Al2O3初始质量分数为20%时,还原率最高,为61.75%;当Al2O3初始质量分数为5%时,还原率最低,为40.61%;而当Al2O3初始质量分数为15%和25%时,其还原率介于二者之间。在初始Al2O3质量分数为20%时,还原率随碱度的增加而降低。

图1 不同初始Al2O3含量和碱度下还原率随时间的变化
Fig.1 Variation of reduction rate with time at different initial Al2O3 contents and basicities
图2所示为根据实验结果计算出的熔渣1 min内的平均脱氧速率vav-1 min与熔渣初始Al2O3初始含量w(Al2O3)和碱度w(CaO)/w(SiO2)的关系。从图2可以看出:在初始碱度为3时,平均脱氧速率随初始Al2O3的初始质量分数的增加逐渐增大后具有降低的趋势;当初始Al2O3初始质量分数为20%时,平均脱氧速率随初始碱度的增大先升高后降低。可见:熔渣初始成分对脱氧速率具有重要影响。

图2 1 min内熔渣平均脱氧速度与初始Al2O3含量和碱度的关系
Fig.2 Relationship of average deoxidization rate and initial Al2O3 content and basicity within 1 min
3 熔渣脱氧过程动力学分析
3.1 脱氧反应的控制环节
金属铝粒加入熔渣后,形成熔融金属铝液滴,根据双膜理论,还原反应将在液态金属铝和熔渣所形成的界面上进行,可用式(2)和(3)表示:
Al+3Fe3+=Al3++3Fe2+ (2)
2Al+3Fe2+=2Al3++3Fe (3)
上述反应过程主要包括以下5步:熔渣中Fe2+和Fe3+向反应界面扩散;金属铝原子向反应界面扩散;界面化学反应;反应产物Al3+向熔渣中扩散;反应产物金属铁向金属铝中扩散。在高温条件下,界面化学反应速度很快,一般不会成为限制性环节;金属中原子的扩散系数通常比金属离子在熔渣的扩散系数大1~2个数量级,所以,金属铝和还原产物金属铁的扩散也不会成为限制性环节,反应的限制环节只能是金属离子在熔渣中的扩散。
熔渣中离子扩散系数可用Eyring方程[9]计算:
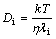 (4)
(4)
式中:Di为扩散系数,m2/s;k为玻尔兹曼常数,1.38×10-23 J/K;T为热力学温度,K;η为黏度,Pa・s;λi为扩散离子直径,m。从式(4)可以看出,在温度一定时,熔渣黏度越大,扩散离子直径越大,扩散系数越小。由于Al3+直径(0.114 nm)小于Fe3+直径(0.128 nm)和Fe2+直径(0.166 nm),反应速率主要受铁离子扩散的控制。熔渣成分决定了熔渣结构或聚合程度,进而决定了熔渣黏度和扩散离子直径,也就是说,熔渣成分通过黏度和扩散离子直径2个方面控制着脱氧反应 进程。
3.2 实验渣熔体结构
熔体结构复杂程度或聚合程度常用单位四面体中非桥氧的数目n(NBO/T) [10-13]表示,其值等于整个网络中氧的总化学键数与氧的桥氧键数之差除以总的四面体数,可根据化学计量和电荷平衡计算得到,如式(5)所示:
 (5)
(5)
式中:xO为氧的摩尔分数;xT为四面体摩尔分数。在硅酸盐熔体中,Si4+,Al3+,Fe3+和Fe2+均可以形成四面体结构[14-15],根据离子半径,四面体结构形成的优先顺序为 ,
, ,
,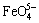 和
和 。
。
在本实验条件下,脱氧剂加入前,熔渣中铁离子存在以下平衡:
4Fe3++2O2-=4Fe2++O2 (6)
 (7)
(7)
式中: ,
, 和
和 分别为Fe3+,Fe2+和O2-的活度;
分别为Fe3+,Fe2+和O2-的活度; 和P0分别为氧分压和系统总压。当温度和氧分压一定时,Fe3+与Fe2+的存在比例主要受熔渣结构的影响[5,14]。假设熔渣中优先形成
和P0分别为氧分压和系统总压。当温度和氧分压一定时,Fe3+与Fe2+的存在比例主要受熔渣结构的影响[5,14]。假设熔渣中优先形成 和
和 四面体结构,剩余O2-与铁离子形成四面体结构,没有形成四面体结构的铁离子作为网络修饰体存在。计算结果表明,在实验渣成分条件下,熔渣中O2-完全存在于四面体结构中,
四面体结构,剩余O2-与铁离子形成四面体结构,没有形成四面体结构的铁离子作为网络修饰体存在。计算结果表明,在实验渣成分条件下,熔渣中O2-完全存在于四面体结构中, →0,根据式(7),可以认为熔渣中铁离子完全以三价形式存在。
→0,根据式(7),可以认为熔渣中铁离子完全以三价形式存在。
依据式(5)和实验渣成分,计算得到n(NBO/T)随Al2O3含量和碱度的变化,如图3所示。从图3可以看出:在一定碱度条件下,当Al2O3含量增加到一定程度(w(CaO)/w(SiO2)=3,w(Al2O3)≈15%;w(CaO)/ w(SiO2)=5,w(Al2O3)≈20%;w(CaO)/w(SiO2)=7,w(Al2O3)≈ 22.3%),n(NBO/T)逐渐降低,聚合程度增强。具体为:在w(CaO)/w(SiO2)=3条件下,当w(Al2O3)<15%时,n(NBO/T) 4,部分Fe3+形成
4,部分Fe3+形成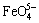 四面体,Fe3+和
四面体,Fe3+和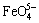 同时存在;随着Al2O3含量的增加,
同时存在;随着Al2O3含量的增加,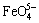 逐渐被
逐渐被 替代,当w(Al2O3)≈15%时,
替代,当w(Al2O3)≈15%时,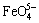 完全被
完全被 替代;当w(Al2O3)>15%时,n(NBO/T)<4,熔体中
替代;当w(Al2O3)>15%时,n(NBO/T)<4,熔体中 和
和 将发生聚合反应,而Fe3+将完全作为网络修饰体存在。
将发生聚合反应,而Fe3+将完全作为网络修饰体存在。

图3 单位四面体中非桥氧数随Al2O3含量和碱度的变化
Fig.3 Variation of non-bridged oxygen with content of Al2O3 and basicity
3.3 铁离子扩散系数
从上述分析可知,随着熔渣成分的变化,Fe3+的存在形式发生变化,将导致铁离子扩散尺寸发生变化。根据式(7)可以计算出铁离子的初始平均扩散直径:
 (8)
(8)
式中: 为铁离子平均扩散直径;
为铁离子平均扩散直径; 和
和 分别为Fe3+和
分别为Fe3+和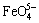 的物质的量,可根据形成
的物质的量,可根据形成 和
和 四面体后剩余的O2-物质的量计算得到;
四面体后剩余的O2-物质的量计算得到; 和
和 分别为Fe3+和
分别为Fe3+和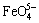 的直径。
的直径。
硅酸盐熔体的黏度是熔体结构的函数[16-19]。把SiO2和Al2O3作为网络形成物质,CaO和MgO作为网络修饰物质,Fe2O3作为两性氧化物处理,参考Urbain等[18]建立的熔体黏度模型,计算实验熔渣的初始黏度,其主要计算公式如下:
 (9)
(9)
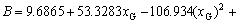


式中:x为摩尔分数;下标G表示网络形成物质;下标Fe2O3-T表示以四面体存在的Fe2O3。
图4所示为在1 823 K和w(CaO)/w(SiO2)=3条件下,根据实验渣成分和式(4)计算的铁离子平均扩散直径、熔渣黏度和铁离子扩散系数 随Al2O3含量的变化。从图4可以看出:当w(Al2O3)<15%时,铁离子平均扩散直径随Al2O3含量的增加而减小,当w(Al2O3)>15%时,铁离子平均扩散直径保持不变;从黏度的变化看,当w(Al2O3)<15%时,黏度缓慢增大,当w(Al2O3)>15%时,黏度快速升高;在二者综合作用下,铁离子扩散系数先升高后降低,其变化趋势与图2中1 min内平均脱氧速率随Al2O3含量的变化趋势是一致的。
随Al2O3含量的变化。从图4可以看出:当w(Al2O3)<15%时,铁离子平均扩散直径随Al2O3含量的增加而减小,当w(Al2O3)>15%时,铁离子平均扩散直径保持不变;从黏度的变化看,当w(Al2O3)<15%时,黏度缓慢增大,当w(Al2O3)>15%时,黏度快速升高;在二者综合作用下,铁离子扩散系数先升高后降低,其变化趋势与图2中1 min内平均脱氧速率随Al2O3含量的变化趋势是一致的。

图4 扩散系数、铁离子直径和熔渣黏度随Al2O3含量的变化
Fig.4 Variation of radius of ferrous ions, diffusion coefficient and slag viscosity with content of Al2O3
图5所示为1 823 K和w(Al2O3)=20%条件下,铁离子平均扩散直径、熔渣黏度和铁离子扩散系数随碱度的变化。从图5可以看出:随着碱度的升高,铁离子平均扩散直径增大,而熔渣黏度降低,在二者共同作用下,铁离子扩散系数随碱度的升高先增大后逐渐降低,对比图2中1 min内平均脱氧速率随碱度的变化情况,二者的变化趋势也是较一致的。
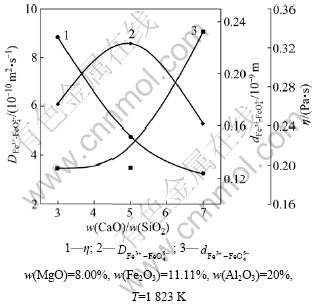
图5 扩散系数,铁离子直径和熔渣黏度随碱度的变化
Fig.5 Variation of radius of ferrous ions, diffusion coefficient and slag viscosity with basicity
从熔体结构对钢包渣中铁离子扩散行为的影响可以看出:为保证具有较高的铁离子扩散系数,需要对成分进行适当的控制,并要求Al2O3含量与碱度相适应。综合实验和理论分析结果,在工业生产钢包渣改质过程中,LF精炼前钢包渣成分调整目标为:w(CaO)/w(SiO2)=4~5,w(Al2O3)=18%~20%。
在实际工业生产中,钢包渣与钢水平衡,渣中铁主要以Fe2+存在;在碱性渣中,Fe2+同样可以形成四面体结构,上述分析过程和结果同样适用。
4 结论
(1) 熔渣初始脱氧速率受到熔渣初始Al2O3含量和碱度的控制;铁离子扩散为熔渣脱氧反应的控制环节。
(2) 实验渣熔体结构分析表明,随着Al2O3含量的升高,熔渣聚合程度增强,黏度升高,铁离子平均扩散尺寸减小;随着碱度的升高,熔渣聚合程度减弱,黏度降低,铁离子平均扩散尺寸增大;铁离子扩散系数随Al2O3含量和碱度的升高先增大后减小,其变化趋势与熔渣初始脱氧速率变化趋势相一致。
(3) 为提高LF精炼过程钢包渣的脱氧速率,LF精炼前钢包渣成分调整目标为:w(CaO)/w(SiO2)=4~5,w(Al2O3)=18%~20%。
参考文献:
[1] Domizzi G, Anteri G, Ovejero G J. Influence of sulphur content and inclusion distribution on the hydrogen induced blister cracking in pressure vessel and pipeline steels[J]. Corrosion Science, 2001, 43(2): 325-339.
[2] 孟劲松, 姜茂发, 王德永, 等. LF炉合成精炼渣成分优化[J], 东北大学学报: 自然科学版, 2006, 27(10): 1110-1113.
MENG Jin-song, JIANG Mao-fa, WANG De-yong, et al. Composition optimizing of lab-prepared refining slag for LF[J]. Journal of Northeastern University: Natural Science, 2006, 27(10): 1110-1113.
[3] 成国光, 宋波, 陆钢, 等. 钢液深脱硫精炼工艺的研究[J]. 钢铁, 2001, 36(3): 22-25.
CHENG Guo-guang, SONG Bo, LU Gang, et al. Deep desulphurization refining process of steel[J]. Iron and Steel, 2001, 36(3): 22-25.
[4] Mysen B O. Relationships between silicate melt structure and petrologic processes[J]. Earth-Science Reviews, 1990, 27(4): 281-365.
[5] Mysen B O. The structural behavior of ferric and ferrous iron in aluminosilicate glass near meta-aluminosilicate joins[J]. Geochimica et Cosmochimica Acta 2006, 70(9): 2337-2353.
[6] Mysen B O, Toplis M J. Structural behavior of Al3+ in peralkaline, meta-aluminous, and peraluminous silicate melts and glasses at ambient pressure[J]. American mineralogist, 2007, 92(5/6): 933-946.
[7] Christian R, Achim W. The effect of glass composition on the thermodynamics of the Fe2+-Fe3+ equilibrium and the iron diffusivity in Na2O-MgO-CaO-Al2O3-SiO2 melts[J]. Chemical Geology, 2004, 213(1/3): 125-135.
[8] 朱苗勇, 萧泽强. 钢的精炼过程数学物理模拟[M]. 北京: 冶金工业出版社, 1998: 243-246.
ZHU Miao-yong, XIAO Ze-qiang. Mathematical and physical simulation of steel refining process[M]. Beijing: Metallurgical Industry Press, 1998: 243-246.
[9] Shimizu N, Kushiro I. Diffusivity of oxygen in jadeite and diopside melts at high pressures[J]. Geochimica et Cosmochimica Acta, 1984, 48(6): 1295-1303.
[10] Iwamoto N, Makino Y. Determination of ionic distributions of three sorts of oxygens in a few binary silicate glasses from molar refractivity[J]. Journal of Non-Crystalline Solids, 1979, 34(3): 381-391.
[11] Mysen B O. Partitioning of calcium, magnesium, and transition metals between olivine and melt governed by the structure of the silicate melt at ambient pressure[J]. American Mineralogist, 2007, 92(5/6): 844-862.
[12] Stebbins J F, Xue Z. NMR evidence for excess nonbridging oxygen in an aluminosilicate glass[J]. Nature, 1997(390): 60-62.
[13] Lee S K. Structure of silicate glasses and melts at high pressure: Quantum chemical calculations and solid-state NMR[J]. Physical Review B, 2004, 108(19): 5889-5900.
Quantum chemical calculations and solid-state NMR[J]. Physical Review B, 2004, 108(19): 5889-5900.
[14] Fargesa F, Lefrèrec Y, Rossano S, et al. The effect of redox state on the local structural environment of iron in silicate glasses: A combined XAFS spectroscopy, molecular dynamics, and bond valence study[J]. Journal of Non-Crystalline Solids, 2004, 344(3): 176-188.
[15] Jackson W E, Farges F Y, Eager M, et al. Multispectroscopic study of Fe(Ⅱ) in silicate glasses: Implications for the coordination environment of Fe(Ⅱ) in silicate melts[J]. Geochem et Cosmochim Acta, 2005, 69(17): 4315-4332.
[16] Gerlach S, Clau?en O, Rüssel C. Self-diffusivity of iron in alkali-lime-alumosilicate glass melts[J]. Journal of Non- Crystalline Solids, 1998, 240(1/3): 110-117.
[17] Joo H P, Dong J M. Effect of fluorspar and alumina on the viscous flow of calcium silicate melts containing MgO[J]. Journal of Non-Crystalline Solids, 2004, 337(2): 150-156.
[18] Urbain G, Cambier F, Deletter M, et al. Viscosity of silicate melts[J]. British Ceramic Transactions, 1981, 80(1): 139-141.
[19] Toplis M J, Dingwell D B. Shear viscosities of CaO-Al2O3-SiO2 and MgO-Al2O3-SiO2 liquids: Implications for the structural role of aluminium and the degree of polymerisation of aluminosilicate melts[J]. Geochimica et Cosmochimica Acta, 2004, 68(24): 5169-5188.
(编辑 张曾荣)
收稿日期:2010-07-21;修回日期:2010-09-27
基金项目:国家自然科学基金资助项目(50904017)
通信作者:闵义(1972-),男,辽宁海城人,博士,讲师,从事洁净钢冶炼工艺与理论等方面的研究;电话:13897996336;E-mail: miny@smm.neu.edu.cn