DOI: 10.11817/j.ysxb.1004.0609.2021-37937
Na2CO3�����º�������ǵ���̼�Ȼ�ԭ����ѧ�о�
�Խ���1��������1����ѧ��1����־��1[*]��֣����2����ѧΰ1
��1�����ѧ���Ͽ�ѧ�빤��ѧԺ�����죬400044��
2����������ѧʡ������������ɫ������Դ������ù����ص�ʵ���ң�������650093��
ժҪ�� �����ȷ�������ѧ�������о���Na2CO3�����¹�þ���ͺ�������ǵ���̼�Ȼ�ԭ�Ķ���ѧ���ɣ�ȷ������Ҫ�Ķ���ѧ�����������˻�ԭ���̵�����仯���������������Na2CO3����̼�Ȼ�ԭ��ʼ�¶�Լ250�棬������̼��������Ӧ��̼�Ȼ�ԭ���̿ɷ�Ϊ�����Σ���ʼ�Σ���=0~0.15�������ڽΣ���=0.15~0.60����˥��Σ���=0.60~1.0������ʼ�εĻ�����Ż�ԭ��Ӧ�Ľ�����223kJ/mol�����½���76kJ/mol���ܶ�ά��ɢ���ƣ����ڽλ�������Ӻͣ��ý��ܻ�ѧ��Ӧ���ƣ�˥�����Ҫ����FeO��Fe2SiO4�Ļ�ԭ��Ӧ�������184 kJ/mol������С��132 kJ/mol����������ӵ�173 kJ/mol���ý��ܻ�ѧ��Ӧ���ơ��������Ӽ���ȣ�����Na2CO3��شٽ��˺��������̼�Ȼ�ԭ���������������̵Ļ�ܡ�
�ؼ��ʣ�
��������������ѧ���ǵ�����̼�Ȼ�ԭ��̼������
��ͼ����ţ�TF815
�������������������ܣ��ҳ���Ϊ�Ͻ�Ԫ��������������֡����ºϽ�ֵȣ��ھ��¡���ҵ����������Ӧ�ù㷺�������������緶Χ�ڶ�����Դ���������������ȫ��ɹ����ɵ�����Դ�У�Լ28%������������72%�Ǻ�������������������Դ������ݽߣ�������������Դ�ḻ���ѳ�Ϊ����������Ҫԭ�ϣ����������ֿɷ�Ϊ�������͡����ɲ��ͺ�þ����[1,2]��
���к�������ұ�������У���Թ�þ���ͺ�����ұ����������̶̡����ճ���������ѳ�Ϊ��������[3]�����հ�����¯ұ������תҤ-��¯������RKEF������תҤ����������ɽ������ֱ�ӻ�ԭ-��ѡ��[3,4]����¯ұ������ԭ�ϵ���Ӧ�Խϲ���������и�����Ʒ����ұ��ǰ��Ҫ������飬�������ܺĺ���Ⱦ��RKEF���ճ��죬��ԭ����Ӧ�Խ�ǿ����ʵ�ִ��ģ������������Ʒ�����������������иߵ������������Ȼ����RKEF���յ�Ĵ���¯��������ĵ��Լռ�����ɱ���50%���ϣ���˶Ե����Ĺ�ӦҪ��dz��ߡ���תҤ������ʵ����һ�ְ���̬ұ�����գ����ܺķ������һ�������ƣ����Ǹ÷����Բ�����������Ҫ����̣����Ʋ������»�תҤ��Ȧ�������˸ù��յ��ƹ�Ӧ�á���������������ѧ�߶�ֱ�ӻ�ԭ-��ѡ���ս����˴������о������ڻ�ԭ��������Խϵ͵Ļ�ԭ�¶ȣ���˿ɽ����ܺ�[5-7]�������ڻ�ԭ����Ϊ��ʹ���������ۼ����ٽ������Ĵ�ѡ����������Ļ��գ�ͨ����Ҫ�Թ��̼���ǿ��������ͨ����������������ܵ��أ����ɾֲ���Һ�࣬��ǿ�����������ľۼ������õ����Ӽ�����Na2CO3��Na2SO4��CaF2��CaO��[8-9]�����У��������Ӽ�����ǿ��Ч���ã��о���Ϊ�㷺���о����֣������ӿ��ƻ������εĽṹ�����չ��̵õ�Na2O������ο������Ӧ����ϼʯ��ϼʯ�����ɼ����˽���������Ǩ�ơ�Na2SO4�ڻ�ԭ�����л���������FeS��FeS��������γɵ��۵�����࣬�����ڴ�����̣��Ӷ��ٽ��������������ľۼ�[10]��
��ԭ���̽����ۼ�����������ǰ�������������ﱻ��ԭΪ����̬����Ի�ԭ����ѧ�о������ݻ�ԭ������IJ�ͬ���������廹ԭ������ʯī��ú�ۣ���CO��H2�������о������IJ�ͬ����Ϊ���¶���ѧ�ͷǵ��¶���ѧ[11-14]����Ȳ��÷ǵ��¶���ѧ�������Ժ���������ԭ����ѧ�������о�����ʧ������ȷ���˺���������ԭ�ķ�Ӧ��������������˶���ѧ����[15]��Jankovic�Ȳ��ó�������ʵ�鷽���о�����������H2�зǵ��»�ԭ�Ķ���ѧ������������Ӧ�Ķ���ѧ����ģ��[16]������CO��Ϊ��ԭ��ʱ�����ͨ�����Ƶķ���������ԭ���̵Ļ���ģ�ͣ��õ���صĶ���ѧ����[17]�������о�������ʹ��ԭ�ϵ����ܴ���һ�����죬��õĶ���ѧ���������ͬ�������о����ǻ��������Ӽ����������õ��Ľ��������������Ӽ���ǿ����Ŀǰ���о���Ҫ���������δٽ������ۼ�������������[18,19]������ѧ�о�������١��������ȶ�Na2SO4�����º�����Ļ�ԭ/����Ϊ������������о��������˻�ԭ��ѡ�����Ķ���ѧ���ɣ�����˻���ģ�ͺͶ���ѧ�������о�����������������»�ԭ���չ����У���������Ļ�ԭ��Ӧ�ܽ��滯ѧ��Ӧ���ƣ���������Ļ�ԭ�������������Ӧ�����һ����ѧ��Ӧ���ƣ��������ﻹԭ������������Ӧ�����ʳ�����Զ������������Ļ�ԭ��Ӧ���ʳ����������������������ѡ���Ի�ԭ/���ԣ������¶Ȳ�����������������֮���ѡ���Ի�ԭ[20]�����߲����ȷ�������ѧ�ķ����о���Na2SO4��̼�Ȼ�ԭ���������Ӱ��[21]���������������Na2SO4��������ԭ��ʼ�¶���������Ӽ�ʱ��ǰ100oC���ң�̼��������Ӧ��ʼ�¶�Ҳ��ǰ100oC���ң����������仯��ʾ�˻�ԭ���̻�����ǿ�����ơ�
��������ԭ����ѧ���о����������Ӽ�����µĻ�ԭ���̣��������Ӽ�ʱ��������ԭ����ѧ�о����١�������ǿ��������ԭ���̵���Ҫ���Ӽ���Na2CO3���Դٽ�����������Ļ�ԭ��Na2SO4���Դٽ������ľۼ��ͳ�����Ӱ������Ĵ�ѡ���롣���о���Ŀ���ǿ���Na2CO3����ʱ��������Ļ�ԭ����ѧ��Ϊ������ʯī����Ϊ��ԭ�����ų��˻ӷ��Գɷֵ�Ӱ�죬��������-����������ԭλ��ԭ����������ɵı仯���ɣ�ͨ��������ȷ�������ѧģ�����ȷ���ǵ��»�ԭ�Ķ���ѧ���ɣ���ϸ��λ�ԭ���������������������ɱ仯��̽�ַ�Ӧ���������о�����ߺ���������Դ������ˮƽ������Ҫ���塣
1 ʵ��ԭ�Ϻͷ���
1.1 ʵ��ԭ��
���о�ʹ�õĺ���������ڷ��ɱ����仯ѧ�ɷ����1��ʾ���ɱ��п��Կ�����ԭ��TFe����Ϊ17.87%��Ni����Ϊ1.81%��SiO2��MgO�����ϸߣ��ֱ�Ϊ34.97% ��13.5%�����ڵ��͵Ĺ�þ�ͺ�������ԭ����CaO����Ϊ1.54%��S��P ���к����ʺ����ϵ͡�
��1 ��������Ļ�ѧ�ɷ�
Table 1 Chemical composition of nickel laterite ore (wt.%)
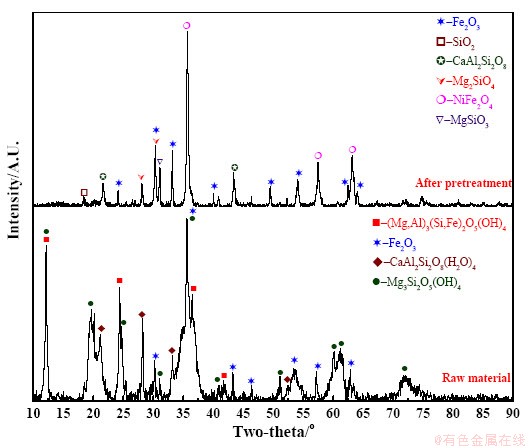
ͼ1 ��������XRDͼ��
Fig. 1 XRD pattern of nickel laterite ore
���ں����������д����Ľᾧˮ������ߴ�17.35%����ˣ�������-����ʵ��֮ǰ���Ƚ������������ڱ���¯�н���Ԥ������1000�決��2h������ȥ��ԭ���еĽᾧˮ����������Ԥ����ǰ���XRDͼ����ͼ1��ʾ�����������ԭ��������Ҫ�Գ�����Fe2O3������ʽ���ڣ���ʯ�������б����ʯ[CaAl2Si2O8(H2O)4]��Ҷ����ʯ[Mg3Si2O5(OH4)]��������ʯ[(Mg,Al)3(Si,Fe)2O5(OH)4]��Ԥ��������������еĽᾧˮ���ǻ����ѳ�ȥ��ͬʱ����ʯ��ֽ�Ϊ���ʯ(Mg2SiO4)������ʯ(MgSiO3)�����⣬�������������Ӧ����NiFe2O4��
1.2 ʵ�鷽��
�Ծ���Ԥ�����ĺ�����ʯ������ĥ��ȷ����Ʒ����100%С��0.074mm����ʯī����Ϊ��ԭ������C/OԪ��Ħ���ȹ̶�Ϊ1.2�������ϲ���ֻ��ȣ�Ȼ������Ʒ����4.47wt.% Na2CO3��C/OĦ�����е�O������ʾ�������������е��ܵ���Ԫ�غ��������أ�TG��ʵ�����SetaramEvo TG-DTA1750�����ǽ��У���Լ20mg����Ʒװ�������������ڣ���6mm��8mm��������������װ�õ���Ʒ̨�ϡ��趨�ü������ʺ��ڱ�������ΪAr�������½�������ʵ�飬��������Ϊ20mL��min-1���������ʷֱ�Ϊ10K/min��15K/min��20K/min�����������ǣ�TILON LC D200��AMETEK LLC��ԭλ�������ʵ�������β�����������������CO2��CO�ǻ�ԭ�����е�������Ҫ���塣
Ŀǰ���о��ǵ��¶���ѧ����������Եķ��������У����ؼ��������µķǵ����ȷ�����Ӧ����Ϊ�㷺������ʵ�������ֻ��������ϵļ��������½��У�����ѧ�����ļ�����õ�ת���ʷ���������ʵ�����õĶ����ȷ���������ͬת���ʦ�ʱ�����������ж���ѧ�������㣬�����ַ����ֱ���Ϊ��ת���ʷ���iso-conversional method������ת���ʷ��ܹ��ں��Ի�ѧ��Ӧģʽ��������������ý�Ϊ�ɿ��Ļ��ֵ����˸÷���Ӧ�ù㷺��Kissinger-Akahira-Sunose��KAS����Flynn Wall Ozawa��Friedman���������־��д����Եĵ�ת���ʷ���[22-25]���ڱ��о��У��������KASģ�͵õ�����ģ�ͱ��㷺Ӧ���ڶ���ѧ������ȷ����ͨ��ģ����Ͽ�ȷ����Ӧ�Ļ���������
2 ���������
2.1 ����ʵ�鼰��ԭβ������
�ֱ���10K/min��15K/min��20K/min���ֲ�ͬ�ļ��������½��зǵ��»�ԭʵ�飬�õ�TG������ͼ2��ʾ����ͼ�п��Կ���������Na2CO3��ͬ���������µõ���ʧ�����������ơ���������Ϊ 10K/minʱ��������ʧ�Դ�������������������ʱ��������ʧ�������յ�������ʧ������ͬ��������Ϊ�ڽϵ͵ļ��������£����������ȵ���ͬ�¶������ʱ��ϳ�������ͬ�¶��·�Ӧ����ʱ���ʱ��������ڲ�ͬ�ļ��������£����¶ȵ���600��ʱ��ʼ�۲쵽������ʧ�����¶����Ե���û������Na2CO3ʱ���¶ȣ���Լ950�棩�����ҿ��Կ����ڷ�Ӧ���ں��������ʧ���������Լӿ�[26, 27]�����¶�����1500�������TG��������ƽ������ԭ���̻����������Ա�����Na2SO4��ʵ������֪������Na2CO3��ԭ��Ӧ��ʼ�¶ȱ�����Na2SO4ʱ��ǰ��250oC����[21, 27]���������̼���εĴ����Դ��������εĴ����ԣ�̼���ζ��ƻ�MgSiO3��Mg2SiO4�Ƚṹ�����ø��������ڸ��������е�����������Ļ�ԭ��
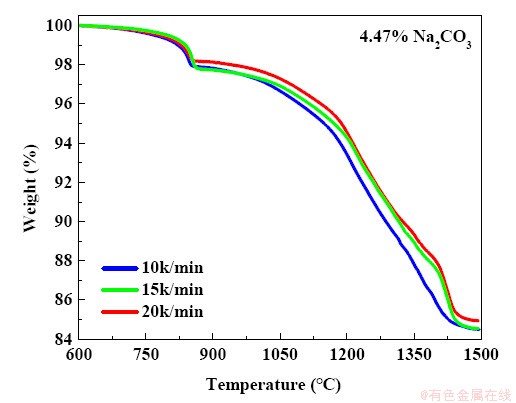
ͼ2 ����Na2CO3ʱ��������̼�Ȼ�ԭTG����
Fig. 2 TG curves of carbothermic reduction of nickel laterite ore with Na2CO3
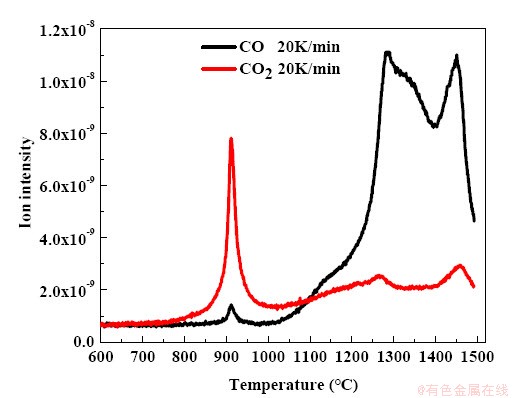
ͼ3 ��������ԭ����β����������ǿ��
Fig. 3 The intensity of ion current detected by mass spectrometry
��ԭ����ʹ�������Ƕ�β��������ʵʱ��⣬CO��CO2��������ǿ�����¶ȵĹ�ϵ��ͼ3��ʾ������Na2CO3��CO2��������ǿ����700~1100��֮��������ǿ��������ڸ��¶�������������̼�Ȼ�ԭ��Ӧ���ʽϿ죬֤��Na2CO3�Ը��¶������µĺ�������̼�Ȼ�ԭ��Ӧ�дٽ����á��¶�����1100���CO����������������ߣ�������CO2���������ʣ������������̼��������Ӧ��ǿ���Ա������Ӽ�ʱ�Ľ����֪[21, 27]��Na2CO3������̼������Ӧ�Ľ��С����¶�������1300��ʱ��CO��������ǿ�ȿ�ʼ���ͣ����¶�������1400��ʱ��CO��������ǿ���ֶ�Ȼ������ֱ���¶ȴﵽ1450��ʱ��CO��������ǿ���ٴ����͡�CO2��������ǿ����1100��~1250��֮�仺�����ӣ������1300��~1400��֮������ȶ�����1400��~1450����������ʱ��1450��ʱCO2��������ǿ�������ͣ�ֱ������̼�Ȼ�ԭ���̽�����
2.2 ת����
��ԭ���̵�������ʧ��CO��CO2��ɣ�����O��Ҫ���������������������о����̺�����Na2CO3�е�̼����ʧ����ˣ���Ʒ��ʧ����ͨ����ʽ��1�����㣺
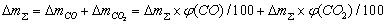 (1)
(1)
���У�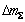 ��ʾ��Ʒ��ʧ��������(g)��
��ʾ��Ʒ��ʧ��������(g)��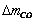 ��ʾ��CO����ʽ��ʧ������(g)��
��ʾ��CO����ʽ��ʧ������(g)�� ��ʾ��CO2����ʽ��ʧ������(g)��CO��CO2�������ٷֱȱ�ʾΪ
��ʾ��CO2����ʽ��ʧ������(g)��CO��CO2�������ٷֱȱ�ʾΪ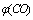 ��
��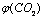 ������
������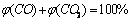 ��
��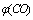 ��
��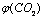 �ɹ�ʽ��2�����㣺
�ɹ�ʽ��2�����㣺
 (2)
(2)
ʽ�У� ��
��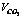 ��ʾ��ԭβ����CO��CO2������ٷֱȣ���ֵ����ͨ��ͼ3��CO��CO2��������ǿ�ȵı�ֵ��á�
��ʾ��ԭβ����CO��CO2������ٷֱȣ���ֵ����ͨ��ͼ3��CO��CO2��������ǿ�ȵı�ֵ��á�
��ijһʱ����Ʒ��ʧ������ͨ����ʽ��3�����㣺
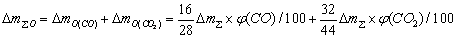 (3)
(3)
ʽ�е�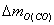 ��
��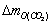 �ֱ��ʾCO ��CO2���ߵ���ԭ�ӵ�������
�ֱ��ʾCO ��CO2���ߵ���ԭ�ӵ�������
ת���ʦ�����Ϊ��Ʒijһʱ��ʧ��������Ʒ�ܵ�ʧ�����ı�ֵ�������ʽ�繫ʽ(4)��ʾ��
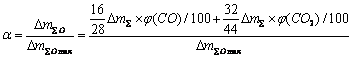 (4)
(4)
���У�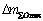 Ϊ��Ʒ�ܵ�ʧ������
Ϊ��Ʒ�ܵ�ʧ������
����������ͬ���������µ�ת���ʡ��¶����߱仯���ƽӽ�����˱�ʵ�������������Ϊ20K/min�Ļ�ԭʧ�����ݣ�̽��Na2CO3�Ժ�������ԭ���̶���ѧ��Ӱ�졣����ѧ����ʱ�����ȼ���������Na2CO3ʱ��������ԭת�������¶ȵĹ�ϵ����ͼ4��ʾ����ת���ʶ�ʱ���������ԭ������ת���ʵĹ�ϵ��ͼ5��ʾ����ͼ�п��Կ�������������̼�Ȼ�ԭת�������¶Ȳ����ϴ�����ʼ��ٵ����ơ�ͨ����Ӧ���ʵ�����ͼ���ɽ�������������Na2CO3���̼�Ȼ�ԭ���̷�Ϊ�����Σ��ֱ�Ϊ����=0~0.15����=0.15~0.60����=0.60~1.0��
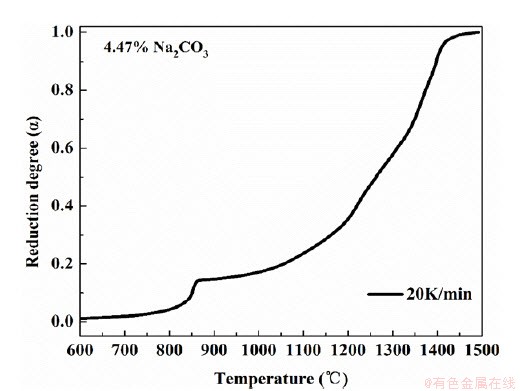
ͼ4 ����Na2CO3ʱ��������ԭת�������¶ȵĹ�ϵ
Fig. 4 The conversion degree (��) as a function of temperature with Na2CO3
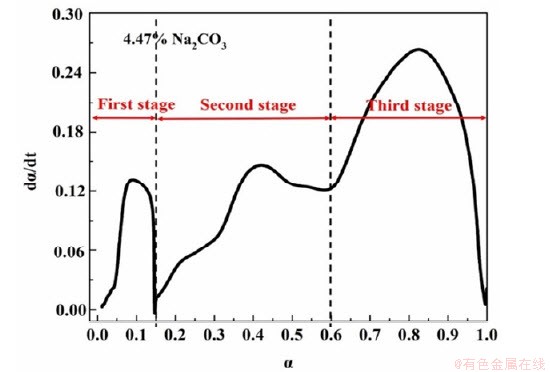
ͼ5 ����Na2CO3ʱ��������̼�Ȼ�ԭ������ת���ʵĹ�ϵ
Fig. 5 The first derivatives of conversion degree (��) versus time with Na2CO3
2.3 ���
���о�ͨ��KAS�����㻹ԭ��Ӧ�Ļ��Eֵ������KASģ�ͼ��㲻ͬת���������µĻ�ܣ����㹫ʽ���£�
 (5)
(5)
�ɹ�ʽ5��֪���ڼ���������ͬ������£�ln(��/T2)��1/T�����ȡ���ˣ�ͨ������б�ʻ�û�ܣ�����ȷ��ģ�ͺ�����õ�ǰָ������A����ʧ�������Ͻ�ȡ��ͬ�������ʦ�����ͬת���ʦ�ʱ�¶�T��ֵ����ln(��/T2)��1/T��ɢ��ͼ��ͨ����С���˷���ln(��/T2)��1/T���Իع飬�������Իع�ֱ��б�ʼ���ת����Ϊ��ʱ��Ӧ�Ļ�ܣ�ͼ6��ʾΪ��ܼ�������
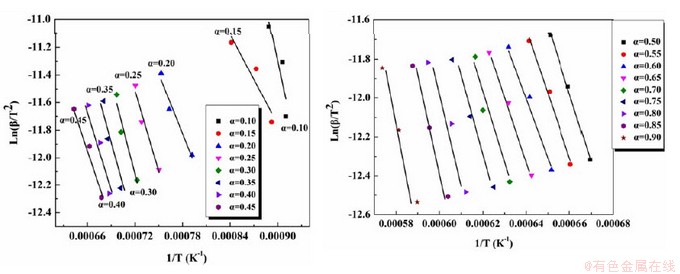
ͼ6 ����KAS��������ĵ�ת�������ֱ��
Fig. 6 Calculated iso-conversional plots based on KAS method
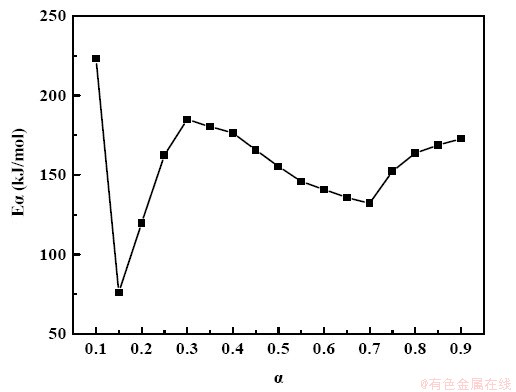
ͼ7 ��������̼�Ȼ�ԭ���̵Ļ����ת���ʵĹ�ϵ
Fig. 7 Activation energies obtained by KAS methods as a function of conversion degree
ͼ7�Ǹ���KAS�������õ�̼�Ȼ�ԭ��Ӧ���Eֵ����ͼ�п��Կ�������ܵı仯Ҳ��Ϊ�����Σ���һ��(��=0~0.15)��������Ż�ԭ��Ӧ�Ľ��п����½�����223kJ/mol���͵�76kJ/mol����ԭ��Ӧ�ڵڶ��Σ���=0.15~0.60��ʱ����ܵĿ������ӣ���76 kJ/mol���ӵ�184 kJ/mol����Ӧ���е���=0.30��ܿ�ʼ���½�����Ӧ���е������Σ���=0.60~1.0��ʱ������ȼ��������½�����184 kJ/mol��С��132 kJ/mol���������е���=0.70ʱ������ֿ�ʼ�������ӣ���132 kJ/mol���ӵ�173 kJ/mol�����о���õĻ������ڴ�ͳ���о��ϸߣ�����Ҫ������ԭ����1000���½�����2Сʱ��Ԥ������ȥ���ᾧˮ������Na2CO3��ѧ��Ӧ�Ļ��ֵ�������Na2SO4ʱ���ͣ��ʹٽ���������ԭ���棬̼���ƴ�����ǿ�������ơ�
2.4 ����ѧ����ģ��
����Coats��Redfern�����ģ����Ϸ����õ����ܵĻ���ģ�ͣ�����ʽ��6����֪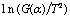 ��1/T��ͼ������С���˷��������Իع飬��ɵõ�һ��ֱ�ߣ�������϶�R2���ƶϳ�����ܵĻ���������ͼ8��ʾ��
��1/T��ͼ������С���˷��������Իع飬��ɵõ�һ��ֱ�ߣ�������϶�R2���ƶϳ�����ܵĻ���������ͼ8��ʾ��
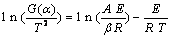 (6)
(6)
����Na2CO3�ķǵ��»�ԭ���̰��������Σ���ʼ��(��=0~0.15)�����ڽΣ���=0.15~0.60����˥��Σ���=0.60~1.0�������ڳ�ʼ��(��=0~0.15)����Ӧ����Ϊ��ά��ɢ��������ʽΪ ��Coats-Redfern�����Ա�ʾΪ��7����
��Coats-Redfern�����Ա�ʾΪ��7����
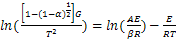 (7)
(7)
��Ӧ���ڽΣ���=0.15~0.60������Ӧ����Ϊ��ѧ��Ӧ�����������Ļ��ֱ���ʽΪ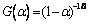 ��Coats-Redfern�����Ա�ʾΪ��8����
��Coats-Redfern�����Ա�ʾΪ��8����
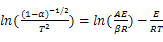 (8)
(8)
˥��Σ���=0.60~1.0�������������Ļ��ֱ���ʽΪ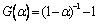 ����Ӧ����Ϊ��ѧ��Ӧ��Coats-Redfern�����Ա�ʾΪ��9����
����Ӧ����Ϊ��ѧ��Ӧ��Coats-Redfern�����Ա�ʾΪ��9����
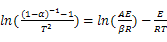 (9)
(9)
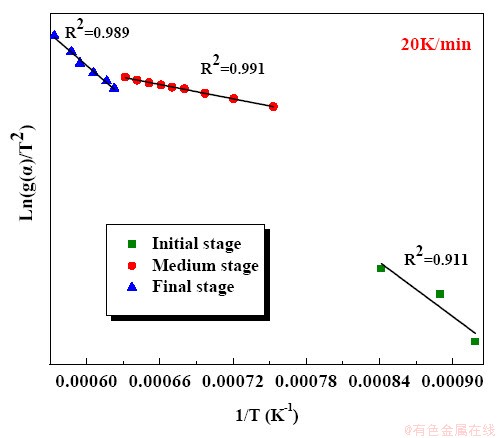
ͼ8 ����Coats-Redfern��ʽ�����ģ�������
Fig. 8Model-fitting plots of carbothermic reduction process
3 ��ԭ��������
���Na2CO3�����º�������̼�Ȼ�ԭ��Ӧ�������Σ����XRD�������о������β����������ɣ������ͼ9��ʾ����ͼ�п��Կ�������Ӧ��һ�ν�������=0.15ʱ���������Ϊ��SiO2��Fe3O4��Mg2SiO4��(Mg,Fe)2SiO4��Na2Mg2Si2O7�����û��Fe2O3��������ڵ�һ��Fe2O3��������ԭΪFe3O4����һ�η�������Ҫ��ѧ��Ӧ������ʾ��
3Fe2O3 (s) + C(s) = 2Fe3O4 (s) + CO (g)
Fe3O4 (s) + C (s) = 3FeO (s) + CO (g)
NiO (s) + C (s) =Ni (s) + CO (g)
ͬʱ�����ܷ������·�Ӧ��
Na2CO3+SiO2= Na2O��SiO2+CO2
Na2CO3+Al2O3=2NaAlO2+CO2
Al2O3+6SiO2+ Na2CO3= Na2O��Al2O3��6SiO2+CO2
Na2CO3(s) + 2MgSiO3(s) = Na2Mg2Si2O7 (s) + CO2 (g)
̼�Ȼ�ԭ��Ӧ���ڣ���Ҫ�����ķ�ӦΪFe2O3����ԭΪFe3O4�ķ�Ӧ���Լ�NiO����ԭΪNi�ķ�Ӧ����ʱ��ҪΪ�̷̹�Ӧ����˷�Ӧ����������ͼ3��֪���ڻ�ԭ��Ӧ���ڣ�β���е�CO ��CO2�ĺ����ܵͣ��Ӳ���֤���˻�ѧ��Ӧ���ʻ��������ŷ�Ӧ�Ľ��У�Na2CO3������ʯ��MgSiO3��Ӧ���ɸ��ӹ����Ρ������������ࣨNa2O��SiO2��NaAlO2��Na2O��Al2O3��6SiO2��Na2Mg2Si2O7��������CO2�ȡ��������ƻ�MgSiO3��Mg2SiO4�ȵĽṹ�������ڸ��������е�������������Ļ�ԭ��
̼�Ȼ�ԭ��Ӧ�ڶ��ν���ʱ������=0.60�����д����Ľ���������FeNi�����ɣ�ͬʱFe3O4�������ȫ����ʧ������������FeO���������ڣ������Fe3O4�ֱ���ԭΪ��������Fe��������������ԭΪFeO����ʱ�Ŀ������Ϊ��FeNi��FeO��Fe2SiO4��SiO2��Mg2SiO4��(Mg,Fe)2SiO4��Na2Mg2Si2O7�ڶ��η�������Ҫ��ѧ��ӦΪ��
CO2 (g) + C (s) = 2CO (g)
Fe3O4 (s) + C (s) = 3FeO (s) + CO (g)
FeO (s) + CO (g) = Fe (s) + CO2 (g)
2 FeO (s) + SiO2 (s) =Fe2SiO4 (s)
�ڶ��γ��ڣ���=0.15~0.30������ͼ3�������¶���900oC~1000oC֮��ʱ��CO2�ĺ�������CO�����̼��������Ӧ��δ������������ʱ����������ҪΪFe3O4�����¶�����1000���ԭβ����CO�������ʴ���CO2�������ʣ������̼������ӦѸ�ٷ�����
����������ӿɽ���FeO�����¾�����䣬�Ӷ��ٽ�FeO����ԭΪFe����һ���棬��ԭ���ɵĽ���Fe��̼��������Ӧ�������á���ˣ������¶ȵ����ߣ�������Ӧ���ٽ���[21]������Na2CO3��������Ӧ��ʼ�¶�������Na2SO4ʱ�����ǰ��100oC���ң������̼���ζ�̼������Ӧ�Ĵ����ø������ԡ���ȹ��廹ԭ��ʯī�ۣ����廹ԭ��CO�����״ӷ�Ӧ����ɢ��δ��Ӧ�㣬�ٽ���̼�Ȼ�ԭ��Ӧ���̡���ˣ���������̼�Ȼ�ԭ��Ӧ����ڦ�=0.30 ��ʼ���͡��������ŷ�Ӧ�Ľ��У�ʣ���FeO��SiO2��Ӧ����Fe2SiO4����±���ԭ�Ľ�����������٣����廹ԭ����CO2���������٣����̼��������Ӧ���裬CO��CO2��������ǿ����Ӧ���ͣ���Ӧ���ʼ�����
̼�Ȼ�ԭ��Ӧ����������=1.0ʱ������������FeNi����������ǿ��������и���Ľ����������ɡ����⣬Fe2SiO4��FeO���������һ����ʧ�������Fe2SiO4��FeO����ԭ���������ڼ���Ĺ���ʯī�ۣ���˵���������̼�Ȼ�ԭ��Ӧ��������Ȼ��̼ʣ�ࡣ��ʱ�Ŀ������Ϊ��FeNi��SiO2��Mg2SiO4��Na2Mg2Si2O7����ˣ�̼�Ȼ�ԭ��Ӧ�����η�������Ҫ��ѧ��Ӧ������ʾ��
FeO (s) + CO (g) = Fe (s) + CO2 (g)
2 FeO (s) + SiO2 (s) =Fe2SiO4 (s)
Fe2SiO4(s)+2CO(g)=2Fe(s)+SiO2(s)+2CO2(g)
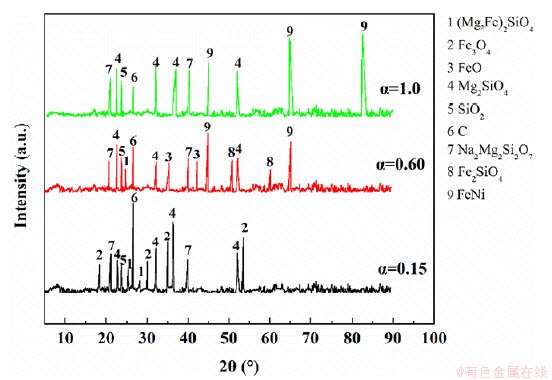
ͼ9 ����Na2CO3��ͬ�κ�������̼�Ȼ�ԭ����XRDͼ��
Fig. 9 XRD patterns of the reduction products at different stage with Na2CO3 addition
��ԭ���̵�����(��=0.60~1.0)����Ҫ�����ķ�ӦΪFeO��Fe2SiO4�ı���ԭΪFe�ķ�Ӧ����������Fe2SiO4���ѱ���ԭ����˻�������ߡ��������ڼ���������ӿ������̼�ķ�Ӧ���ԣ�ͬʱ���ڻ�ѧ�����Ļ�ԭ����õ�������FeO��Fe2SiO4�Ļ�ԭ��Ӧ���Դٽ���������廹ԭ����CO���ӡ�ͨ��ͼ3���֣�CO��������ǿ����1400oCʱ��Ȼ��������֤�����������ۡ�����ʣ��Fe2SiO4���٣�CO2���������٣�CO��������Ҳ��֮���٣���˷�Ӧ���ʴﵽһ����ֵ���������½���
4 ����
�����о�������Na2CO3ʱ��������ķǵ���̼�Ȼ�ԭ����ѧ�����������������̽�֡��ó����½��ۡ�
��1������Na2CO3��������̼�Ȼ�ԭ��ʼ�¶���������Ӽ�ʱ��ǰ��350oC���ң�������Na2SO4ʱ�����ǰ��250oC���ң�̼��������Ӧ��ʼ�¶���������Ӽ�������Na2SO4ʱ�ֱ���ǰ100oC��200oC��
��2����Coats-Redfern��ȷ���˲�ͬ�εĻ������������ڳ�ʼ��(��=0~0.15)����Ӧ����Ϊ��ά��ɢ��������ʽΪ �����ڽΣ���=0.15~0.60������Ӧ����Ϊ��ѧ��Ӧ�����������Ļ��ֱ���ʽΪ
�����ڽΣ���=0.15~0.60������Ӧ����Ϊ��ѧ��Ӧ�����������Ļ��ֱ���ʽΪ ��˥��Σ���=0.60~1.0�������������Ļ��ֱ���ʽΪ
��˥��Σ���=0.60~1.0�������������Ļ��ֱ���ʽΪ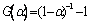 ����Ӧ����Ϊ��ѧ��Ӧ��
����Ӧ����Ϊ��ѧ��Ӧ��
��3����ԭ��Ӧ��һ�Σ���=0~0.15����������Ż�ԭ��Ӧ�Ľ�����223kJ/mol�����½���76kJ/mol��Na2CO3������ʯMgSiO3��Ӧ����Na2Mg2Si2O7���ƻ�����ʯ�ṹ�������ڸ��������е�������������Ļ�ԭ���ڶ��Σ���=0.15~0.60���������76 kJ/mol�������ӵ�184 kJ/mol�����ʼ���½�����ʱ̼��������Ӧ����������Ӧ��ܽϴ���������Լ�ӻ�ԭ��ӦΪ������������½��������Σ���=0.60~1.0������Ҫ�����ķ�ӦΪFeO��Fe2SiO4�Ļ�ԭ��Ӧ����ܿ�ʼ��184 kJ/mol������С��132 kJ/mol������ԭ��Ӧ�������е���=0.70ʱ������ֿ�ʼ�������ӣ���132 kJ/mol���ӵ�173 kJ/mol��
REFERENCES
[1] ����,������,ʩ��,������,��ǿ,����,��Դ,������.��þ��������������о���״[J].���ϵ���,2020, 34(Z1):261-267.
QU Tao, GU Xu-peng, SHI Lei, LUO Ming-yang, WANG Qiang, LYU Fei, TIAN Yuan, DAI Yong-nian. Research Status of Development and Utilization of Garnierite [J]. Materials Reports, 2020, 34(Z1): 261-267.
[2] ����,��־��,����,���˳,��Ҷ,�Դ���.�Ȼ��ѡ���Խ������������м۽���[J]. �й���ɫ����ѧ��, 2019, 29(5): 1049-1057.
LI Jin-hui, XU Zhi-feng, GAO Yan, LI De-shun, LIU Ye, ZHAO Chun-die. Selectively leaching valuable metals from laterite nickel ore by ammonium chloride[J]. The Chinese Journal of Nonferrous Metals, 2019, 29(5): 1049-1057.
[3] ���ǿ, ��Ԩ��, �ܺ���,��½��, ������.���������ұ��������״����չ[J]. ����ۺ�����, 2020, (3): 78-83+93.
WU Bing-qiang, QI Yuan-hong, ZHOU He-min, HONG Lu-kuo, ZOU Zong-shu. Status and Progress in Pyrometallurgy Processes of a Laterite Nickel Ore[J]. Multipurpose Utilization of Mineral Resources, 2020, (3): 78-83+93.
[4] ��־��,�����,����ƽ.���ʺ�þ�ʺ�������ֱ�ӻ�ԭ-��ѡ���նԱ�[J]. �й���ɫ����ѧ��, 2017, 27(3): 594-604.
LIU Zhi-guo, SUN Ti-chang, WANG Xiao-ping. Comparison of direct reduction-magnetic separation process on ferruginous and magnesian laterite ore [J]. The Chinese Journal of Nonferrous Metals, 2017, 27(3): 594-604.
[5] ����, ������, ����, ������, ʷ����, ��Ԫ��, ������. ��������ԭ����-��ѡ��ȡ�����Ͻ�ԭ�ϵ��¹���[J]. �й���ɫ����ѧ��, 2011, 21(12): 3137-3142.
LI Guang-hui, RAO Ming-jun, JIANG Tao, HUANG Qing-qing, SHI Tang-ming, ZHANG Yuan-bo. Innovative process for preparing ferronickel materials from laterite ore by reduction roasting-magnetic separation[J]. The Chinese Journal of Nonferrous Metals, 2011, 21(12): 3137-3142.
[6] YUAN Shuai, ZHOU Wen-tao, LI Yan-jun, HAN Yue-xin. Efficient enrichment of nickel and iron in laterite nickel ore by deep reduction and magnetic separation [J]. Transactions of Nonferrous Metals Society of China, 2020, 30: 812-822.
[7] ��־��,�,κ����.���������¹�þ�ͺ�������ĵ��»�ԭ����[J]. �й���ɫ����ѧ��, 2018, 28(8): 1669-1675.
DING Zhi-guang, LI Bo, WEI Yong-gang. Reduction characteristic of garnieritic laterite ore using hydrogen at low temperature[J]. The Chinese Journal of Nonferrous Metals, 2018, 28(8): 1669-1675.
[8] ZHOU Shi-wei, DONG Jing-cheng, LU Chao, LI Bo, LI Fan, ZHANG Bing, WANG Hua, WEI Yong-gang. Effect of sodium carbonate on phase transformation of high�Cmagnesium laterite ore[J]. Materials Transactions, 2017, 58(5): 790-794.
[9] LV Xue-ming, LV Wei, LIU Mei, YOU Zhi-xiong, LV Xue-wei, BAI Chen-guang. Effect of sodium sulfate on preparation of ferronickel from nickel laterite by carbothermal reduction[J]. ISIJ International, 2018, 58(5): 799-805.
[10] ����ƽ,�����,��־��,�����,�. Na2SO4�ڸ��������ͺ�������ѡ���Ի�ԭ�����е����û���[J]. �й���ɫ����ѧ��, 2016, 26(10): 2197-2204.
WANG Xiao-ping, SUN Ti-chang, LIU Zhi-guo,XU Cheng-yan , LI Chuan. Mechanism of sodium sulphate on selective reduction roasting of high iron and low nickel content laterite[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(10): 2197-2204.
[11] PETRUS H T B M, PUTERA A D P, SUGIARTO E, Perdana I, WARMADA I W, NURJAMAN ASTUTI F W, MURSITO A T. Kinetics on roasting reduction of limonitic laterite ore using coconut charcoal and anthracite reductants[J]. Minerals Engineering, 2019, 132: 126-133
[12] LI Bo, WANG Hua, WEI Yong-gang. Kinetic analysis for non-isothermal solid state reduction of nickel laterite ore by carbon monoxide[J]. Mineral Processing and Extractive Metallurgy, 2012, 121(3): 178-184.
[13] ADNADEVIC B, JANKOVIC B. Dispersive kinetic model for the non-isothermal reduction of nickel oxide by hydrogen[J]. Physica B-Condensed Matter, 2008, 403(21-22): 4132-4138.
[14] VYAZOVKIN S, WIGHT C A. Isothermal and non-isothermal kinetics of thermally stimulated reactions of solids [J]. International Reviews in Physical Chemistry, 1998, 17: 407-433.
[15] �,κ����,����.��������Ĺ��ԭ����ѧ[J]. ���̹���ѧ��, 2011, 11(5): 767-771.
LI Bo, WEI Yong-gang, WANG Hua.Solid state deoxidization kinetics of nickel laterite Ore[J]. The Chinese Journal of Process Engineering, 2011, 11(5): 767-771.
[16] JANKOVIC B, ADNAYEVIC B, MENTUS S. The kinetic study of temperature-programmed reduction of nickel oxide in hydrogen atmosphere[J]. Chemical Engineering Science, 2008, 63(3): 567-575.
[17] LI Bo, DING Zhi-guang, WEI Yong-gang, WANG Hua, YANG Yin-dong, BARATI M. Kinetics of Reduction of Low-Grade Nickel Laterite Ore Using Carbon Monoxide[J]. Metallurgical and Materials Transactions B, 2018, 49B: 3067-3073.
[18] ����, ������, ����, ʷ����, ������. �����������λ�ԭ����-��ѡ�Ļ���[J]. �й���ɫ����ѧ��, 2012, 22(1): 274-280.
LI Guang-hui, RAO Ming-jun, JIANG Tao, SHI Tang-ming, HUANG Qing-qing.Reduction roasting-magnetic separation mechanisms of nickelferous laterite ore in presence of sodium salts[J].The Chinese Journal of Nonferrous Metals, 2012, 22(1): 274-280.
[19] RAO Ming-jun, LI Guang-hui, ZHANG Xin, LUO Jun, PENG Zhi-wei, JIANG Tao. Reductive roasting of nickel laterite ore with sodium sulfate for Fe-Ni production. Part I: reduction/sulfidation characteristics[J].Separation Science & Technology, 2016, 51(8): 1408-1420.
[20] RAO Ming-jun, LI Guang-hui, ZHANG Xin, LUO Jun, PENG Zhi-wei, JIANG Tao. Reductive roasting of nickel laterite ore with sodium sulphate for Fe-Ni production [J]. Part II: Phase transformation and grain growth. Separation Science and Technology, 2016, 51(10): 1727-1735.
[21] LIU Yong-jie, LV Xue-ming, YOU Zhi-xiong, LV Xue-wei, Kinetics study on non-isothermal carbothermic reduction of nickel laterite ore in presence of Na2SO4[J], Powder Technology, 2020, 362: 486-492.
[22] KISSINGER H E. Reaction kinetics in differential thermal analysis [J]. Analytical Chemistry, 1957, 29: 1702-1706.
[23] OZAWA T. Estimation of activation energy by isoconversion methods [J]. ThermochimicaActa, 1992, 203: 159-165.
[24] FLYNN J H. Thermal analysis kinetics �C past, present and future[J]. ThermochimicaActa, 1992, 203: 519-526.
[25] FRIEDMAN H L. Kinetics of thermal degradation of char-forming plastics from thermogravimetry. Application to a phenolic plastic [J]. Journal of Polymer Science Part C: Polymer Symposia, 1964, 6: 183-195.
[26] LV Xue-ming, LV Wei, YOU Zhi-xiong, LV Xue-wei, BAI Chen-guang. Non-isothermal Kinetics Study on Carbothermic Reduction of Nickel Laterite Ore[J]. Powder Technology, 2018, 340: 495-501.
[27] ��ѧ��.�������������̬ұ�����������ۻ����������о�[D]. ���죺�����ѧ, 2019: 47-60.
LV Xue-ming. Research on the Foundamentals and Process for Ferronickel Production from Laterite Based on Semi-mloten Smelting[D]. Chongqing, Chongqing University, 2019: 47-60.
Kinetics of non-isothermal carbothermic reduction of nickel laterite ore in the presence of Na2CO3
ZHAO Jian-bo1, MA Dong-lai1, Fan Zi-long1, LV Xue-ming1, YOU Zhi-xiong1*, ZHENG Yong-xing2, LV Xue-wei1
(1 College of Materials Science and Engineering, Chongqing University, Chongqing 400044, China;
2 State Key Laboratory of Complex Nonferrous Metal Resources Clean Utilization, Kunming University of Science and Technology, Kunming 650093, China)
Abstract: Kinetics on non-isothermal carbothermic reduction of nickel laterite ore in the presence of Na2CO3. Based on the thermogravimetry and kinetic analysis methods, relevant kinetic parameters were determined and the phase transformation during reduction was revealed. The results indicated that the starting temperature of carbothermic reduction was reduced and the gasification of carbon was intensified after adding Na2CO3. The reduction process can be divided into three stages: the initial stage (��=0~0.15), the middle stage (��=0.15~0.60) and the decaying stage (��=0.60~1.0). The activation energy of initial stage decreased from 223 kJ/mol to 76 kJ/mol in which the two-dimensional diffusion was identified as the mechanism function. For the middle stage, the activation energy increased and then decreased. The chemical reaction mechanism was found to be the best fit. The decaying stage also belonged to chemical reaction mechanism, while the activation energy of this stage decreased from 184 kJ/mol to 132 kJ/mol and then increased to 173 kJ/mol. The reduction of Fe and Fe2SiO4 was the main reactions in this stage. Compared to the reduction in the absence additive, the reduction process was enhanced and the corresponding activation energy can be reduced after adding Na2CO3.
Key words: Nickel laterite ore; Kinetics; Non-isothermal; Carbothermic reduction; Na2CO3
������Ŀ (Foundation item)��������Ȼ��ѧ����������Ŀ��51904047����ʡ������������ɫ������Դ������ù����ص�ʵ���ҿ��Ż���CNMRCUKF2004����
ͨ�����ߣ���־�ۣ������ڣ���ʿ�����¸��ӿ��Ч�����о���E-mail: youzx@cqu.edu.cn��Tel��023-65112631��
[3] ���ǿ, ��Ԩ��, �ܺ���,��½��, ������.���������ұ��������״����չ[J]. ����ۺ�����, 2020, (3): 78-83+93.
[4] ��־��,�����,����ƽ.���ʺ�þ�ʺ�������ֱ�ӻ�ԭ-��ѡ���նԱ�[J]. �й���ɫ����ѧ��, 2017, 27(3): 594-604.
[7] ��־��,�,κ����.���������¹�þ�ͺ�������ĵ��»�ԭ����[J]. �й���ɫ����ѧ��, 2018, 28(8): 1669-1675.
[15] �,κ����,����.��������Ĺ��ԭ����ѧ[J]. ���̹���ѧ��, 2011, 11(5): 767-771.
[27] ��ѧ��.�������������̬ұ�����������ۻ����������о�[D]. ���죺�����ѧ, 2019: 47-60.


