ǰ�������-������ĥ��ԭ�Ʊ�Ti4+����LiFePO4
�� �裬��־�ˣ����º����������֣��������������������
(���ϴ�ѧ ұ���ѧ�빤��ѧԺ������ ��ɳ��410083)
ժ Ҫ��
ժ Ҫ�����ù��������Ʊ��˲�Ti4+ǰ����FePO4��2H2O�������Ҷ���Ϊ��ԭ������Li2CO3��Ӧ�ڳ�������ĥ�ϳ�LiFePO4ǰ���������ȴ��������ʯ��LiFePO4����SEM��XRD��EIS�ͺ�����ŵ�ȶ���Ʒ���б������о����������3%(Ħ������)Ti4+���ӵ�LiFePO4ӵ�����ŵĵ绯ѧ���ܣ�����Ʒ��0.1C��1C��2C�����µij�ʼ�ŵ�������ֱ�Ϊ150��130��125 mA��h/g����1C������ѭ��100�κ�ķŵ�������ߴ�133 mA��h/g��
�ؼ��ʣ�
LiFePO4��ǰ������Ti4+��������ĥ�����»�ԭ��
��ͼ����ţ�TM912.9 ���ױ�ʶ�룺A ���±�ţ�1672-7207(2009)02-0288-06
Preparation of Ti4+-doped LiFePO4 by precursor-doping and room temperature reduction via ball-milling
WU Ling, WANG Zhi-xing, LI Xin-hai, LI Ling-jun, ZHENG Jun-chao, GUO Hua-jun, LIU Jiu-qing
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China
Abstract: Ti4+-doped precursors (FePO4��2H2O) were prepared via co-precipitation method. LiFePO4 precursor-mixtures were obtained by ball-milling at room temperature, using FePO4��2H2O, Li2CO3 and oxalic acid as raw materials, and then olivine-type LiFePO4 were synthesized by the following heat treatment. The samples were characterized using scanning electron microscope, X-ray diffraction, electrochemical impedance spectroscopy and galvanostatic charge/discharge test. The results show that the sample doped with 3% Ti4+ (molar fraction) has the most impressive electrochemical performance as follows: its initial discharge capacities are 150, 130 and 125 mA��h/g at 0.1C, 1C and 2C rates, respectively, without capacity fading even after 100 cycles at 1C rate. Key words: LiFePO4; precursor; Ti4+-doping; ball-milling; room temperature reduction
���������������ʯ�ṹ�Ļ�����LiMPO4(M=Fe, Mn, Ni��Co)��Ϊ����ӵ����������������о��ȵ�[1-4]������Щ�������У�LiFePO4����������۱������ߡ���������ȫ�������ȶ����ŵ㣬��Ϊһ�ַdz���ǰ��������ӵ���������ϡ�Ȼ����LiFePO4���м��͵ĵ��ӵ�����(10-9~10-10 S/cm)[5]���������ɢ����(1.8��10-14 cm2/s)[6]��ʹ����߱����µĵ绯ѧ���ܺܲĿǰ��Ҫ�ĸĽ������У�a. ��LiFePO4����������������(̼�������ĩ)[7-8]����߷������ĵ絼�ʣ�b. ���Ӹ۽���������[5]������䱾���絼�ʣ�c. �Ż��ϳɹ��գ��Ʊ���ϸ(������������)LiFePO4��ĩ[9]������Li+����ɢ·����
Ŀǰ����LiFePO4���ӵ��о���Ϊ���෨[10-11]���ܽ�-������[12-13]�����У����෨������Ҫ���£��Ҳ���Ԫ������ͨ����е�ķ�����ԭ�ϻ�Ͼ��ȣ���ˣ������Ʊ������Ӿ��ȵ�LiFePO4��ϸ��ĩ���ܽ�-�������ijɱ��ߣ���ҵӦ�ü�ֵ���������߲���һ��ȫ�µIJ��ӷ�ʽ����ͨ��������ʹ��Ti4+������FePO4��2H2O�����������ȵؽ���������ڲ����Ӷ��õ���Ԫ�ؾ��Ȳ��ӵ�ǰ����FePO4��2H2O������ѡ��һ�����͵Ļ�ԭ�������Ҷ��ᣬ�û�ԭ���ڳ���������Դ���Դ��ĥ��ϣ��õ�dz��ɫ��LiFePO4ǰ���������ȴ��������ʯ���Ѳ���LiFePO4��һ���棬���������Ʊ���ǰ�������ϸС���������̼��ɱ��ϵͣ���һ���棬������ĥ��ԭʹ�ú����ȴ������յ��¶ȴ�ͣ���Ʒ��������С�����й����Ĺ�ҵǰ�����������߶�ǰ������Ӻͳ�����ĥ��ԭ����̽�֣��ص��о�Ti4+���Ӷ�LiFePO4����ò���ṹ�Լ��绯ѧ���ܵ�Ӱ�졣
1 ʵ ��
1.1 ���ϵ��Ʊ�
1.1.1 ǰ������Ʊ�
�ֱ��ȡ1 mol FeSO4��7H2O(AR)��1 mol H3PO4 (AR)��0, 0.01, 0.03��0.05 mol Ti(SO4)2��H2O(CP)������ȥ����ˮ�У���ǿ�ҽ����¼���������H2O2(AR)����NH3��H2O(AR)����pHֵ��2.1���ң���Ӧ10 min�����õ������ɫ����ϴ�ӡ��������Σ�Ȼ����120 �����12 h���ò�ͬ��Ti4+����FePO4��2H2O������Ti4+���ֱ�Ϊ0%��1%��3%��5%����Ʒ��ΪP0��P1��P3��P5��
1.1.2 LiFePO4���Ʊ�
����ѧ�����ȳ�ȡһ������ǰ���塢Li2CO3(AR)���Ҷ���(AR)�����Ҵ�(AR)Ϊ���ʣ��ڳ�������ĥ3 h��õ�dz��ɫ����ǰ���������������80 ���ɺ����������¹�ʽ¯���ڸߴ��(99.999%)�ı�������600 ������12 h����¯��ȴ�������ʯ��Ti4+����LiFePO4��
1.2 ���ϵı���
��ʵ������ձ�Rigaku D/max2550VB+18KWת��X���������ǽ������������
����������Cu K�����䣬40 kV��300 mA������0.02?����WinPLOTR�������㾧������������JEOL��˾��JSM-5600LVɨ��羵��20 kV�۲���Ʒ�ı�����ò��
Ԫ�ط������õ����Ϲ���ICP(IRIS intrepid XSP�������巢������ǣ�Thermo electron corporation)�ⶨǰ������Ѻ��������ظ���صζ���(SnCl2-HgCl2������)�ⶨǰ��������������õ¹�CS800����̼�����Ƿ���LiFePO4��Ʒ��̼������
1.3 ��ص���װ�����
��LiFePO4������̿�ں�ճ���(PVDF)��������8?1?1��ϣ�������Ϊ�����Ʊ���ֱ��Ϊ14 mm������Ƭ��������Ƭ�븺��Ƭ(Li��ֱ��Ϊ14 mm)�����Һ(1 mol/L��LiPF6/EC+EMC+DMC(�����1?1?1))��Ĥ(Celgard 2300 PP/PE/PP)�ڳ������������������װ��CR2025�Ϳ�ʽ��أ���ؾ���12 h��������BTS-5 V/1 mA��ز���ϵͳ���в��ԣ���������Ϊ�����£�2.5~4.1 V����0.1C��1C��2C������ŵ硣�����迹����������CHI660�绯ѧ����վ����ɣ�����Ƶ��Ϊ0.01 Hz~100 kHz�����Ҳ����Ϊ5 mV����ZView2�������迹������ϡ�
2 ���������
2.1 ǰ����
2.1.1 ǰ��������༰�ɷ�
ͼ1��ʾΪǰ����FePO4��yH2O��XRDͼ�ס���ͼ1��֪������Ʒ��XRDͼ�������Ե�����壬˵��FePO4��yH2OΪ���νṹ����������[14-15]�����Ľ��һ�¡�Ԫ�ط���������P0��P1��P3��P5��Fe�����ֱ�Ϊ30.18 %��29.86 %��29.80 %��29.62 %�����ӽ���FePO4��2H2O������������29.89%����ˣ�ǰ����Ľᾧˮ����Ϊ2��P1��P3��P5�IJ�Ti4+���ֱ�Ϊ0.96 %��2.97 %��4.95 %����Ŀ��ֵ(1 %��3 %��5 %)�dz��ӽ��������������Ʊ�ǰ����ʱTi4+����ȫ������ǰ�����С�
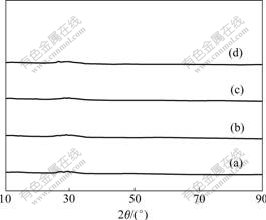
(a) P0��Ʒ; (b) P1��Ʒ; (c) P3��Ʒ; (d) P5��Ʒ
ͼ1 ǰ�����XRDͼ��
Fig.1 XRD patterns of precursors
2.1.2 ǰ�������ò
ͼ2��ʾΪ��ͬǰ�����SEM��Ti4+�IJ����ǰ�������òӰ�첻����Ʒ��һ�ο���������Ϊ0.1~0.5 ��m��һ�ο����ž۳ɶ�Ķ��ο������������ɵĽṹ���кܴ�ıȱ������������ǰ�������Դ�Լ���ԭ���Ӵ����Ӷ�ʹ��Ӧ���ӳ�֡�

(a) P0��Ʒ; (b) P1��Ʒ; (c) P3��Ʒ; (d) P5��Ʒ
ͼ2 ǰ�����SEM��
Fig.2 SEM images of precursors
2.2 LiFePO4
2.2.1 LiFePO4����ò
ǰ����FePO4��2H2O��Li2CO3���Ҷ����Ϊ��ɫ��������ĥ��Ļ����Ϊdz��ɫ�������п���ʾ��ɫ��ֻ��Fe(��)����ˣ��϶�������Fe(��)�Ļ�ԭ��Ӧ���ɴ��Ʋ����������ε�LiFePO4�����ڳ�����ĥ��ԭ���о��������[14]��
LiFePO4��Ʒ���ʻ�ɫ��̼�������������Ʒ������̼��ͼ3��ʾΪLiFePO4��Ʒ��SEM����Ʒ��ͬʱ����ϸС��һ�ο���(������1 ��m)����һ�ο����ž۶��ɵĶ��ο��������У�δ������Ʒ�Ŀ����ž۵ý����أ�������Ʒ�Ŀ����Ϸ�ɢ�����Ҳ�����Խ����Ʒ���ž۵Ŀ���Խ�٣���˵��Ti4+�IJ�������Ч�����ƿ����žۣ�ʹ����ϸ�������������Խ��Li+�ڹ�������ɢ��·��Խ�������ϵĵ绯ѧ���ܾ�Խ������Li+����ɢ����˿���ϸ��������LiFePO4�����ķ���[16]�����⣬����ϸ�������˲��ϵıȱ�������Ӷ���������ߴ�����ŵ�ʱLiFePO4��������[1]��

(a) P0��Ʒ; (b) P1��Ʒ; (c) P3��Ʒ; (d) P5��Ʒ
ͼ3 ��ͬ��Ti4+��LiFePO4��Ʒ��SEM��
Fig.3 SEM images of LiFePO4 samples with different Ti4+ contents
2.2.2 LiFePO4�Ľṹ
ͼ4��ʾΪLiFePO4��Ʒ��XRDͼ�ף�Ƕ���СͼΪ(131)�������ľֲ��Ŵ�ͼ����LiFePO4�ı�ͼ��(JCPDS No.40-1499)��ȣ���Ti4+����3%���µ���Ʒ��Ϊ���࣬������Ti4+���ߴ�5%ʱ�����Li4P2O7���ࡣ����Chung��[5]����IJ��ӻ������������ӿ���ռ��M1(Li)λ����M2(Fe)λ����ռ��M1λʱ������������LiFePO4�γɹ����壬�����������[10, 12]��������������ռ��M2λʱ���ܳ���Li3PO4��Fe3P��Li3Fe2(PO4)3������[11, 13]������Ti4+�İ뾶(0.064 nm)��Li+�뾶(0.068 nm)�����С��Fe2+�İ뾶(0.074 nm)��Ti4+��������ȡ��Li+��ռ��M1λ����ˣ�����Ti4+���ϵ�ʱ��Ti4+����ռ��M1λ����LiFePO4�γ��˹����壬��������ࣻ��Ti4+���ϸ�ʱ������Ti4+ռ����M2λ�������������Li4P2O7��
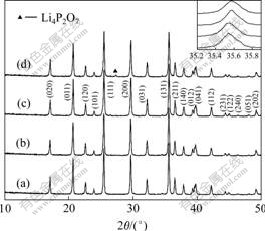
(a) P0��Ʒ; (b) P1��Ʒ; (c) P3��Ʒ; (d) P5��Ʒ
ͼ 4 ��ͬ��Ti4+��LiFePO4��Ʒ��XRDͼ��
Fig.4 XRD patterns of LiFePO4 samples with different Ti4+ contents
����ǿ��ľֲ��Ŵ�ͼ��֪�����Ų�Ti4+�������ߣ���ǿ����߽Ƕ�ƫ�ơ�����Bragg����(ʽ1)����λ��߽Ƕ�ƫ�ƣ�������d ��С������Scherrer��ʽ(ʽ2)��֪������ֱ��(D)�������İ�߿��ɷ��ȣ�����(131)������������ľ����ߴ�D131���1��ʾ���ɼ��������ߴ����Ų�Ti4+�������߶��Լ�С��
![]()
![]()
���У���Ϊ�����߲�������Ϊ����������ǣ�KΪScherrer������K=0.89����Ϊ�����İ�߷����
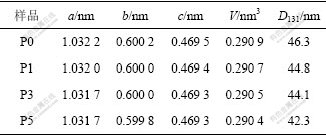
��1��ʾΪ���������ݼ�����ľ�������ֵ����������a��b��c�;������V�����Ų�Ti4+�������߶����м�С���������ڵ��������ϵ�ʱ��1 mol Ti4+ռ��M1λ����4 mol �ȱ�ݣ�����Li+��Ũ�Ƚ��ͣ��Ӷ��������������������ϸ�ʱ������Ti4+ռ��M2λ������Ti4+�뾶��Fe2+�뾶С���Ӷ��������������⣬�ȱ�ݵIJ������Դ�����LiFePO4�ĵ����ԡ�����Chung��[5]���������ģ�ͣ�LiFePO4����Ƕ﮹�����Fe3+��Fe2+�ĺ��������仯���Ӷ�����LiFePO4��P�ͺ�N��֮��ת������Ƕ�̬���ȱ�ݵĴ���ʹFe3+�������ӣ���LiFePO4��P�ͳɷ����ӣ������̬�����෴��N�ͳɷ����ӡ�Ƕ�̬ʱ�ɷ�Ϊ![]() �����̬ʱ�ɷ�Ϊ
�����̬ʱ�ɷ�Ϊ![]() �����У�xΪTi4+�IJ�������(a+x)ΪLi��ȱ������Fe3+/Fe2+��ϼ�̬���γɼ���������LiFePO4�ĵ�����[5, 17]��
�����У�xΪTi4+�IJ�������(a+x)ΪLi��ȱ������Fe3+/Fe2+��ϼ�̬���γɼ���������LiFePO4�ĵ�����[5, 17]��
�� 1 ��ͬ��Ti4+��LiFePO4��Ʒ�ľ��������;����ߴ�
Table 1 Lattice parameters and crystallite size of LiFePO4 samples with different Ti4+ contents
2.2.3 LiFePO4�ĵ绯ѧ����
ͼ5��ʾΪLiFePO4��Ʒ�Ľ����迹�����Ч��·ģ�����ߡ���ͼ5�ɼ���ģ��������Խ�������Ǻϣ�˵����Ч��·�Ǻ����ġ���Ч��·�У���Re�������Һ���裬���迹���б���Ϊ����Ƶ����z����Ľؾࣻ��Rf��CPE1(Cb)��������Li+�ڲ��ϱ������Ĥ��Ǩ���������Ĥ�����Ĥ���ݣ���Rct��CPE2(Cdl)��������Li+ �ڻ������ʱ���ͽ���Ĥ֮��ĵ��Ǩ�Ƶ����˫����ݣ����У�����λԪ��CPE1��CPE2��Ϊ������������ʵ�����[18]�����յ�Ч��·���迹���и�Ƶ������Ƶ��Ӧ�÷ֱ���1����Բ����ʵ����ֻ��1����Բ����ˣ���Բ���Կ����Ǹ�Ƶ������Ƶ����2����Բ���Ӷ��ɣ���ֱ��D����Ĥ�迹����Ǩ���迹֮��(��ΪZf+ct)��Li+�ڵ缫��������ɢ�������Warburg�迹��Zw���������迹���б���Ϊ��Ƶ����ֱ�ߡ���ͼ 5��֪��Ti4+�IJ���ʹZf+ct����С��3% Ti4+���ӵ���Ʒ��δ���ӵ���Ʒ��ȣ�Zf+ct��830 �����͵�130 ������˵��Ti4+ �����ܴ�������LiFePO4�缫����ĵ�ɴ������ʣ����⣬Ti4+�IJ���Ҳʹ�õ�Ƶ��ֱ�ߵ�б������Warburg�迹��С���Ӷ�������Li+�ڵ缫�����е���ɢ��Zf+ct��Zw�ļ�С�����ڿ˷���ŵ�����еĶ���ѧ���ƣ�ʹ��Li+��LiFePO4�����е���/Ƕ��ȵõ���ߣ�������Li+�ڿ����ڲ��ͱ����Ũ�Ȳ�Ӷ������ڲ��ϱ���������ߺ�ѭ�����ܵĸ��ơ�

1��P0��Ʒ; 2��P1��Ʒ; 3��P3��Ʒ; 4��P5��Ʒ; 5����Ͻ��
ͼ 5 ��ͬ��Ti4+��LiFePO4��Ʒ�Ľ����迹�����Ч��·ģ������
Fig.5 EIS and equivalent circuit fitting results of LiFePO4 samples with different Ti4+ contents
ͼ6��ʾΪLiFePO4��Ʒ�ڲ�ͬ�����µ��״ηŵ����ߡ���ͼ6��֪�����Ų�Ti4+����������Ʒ��0.1C��1C��2C�����µ��״ηŵ���������ϴ�������ߣ�����Ti4+��Ϊ3%ʱ�ﵽ���ֵ��3% Ti4+���ӵ�LiFePO4��0.1C��1C��2C�����µij�ʼ�ŵ�������ֱ�Ϊ150��130��125 mA��h/g����δ������Ʒ�ֱ������4.2%(144 mA��h/g)��15.0%(113 mA��h/g)��27.6%(98 mA��h/g)������ǰ��ķ�����Ti4+��LiFePO4�ĵ绯ѧ�������������ƣ�������Ϊ��Ti4+�IJ��������Ч������LiFePO4�������žۣ�ʹ����ϸ�����Ӷ�������LiFePO4�����ķ��ӣ�Fe3+/Fe2+��ϼ�̬���γ������LiFePO4�ĵ����ԣ�Ti4+ �����ܴ�������LiFePO4�缫�����Լ��缫�����еĵ�ɴ������ʡ����ǣ�����Ti4+ ����������ʱ���ŵ������������С��5%Ti4+���ӵ�LiFePO4��0.1C��1C��2Cʱ�ķŵ�������ֱ�Ϊ141��123��112 mA��h/g����3% Ti4+���ӵ���Ʒ��ȷֱ��С6.0%��5.4%��10.4%��������������(Li4P2O7)�ij��ֵ����������͡�
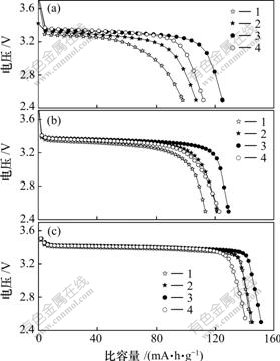
(a) 2C; (b) 1C; (c) 0.1C
1��P0��Ʒ; 2��P1��Ʒ; 3��P3��Ʒ; 4��P5��Ʒ
ͼ 6 ��ͬ��Ti4+��LiFePO4��Ʒ�ڲ�ͬ�����µ��״ηŵ�����
Fig.6 Initial discharge curves of LiFePO4 samples with different Ti4+ contents at various rates
ͼ7��ʾΪLiFePO4��Ʒ��1C�����µ�ѭ�����ܡ���Ti4+��Ϊ0%��1%��3%��5%��LiFePO4��Ʒ��1C�����µ��״ηŵ�������ֱ�Ϊ113��122��130��123 mA��h/g��ѭ��40�κ�ķŵ�������ֱ�Ϊ104 mA��h/g(˥��8.0%)��117 mA��h/g(˥��4.1%)��133 mA��h/g(����2.3%)��128 mA��h/g(����4.1%)���ɼ���Ti4+���������ظ�����LiFePO4�ڴ�����ŵ�ʱ��ѭ�����ܣ����䵱�������ﵽ3%����ʱЧ���ر����ԣ���Ti4+ 3%��5%��LiFePO4��Ʒ��ѭ��40�κ�ķŵ����������û�н��ͣ������������ߣ����ǻ���������ѭ�������������ġ�3% Ti4+���ӵ�LiFePO4ѭ��100�κ�ķŵ�������Ըߴ�133 mA��h/g�����������ѭ������ʹ�����dz��ʺ�����Ϊ���۵Ķ�������������ϡ�
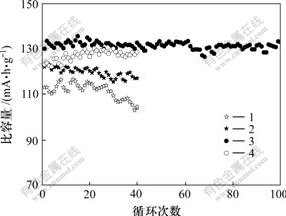
1��P0��Ʒ; 2��P1��Ʒ; 3��P3��Ʒ; 4��P5��Ʒ
ͼ7 ��ͬ��Ti4+��LiFePO4��Ʒ��1C�����µ�ѭ������
Fig.7 Cycling performance of LiFePO4 samples with different Ti4+ contents at 1C rate
3 �� ��
a. ��Ti4+���ܵ�FePO4��2H2O�����У�������LiFePO4������һ��ȫ������Ч�IJ��ӷ�ʽ��ǰ�����е��Ѻ������ӽ������Ti4+����
b. ���Ҷ���Ϊ��ԭ������������ĥ��Fe(��)��ԭ��Fe(��)����ĥʹ�ú����ȴ����¶Ƚϵͣ���Ʒ����ϸС��������ĥ��ԭ-�����ս�ᾧ��ΪLiFePO4�ĺϳ��ṩ��һ���·�����
c. Ti4+��������Ч������LiFePO4�����žۣ����Ҳ�����Խ����Ʒ���ž۵Ŀ���Խ�١�������Ti4+���Ӳ���ı�LiFePO4�ľ���ṹ������������Сʱ��Ti4+����ռ��Liλ����LiFePO4�γɹ����壻���������ϴ�ʱ������Ti4+ռ��Feλ����������Li4P2O7��Ti4+���Ӽ���������LiFePO4�ĵ绯ѧ���ܣ��ر��Ǵ����µ�ѭ�����ܡ�
�ο����ף�
[1] Padhi A K, Nanjundaswamy K S, Goodenough G B. Phospho-olivines as positive-electrode materials for rechargeable lithium batteries[J]. J Electrochem Soc, 1997, 144(4): 1188-1194.
[2] Li G, Azuma H, Tohda M. LiMnPO4 as the cathode for lithium batteries[J]. Electrochem Solid-State Lett, 2002, 5(6): A135-A137.
[3] Wolfenstine J, Allen J. LiNiPO4-LiCoPO4 solid solutions as cathodes[J]. J Power Sources, 2004, 136: 150-153.
[4] Rabanal M E, Gutierrez M C, Garcia-Alvarado F, et al. Improved electrode characteristics of olivine-LiCoPO4 processed by high energy milling[J]. J Power Sources, 2006, 160: 523-528.
[5] Chung S Y, Bloking J T, Chiang Y M. Electronically conductive phospho-olivines as lithium storage electrodes[J]. Nat Mater, 2002, 1(2): 123-128.
[6] Prosini P P, Lisi M, Zane D, et al. Determination of the chemical diffusion coefficient of lithium in LiFePO4[J]. Solid State Ionics, 2002, 148: 45-51.
[7] �� ��, ���º�, ���Ȩ, ��. ���ºϳ�LiFePO4/C�������ϼ���绯ѧ����[J]. ���ϴ�ѧѧ��: ��Ȼ��ѧ��, 2006, 37(3): 505-508.
ZHANG Bao, LI Xin-hai, ZHU Bing-quan, et al. Low temperature synthesis and electrochemical properties of LiFePO4/C cathode[J]. J Cent South Univ: Science and Technology, 2006, 37(3): 505-508.
[8] Croce F, Epifanio A D, Hassoun J, et al. A Novel concept for the synthesis of an improved LiFePO4 lithium battery cathode[J]. Electrochem Solid-State Lett, 2002, 5(3): A47-A50.
[9] Wang L, Huang Y, Jiang R, et al. Preparation and characterization of nano-sized LiFePO4 by low heating solid-state coordination method and microwave heating[J]. Electrochimica Acta, 2007, 52: 6778-6783.
[10] HU Guo-rong, GAO Xu-guang, PENG Zhong-dong, et al. Influence of Ti4+ doping on electrochemical properties of LiFePO4/C cathode material for lithium-ion batteries[J]. Trans Nonferrous Met Soc China, 2007, 17: 296-300.
[11] SUN Yu-heng, LIU Xing-quan. Preparation and characterization of novel Ti-doped M-site deficient olivine LiFePO4[J]. Chinese Chem Lett, 2006, 17(8): 1093-1096.
[12] Hu Y, Doeff M M, Kostecki, et al. Electrochemical performance of sol-gel synthesized LiFePO4 in lithium batteries[J]. J Electrochem Soc, 2004, 151(8): A1279-A1285.
[13] Wang G X, Bewlay S, Needham S A, et al. Synthesis and characterization of LiFePO4 and LiTi0.01Fe0.99PO4 cathode materials[J]. J Electrochem Soc, 2006, 153(1): A25-A31.
[14] ZHENG Jun-chao, LI Xin-hai, WANG Zhi-xing, et al. LiFePO4 with enhanced performance synthesized by a novel synthetic route[J]. J Power Sources, 2008, 184(2): 574-577.
[15] ������, ������, �ƿ���, ��. �����¶ȶԺϳ�LiFePO4�IJ�����ɺ͵绯ѧ���ܵ�Ӱ��[J]. ������ѧѧ��, 2007, 23(7): 1117-1122.
LIU Su-qin, GONG Ben-li, HUANG Ke-long, et al. Effect of calcination temperature on the compositions and electrochemical performance of products in the synthesis of LiFePO4[J]. Acta Phys Chim Sin, 2007, 23(7): 1117-1122.
[16] Prosini P P, Carewska M, Scaccia S, et al. A new synthetic route for preparing LiFePO4 with enhanced electrochemical performance[J]. J Electrochem Soc, 2002, 149(7): A886-A890.
[17] Thackeray M. Lithium-ion batteries: an unexpected conductor[J]. Nat Mater, 2002, 1(2): 81-82.
[18] Chang Y C, Sohn H J. Electrochemical impedance analysis for lithium ion intercalation into graphitized carbons[J]. J Electrochem Soc, 2000, 147(1): 50-58.
�ո����ڣ�2008-07-20�������ڣ�2008-10-30
������Ŀ�������ص�����о���չ�ƻ�(973�ƻ�)������Ŀ(2007CB613607)
ͨ�����ߣ���־��(1970-)���У�����¦���ˣ���ʿ�����ڣ����µ绯ѧ���̬��ѧ�о����绰��0731-8836633��E-mail: wuling19840404@163.com


