�й���ɫ����ѧ�� 2004,(08),1426-1430 DOI:10.19476/j.ysxb.1004.0609.2004.08.030
�����Ʊ�LaF3��ϸ��
������ѧ������ұ��ѧԺ,������ѧ������ұ��ѧԺ,������ѧ������ұ��ѧԺ,������ѧ������ұ��ѧԺ,������ѧ������ұ��ѧԺ,������ѧ������ұ��ѧԺ ����110004 ,����110004 ,����110004 ,����110004 ,����110004 ,����110004
ժ Ҫ��
��La2O3��HClΪԭ���Ʊ���LaCl3,��ֱ����˫����,��LaCl3��ҺͬNH4HCO3��Һ���úϳ������Ƚ�С��La2(CO3)3����;�Է���La2(CO3)3Ϊ��Դ��NH4F���,���������¾������ѧ��Ӧ,�ϳ���LaF3��ϸ��;�о��˲�ͬ��ɢ���ȷ�Ӧ�����Ժϳ�LaF3��ϸ�۵����Ⱥʹ��ȵ�Ӱ��;ͨ��X��������(XRD)����˲�ͬ;���ϳɵ�LaF3��ϸ����Ĵ���,ͨ��ɨ��羵(SEM)����羵(TEM)�����˲�ͬ;���ϳɵ�LaF3��ϸ������������Ⱥ���ò���������:���Ҵ���Ϊ��ɢ���������ȹ���ϳɵõ��˴��Ƚϸ�,ƽ������ԼΪ50nm��LaF3��ϸ�ۡ�
�ؼ��ʣ�
��ͼ����ţ� TB444
����飺��Ԫɽ(1962),��,������,��ʿ�о���.�绰:13050151892;E mail:hysh 7689@163.com;
�ո����ڣ�2003-12-02
����������Ȼ��ѧ����������Ŀ(50174015);
Preparation of superfine powder of LaF3 by microwave method
Abstract��
The LaF3 superfine powder was synthesized. Superfine powder of La2(CO3)3 was first synthesized by means of double pillar method in the reaction that LaCl3 solution(got from La2O3, HCl as raw material ) reacted with NH4HCO3 solution.Then LaF3 superfine powder was got by means of mixing solid La2(CO3)3 and NH4F under the microwave condition when the diluent of H2O and C2H5OH were used.The influence of diluent (H2O, C2H5OH) on grain degree or pure degree was discussed. The crystal purity of LaF3 superfine powder was tested by XRD.The granularity and shape of LaF3 superfine powder was tested by SEM and TEM. The results show that the purity of LaF3 superfine powder is very well when used C2H5OH by means of microwave heat, and LaF3 superfine powder is 50 nm in size in the direct solid synthesis.
Keyword��
LaF3; microwave; superfine powder;
Received�� 2003-12-02
LaF3�����������ӵ絼����ߵķ����ӵ���, ���㷺�������������ϡ� LaF3��LaF3����CaF2���Ͽ�������Ƭ״��Ĥ, ���LaF3�������������崫����, �����о�����������F2�� H2�� CO�� O2�� SO2�� CO2�ȳɷ֡� ��LaF3�����Ʊ�������ѡ��缫, �������������Һ�з�����Ũ�ȡ� ����LaF3��LaF3���Ӳ����ڹ������ʴ������� ����ѡ��缫������Ĺ㷺����, ʹ�ø����о��߷�עLaF3������Ʊ�
LaF3��ϸ������������������ԡ� LaF3�Ƴɳ�ϸ��, ����������ű���������Ӷ�����, �ȿ��Դٽ�������������Ӽ�������, �ֿ��Խ����Ʊ�LaF3�����Ͷྦྷ�Ȳ���ʱ���ս��¶ȡ� ��ϸ��LaF3����������֬�����Ӽ�, �������������֬����ѹ���ܡ� �������ԺͿ���������, ��һ������ĥ���Ħ���� �ڴż�¼Ԫ����Ϳ������LaF3��ϸ����Ϊ������, ʹͿ�㼰��ͷ���������100��� ����, LaF3���ǽ����Ȼ�ԭ����ȡ��һϡ����������Ҫԭ��, ���ڷ������ ��������ɫ�����Ͻ����Ӽ��� ���Ų��ϡ� ����Ͻ�ȷ���Ҳ������Ҫ����;
��ͳ�Ʊ�LaF3 ���巽����
����������La2O3 �� �����NH4HCO3Ϊԭ��, ����˫�����Ʊ����̼���Ρ�La2(CO3)3, ����La2(CO3)3Ϊ��Դ, ��NH4F�ڹ���ֱ�ӻ��, ���������ºϳ�LaF3��ϸ�ۡ�
1 ʵ��
1.1 ԭ��
��La2O3�� ��������ȡLaCl3, ʹLaCl3�뱥��NH4HCO3��Һ��ַ�Ӧ�Ƶ��м����La2(CO3)3
��Ӧ(3)�����������½��е�, �����˸�������, �ⲻ���ٽ��˷�Ӧ���ҽ���, ���Բ������˽����ϸ�������á�
1.2 �Լ�������
������(La2O3)�� ̼�����(NH4HCO3)�� Ũ����(HCl)�� ������(NH4F)��ΪAR���� NH4F��80 �������ճ�������24 h, �������ĥ�õ��� ����4B76120B�� LG������¯��Ϊ��ѧ��Ӧ�ļ���װ��, �ֱ����ձ���ѧD/max-3A��ĩ�����ǡ� �ձ�����SSX-550ɨ��羵�� ����������EM400T��羵�۲���崿�Ⱥ���ò������
1.3 ����
����˫����
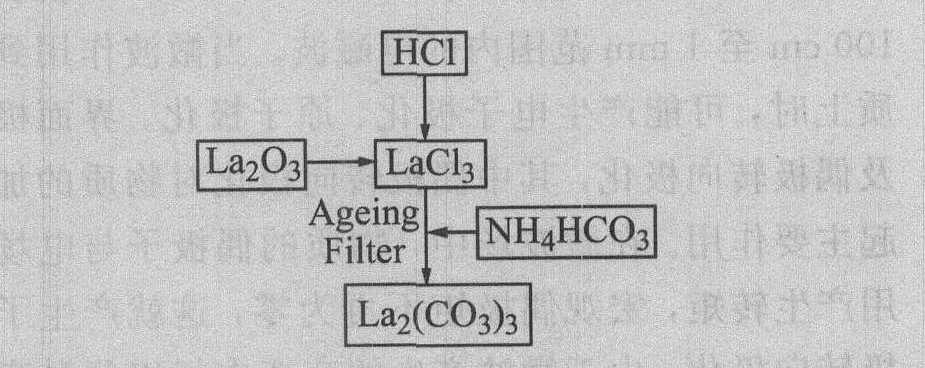
˫�����Ʊ�La2(CO3)3�Ĺ���������ͼ1��ʾ�� ��ȡһ������La2O3, ȡ������Ũ���Ὣ��ϡ�ͺ���La2O3���, ����70��80 ��ˮԡ��, ����15 min��ַ�Ӧ, ������Һ��ȫ�����LaCl3�� ������LaCl3��Һͬ�����NH4HCO3������Һ, �ֱ�LaCl3��Һ�ͱ���NH4HCO3��Һװ������Һ����, ��2����Һ����ͬ���ٶȵε����Ͻ���ķ�Ӧ���ڻ������̼����La2(CO3)3������ ���������»�����ˡ� ϴ��, �����ں�������100 ���¸���12 h�� ���ڳ�����Ӧ���ɵ�La2(CO3)3����Ѹ�����߷�ɢ��������, �Ӷ��õ���La2(CO3)3���������С�� ������Ϊ��Դ, �������ڵõ�����С�ҷֲ�խ��LaF3��ϸ�ۡ�
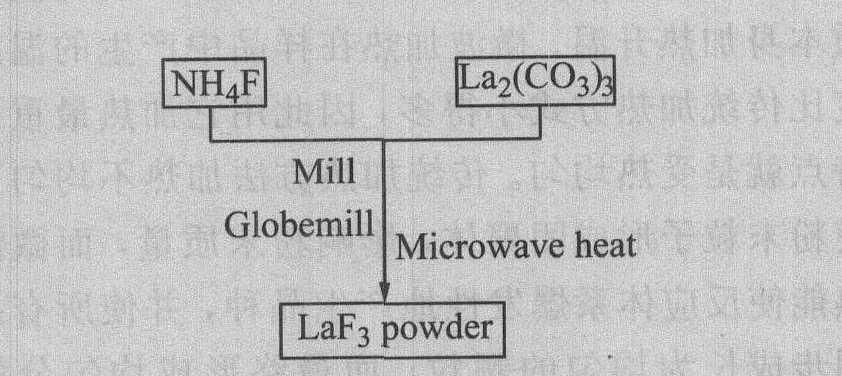
����������, ��La2(CO3)3Ϊ��Դ��NH4F��Ӧ�Ʊ�LaF3��ϸ�۵Ĺ���������ͼ2��ʾ��
����ѧ�����ȳ�ȡNH4F��La2(CO3)3, �ֱ���ˮ�� ��ˮ�Ҵ�����ɢ��, �� La2(CO3)3�� NH4F ��ĩ�ͷ�ɢ��������в���Ϻ����������ĥ���н�һ����ĥ���24 h, �ٽ���Ϸ�ĩ������¯�����»��ʼ��ȡ� �����о���ͬ����ʼ��Ӧ���������ʧ���, ȷ����ַ�Ӧ��ʱ��, Ȼ���Ʊ�����Ҫ����Ʒ��
ͼ1 ˫�����Ʊ�La3(CO3)3�Ĺ�������
Fig.1 Technological process of preparation of La2(CO3)3 by double pillar
ͼ2 �����Ʊ�LaF3��ϸ�۵Ĺ�������
Fig.2 Technological process of preparation of LaF3 superfine powder by microwave
2 ���������
2.1����˫�����Ʊ�La2(CO3)3
����˫�����Ʊ���La2(CO3)3��ĩ��SEM��ò��ͼ3��ʾ�� ���Կ���, La2(CO3)3��ĩ������һ����1 ��m����, �ֲ��Ͼ���, �Դ�Ϊ�����Ʊ�LaF3��ϸ�۵���Դ, �������ںϳɷֲ�խ��LaF3��ϸ�ۡ�
ͼ3 La2(CO3)3��ĩ��SEM��ò
Fig.3 SEM image of La2(CO3)3 powder
2.2LaF3��ϸ�۵����ϳ� [14,15]
����Ƶ��ԼΪ300 MHz��300 GHz, ������100 cm��1 mm��Χ�ڵĵ�Ų��� �������õ�������ʱ, ���ܲ������Ӽ����� ԭ�Ӽ����� ���漫����ż��ת��, ����ż��ת�������ʵļ�������Ҫ���á� ��������, ���ʵ�ż������糡���ò���ת��, ���ż���ز���Ϊ��, ��Ͳ�����ż��ת���� �����������Ľ���糡��ÿ��ߴ����ڴεĸ��ٱ���, ż��ת�����߱�Ѹ�ٸ��Ͻ���糡���������ͺ��ڵ糡, �Ӷ����²����ڲ����ʺ�ɢ, һ��������ת��Ϊ����, �ɴ�ʹ�����ʱ����������¡� ����������Ʒ�в������¶��ݶȱȴ�ͳ���ȷ�ʽС�ö�, ���������������Ҫ���ص�������Ⱦ��ȡ� ��ͳ���ȷ������Ȳ����ȿ���ʹ��ĩ�����γ��ž���, Ӱ���ĩ����, ����������ʹ��Ӧ��ϵ�����Եز�������, ��ʹ���о���ͬ���ɳ�Ϊ���ȵĿ���, �������γɾ��ȷ�ɢ��ϵ�� �봫ͳ�������, �������������ŵ�: 1) �������������ڵ�ų�������������Ķ�������������, ��ʵ�ַ���ˮƽ�ϵĽ���, ���Ⱦ���, �¶��ݶ�С, �����������ڶ��¶��ݶȺ����еķ�Ӧ; 2) ��������������������ȡ���������Ľ������, ��������ɸ�����Ҫ�Ի�������еĸ�����ֽ���ѡ���Լ���, �����ѡ��ͬ�ķ�ɢ�������Ʒ�Ӧ�����������; 3) ���������ͺ�ЧӦ, ���ر���Դ��, ������������������, ������һ���Կɽ��ж��¶ȿ���Ҫ��ܸߵķ�Ӧ; 4) ��������������Ч�ʸ�, �������·dz�Ѹ��, ���õõ��ɼӿ촦�������ٶ�, ����Լ��Դ��
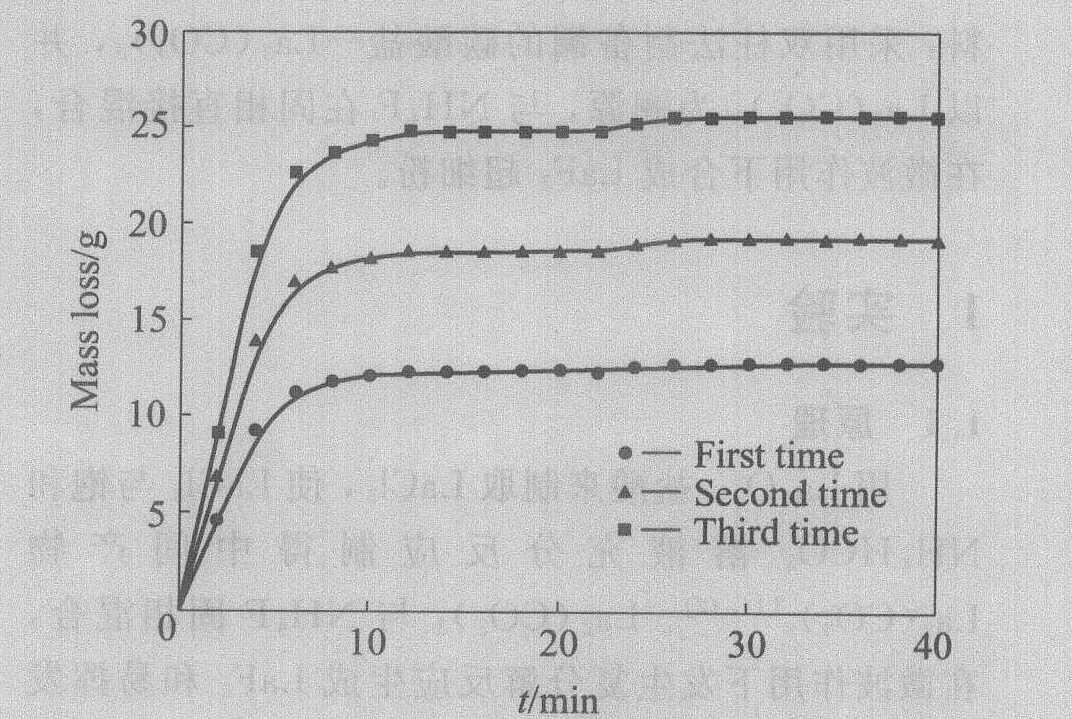
��La2(CO3)3Ϊ��Դ, ��Ӧ����ʱ���������ʧ�仯��ͼ4��ʾ�� ��ͼ4�ɿ���, ��ͬ�����ķ�Ӧ�����ķ�Ӧ��Ҫ�������������12 min����, ��30��40 min֮�䷴Ӧ��������������䡣 ��˽�����ʱ��ȷ��Ϊ40 min, ���Ա�֤��Ӧ�ij�ֽ��С�
ͼ4 ������ʧ����
Fig.4 Curves of mass loss
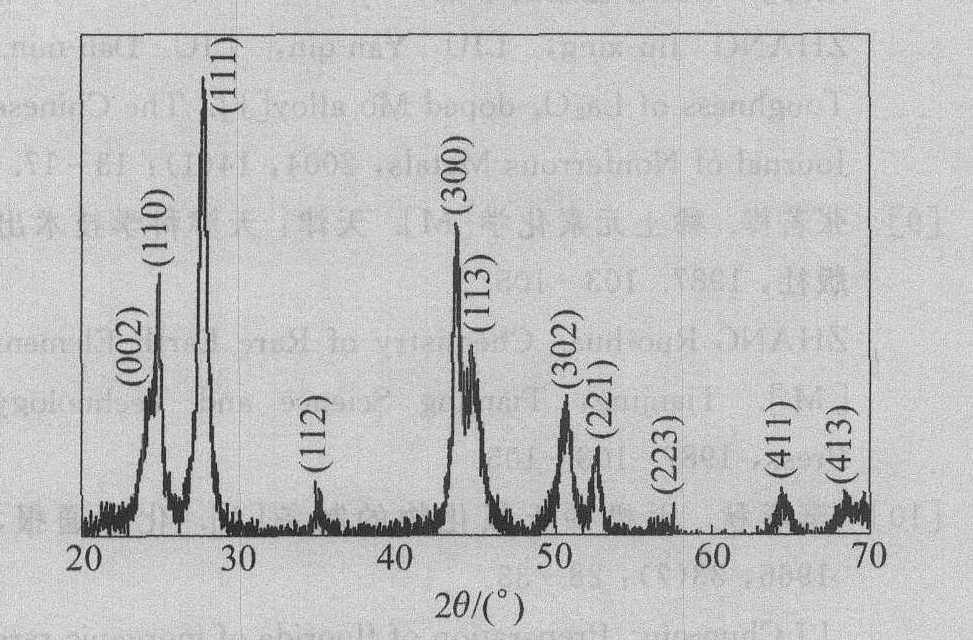
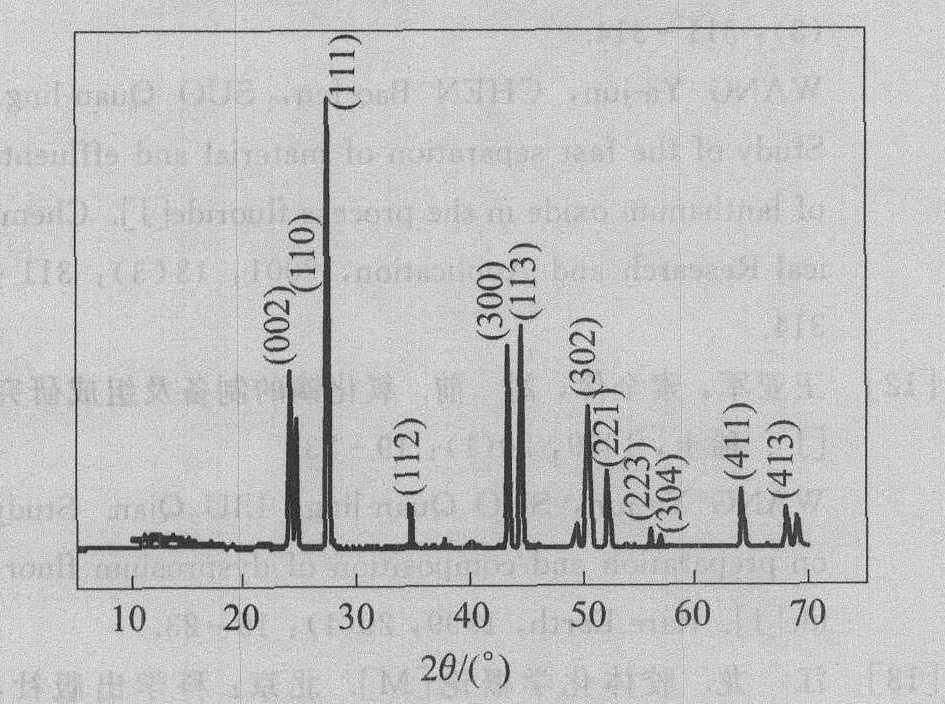
��La2(CO3)3ͬNH4F������, ����¯�»���, ��ɢ���ֱ�ѡ�ô�ˮ����ˮ�Ҵ�ʱ, �Ƶõ�LaF3��ϸ�۵�XRD�ֱ���ͼ5�� 6��ʾ, SEM�� TEM��ò�ֱ���ͼ7�� 8��ʾ��
��ͼ5��6���Կ���,����ˮ�Ҵ��ȴ�ˮ����ɢ���õ���LaF3��ϸ�۵Ĵ��ȸߡ�����������ˮ��NH4F��La2(CO3)3���ܽ�ȴ�ö�,����ˮ����ɢ��ʱ,һ��ˮ������,NH4F�״������ϲ��ˮ��,�����ȿ��ٳ�ˮ��,һ����NH4Fֱ�������ڻ����ı���,�����������NH4F��La2(CO3)3û����ȫ���Ȼ�ϡ���NH4F��La2(CO3)3������ˮ�Ҵ����ܽ�Ⱥ�С,��ˮ�Ҵ�����Ϊ��ɢ������ʵ�־��Ȼ�ϡ�����,ˮ����ˮ�Ҵ����������ղ�ͬ,Ҳ�ᵼ�¶����ȹ�����һ���IJ��졣
ͼ5 ��ˮΪ��ɢ����LaF3��ϸ�۵�X����������
Fig.5 XRD pattern of LaF3 superfine powder with water diluent
ͼ6 ����ˮ�Ҵ�Ϊ��ɢ���Ƶõ� LaF3��ϸ�۵�X����������
Fig.6 XRD pattern of LaF3 superfine powder with alcohol diluent
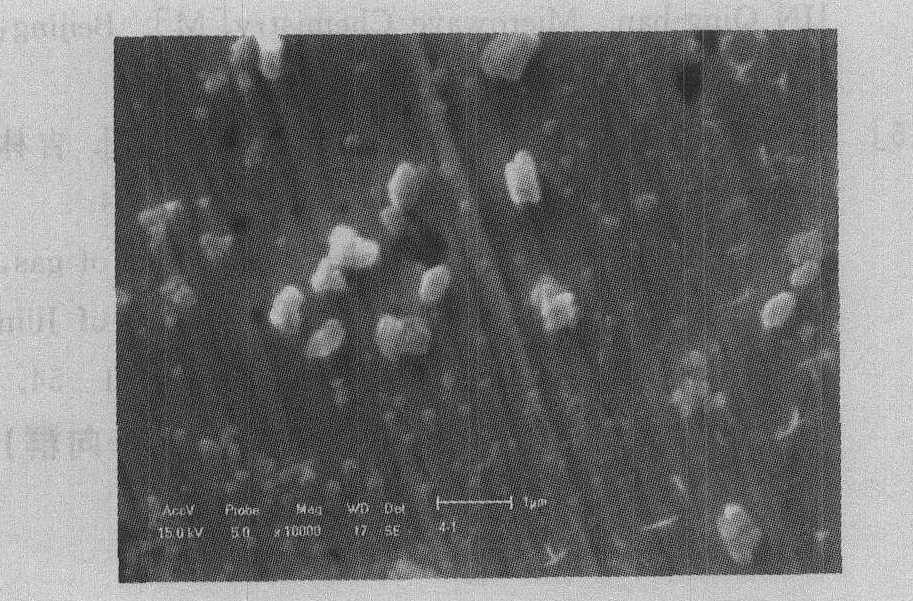
ͼ7 ��ˮΪ��ɢ����LaF3��ϸ�۵�SEM��ò
Fig.7 SEM image of LaF3 superfine powder with water diluent
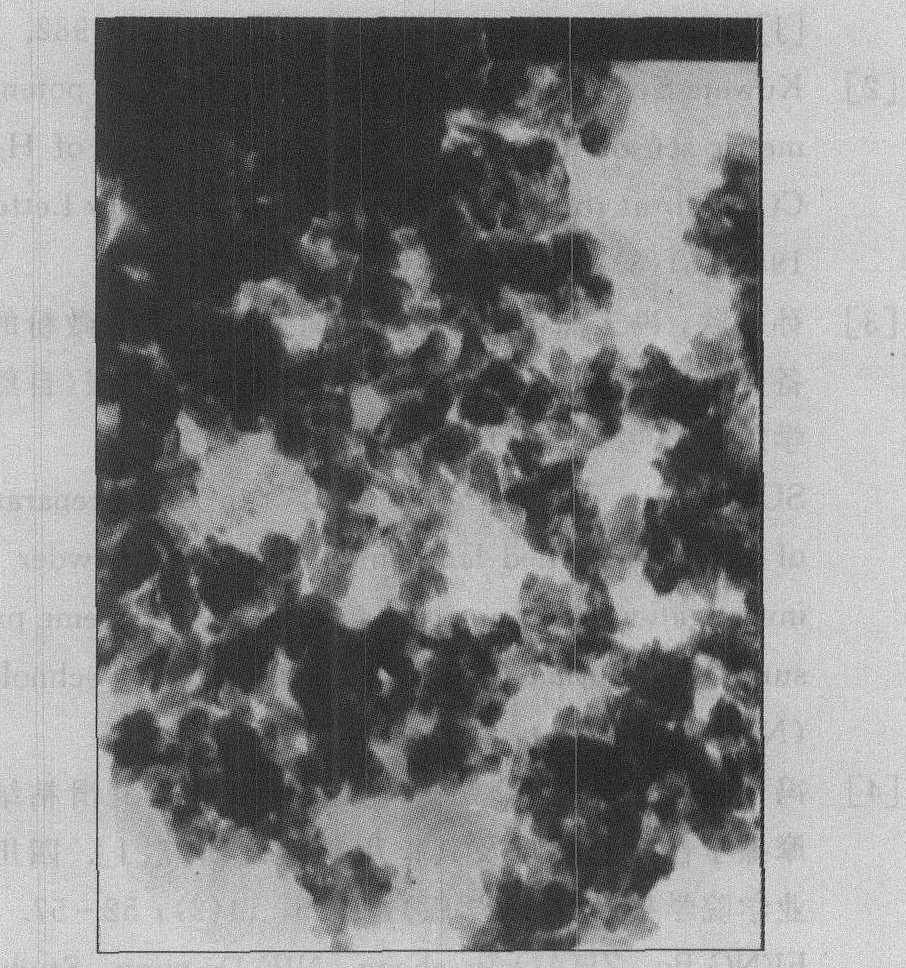
��ͼ7����,ʹ��ˮ����ɢ���õ���LaF3�����ϴ�,����������״�������,һ��ԼΪ200nm����ͼ8Ϊʹ����ˮ�Ҵ�����ɢ���õ��IJ������ȽϾ���(�������ž�),�����ȶ���С,һ��Ϊ50 nm���ҡ�ˮΪ��ɢ��ʱ�õ������ӽϴ�,��Ϊˮ���ӵ��ǻ�����ˮ�Ҵ����ǻ��Ļ��Ը�,NH4F�������ܽ�Ƚϴ��La2(CO3)3��С��������ʱ,�˴�����ʵ�־��Ȼ��,ʹ��LaF3�����ڷ�Ӧ��ϵ����������,������������������ϴ�����ӡ���ˮ�Ҵ���ɢ��ʱ,�������žۿ�������Ϊ���ȳɺ����õ���С�����й�ʣ�ıȱ���������,ʹ�����Ӽ���������žۡ�
ͼ8 ����ˮ�Ҵ�Ϊ��ɢ���Ƶõ� LaF3��ϸ�۵�TEM��ò
Fig.8 TEM image of LaF3 superfine powder with alcohol diluent
3 ����
1) ��La2O3�� HCl(Ũ)Ϊ��ʼ��Ӧ���Ʊ���LaCl3, ����˫����ͨ��LaCl3��NH4HCO3����, �Ʊ������ȷֲ����ȵ�La2(CO3)3���塣
2) �ֱ��Դ�ˮ����ˮ�Ҵ�����ɢ��, ��La2(CO3)3Ϊ��ԴͬNH4F����, ������¯���»���, ��ֱ�ӵĹ��෴Ӧ�õ���LaF3���塣 ������ˮ�Ҵ�Ϊ��ɢ���õ���LaF3���Ƚϸ�, ƽ������ԼΪ50 nm��
�����
[1] ��KuwataS,MiuraN.ApotentiometricoxygensensorusingLaF3singlecrystaloperativeatroomtemperature[J].