DOI��10.19476/j.ysxb.1004.0609.2017.10.21
����Ĥ��ⷨ�����Ȼ�����Һ�к���ͭ��
�� ��1��������1�������1��������1, 2
(1. ���ϴ�ѧ ұ���뻷��ѧԺ����ɳ 410083��
2. ���ϴ�ѧ ϡ�н���ұ��������Ʊ�����ʡ�ص�ʵ���ң���ɳ 410083)
ժ Ҫ��
�������г�����ͭ���ڽ���ʱ����ͭ����ͬ���������Һ��������ͭ����ѧ������������Է��롣�����һ���⣬����������Ĥ��⣬ͨ�����Ʋ۵�ѹ��������Һ�е�ͭ�������켫�ࡢ���Һ�¶ȡ��۵�ѹ��ͭ��Ũ�ȵ����ض�ͭ������Ч����Ӱ�졣�������������Һ��Cu2+ 25 g/L��Ni2+ 37.5 g/Lʱ���ڼ���4 cm�����Һ�¶�40 �桢�۵�ѹ0.53 V�����10 h�������£�����Һ�в�����ͭŨ�ȿɽ���0.24 g/L����Ni/Cu��Ϊ155.7��ͭ������Ч�����á�
�ؼ��ʣ�
������Ĥ�����ͭ��������������������Һ��
���±�ţ�1004-0609(2017)-10-2128-08���� ��ͼ����ţ�TF803.27���� ���ױ�־�룺A
���ǹ��á���ᷢչ��������ҵ����ز����ٵĻ������Ϻ���Ҫ���ʣ����������ʴ�ԺͿ����Ժá������Լѵ��������ԣ��㷺Ӧ����ұ�𡢻������������պ��졢�����������ҵ[1-4]���ҹ����������С�������֮�ƣ�ͭ�������ḻ��Ϊ�����ڲɵĵ�����ͭ����������д���Լռȫ����61.9%�����ҹ���������Ʒ����Ҫ����[5-6]����ͳ��������ұ������Ϊ��ĥ�����롪����������⡱���գ��ù��ճ���ɿ��������ȶ����������Ž���ֱ���ʵ͡��������ʧ���ܺĸߡ������ϡ�����ͻ��������ȱ�㡣��ˣ����������о��߿�����һϵ��ʪ���������ڽ����Щ���⣬�������Ȼ�����������Ϊͻ�����������ڹ����ⷢչҲ�ܿ죬�����MUKHERJEE[7]���Ȼ�ͭ������ͭ�����Ľ����ʴ�96.8%��ͭ�Ľ����ʴ�99.7%���ŷ����[8]���������[9]�����Ȼ��������߱����������ܵĽ����ʾ�����90%��ͭ�Ľ����ʴ�98%����һ����ʵ���˸߱���������ͭ��ͬ��������Ȼ�������ڻ�ѧ�����������Һ�е�ͭ�����Է��롣��ͳ����ʪ��ұ������У�ͭ������ķ�����Ҫ�����������ܼ���ȡ�������ӽ��������û�������������ȣ���¬������[10]����ε�[11]�ֱ��ԷǾ�̬����������Ϊ�������������Һ�г�ͭ��������[12]��AMPY-1Ϊ��ȡ���������Һ�г�ͭ���¿��ܵ�[13]�ù轺-�ۺϰ���֬�������Һ�г�ͭ����������[14]�������ҵ�[15]�ֱ������ۺ����۴�ͭ�������Һ���û���ͭ��SO��[16]��KUDELSKI��[17]��READ��[18]������ŷ��[19]�����Ե��������Һ�г�ͭ����Ȼ���Ϸ�������ʵ�������Һ��ͭ���ķ��룬����Щ������Ҫ���ڽ������Һ�е�����ͭ���з��룬���е�Cu2+Ũ��ͨ����0.4~0.8 g/L[19]������ͬʱ���к�������ͭ����Һ�����ʵ�ֶ��ߵ���Ч�����Ϊ��һ���µ����⡣
ͭ�������ӵı���ԭ��λ��ϴ�[20]���ﵽ0.59 V����������һ������ʵ����Һ�к���ͭ�����ķ��롣����ͭ�Ļ�ԭ��λ�����Ļ�ԭ��λ������ͨ��������ϵ�ĵ��ƣ�����ʹ��Һ�еĴ�ͭ���ȳ���������������������Һ�У��õ�������ͭ������Һ�����һ��������ô�ͳ�ķ���������ͭ������������������Ҫ����ˣ�����������Ժ��д�������ͭ����Һ�е�ͭ�����������̽�����ڴ˻����Ͽ�չ��ϵͳ��ʵ���о�������Ϊ��Һ�к���ͭ���ķ��뿪����һ���µ�;����
1 ʵ��
1.1 �����������߲���
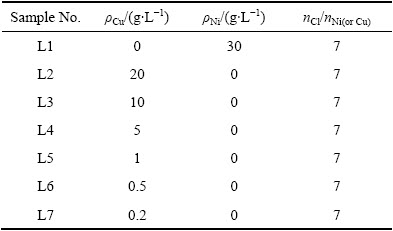
������˹�ٵ绯ѧ����վ(�ͺţ�VersaSTAT4)���в��ԣ��������缫��ϵ�������缫�����缫��Ϊ���缫���ߴ�ֱ�Ϊ1 cm��1 cm��4.5 cm��5.5 cm���αȵ缫Ϊ���ʹ��缫�������缫�����缫ʹ��ǰ��ϡ�������5 min�������������ȥ����ˮ��ϴ�ɾ������Һ�ֱ�ΪCuCl2��Һ��NiCl2��Һ����������1��ʾ��ɨ�跶ΧΪCuCl2��Һ��-0.5~0.5 V(vs SCE)��NiCl2��Һ��-0.8~0.5 V(vs SCE)��������ɨ�裬ɨ������1 mV/s��
��1 ���Һ����ֺ���
Table 1 Components of electrolytes
1.2 ������Ĥ���ʵ��ԭ��
ʵ��������ƾ��ķ���ϩ���ۣ�������������ͭ��Ϊ�缫(���14.5 cm��14.5 cm)���缫ʹ��ǰ����������1.1������ͬ��������ĤΪ��������������Ĥ��������������ҺΪCuCl2��NiCl2�����Һ(Ni��Cu������Ϊ1.5��Cl��CuĦ����ԼΪ7��pH=0)��֧�ֵ������ҺΪNaCl+HCl�����Һ(NaClĦ��Ũ��2.5 mol/L��pH=0)��
1.3 ����Һ����ͭ�ȵļ���
������������Һ����ͭ��Ϊ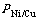 �����㹫ʽ��ʽ(1)��ʾ��
�����㹫ʽ��ʽ(1)��ʾ��
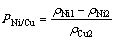 (1)
(1)
ʽ�У�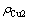 ��ʾ������ʱ����Һ�е�ͭ����Ũ�ȣ�
��ʾ������ʱ����Һ�е�ͭ����Ũ�ȣ� ��ʾ����Һ�������ӵij�ʼŨ�ȣ�
��ʾ����Һ�������ӵij�ʼŨ�ȣ� ��ʾ������ʱ��ɢ���������ҵ������ӵ�Ũ�ȡ�
��ʾ������ʱ��ɢ���������ҵ������ӵ�Ũ�ȡ�
2 ���������
2.1 �������������о�
CuCl2��Һ��NiCl2��Һ��ѭ������������ͼ1��2��ʾ��
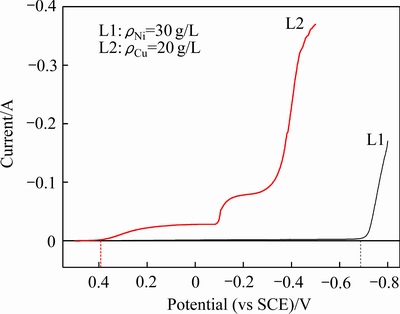
ͼ1 NiCl2��CuCl2��Һ������������
Fig. 1 Cathodic polarization curves of NiCl2 solution and CuCl2 solution

ͼ2 ��ͬCu2+Ũ��������������
Fig. 2 Cathodic polarization curves at different mass concentrations of Cu2+
��ͼ1��֪��������Һ��Ni2+Ϊ30 g/Lʱ����Լ-0.69 V(vs SCE)ʱNi2+��ʼ����ԭ����ͭ��Һ��Cu2+Ũ��Ϊ20 g/Lʱ����ͬɨ���ٶ��£���Լ0.39 V(vs SCE)��Cu2+����ʼ����ԭ��ʵ������������Թ۲쵽�缫������ͭ�ij�����Cu2+��Ni2+֮��Ļ�ԭ��λ��dz��������ﵽ����1.1 V����ͼ2���Կ�����������Һ��Cu2+Ũ�ȵIJ��Ͻ��ͣ��仹ԭ��λ���ƣ���������Һ��Cu2+Ũ�Ƚ�����0.2 g/Lʱ��ͭ��Һ��Cu2+�Ļ�ԭ��λ��Լ0.19V(vs SCE)��Զ����Ni2+�Ļ�ԭ��λ(-0.69 V(vs SCE))�����Ͻ�������������ں�����������ͭ�����ں���������ͭ������£���ȫ����ͨ����λ�Ŀ�����ʵ����Һ��ͭ������Ч���룬��Ϊ�������о��춨�����ۻ�����
2.2 ����Ĥ����
��ʵ�ʵ�ͨ�����Ƶ�λ����ʵ��ͭ�����빤�չ�������У�������Ҫ����Cu2+��Ni2+ ��������������λ�IJ������ѡ��Թ���Ҳ������Ҫ��һ���棬������ѡ���������������ϵ�IJ۵�ѹ�����ش�Ӱ�죬�������缫��Ӧ��λ��Խ���յIJ۵�ѹҲԽ���ܺ���Խ�ߣ���һ���棬��ͬ������ѡ��������Ӧ�ڲ�ͬ��������Ӧ����������Ӧ�����ͶԵ����ϵ���ȶ��Ծ��о��������á�������Ϊ������Ӧʱ����Һ��ϵ��Ȼ����ߣ�����Ϊ���ȷ�Ӧʱ������ʹ���Һ������ӣ������������ں��豸�����Ѷȡ����ң��Ƹ���������ͭҲ����Ҫר�ŵĹ����Ѷơ�
�ڴ�ͭ�ĵ�⾫�������У����������еIJ۵�ѹ��Ϊ0.2~0.3 V����Һ��Ȼ������ֲ��䡣��ˣ��ܷ�����ͭ��⾫���IJ�����ʽ��������Һ�г�ͭ�أ���Ҫע����ǣ���ͭ�ĵ�⾫�������У����Һ�е�ͭ��Ȼ��������������������ͬʱ�����е�ͭҲ�ڲ����ܽ���뵽���Һ�С���ˣ�ʵ��ͭ������Ĺؼ�������α��������ܽ��Cu2+���뵽������Һ�С�
������һ˼����������������ӽ���Ĥ�����۷ָ��������Һ������ң��������У�����Һ�е�Cu2+���������ϳ�����ͭ�������ܽ��������Һ�����������ӽ���Ĥ��ֹ������ͨ�����������е����������������ݴ����룬�������ͼ3��ʾ��ͭ�����������Ĥ���װ�ã�����������ͭ��Ϊ�缫�����������������ӽ���Ĥ�����������д�������ͭ����Һ���뵽�������У��������м��벻������֧�ֵ������Һ���ڵ糡�����£�����Һ�е�Cu2+�����õ�����ͭ���������е�ͭ�������ܽ���뵽����Һ�У����������ӽ���Ĥ��ֹ�����ӵĴ����������е����������������Ĥ�����������У�������ϵ��ɵ�ƽ�⣻ ���һ���ں����µ�����Һ������Һ��������������Ե����������е�⣬������������ͬ�����ѭ�����ɲ��Ͻ���������Һ�е�ͭ��ȡȥ��������������Һ�У�ʵ������Һ�к�����ͭ�ķ��롣
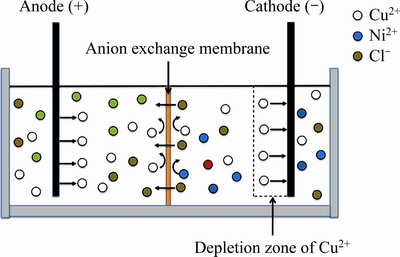
ͼ3 ���۽ṹ��ԭ��
Fig. 3 Electrolytic cell structure and electrolysis principle
2.2.1 �����Ӱ��
����(d)��ͭ������Ч����Ni2+�����ʵ�Ӱ����ͼ4��5��ʾ��������������Һ�еĦ�Ni/Cu�ȼ���2(���Ц�Cu1Ϊ����Һ�г�ʼͭŨ�ȣ���ͬ)��
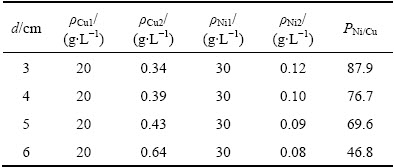
��2 ������������Һ����ͭ��
Table 2 ��Ni/Cu in catholyte after electrolysis

ͼ4 �����ͭ������Ч����Ӱ��
Fig. 4 Effect of polar distance on separation of copper from nickel
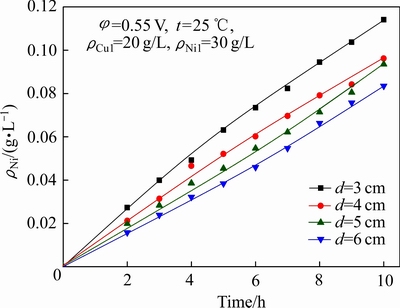
ͼ5 �����Ni2+�����ʵ�Ӱ��
Fig. 5 Effect of polar distance on permeation rate of Ni2+
��ͼ4��ͼ5����2���Կ��������ż���ļ�С����������Cu2+�ĵ�������ʺ�Ni2+�������ʾ�������������������6 cm��С��3 cmʱ��10 h������Һ�в���ͭ(����Cu2+��Cu+����ͬ)Ũ����0.64 g/L������0.34 g/L����Ni/Cu����46.8������87.9��������Һ��Ni2+Ũ����0.08 g/L����0.12 g/L����С������������Һ����Ľ��ͣ��Ӷ���Ч��������Һ�е�ͭ������Ч������ͬʱ���ڼ�����С����ϵ�����ܶ�������������ǿ��ʹ������Һ��Ni2+�������ʼӿ죬ʹ���������ӽ���Ĥ�����������������Һ��Ni2+����ʧ����ˣ��ں�����������Һ��Ni 2+����ʧ��ǰ���£���С������������߷�Ӧ���ʣ�����ͭ������Ч����
2.2.2 ���Һ�¶ȵ�Ӱ��
���Һ�¶ȶ�ͭ������Ч����Ni2+�����ʵ�Ӱ����ͼ6��7��ʾ��������������Һ�Ц�Ni/Cu����3��
��3 ������������Һ�е���ͭ��
Table 3 ��Ni/Cu in catholyte after electrolysis


ͼ6 ���Һ�¶ȶ�ͭ������Ч����Ӱ��
Fig. 6 Effect of electrolyte temperature on separation of copper from nickel

ͼ7 ���Һ�¶ȶ�Ni2+�����ʵ�Ӱ��
Fig. 7 Effect of electrolyte temperature on permeation rate of Ni2+
��ͼ6��ͼ7�ͱ�3���Կ��������ŵ��Һ�¶ȵ����ߣ���������Cu2+�ĵ�������ʺ�Ni2+�������ʾ����������������������ߵ��Һ�¶�������������ɢ��ʹ��Ũ�������������Ӷ��ƶ���Һ�е�ͭ�������ϳ����������Һ�¶���25 ��������40 ��ʱ��10 h������Һ�в���ͭŨ����0.39 g/L������0.21 g/L����Ni/Cu����76.7������142.2����һ�����¶���ߵ�45 ��ʱ����Ч����40 ��ʱ�������⣬����˹�ط���[21](ʽ2)��֪�����Һ�¶����ߣ�ʹ��Cu2+��ԭ��λ���ƣ����������ͭ���������ȡ�Ȼ�������ߵ��Һ�¶Ȼ�ʹ����Һ��Ni2+�������ʼӿ죬ʹ���������ӽ���Ĥ�����������������Һ��Ni2+����ʧ����ˣ����о�ѡ���¶�Ϊ40 �档
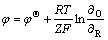 (2)
(2)
ʽ�У�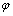 Ϊƽ���ѹ��
Ϊƽ���ѹ�� Ϊ�����ƣ�RΪĦ�����峣����8.3143 J/(K��mol)��TΪ����ѧ�¶ȣ�K��ZΪ�缫��Ӧ�е�ʧ�ĵ�������FΪ�����ڳ�����
Ϊ�����ƣ�RΪĦ�����峣����8.3143 J/(K��mol)��TΪ����ѧ�¶ȣ�K��ZΪ�缫��Ӧ�е�ʧ�ĵ�������FΪ�����ڳ�����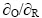 Ϊ����̬�ͻ�ԭ̬�ı�ֵ��
Ϊ����̬�ͻ�ԭ̬�ı�ֵ��
2.2.3 �۵�ѹ��Ӱ��
�۵�ѹ��ͭ������Ч����Ni2+�����ʵ�Ӱ����ͼ8��9��ʾ��������������Һ�Ц�Ni/Cu����4��
���ͼ8��ͼ9�ͱ�4���Կ��������Ų۵�ѹ�����ߣ���������Cu2+�ĵ�������ʺ�Ni2+�������ʾ��������������۵�ѹ��0.48 V������0.58 Vʱ�� 10 h������Һ�в���ͭŨ����3.30 g/L������0.21 g/L����Ni/Cu����9.1������142.2��������Һ��Ni2+Ũ����0.11 g/L����0.14 g/L����߲۵�ѹ������ͭ�������ϵij������������Һ��ͭ���������ȡ�������۵�ѹ�ᵼ������Һ��Ni2+�������ʼӿ죬ʹ���������ӽ���Ĥ�����������������Һ��Ni2+����ʧ��ͬʱ�۵�ѹ�������ܵ������������ϳ�������ˣ�Ϊ��ʵ������Һ��ͭ�������ͬʱ�ּ�������Һ��Ni2+����ʧ����ʵ��ѡ��۵�ѹΪ0.53 V��
��4 ������������Һ�е���ͭ��
Table 4 ��Ni/Cu in catholyte after electrolysis
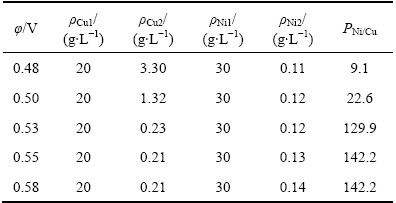
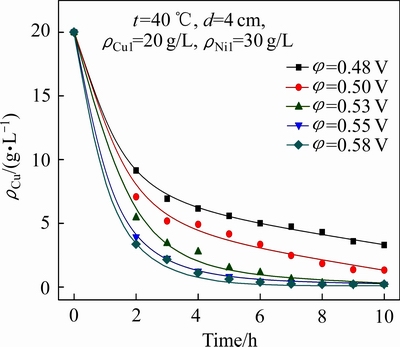
ͼ8 �۵�ѹ��ͭ������Ч����Ӱ��
Fig. 8 Effect of cell voltage on separation of copper from nickel
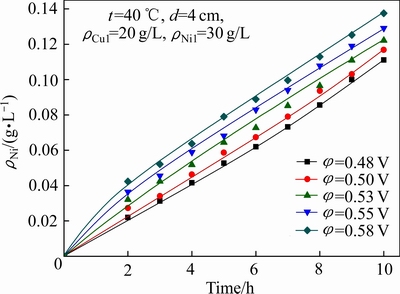
ͼ9 �۵�ѹ��Ni2+�����ʵ�Ӱ��
Fig. 9 Effect of cell voltage on permeation rate of Ni2+
��5 ���������Һ�е���ͭ��
Table 5 ��Ni/Cu in catholyte after electrolysis
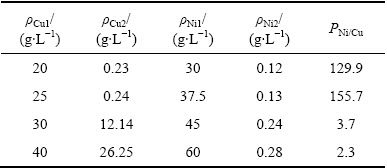

ͼ10 ��ʼCu2+Ũ�ȶ�ͭ������Ч����Ӱ��
Fig. 10 Effect of initial Cu2+ concentration on separation of copper from nickel
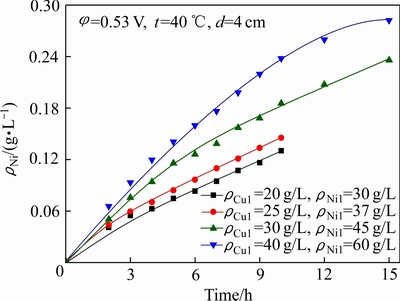
ͼ11 ��ʼNi2+Ũ�ȶ�Ni2+�����ʵ�Ӱ��
Fig. 11 Effect of initial Ni2+ concentration on permeation rate of Ni2+
2.2.4 ��ʼͭ��Ũ�ȵ�Ӱ��
��ʼͭ��Ũ�ȶ�ͭ������Ч����Ni2+�����ʵ�Ӱ����ͼ10��11��ʾ��������������Һ�Ц�Ni/Cu����5�����ͼ10��ͼ11�ͱ�5���Կ���������Cu1Ϊ20��25 g/Lʱ��ͭ��������ʽϿ죬������������Һ�в���ͭŨ�����ֱ�Ϊ0.23��0.24 g/L����Ni/Cu�ֱ�Ϊ129.9��155.7��ͭ������Ч���Ϻã�����Cu1Ϊ30��40 g/Lʱ��ͭ��������ʽ���������15 h��⣬����Һ�в���ͭŨ����Ȼ��12.14��26.26 g/L����Ni/Cu�ȷֱ�ֻ��3.7��2.3������Ч���ϲ����Ҫ������ʴ�̷�Ӧ�����[24]��������Һ��Cu2+Ũ�Ƚϸ�ʱ����������������ϵ�ͭ������ʽ(3)��ʾ��ʴ�̷�Ӧ��
Cu2++Cu+2Cl-=2CuCl (3)
�൱������Һ�е�Cu2+��Ϊ�������������Ѿ����������������ͭ�������ڱ��о��������õ�����Һ��n(Cl)/n(Cu)ʼ�ձ�����7���ң����е�Cl-����������������Cl-��CuCl������ɿ����Ե�[CuCl3]2-��ʹ�ó����������ϵ�ͭ���������ֽ��뵽����Һ�У�������ͭ������Ч������ˣ��ڱ��о��̶���n(Cl)/n(Cu)��ǰ���£�Ϊ��ʵ�ֽϺõ�ͭ������Ч��������Һ��ͭ����Ũ����Ҫ������25 g/L����Ϊ�ˡ�
3 ����
1) ������������Һ��ͭ��Ũ�ȸߡ����Է�������⣬����˲��������ӽ���Ĥ��ⷨ���к���ͭ�����룬�����������߽�������������ں�����������ͭ���Ǻ���������ͭ������£�Ni2+��Cu2+�����ڽϴ�Ļ�ԭ��λ�ͨ����λ���ؿ���ʵ����Һ��ͭ������Ч���롣
2) ������ͭ������Ĺ����о�������Һ��Cu2+ 25 g/L��Ni2+ 37.5 g/Lʱ���ڼ���4 cm�����Һ�¶�40 �桢�۵�ѹ0.53 V���Ż������£����10 h������Һ��ͭ����Ũ�Ƚ�����0.24 g/L����ȫ�������е���������ͭ����Һ��ͭŨ�ȵ�Ҫ��
REFERENCES
[1] �� ��, ����M, �밲��, ̷����. ȫ��������Դ����������״���������[J]. �������������, 2016(1): 64-69.
ZHANG Liang, YANG Hui-peng, FENG An-sheng, TAN Xiu-min. Study on current situation and analysis of supply and demand of global nickel resource[J]. Conservation and Utilization of Mineral Resources, 2016(1): 64-69.
[2] ·��Զ, ³�۸�, ������, �̺�ΰ, �� ��. �й�������Դ��״��������չ[J]. ��Ȼ��־, 2015, 37(4): 269-277.
LU Chang-yuan, LU Xiong-gang, ZOU Xing-li, CHENG Hong-li, XU Qian. Current situation and utilization technology of nickel ore in China[J]. Chinese Journal of Nature, 2015, 37(4): 269-277.
[3] ������, �� ��, �� ��, ������, ��÷÷. �й�����Դ��ҵ��״���ɳ�����չ����[J]. ��Դ���ҵ, 2015, 17(4): 94-99.
ZENG Xiang-ting, XU Hong, TIAN You, LIU Zhi-na, LI Mei-mei. Situation and sustainable development strategy of China��s nickel resources industry[J]. Resources and Industries, 2015, 17(4): 94-99.
[4] REN Xiu-lian, WEI Qi-feng, LIU Zhe, LIU Jun. Electrodeposition conditions of metallic nickel in electrolytic membrane reactor[J]. Transactions of Nonferrous Metals Society of China, 2012, 22(2): 467-475.
[5] ��־ǿ, ����ǰ, �� ǫ, ��˩��. �й�����Դ������״��ɳ�����չ���Լ���ؼ�����[J]. �������������, 2016(2): 58-69.
YANG Zhi-qiang, WANG Yong-qian, GAO Qian, WU Shuan-jun. Present situation and development strategy and key technologies of China��s nickel resources sustainable development[J]. Conservation and Utilization of Mineral Resources, 2016(2): 58-69.
[6] ������, ������, ë�ȳ�, �� Ө, �� ��, �����, �� ��, ������. ��ͭ���������Ԫ�ص���ѧ���켰���ݻ�����[J]. �й���ɫ����ѧ��, 2016, 26(1): 149-163.
ZENG Ren-yu, LAI Jian-qing, MAO Xian-cheng, ZHAO Ying, LIU Pin, ZHU Jia-wei, YUE Bin, AI Qi-xing. Distinction of platinum group elements geochemistry in Jinchuan Cu-Ni sulfide deposit and its implication for magmatic evolution[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(2): 149-163.
[7] MUKHERJEE T K. copper-nickel sulfide concentrate leached by CuCl2-Oxygen[J]. Hydrometallurgy, 1986(15): 25-32.
[8] �ŷ��, ����ͮ, ������, �����. ����ͭ���Ľ�ȡ�� ��[J]. �����Ƽ���ѧѧ��, 1998, 28(2): 231-234.
ZHANG Feng-jun, MA Jiu-tong, LI Luan-ning, WANG Yu-jie. Study on leaching technology of Cu and Ni from brassil[J]. Journal o f Changchun University of Science and Technology, 1998, 28(2): 231-234.
[9] �����, ������, �����. ���Ȼ��������߱���[J]. ������ѧѧ��(��Ȼ��ѧ��), 1998, 19(2): 152-154.
LI Jin-li, ZHANG Ming-jie, WANG Hong-kuan. Nis matte leached by ferric chloride[J]. Journal of Northeastern University (Natural Science), 1998, 19(2):152-154.
[10] ¬����, ������, �����, �� ��, ֣����, ���Խ�, �� ��. ����ͭ���ӻ�ķǾ�̬����������ͭ�о�[J]. �ִ�����, 2014, 34(12): 104-107.
LU Jian-bo, WANG De-xiang, LI Yi-jing, ZHAO Chong, ZHENG Jun-fu, CHEN Zi-jiang, GUO Yong. Removal of copper by amorphous nickel sulfide based on copper ion activation[J]. Modern Chemical Industry, 2014, 34(12): 104-107.
[11] LI Jiang-tao, CHEN Ai-liang. Deep removal of copper from nickel electrolyte using manganese sulfide[J]. Transactions of Nonferrous Metals Society of China, 2015, 25(11): 3802-3807.
[12] �� ��, ������, ����Ƽ, ����Ӣ, ��ʿ��, ����Ԫ. AMPY-1�������������Һ������ͭ���о�[J]. ��ɫ����(ұ������), 2015(10): 10-13.
DAI Kuan, LIU Yun-qing, HU Hui-ping, CHENG Ze-ying, LIU Shi-jun, CHEN Qi-yuan. Removal of copper from nickel anode electrolyte by AMPY-1[J]. Nonferrous Metals (Extractive Metallurgy), 2015(10): 10-13.
[13] WEN Jun-jie, ZHANG Qi-xiu, ZHANG Gui-qing, ZHANG Li-ping. Copper completely removal from artificial nickel sulfate electrolyte by using silica-polyamine resin[J]. Nonferrous Metals, 2009, 61(1): 50-55.
[14] ������, ������, ������. ���������ͭ�����Ļ���[J]. ��������, 2013, 33(6): 531-535.
WANG Chun-hua, ZENG Jia-na, LIN Rui-ling. Recovery of nickel and copper from electroplating sludge[J]. Environmental Protection of Chemical Industry, 2013, 33(6): 531-535.
[15] ������, ������, ������. ����������Һ���á��û�������ͭ�����о�[J]. ��Դ����, 2008, 32(10): 699-700.
WANG Rui-zhong, WANG Zhong-xiang, YIN Ji-liang. Technology study of removing copper in the nitric nickel solution by interchange method[J]. Chinese Journal of Power Sources, 2008, 32(10): 699-700.
[16] SO W W, CHOE S, CHUANG R, LEE C C. Effective diffusion barrier metallization process on copper[J]. Thin Solid Films, 2000, 376(1/2): 164-169.
[17] KUDELSKI A, JANIK-CZACHOR M, BUKOWSKA J, DOLATA M, SZUMMER A. Surface-enhanced Raman scattering (SERS) on copper electrodeposited under nonequilibrium conditions[J]. Journal of Molecular Structure, 1999, 482: 245-248.
[18] READ D T, CHENG Y W, GEISS R. Morphology, microstructure, and mechanical properties of a copper electrodeposit[J]. Microelectronic Engineering, 2004, 75(1): 63-70.
[19] ����ŷ, ��ӱ��, �����. �����������Һ������ͭ�ĵ�������о�[J]. ����ұ��, 1994(4): 11-14.
ZENG Zhen-ou, ZENG Ying-ru, WU Hong-ru. Study of removing copper from nickel anode electrolyte by electrodeposition method[J]. Hunan Metallurgy, 1994(4): 11-14.
[20] ��ά��. ���缫��λ�����ֲ�[M]. ����: ��ѧ������, 1991: 80, 154.
WU Wei-chang. Standard electrode potential datasheet[M]. Beijing: Science Press, 1991: 80, 154.
[21] BARD A J, FAULKNER L R. Electrochemical methods: fundamentals and applications[M]. Austin: Department of Chemistry and Biochemistry University of Texas, 2001: 52.
[22] �� ��, ������, �� ��, ������, �� ��. ��ʴ�̷�Һ�и�Ĥ���������ͭ���¹����о�[J]. ��ɫ����(ұ������), 2011(9): 40-43.
YANG Xing, YANG Sheng-hai, GUO Huan, CHEN Yong-ming, LIU Qing. Study on electrowinning sheet-form copper from acidic etchant waste in diaphragm cell[J]. Nonferrous Metals (Extractive Metallurgy), 2011(9): 40-43.
[23] ��˫��, ����Ƽ, �콨��, �� ��, �� ��. �����Ȼ�ͭʴ��Һԭ����Ӱ�����ط���[J]. �Ƽ���Ϣ, 2006(10S): 8.
CHEN Shuang-kou, GUO Li-ping, ZHU Jian-fang. Brief principles to acid chlorination copper etching solution and factors analysis[J]. Science Information, 2006(10S): 8.
[24] κ ��, �����, ��ɱ�. ӡˢ��·�嶯̬ʴ���о�[J]. �����Ϳ��, 2009, 28(7): 28-30.
WEI Jing, XU Jin-lai, WU Cheng-bao. Study on dynamic etching of printed circuit board[J]. Electropalting and Finishing, 2009, 28(7): 28-30.
Separation of macro amounts copper from nickel in chloride leaching solution by anion membrane electrolysis
HE Yang1, TANG Zhong-yang1, LIU Xu-heng1, CHEN Xing-yu1, 2
(1. School of Metallurgy and Environment, Central South University, Changsha 410083, China;
2. Hunan Key Laboratory for Metallurgy and Material Processing of Rare Metals, Central South University, Changsha 410083, China)
Abstract: Nickel sulfide ore always accompanies by a large amount of copper, and copper can be often leached simultaneously into the nickel leaching solution. However, because of their similar chemical properties, it is difficult to separate. Here, anion exchange membrane electrolysis was provided to separate copper from solution by controlling the cell voltage. The effects of polar distance, electrolyte temperature, cell voltage and concentrations of copper and nickel on separation of copper-nickel were studied and the optimal operation conditions were obtained. The results show that, for solution containing 25 g/L Cu2+ and 37.5 g/L Ni2+,the total residual Cu concentration in catholyte is depressed to 0.24 g/L and the ratio of ��Ni/Cu reaches 155.7 under the optimal conditions of polar distance 4 cm, electrolyte temperature 40 ��, cell voltage 0.53 V, electrolysis time 10 h. A satisfied effect of separation of copper from nickel is obtained.
Key words: anion membrane electrolysis; separation of copper from nickel; nickel sulfide ore; leaching solution
Foundation item: Project(2014CB643405) supported by the National Basic Research Development Program of China
Received date: 2016-10-12; Accepted date: 2017-03-27
Corresponding author: LIU Xu-heng; Tel: +86-731-88830476; E-mail: liuxuheng@csu.edu.cn
(�༭ ��ѧ��)
������Ŀ�������ص�����о���չ�ƻ�������Ŀ(2014CB643405)
�ո����ڣ�2016-10-12�������ڣ�2017-03-27
ͨ�����ߣ�����㣬�����ڣ���ʿ���绰��0731-88830476��E-mail: liuxuheng@csu.edu.cn
ժ Ҫ���������г�����ͭ���ڽ���ʱ����ͭ����ͬ���������Һ��������ͭ����ѧ������������Է��롣�����һ���⣬����������Ĥ��⣬ͨ�����Ʋ۵�ѹ��������Һ�е�ͭ�������켫�ࡢ���Һ�¶ȡ��۵�ѹ��ͭ��Ũ�ȵ����ض�ͭ������Ч����Ӱ�졣�������������Һ��Cu2+ 25 g/L��Ni2+ 37.5 g/Lʱ���ڼ���4 cm�����Һ�¶�40 �桢�۵�ѹ0.53 V�����10 h�������£�����Һ�в�����ͭŨ�ȿɽ���0.24 g/L����Ni/Cu��Ϊ155.7��ͭ������Ч�����á�
[1] �� ��, ����M, �밲��, ̷����. ȫ��������Դ����������״���������[J]. �������������, 2016(1): 64-69.
[2] ·��Զ, ³�۸�, ������, �̺�ΰ, �� ��. �й�������Դ��״��������չ[J]. ��Ȼ��־, 2015, 37(4): 269-277.
[8] �ŷ��, ����ͮ, ������, �����. ����ͭ���Ľ�ȡ�� ��[J]. �����Ƽ���ѧѧ��, 1998, 28(2): 231-234.
[9] �����, ������, �����. ���Ȼ��������߱���[J]. ������ѧѧ��(��Ȼ��ѧ��), 1998, 19(2): 152-154.
[14] ������, ������, ������. ���������ͭ�����Ļ���[J]. ��������, 2013, 33(6): 531-535.
[15] ������, ������, ������. ����������Һ���á��û�������ͭ�����о�[J]. ��Դ����, 2008, 32(10): 699-700.
[19] ����ŷ, ��ӱ��, �����. �����������Һ������ͭ�ĵ�������о�[J]. ����ұ��, 1994(4): 11-14.
[20] ��ά��. ���缫��λ�����ֲ�[M]. ����: ��ѧ������, 1991: 80, 154.
WU Wei-chang. Standard electrode potential datasheet[M]. Beijing: Science Press, 1991: 80, 154.
[23] ��˫��, ����Ƽ, �콨��, �� ��, �� ��. �����Ȼ�ͭʴ��Һԭ����Ӱ�����ط���[J]. �Ƽ���Ϣ, 2006(10S): 8.
[24] κ ��, �����, ��ɱ�. ӡˢ��·�嶯̬ʴ���о�[J]. �����Ϳ��, 2009, 28(7): 28-30.


