���±�ţ�1004-0609(2008)01-0163-08
Zn��FetO-CaO-SiO2-Al2O3��ϵ�еĻӷ���Ϊ
������1����ʿ��1������ �ٻ�2��·��Ƽ1��������1
(1. �����Ƽ���ѧ ұ������̬����ѧԺ������100083��
2. ������ѧ ��Ԫ���ʿ�ѧ�о�������̨ 980-8577���ձ�)
ժ Ҫ��
�о�Zn�ں�Cl��FetO-CaO-SiO2-Al2O3��ϵ�еĻӷ���Ϊ�������ӷ��������ࡢ�ӷ����Լ����������¶ȡ����ɷ֡����Ӽ��ȵ�Ӱ�졣Ӧ�ü���˹��������С��ԭ������ѧ������ʾ�ڱ�ʵ���¶������£���Ʒ90%��+10%ZnO+CaCl2�еĻӷ�����Ϊ����Zn��ZnCl2��FeCl2��ʵ��������������Zn��FeCl2����ӷ������¶����Ӷ����ӣ���ZnCl2������ȴ��֮���͡���Ӧ���ڣ���Ʒ�ӷ��ٶȺܿ죬10 min����������ȶ���ZnCl2��Ҫ�γ�����Ʒ�����ڼ�(������ʵ���¶�1 190 ��)�������ڼ䣬���ɵ�ZnCl2��FeO��Ӧ����FeCl2���弰ZnO�������ֱ�FeO��ԭ�ɽ���Zn���塣���ɷ��У�FeO�����Ͷ�Ԫ���CaO/SiO2��Zn�Ļӷ��������༰�ӷ�������ҪӰ�졣���ӻ�ԭ����C�ۿ��������Zn�Ļӷ��ʡ�
�ؼ��ʣ�
FetO-CaO-SiO2-Al2O3��ϵ��Zn���ӷ���Ϊ��
��ͼ����ţ�TF 803.1���� ���ױ�ʶ�룺A
Vaporization behaviors of Zn in FetO-CaO-SiO2-Al2O3 slag system
ZHANG Yan-ling1, LI Shi-qi1, KASAI Eiki2, LU Jun-ping1, GUO Xiao-dong1
(1. School of Metallurgical and Ecological Engineering, University of Science and Technology Beijing,
Beijing 100083, China;
2. Institute of Multidisciplinary Research for Advanced Materials, Tohoku University, Sendai 980-8577, Japan)
Abstract: Vaporization behavior of zinc in the slag system FetO-CaO-SiO2-Al2O3 was examined, including the formation ratio of vapor species and their partitioning as well as the effect of process factors such as temperature, holding time, slag composition, and addition of reductive agents. A thermodynamic estimation with the principle of Gibbs free energy minimization shows that the major vapor species from the sample of FeO-CaO-SiO2-Al2O3 system+ZnO+CaCl2 are metallic Zn, ZnCl2 and FeCl2 in the experimental temperature range. The results suggest that the formation ratio of metallic Zn and FeCl2 increases with temperature increasing , while that of ZnCl2 decreases. The evaporation of sample is initially fast and becomes steady after holding for 10 min. Gaseous ZnCl2 is mainly formed during heating period, at the holding stage it reacts with FeO to produce gaseous FeCl2. With regard to slag compositions, FeO and basicity significantly affect the evaporation of zinc. The evaporation ratio of zinc can be enhanced by the addition of reductants such as carbon powder.
Key words: FetO-CaO-SiO2-Al2O3 slag system; zinc; vaporization behaviors
�����������պ����������ķɻҼ��۳��������������ں��й��ߵĶ������к����ؽ�����Pb��Cd�ȶ�����ȷ����ΪΣ����Ʒ���辭��������������Ϊ��ȫ�ĵط�[1]�����������������سɱ����Լ���ʱ����ú��к������ݳ��Ŀ����Ե����������������������ʹ�á����ڴ���Ŀǰ��һ�ֱȽ���Ӧ��ǰ���ķ���[2?3]�������������ŵ㣺1) ��Ч���ݣ�2) ���������£��ؽ����Ļӷ��Ըߣ���ͨ��һ����ʩ��������ؽ�����Դ��3) ���������·ɻ��������еĶ���Ӣ��Ⱦ��л����ʿ����Ч�������ƻ�����������к��ؽ����ӷ����뵽һ���̶ȣ��ɴﵽ���ղ�����ij���������
����ɻҼ��۳��У������Ļ��������CaO��SiO2��FeO/Fe2O3��Al2O3�ȣ�ͬʱ���в���K��Na��S��Cl�Լ��ؽ���Zn��Pb��Cd��[4]�����ڴ��������У���Щ�ɷֹ�����һ�����ӵĶ�Ԫ����/������ϵ��Ϊ����Ч�����ؽ�����ȥ�����������˽��ؽ����ڸ�����/������ϵ�еĻ�������ѧ��Ϊ���ܶ����ѧ ��[5?6]�Լ��ҹ�����骵�[7]����ѧ�ε�[8]�о����ؽ��������ڴ������������µĻӷ���Ϊ���о�������Ҫ�Ǽ����ڷ����ӷ����ʡ������༰��������ʡ�����ͣ����̬�Լ��������������¶ȡ����ա�ʱ��ȵ�Ӱ�죬�������ؽ���������/������ϵ�еĻӷ��������ࡢ��������ѹ���Լ���ȵȻ�������ѧ��Ϊ���о���Ϊ���ޡ�
���о�����[9]���ؽ����Ļӷ���Ϊ��Ԫ��Cl������أ���˱��������Գ����ؽ���ZnΪ�����о���Zn�ں�Cl��FeO-CaO-SiO2-Al2O3-Fe2O3��ϵ�еĻ����ӷ���Ϊ��������������ѧ����FactSage[10]ģ�������Zn���ܵĻӷ��������ࡣ��Σ�����ʵ����ʵ���о���Zn�ڸ�������ϵ�еĻӷ��������ࡢ�ӷ�ȥ���ʵȣ������˸������������¶ȡ�����ʱ�䡢���ɷ֡���ԭ���ȵ�Ӱ�죬���������ѧ���������ijЩDZ�ڵ�Ӱ�������
1 ����ѧ����
��������ѧ����FactSage��Ӧ�ü���˹��������С��ԭ�����Zn �ں�Cl��FeO-CaO-SiO2-Al2O3- Fe2O3��ϵ�п��ܵĻӷ��������ࡣ�������������ķ�Ӧ������ZnO��FeO��Fe2O3��CaO��SiO2��Al2O3�Լ�CaCl2��������Ũ�����ⶨ��ʵ��������ͬ������ZnO�ij�ʼŨ������Ϊ10%������(FeO��Fe2O3��CaO��SiO2��Al2O3����)ռ90%��CaCl2������ZnO��ͬĦ�������ӣ���Ħ����n(ZnO)?n(CaCl2)=1?1�����ɷ���Al2O3 �̶�Ϊ5%������ɷ��� FeO��Fe2O3��CaO��SiO2���������ⶨ��w(FeO)��Fe2+/Fe3+���Լ����CaO/SiO2���á��¶�Ϊ673~2 073 K����ѹΪ1.01��105 Pa��ָ������Ϊ��Ar���գ�����������Ϊ���ֲ����������������̬����������ͼ1��ʾ���ɼ��ڸ�ϵͳ�����£���Ҫ��3�ֻӷ��������ɡ�����Zn��ZnCl2��FeCl2�����н���Zn��ZnCl2��������ɷ�Ӧ�ֱ�Ϊ
![]()
FeCl2�����п������������·�Ӧ��
![]()
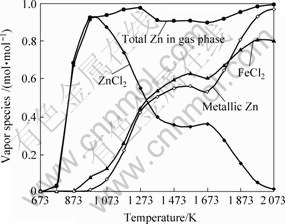
ͼ1 ��Ʒ90%��+10%ZnO+CaCl2(n(ZnO)?n(CaCl2)=1?1)�еĻӷ�����
Fig.1 Vapor species from sample of 90%slag+10%ZnO+ CaCl2 (n(ZnO)? n(CaCl2)=1?1)
2 ʵ��
2.1 �����Ʊ�
Ϊ��ģ��ɻ��г����Ļ���ɷ֣����о���FeO-CaO-SiO2Ϊ������ϵ��ѡ����ͼ2��ʾ��3�����ɷ֡���3����������ͬ�ҽϵ͵��۵�1 150 �棺F-slag��FeO������ߣ�C-slag��CaO������ߣ�S-slag��SiO2������ߡ�ÿ����������5%��Al2O3��
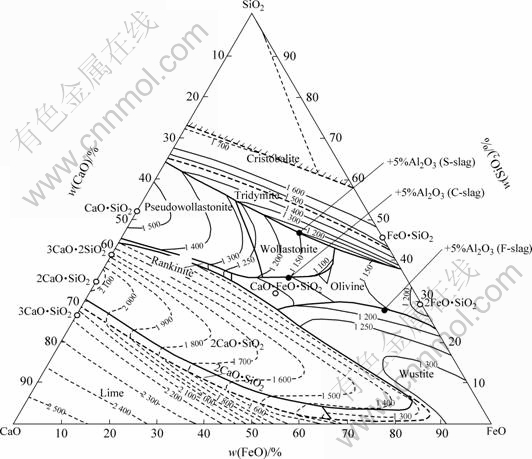
ͼ2 FeO-CaO-SiO2��ͼ������ѡȡ�����ɷ�
Fig.2 Phase diagram of FeO-CaO-SiO2 system and composition of slag used for experiment
���ô���ѧ�Լ�����Fe�ۣ�Fe2O3��SiO2��CaCO3�� Al2O3����ͼ2��ʾ�ijɷ�Ҫ������������Ȼ�ϡ���Ϻ�������¯�ڵĸ��������У�����Ar������������1 210 �����2 h�������Ar������������ȴ��ȡ���������ɷ����ڱ�1��
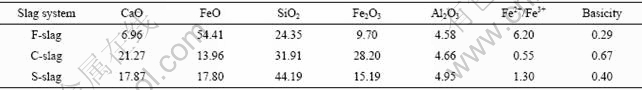
��1 �����Ļ�ѧ�ɷ�
Table 1 Slag composition (mass fraction, %)
���������鲢��ĥ�ɷ�ĩ��Ȼ���뻯ѧ�Լ�ZnO��CaCl2��ϡ�ZnO��������ȷֱ�Ϊ10%��90%��CaCl2���չ̶���Ħ����n(CaCl2)/n(ZnO)=1���ӡ��ڿ��컹ԭ����Zn�ӷ���Ϊ��Ӱ��ʱ������Ʒ�����C�ۣ������������Ʒ�����ĸ�������(0.3%��1.0%)���ӣ�������Ȳ��䡣
2.2 ʵ��װ���벽��
��ʵ����װ����ͼ3��ʾ��ȡԼ3 g��Ʒ���������ڣ����������ڵ���¯�ڵķ�Ӧ���С�����ǰ1 h���ӷ�Ӧ�ܵײ���2.0 L/min������ͨ�봿Ar�����Ա�֤ʵ���������Ҫ�Ķ������ա�֮����30 min�ڽ���Ʒ�¶ȼ����������¶�1 000~1 300 �档����һ���ĺ���ʱ���ֹͣ���ȣ�����Ar����������ȴ��Ʒ�����ȡ����������������ʵ���������ڱ�2��
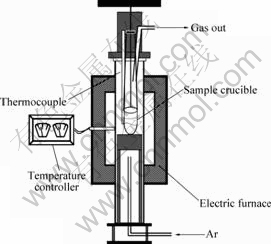
ͼ3 ʵ��װ��ͼ
Fig.3 Schematic of experimental apparatus
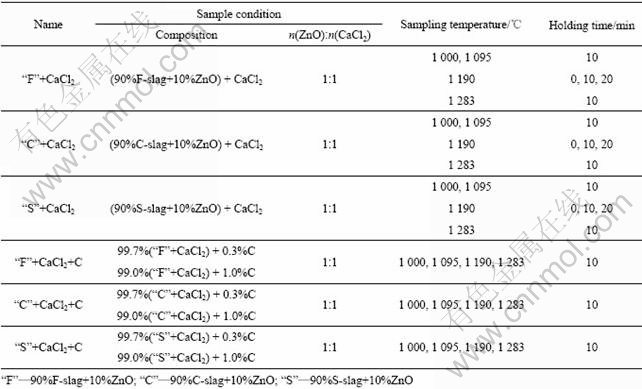
��2 ʵ������
Table 2 Experimental condition
2.3 ��Ʒ����
ʵ���������Ʒ��Ar��������ȴ����ICP�����ӹ������Dz������Ԫ��Zn��Fe��Ũ�ȣ���ԭʼ��Ʒ��Zn��FeԪ�صij�ʼ����Ƚϣ��ɵõ�ʵ�������Zn��Fe�Ļӷ������ֱ��ʾΪm(Znloss)��m(Feloss)����ǰ������ѧ������֪���ڱ�ʵ���¶� (1 000~1 300 ��)��������Ҫ��3�ֻӷ��������ɡ���ZnCl2��FeCl2�ͽ���Zn����ˣ�Ԫ��Cl�Ļӷ���(m(Clloss))�ɱ�ʾΪ
![]()
����FeCl2��FeԪ��Ωһ�Ļӷ����࣬��ˣ��ӷ�����FeCl2����(FeCl2vap)������ʽ�õ���
![]()
��ZnCl2������ߵ�Cl(![]() )Ϊ
)Ϊ
![]()
�������ӷ���ZnCl2����(![]() )�ͽ���Zn������(
)�ͽ���Zn������(![]() )�ɷֱ��ʾΪ
)�ɷֱ��ʾΪ
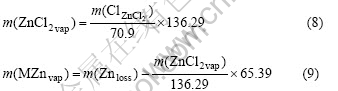
����ʵ�鼰���������д��������������![]() ��
��![]() ����ָ�ֵ����ʱ���ٶ����߾�Ϊ�㡣��
����ָ�ֵ����ʱ���ٶ����߾�Ϊ�㡣��![]() Ϊ�㣬����ΪZnCl2��ZnΩһ�Ļӷ����塣
Ϊ�㣬����ΪZnCl2��ZnΩһ�Ļӷ����塣
![]()
3 ���������
3.1 �¶ȶԻӷ������������ɵ�Ӱ��
ͼ4(a)��ʾΪ��F��+CaCl2��Ʒ���¶ȶԻӷ��������༰������������Ӱ�졣��������������Ϊ

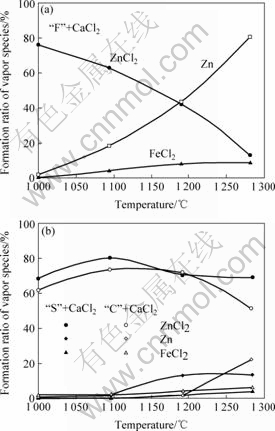
ͼ4 �¶ȶԻӷ��������༰������Ӱ��
Fig.4 Formation ratio of vapor species as function of temperature (holding for 10 min)
��ͼ4(a)�ɼ�������Zn������FeCl2���������¶����߶����ߣ���ZnCl2������ȴ��֮�½�����˵���ڵ�����Zn�Ļӷ�������Ҫ���Ȼ��������Zn�����ڸ����¸�Ϊ�ȶ���ǰ��[11?12]�о����֤��FeO-CaO- SiO2��CaO-SiO2-Al2O3��ϵ��Cl�Ļ��ϵ�����¶����߶����ͣ�˵���ϸߵ��¶ȷ��������Ȼ�������ɣ���Ҳ�뱾ʵ������һ�¡�����һ������ZnCl2���������͵�ԭ������Ǹ�����ZnCl2�ֽ⣬�ֽ������Cl����FeCl2��������ɡ�
��C��+CaCl2�͡�S��+CaCl2��Ʒ�и��ӷ����������¶ȵĹ�ϵ��ͼ4(b)��ʾ�����Կ�������Ȼ�����ϳ��ֳ���ͼ4(a)���Ƶ����ƣ����롰F��+CaCl2��Ʒ��Ƚ���Zn����Ļӷ����dz��١�����������ڡ�C��+CaCl2�͡�S��+CaCl2��Ʒ��FeO������Fe2+/Fe3+�������Ƚϵͣ����������ZnO��ԭ�ɽ���Zn��
3.2 ����ʱ���Ӱ��
ͼ5��ʾΪ����ʱ�����Ʒ������ʧ��Ӱ�졣���Կ�������Ʒ�������ڼ����в��������γɣ����ӷ�ȥ�������³��ڣ���Ʒ�ӷ��ٶȱȽϿ죬��ʱ���ӳ������ͣ���Լ10 min���ѻ�������ƽ����
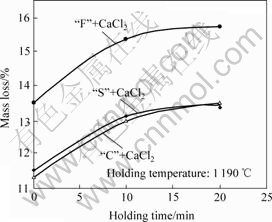
ͼ5 ��Ʒ������ʧ����´���ʱ��Ĺ�ϵ
Fig.5 Mass loss of sample as function of holding time
��1 190 ���£���F��+CaCl2��Ʒ�и��ӷ�����������´���ʱ��Ĺ�ϵ��ͼ6��ʾ�����Կ���������ʱ��Ը��ӷ����������кܴ�Ӱ�죺�¶�����1 190 ���ڼ䣬��Ҫ������ZnCl2���塣��1 190 �������10 min�ڣ� FeCl2�ͽ���Zn�����������Ѹ����������ZnCl2����������Ѹ���½���10 min����ӷ��������������ֲ��䡣��ͼ6�пɷ�������һ���������ƣ���FeCl2��������ɰ�����ZnCl2��������ģ�˵��FeCl2�����е�Cl�ܿ�����������ZnCl2(��Ӧ(3))������CaCl2(��Ӧ(4))��
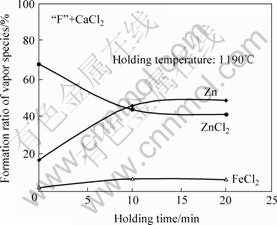
ͼ6 ���´���ʱ��ԡ�F��+CaCl2��Ʒ�лӷ����������Ӱ��
Fig.6 Formation ratio of vapor species as function of holding time
ͼ7��ʾΪ��Ӧ(3)��(4)�ı�����˹�����ܡ���ͼ�ɼ�����923~1 323 ���¶������£���Ӧ(3)�ȷ�Ӧ(4)�߱�����������FeCl2���������ѧ���������һ��˵����Ӧ�����γɵ�ZnCl2��������FeO��Ӧ����FeCl2�����ZnO(��Ӧ(3))�����ɵ�ZnO�ֱ�FeO��ԭ�ɽ���Zn����(��Ӧ(1))��
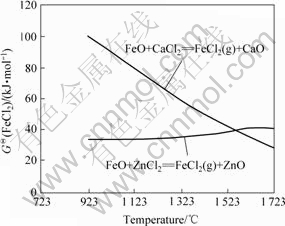
ͼ7 FeCl2���ɵı�����˹������
Fig.7 Standard Gibbs free energy for formation of FeCl2
3.3 ���ɷֵ�Ӱ��
ͼ8��ʾΪ��ͬ�¶��²�ͬ��Ʒ��Zn�Ļӷ��������༰�ӷ�ȥ���ʡ����Կ�����3����Ʒ��Zn�� ��ȥ���ʳ��ֳ�����˳��F��+CaCl2����S��+ CaCl2����C��+CaCl2����ϱ�1�����ݷ��֣����Ķ�Ԫ���CaO/SiO2Խ��Zn��ȥ����Խ�͡�������ѧ�Ƕȷ�������Ԫ���CaO/SiO2Խ��ʹ������CaO������ӣ������˷�Ӧ(2)���ҽ��У�����������ZnCl2��������ɺͻӷ���ǰ�˵��о�[13]��Ҳ������ͬ�������ƣ���������������SiO2�ɴ��ٽ��ɻ����ؽ�����Pb��Zn��Cd�Ļӷ�����������[11?12]������CaO-SiO2-FeO/Al2O3��ϵ��Cl�Ļ��������Ԫ���CaO/SiO2�����Ӷ���С��ͬ��֤����Ȼ�����ZnCl2���γɺͻӷ���
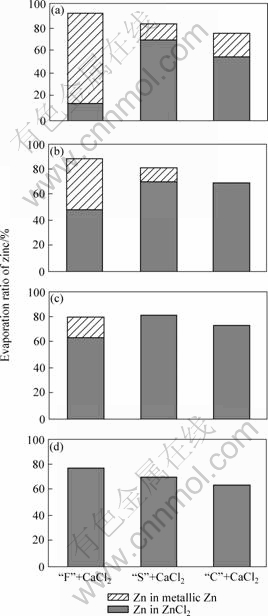
ͼ8 ����Ʒ��Zn�Ļӷ��������༰�ӷ�ȥ����
Fig.8 Evaporation ratio of zinc as function of temperature for different samples
���⣬ͼ8��ʾ�����¡�F��+CaCl2��Ʒ�д���Zn�����Խ���Zn�������ʽ�ӷ��ģ�����C��+CaCl2�͡�S��+CaCl2��Ʒ�У��ȱ��ǽϸߵ��¶���Zn����Ҫ�ӷ���ʽ��Ȼ��ZnCl2���塣ͨ������Ϊ����Ҫ��ΪC-slag��S-slag��FeO������Fe2+/Fe3+�������ϵͣ����Ļ�ԭ�����������ǽϸߵ��¶���Ҳ����������Ľ���Zn����(��Ӧ(1))��������ѧ����FactSageģ������������ͼ9��ʾ��������FeO�������ߣ�����Zn������������������(ͼ9(a))����Fe2+/Fe3+�����Դ˵�Ӱ��ȴ�dz�С(ͼ9(b))�����⣬ǰ�ڽ���о�[14]Ҳ����������Zn����ı�������ѹ������FeO�������Ӷ����ӣ�����Fe2+/Fe3+��ȴû�����Թ�ϵ��������Щ�����˵��FeO��������Ҫ��������������ã����ǻ�ԭ���á���Ҳ��һ��֤����Ȼ�ٽ�����Zn��������ɣ���ZnCl2��������ɺͻӷ��ܵ����ơ�
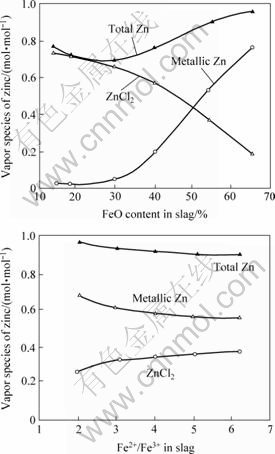
ͼ9 ����ѧ��������FeO������Fe2+/Fe3+�ȶ�Zn�ӷ���Ϊ��Ӱ��
Fig.9 Formation ratios of zinc vapor species as function of FeO content and Fe2+/Fe3+ in slag: (a) Basicity 0.29%, Fe2+/Fe3+=6.20; Basicity 0.29, w(FeO)=39%
3.4 ���ӻ�ԭ����Ӱ��
��ǰ��������ʵ��������Zn����ȥ���ʴ�Լ��60%~92%֮�䲨��(��ͼ8)��Ϊ�˽�һ���ٽ�Zn�Ļӷ�����ʵ���о������ӻ�ԭ����C�۵�Ӱ�졣
����C�ۺ���Ʒ��F��+CaCl2+C����S��+CaCl2+C�͡�C��+CaCl2+C��Zn����ȥ���ʷֱ���ͼ10(a)~(c)��ʾ�����Կ�����������Zn�Ļӷ�Ч����C�������������Ӷ����ӡ�ԭ����һ����C���ܹ��ٽ�FeO���γɣ���������ZnO��ԭΪ����Zn���壬��һ����C����Ϊ��ԭ���ܹ���Ч���ZnO�����еĻ�ȣ�����ZnO�����෴Ӧ�γɸ��ӻ�������Zn2SiO4��ZnAl2O4�ȡ����������������еĿ�����[9]��
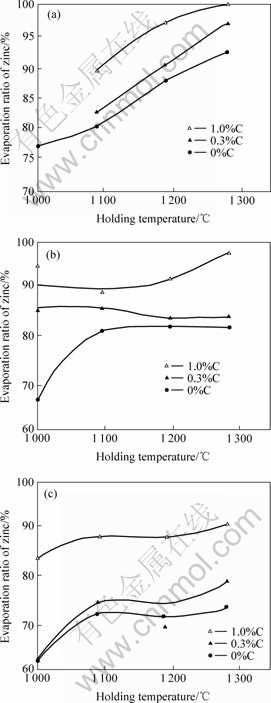
ͼ10 ����C�۶�Zn�ӷ��ʵ�Ӱ��
Fig.10 Effects of carbon on evaporation ratio of zinc: (a) ��F��+CaCl2+C; (b) ��S��+CaCl2+C; (c) ��C��+CaCl2+C
���⣬��ͼ10���Կ�������ͬ��Ʒ��Zn�Ļӷ������¶�֮��Ĺ�ϵ�ʲ�ͬ�ı仯���ơ���F��+ CaCl2+C��Ʒ��Zn�Ļӷ������¶����߶��������ߣ�����S��+CaCl2+C�͡�C��+CaCl2+C��Ʒ���¶ȶ�Zn�Ļӷ��ʵ�Ӱ�첢�����ԡ����������ڡ�F��+CaCl2+C��Ʒ�У�����������C�۵������ܹ���ʹ�����ZnO��FeO��ԭΪ����Zn���壬Zn��ȥ�������¶����߶����ߡ����ڡ�S��+CaCl2+C�͡�C��+CaCl2+C��Ʒ�У�����S-slag ��C-slag����FeO�����ϵͣ������ӵ�C������Ϊ����(���Ϊ1%)������£���ƷZn�Ļӷ�������Ȼ����ZnCl2Ϊ����ǰ���о�[6, 15]ָ��ZnCl2�Ļӷ���Ҫ�ܿ��ڴ�����������Ĵ��ʹ��̣���ˣ�Zn�Ļӷ������¶�Ӱ�첢�����ԡ�
4 ����
1) ������Ʒ90%��+10%ZnO+CaCl2(Ħ����ZnO?CaCl2=1?1)��Ӧ�ü���˹��������С��ԭ�������ʾ�ڱ�ʵ�������»ӷ�������Ҫ��ZnCl2������Zn����FeCl2��
2) ���ڡ�F��+CaCl2��Ʒ������Zn��FeCl2����ӷ������¶������������ߣ���ZnCl2������ȴ��֮���͡����ڡ�S��+CaCl2�͡�C��+CaCl2��Ʒ��Zn�Ļӷ�������Ҫ��ZnCl2����1 190~1 300 �������ֻ����������Zn�������ɡ�
3) ��Ӧ������Ʒ�ӷ��ٶȽϿ죬10 min����������ȶ���ZnCl2������Ҫ���¶�����1 190 ��Ĺ������γɣ������ڼ䣬ZnCl2�����е�FeO��Ӧ����FeCl2������ZnO�������ֱ�FeO��ԭΪ����Zn���塣
4) ����ɷ��У�����Zn�Ļӷ���ΪFeO��Ҫ����������������ã����ǻ�ԭ���á���ȴٽ�����Zn��������ɣ���ZnCl2�����ɺͻӷ��ܵ����ơ�
5) ����C�ۿ������������Zn�Ļӷ��ʡ�
[1] REIJNDERS L. Disposal, uses and treatments of combustion ashes: A review[J]. Resources, Conservation and Recycling, 2005, 43: 313?336.
[2] YOO J, KIM B, LEE J, et al. Kinetics of the volatilization removal of lead in Electric Arc Furnace dust[J]. Materials Transactions, 2005, 46(2): 323?328.
[3] ABDEL-LATIF MASUD A. Fundamentals of zinc recovery from metallurgical wastes in the Enviroplas process[J]. Minerals Engineering, 2002, 15(11): 945?952.
[4] YOSHIIE R, NISHIMURA M, MORITOMI H. Influence of ash composition on heavy metal emissions in ash melting process[J]. Fuel, 2002, 81(10): 1335?1340.
[5] CERQUEIRA N, VANDENSTEENDAM C, BARONNET J, GIROLD C. Heavy metals volatility during thermal plasma vitrification of mineral waste[J]. Environmental Engineering Science, 2004, 21(1): 83?92.
[6] STUCKI S, JAKOB A. Thermal treatment of incinerator fly ash: factors influencing the evaporation of ZnCl2[J]. Waste Management, 1997, 17(1): 231?236.
[7] �� �, ������, ɽ�� ��. �������ջ������ڴ����ؽ����Ȼ�?�ӷ���Ӧ����[J]. ������ѧѧ��, 2005, 26(9): 874?877.
WANG Nan, ZOU Zong-shu, YAMAGUCHI Shu. Thermodynamic analysis of chlorination-evaporation of heavy metals during melting of ash from municipal waste incineration[J]. Journal of Northeastern University, 2005, 26(9): 874?877.
[8] ��ѧ��, ����, ����ƽ, ��С��. ���նԷ��շɻ����ڹ������ؽ�����Ϊ��Ӱ��[J]. �й��������ѧ��, 2006, 26(7): 47?52.
WANG Xue-tao, JIN Bao-sheng, ZHONG Zhao-ping, DANG Xiao-jian. Influence of atmospheres on behavior of heavy metals during melting process of fly ashes from municipal solid waste incinerator[J]. Proceedings of the CSEE, 2006, 26(7): 47?52.
[9] ZHANG Y, KASAI E. Effect of chlorine on the vaporization behavior of zinc and lead during high temperature treatment of dust and fly Ash[J]. ISIJ International, 2004, 44(9): 1457?1468.
[10] BALE C W, CHARTRAND P, DEGTEROV S A, ERIKSSON G, HACK K, BEN M R, MELANCON J, PELTON A D, PETERSEN S. FactSage thermochemical software and databases[J]. Calphad, 2002, 26(2): 189?228.
[11] MIWA M, MORITA K. Chloride capacities of CaO-SiO2- Al2O3(-FeO, MgO, MnO) slags and their application in the incineration processes[J]. ISIJ International, 2002, 42 (10): 1065?1070.
[12] HIROSUMI T, MORITA K. Solubility of chlorine in aluminosilicate slag systems[J]. ISIJ International, 2000, 40 (10): 943?948.
[13] CHAN CHRIS C Y, KIRK DONALD W. Behavior of metals under the conditions of roasting MSW incineration fly ash with chlorinating agents[J]. Journal of Hazardous Materials B, 1999, 64(1): 75?89.
[14] ZHANG Y, KASAI E, NAKAMURA T. Vapor pressure measurements of zinc and its chloride from FeO-CaO-SiO2-Al2O3 slag system[J]. Materials Transactions, 2006, 47(5): 1341?1346.
[15] ABANADES S, FLAMANT G, GAUTHIE D. Kinetics of heavy metal vaporization from model wastes in a fluidized bed[J]. Environment Science and Technology, 2002, 36(17): 3879?3884.
�ո����ڣ�2007- 06-25�������ڣ�2007- 10-26
ͨѶ���ߣ������ᣬ��ʦ����ʿ���绰��010-62332248��13699223791��E-mail: zyl268_ok@126.com
ժ Ҫ���о�Zn�ں�Cl��FetO-CaO-SiO2-Al2O3��ϵ�еĻӷ���Ϊ�������ӷ��������ࡢ�ӷ����Լ����������¶ȡ����ɷ֡����Ӽ��ȵ�Ӱ�졣Ӧ�ü���˹��������С��ԭ������ѧ������ʾ�ڱ�ʵ���¶������£���Ʒ90%��+10%ZnO+CaCl2�еĻӷ�����Ϊ����Zn��ZnCl2��FeCl2��ʵ��������������Zn��FeCl2����ӷ������¶����Ӷ����ӣ���ZnCl2������ȴ��֮���͡���Ӧ���ڣ���Ʒ�ӷ��ٶȺܿ죬10 min����������ȶ���ZnCl2��Ҫ�γ�����Ʒ�����ڼ�(������ʵ���¶�1 190 ��)�������ڼ䣬���ɵ�ZnCl2��FeO��Ӧ����FeCl2���弰ZnO�������ֱ�FeO��ԭ�ɽ���Zn���塣���ɷ��У�FeO�����Ͷ�Ԫ���CaO/SiO2��Zn�Ļӷ��������༰�ӷ�������ҪӰ�졣���ӻ�ԭ����C�ۿ��������Zn�Ļӷ��ʡ�


