���±�ţ�1004-0609(2012)04-1147-09
SnO2/Ni��������ӵ�ظ������ϵ��Ʊ�����绯ѧ����
�� ��������ǿ������ϼ�������棬�˺��
(�㽭��ѧ ���Ͽ�ѧ�빤��ѧϵ, ���� 310027)
ժ Ҫ��
���û�е��ĥ��������SnO2��Ni��ĩ���ϣ���Ϊ����ӵ�ظ������ϡ�����XRD��SEM��TEM��EDS������ĥ�����в��Ͻṹ����ò�ı仯����SnO2/Ni���ϸ������ϵ��״ο���Ч�ʡ�ѭ���ȶ��Լ�CV���ߵȽ��в��Է�������������������Ϸ�ĩ��ĥ�ʵ�ʱ���SnO2��Ni���γɽ�ϳ�֡������ߴ�ϸС���ֲ����ȵĸ��ϲ��ϣ�SnO2��Ni�ĸ��Ͽ���Ч���SnO2���״ο���Ч�ʺ�ѭ���ȶ��ԣ�SnO2/Ni���ϸ������ϵ�ѭ���ȶ�������ĥʱ����ӳ������ӣ����缫���״ο���Ч������ĥʱ����ӳ��������Ӻ��½������ƣ�Ni��������Ч��С��SnO2���״γ�ŵ�ѭ������������Li2O�IJ����淴Ӧ�̶ȣ���������ѭ�������в�����Li-O���������ʽ���п��淴Ӧ��
�ؼ��ʣ�
����ӵ����������������ĥ���绯ѧ������
��ͼ����ţ�TM912 ���� ���ױ�־�룺A
Fabrication and electrochemical properties of SnO2/Ni composite anodes for lithium ion batteries
CHEN Xuan, LIU Ji-qiang, GAO Ming-xia, LIU Yong-feng, PAN Hong-ge
(Department of Materials Science and Engineering, Zhejiang University, Hangzhou 310027, China)
Abstract: Nano SnO2 and Ni powders were ball-milled to form composites as anode materials for lithium ion batteries. The structure and morphology of the composites were analyzed and observed by XRD, SEM, TEM and EDS. The electrochemical properties, including the first coulumbic efficiency, cycle performance and CV curves, were tested. The results show that SnO2 and Ni combine tightly, forming SnO2/Ni composite with small particles. Nano-SnO2 particles disperse uniformly in the Ni-based matrix. The combination of SnO2 with Ni can obviously increase the first coulumbic efficiency and cycle stability of the anode. Moreover, with the increase of the ball-milling time, the first coulumbic efficiency of SnO2/Ni anode first increases then decreases, while the cycle stability almost increases monotonously. The introduction of Ni can reduce effectively the irreversible reaction of SnO2 and Li that forms Li2O and also favors partial Li2O to be reversible in the forms of Li-O compounds in the following cycles.
Key words: lithium ion batteries; anode materials; ball-milling; electrochemical properties
��20����90�������ӵ��������������Ϊ���õĸ�������һֱ��Ҫ��̼���ϡ���������ӵ���ڸ��������������߹��ʵ����������IJ������ӣ��Ե缫�������ܵ�Ҫ��������ߡ�̼�������ϵ�����������Ϊ372 mA��h/g���Ѳ�������Ҫ����ˣ�����������ӵ�ظ������ϵ��о��Ϳ�����Ϊ���С�Si����������[1-3]�����ɽ���������[4-7]��Sn����������[8-11]����Ϊ����ӵ�ظ������Ͼ��иߴ�1~2 A��h/g����ߵ���������������ܵ�����о��ߵIJ������ӣ������״β������������ѭ��˥�˿������ؽ�������
����SnO2���иߴ�1.8 A��h/g ���״ηŵ�����[8]����һ�ּ��߷�չDZ��������ӵ�ظ������ϣ������״β���������Ҳ�ܸߡ�SnO2�����״β��������������Ҫԭ����Ϊ�����״ηŵ������SnO2��Li+��Ӧ�����˻����������Li2O[12]��
![]() ��
��![]() (1)
(1)
���⣬�缫��������Һ��Ӧ�ڵ缫�������ɹ������ʽ���(SEI)Ĥ�������˲���Li+�����µ缫�IJ��������������ŵ������Sn��Li+��Ӧ���ɸ���Li-Sn�Ͻ�[12]��
Sn+xLi++xe![]() LixSn (0��x��4.4) (2)
LixSn (0��x��4.4) (2)
�������̵������ص�������ͣ�ʹSnO2�缫���ڿ��ѡ��ۻ��Ͱ��䣬ʧȥ�绯ѧ���ԣ����½ϲ��ѭ���ȶ��ԡ���ˣ�������ѧ�߲��ö��ַ�������ͨ����СSnO2�ijߴ硢�Ż����۽ṹ�����������ϸ� ���γɸ��ϲ��ϵ��Լ�СSnO2���״β����������������ѭ���ȶ���[13-16]����SnO2������ǻ���/�����Եڶ��࣬����Ϊ��һ������Ч��ֹ�������������͡���ߵ缫����ѭ���ȶ��Ե���Ч����[17-19]��
�������߲��û�е��ĥ���Ʊ�����SnO2/Ni���ϲ��ϣ���ͨ��Ni�����룬�������״γ�ŵ������Li2O�����ɺͼ�СSnO2��ѭ�������е�������ͼ�ʹ����Li2O�ֽⲢʵ�ֲ��ֿ��棬�Ӷ����SnO2�����Ŀ�����������ѭ���ȶ��ԡ����Ը��ϲ��ϵ��Ʊ����ա��ṹ����绯ѧ���ܼ������Խ��з����о���
1 ʵ��
����������SnO2Ϊ��ʼԭ���ϣ�����ò��ͼ1��ʾ����ͼ1��֪������SnO2���нϹ���Ķ�������Σ��ߴ�ԼΪ30 nm����SnO2�ͽ�������(����ԼΪ76 ��m)��������1:1��ϣ����и�����ĥ���Ʊ�SnO2/Ni���ϲ��ϡ����ò������ĥ��ĥ�����ϱ�Ϊ20:1����ĥת��Ϊ500 r/min����ĥʱ��Ϊ1~120 h������X����������(XRD��Rigaku-D/MAX-2550PC�ͣ�������˾����)�����ò���������������ʹ��Cu K������Դ������Ϊ1.540 6 ?��Ni�˲�Ƭ��XRD�Ĺ��ʲ���Ϊ40 kV��20 mA���Բ���ɨ�跽ʽ�ɼ����ݣ�����Ϊ0.02�㣬ÿ������ʱ��Ϊ1 s������ȫ����Ϸ�������Ʒ�и�������ȡ����������;����ߴ硣�����ߴ����Scherrer��ʽ���㣺
![]() (3)
(3)
ʽ�У�![]() Ϊ����(hkl)�����Ӧ�ijߴ磻���������İ�߿������Dz�����ǣ���Ϊ������k�dz�����Ϊ0.9����ĥ�������ò����ɨ��羵(SEM��S-4800���ձ�����)����羵(TEM��JEM-2110���ձ�����)���й۲죬�ɷּ��ֲ��ֱ����SEM��TEM�µ�������(EDS)���з�����
Ϊ����(hkl)�����Ӧ�ijߴ磻���������İ�߿������Dz�����ǣ���Ϊ������k�dz�����Ϊ0.9����ĥ�������ò����ɨ��羵(SEM��S-4800���ձ�����)����羵(TEM��JEM-2110���ձ�����)���й۲죬�ɷּ��ֲ��ֱ����SEM��TEM�µ�������(EDS)���з�����
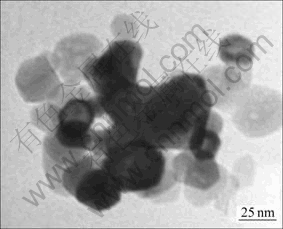
ͼ1 ��ҵ����SnO2��TEM��
Fig. 1 TEM image of commercial nano-SnO2 powders
SnO2/Ni���ϸ������ϵĵ绯ѧ���ܲ�����CR2025�Ϳ�ʽ���Ϊ����ģ�͡���NMPΪ�ܼ�����SnO2/Ni���ϲ��ϡ��������Ȳ�ڼ������ƫ����ϩ(PVDF)��������85:10:5���ɽ��ϣ������Ͼ��ȣ�����Ϳ����ĭ���ϣ�����110 ?C����ո���12 h����Ϊ������������SnO2/Ni��Ϳ����ԼΪ5 mg�����Ƭ(���ȣ�99.9%)Ϊ�Ե缫����Celgard2300�۱�ϩ���ĤΪ��Ĥ����1 mol/L LiPF6��̼����ϩ��EC/̼�������DMC(������Ϊ1:1)�Ļ����Һ��Ϊ���Һ�������װ�ڵ¹�MBRAUN��˾����LABSTAR����������ɣ��������г����ߴ���������װ�����������ģ���ڷ�ĩѹƬ���Ͻ���ؿǷ�ڡ�
��ģ���ؽ��к������ŵ����(Land��ز���ϵͳ���人�н�ŵ��������˾����)��ѭ������(CV)����(Arbin-001 MITS 2.9-BT2000�����ǣ���������)���缫������߲��Եĵ�ѹ��ΧΪ0.01~3.0 V(vs Li/Li+)�������ܶ�Ϊ50 mA/g��CV���ߵIJ��Ե�ѹ��ΧΪ0~3 V��ɨ������Ϊ0.1 mV/s���绯ѧ���ܲ����¶Ⱦ�Ϊ25 �档
2 ��������
2.1 SnO2/Ni���ϲ��ϵĽṹ����ò
ͼ2��ʾΪSnO2��Ni����ͬʱ����ĥ������XRD�ס���ͼ2�ɼ�����ĥ1 h������Ҫ������SnO2(�ķ����ʯ)�ͽ�����(��������)��ɡ������� ��ĥʱ����ӳ���SnO2������������������ĥ120 h��SnO2�������������ʧ������Ҫ����������ĥ������SnO2��������ϸ�����Ǿ�������ġ����⣬��XRD���ɷ��֣�����ĥʱ��ﵽ10 h��������(111)���������������������Ե�������壬��������ĥʱ����ӳ����÷�����ǿ��(����������������ǿ��)������ǿ���ҷ�λ������С�Ƕȷ����ƶ���������(111)�����������ǿ���ϼ���������������ʧ��
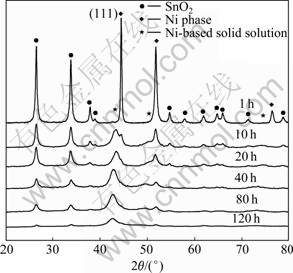
ͼ2 SnO2��Ni����ͬʱ����ĥ������XRD��
Fig. 2 XRD patterns of SnO2 and Ni ball-milled for different times
�Ծ�20��40 h��ĥ��Ʒ�ɷ���SEM�²���EDS������������1���С��ɱ�1�ɼ�����ĥ����Ʒ�г����˽϶��Fe��������Ni������Ҫ������ĥ�����д���ĥ��ĥ������ġ�Fe��Cr��ԭ�Ӱ뾶�ֱ�Ϊ1.71 ?��1.85 ?����Ni��ԭ�Ӱ뾶(1.62 ?) ���ɴ��ƶϣ�����ͬʱ����ĥ��Ni������������С�Ƕȷ���ı仯������������Ni-Fe-Cr�����塣
��1 ��ͬʱ����ĥ��SnO2/Ni��Ʒ�ɷֵ�EDS���Խ��
Table 1 Compositions of SnO2/Ni composites prepared by different times of ball-milling detected by EDS
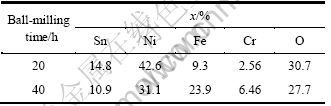
����Ʒ��XRD���ݽ��Jade��Rietical162�������з����������и���ĺ������侧���������ڱ�2����������ĥ������SnO2��Ni�ķǾ��������ຬ�����������ȷ�Խ��ͣ�������������Ƕ���ĥ�����в��Ͻṹ�ݱ�ķ�������һ����ָ�����á�
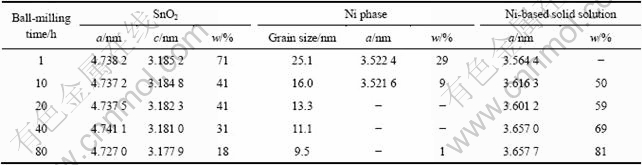
�ӱ�2��֪������ĥʱ����ӳ���SnO2�ľ����ߴ�((110)����)���ϼ�С����SnO2�ľ�����������û�з����仯����Niͬ���������������ṹ��Ni����������ľ�������(a)��Ni���Դ�����ĥʱ����ӳ��������ӣ���Ҳ��Fe��Cr�Ĺ��ܶ�������һ�¡������SnO2�ຬ������ĥʱ������Ӷ����Ͻ��ͣ��� ������XRD���������ֵ������ǿ�Ȳ��ϼ���������������Ǿ���ת����һ�¡�
SnO2��Ni����ͬʱ����ĥ������SEM����ͼ3��ʾ����ĥ1 h����������SnO2�������������ڷ���״̬��û���γ���Ч���(��ͼ3(a))������ĥʱ��Ϊ10��20 hʱ����������SnO2�ѳ�ֽ�ϣ�������SnO2/Ni�����žۣ����С�Ⱦ�1 h��ĥ�����Ҫ�� (�Ա�ͼ3(a)��(c))����ĥʱ���ӳ���40 h��SnO2/Ni������������ϸ��(��ͼ3(d))��������ĥʱ���һ���ӳ���80 h������ʱ���ܴ�һ����SnO2/Ni�����ֿ�ʼ�ž۳���(��ͼ3(e)��(f))��
��2 SnO2��Ni����ͬʱ����ĥ������и��ຬ��������ṹ������SnO2����((110)��)�ߴ�
Table 2 Phase content, cell parameters and grain size of SnO2 (face (110)) of products of SnO2 and Ni ball-milled for different times

ͼ3 SnO2��Ni����ͬʱ����ĥ������SEM��ò
Fig. 3 SEM images of products from SnO2 and Ni ball-milled for different times: (a)1 h; (b) 10 h; (c) 20 h; (d) 40 h; (e) 80 h; (f) 120 h
ͼ4(a)��(b)��(c)��ʾ�ֱ�ΪSnO2��Ni��1��10��20 h��ĥ������TEM��ͼ4(a)������ؿ�������1 h��ĥ�����ε�SnO2��Ni�����ʷ���״̬����ĥ10 h��SnO2��Ni�ѻ�����ϳ�һ��(��ͼ4(b))����ĥ20 h��SnO2��Ni�ѳ�ֽ�ϳ�Ϊһ�塣ͼ5��ʾΪ��20 h��ĥ���SnO2/Ni���ϲ��ϵ�TEM��Ni��Sn��OԪ��EDS��ֲ�����ͼ5��֪��SnO2��Ni������������зֲ����ȡ�SnO2��Ni��10 h������ĥ���γ���SnO2�����ֲ���Ni�����������ĸ��ϲ��ϡ�
2.2 SnO2/Ni���ϵ缫���ϵĵ绯ѧ����
SnO2��Ni����ͬʱ����ĥ����P��ҵ����SnO2���״ηŵ硢����������״ο���Ч�����ڱ�3������Ni����������Ϊ����Ƕ﮻����࣬���ڱ�ʵ���У�����SnO2/Ni�缫�ı�����ʱ�缫����������Ni��������������ϲ��ϵ缫���״ηŵ硢�������������ҵ����SnO2�����Եͣ������״ο���Ч�ʱ���ҵ����SnO2��(56%)�������ӡ�����ĥʱ���1 h���ӵ�10 h��SnO2/Ni���ϸ������״ο���Ч�ʴ�61%���ӵ�75%����ĥʱ��Ϊ20 hʱ���缫�Ŀ���Ч�ʽ�һ�����ӵ�78%��������ĥʱ��Ľ�һ���ӳ������ϵ��״ο���Ч�ʷ��������½�����120 h��ĥ���ϲ��ϵ��״ο���Ч�ʽ���66%�����ϲ��ϸ����״ο���Ч�ʸ��Ƶ���Ҫԭ�������SnO2��Ni���Ϻ������״ηŵ�������γɵķǻ���Li2O�����١�

ͼ4 SnO2��Ni����ͬʱ����ĥ������TEM��
Fig. 4 TEM images of products from SnO2 and Ni ball-milled for different times: (a) 1 h; (b)10 h; (c) 20 h
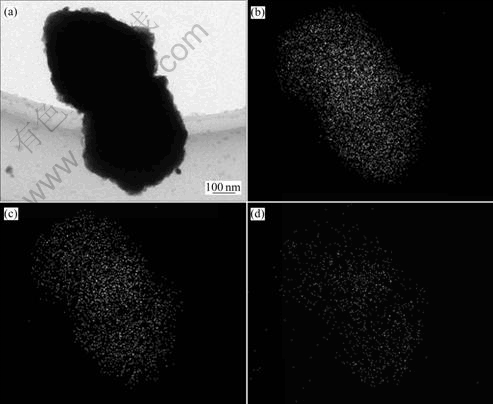
ͼ5 SnO2��Ni��20 h��ĥ������TEM��Ni��Sn��EDSԪ����ֲ�
Fig. 5 TEM image of product from SnO2 and Ni ball-milled for 20 h (a) and its corresponding EDS plane maps of Ni (b), Sn (c) and O (d)
��3 ��ͬʱ����ĥ��SnO2/Ni���ϲ��ϸ�������ҵSnO2�������״ηŵ硢����������״ο���Ч��
Table 3 First discharge, charge capacities and first coulumbic efficiencies of anodes of SnO2/Ni composites prepared by different times of ball-milling and commercial nano-SnO2
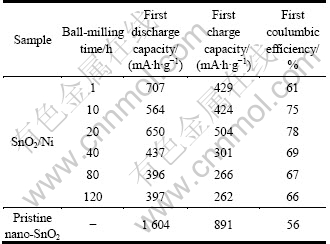
SnO2����������϶̵�ʱ��(1 h)��ĥ����������SnO2�ںܴ�̶��ϴ��ڷ���״̬���Ը���SnO2���״ο���Ч�����û������ޡ�������ĥʱ���ӳ��� 10 h��SnO2��Ni�ij�ֽ�ϣ�Ni�ٽ��˲����ɷ�Ӧʽ(1)���ɵ�Li2O�ķֽ⡣POIZOT��[20]�������ڳ� ������У�Ni��ʹ����Li2O�����ֽ⣬��Ӧ���£�
![]()
![]()
![]() (4)
(4)
�����Ni��������Ч�����SnO2���״ο���Ч�ʡ���������ĥ20 h��SnO2��Ni��Ч��ϣ��γɵ�SnO2/Ni������ϸС��������ʾ�������״ο���Ч�ʼ��״ηŵ�ͳ��������������ĥʱ��Ľ�һ���ӳ���SnO2�Ǿ�����������SnO2/Ni�����žۣ�������ijɷַ����˽ϴ�ı仯���������ǵ��²����״ο���Ч�ʼ����״ηŵ硢��������������͵�ԭ��
ͼ6(a)��(b)��ʾ�ֱ�Ϊ��ʼ����SnO2�缫��SnO2/Ni���ϲ��ϵ缫��ѭ���������ߡ���ͼ6�ɼ�������SnO2��Ȼ���״ηŵ���������ѭ��˥�˷dz��죬��20��ѭ������������Ϊ140 mA��h/g��SnO2��Ni���Ϻ���ѭ���ȶ��Եõ����Ը��ƣ���������ĥʱ�����ӵ�40 h�����ϡ���30��ѭ����1 h��ĥ����Ʒ��������Ϊ100 mA��h/g������40��80 h��ĥ��Ʒ�������ֱ�Ϊ175 mA��h/g��225 mA��h/g�����ϲ��ϵ缫ѭ���ȶ��Եĸ���һ����������Ni��Li2O��Ӧ��ʹ����Li2O�ֽ�������ѭ���������SnO2�������ʣ���һ���棬SnO2/Ni���ϲ����и���ľ���ϸ�������Ǿ�����һ���̶��ϻ����˷ŵ����������Li-Sn�Ͻ�(��ʽ(2))������������͡�
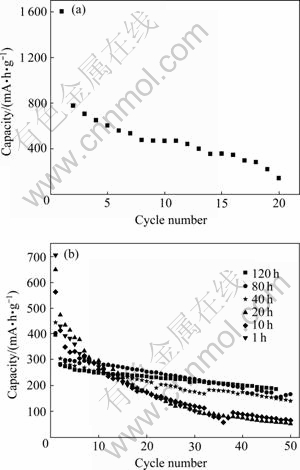
ͼ6 ����SnO2�缫�뾭��ͬʱ����ĥ��SnO2/Ni���ϲ��ϵ缫��ѭ������
Fig. 6 Cycle performance of anodes of pristine SnO2(a) and SnO2/Ni composite(b) prepared by different ball-milling times
ͼ7(a)��(b)��ʾ�ֱ�Ϊ����SnO2�缫��SnO2��Ni��20 h��ĥ��õĸ��ϲ��ϵ缫��ǰ����ѭ���ij�ŵ����ߡ���ͼ7(a)�ɼ���SnO2�缫���״ηŵ�����У���Լ0.85 V����һ�Ͽ��ķŵ�ƽ̨��������ѭ���У���ƽ̨������ʧ����ƽ̨��Ҫ��Ӧ�ڷ�Ӧʽ(1)�����⣬��0.8~0.5 V���ֳ���һ��С�ķŵ�ƽ̨�����ŵ��ѹ�����½���ֱ����ֹ��ѹ���õ͵�ѹ����ķ�Ӧ��Ҫ��Ӧ�ڷ�Ӧʽ(2)���γɲ�ͬ���͵�Li-Sn�Ͻ𡣴��⣬SEIĤ���γ�Ҳͨ����0.8 V���ҵĵ�ѹ��Χ��������SnO2/Ni���ϵ缫���״ηŵ�������λ��0.85 V���ҵķŵ�ƽ̨���Լ�С�������ڵڶ��͵�����ѭ���ķŵ�����и�ƽ̨Ҳ������ʧ�������˵����Ni�����ӿɼ��ٷ�Ӧʽ(1)�IJ������ԡ���SnO2�缫�ij�������ϣ��������״λ���������ѭ���У������������������Ե�ƽ̨��һ������λ��0.5~1.0 V���õ͵�λ���ij��ƽ̨��Ӧ��Li-Sn�Ͻ���Li���ѳ�����һ��������1.0~2.0 V��Χ����ƽ̨ӦΪLi2O��Li�ѳ��ķ�Ӧ��������SnO2/Ni���ϵ缫�ij�����ߣ�����0.5~1.0 V��ѹ��Χ�ĵ�ѹƽ̨���Լ�С����1.0~2.0 V��2.0 V�������ɼ��������ƽ̨�������SnO2�缫��SnO2/Ni���ϵ缫�иߵ�λ����ij����������ڵ͵�λ����ij���������ӣ���Ҳ��һ��˵��Ni�ٽ������״ηŵ�������γɵ�Li2O�ڳ������еIJ��ַֽ⣬���ֽ������ѭ����
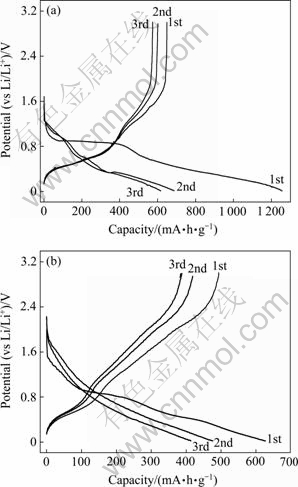
ͼ7 ����SnO2�缫�뾭20 h��ĥ��SnO2/Ni���ϲ��ϵ缫��ǰ���γ�ŵ�����
Fig. 7 Discharge/charge curves of 1st three cycles of pristine SnO2(a) and SnO2/Ni composite prepared by 20 h of ball- milling(b)
ͼ8(a)��(b)��ʾΪ����SnO2�缫�;�20 h��ĥ��SnO2/Ni���ϲ��ϵ缫��ѭ���������ߡ���ͼ8(a)�ɼ�������SnO2�缫���״�ѭ��ʱ����Լ0.65 V��0.75 V��λ�ø�����ǿ�Ⱥܴ�Ļ�ԭ�壬���SnO2�缫���״ηŵ�������ڸõ�ѹ��Χ���ֵ������ŵ�ƽ̨Ҳ���Ӧ���˵�ѹ���ķ�Ӧ��Ҫ�����ڷ�Ӧʽ(1)�����⣬�÷�����ķ�Ӧ���ܻ���SnO2������������Һ���ɶۻ�Ĥ(SEI)�ķ�Ӧ�����Ǹ÷�������ѭ���ж�û�г��֣�Ҳ��һ��˵���÷�Ӧ���кܴ�IJ������ԡ��ڵڶ�������ѭ���У�ȡ����֮����Լ0.85 V�����˿���Ļ�ԭ�壬�õ�ѹ��Χ�Ļ�ԭ�屻��Ϊ�Dz���Li��������Li-O������[21]�����䲻ͬ�ķ�Ӧ��λ��֪�������ɵĻ��������״ηŵ�������γɵ�Li2O������ͬ�������Ӧ��������Ӧ(��﮷�Ӧ)������1.3 V���û�ԭ������Ӧ���нϺõĿ����ԡ���û�ԭ�������Ӧ�ĵ�λ����ŵ�ͳ��������Ҳ������ƽ̨(��ͼ7(a))��ѭ��������������0.3 V���µķ�Ӧ��ΪLi-Sn�Ͻ����ɵķ�Ӧ����ͬ�ķ�λ��Ӧ�ڲ�ͬ�̶ȵ�Ƕ﮷�Ӧ��������SnO2/Ni���ϵ缫����Լ0.65 V���ֵIJ����滹ԭ��������������ϵ缫���״β������������Խ��͡����⣬�ڸ��ϵ缫��û����������SnO2�缫��λ��0.85 V�Ļ�ԭ��Ӧ������Լ1.3 V���Դ��������塣���⣬�ڸ��ߵĵ�λ(Լ1.6 V)�����˻�ԭ�壬��֮���Ӧ����Լ2.1 V��������һ�������塣����KANG��[4]�ı��������������ԭ���Ӧ��Ni��Ϊ������Li2O�IJ��ֿ���������ԭ��Ӧ (��Ӧʽ(4))��SnO2/Ni���ϵ缫��������ԭ��Ӧ�Եĵ�λ�����ŵ������ϳ��ֵ�ƽ̨Ҳ�кܺõ�һ���ԡ��ɼ���Ni�Ĵ��ڸı���Li2O�ķֽ���γ�Li-O������ķ�ʽ���̣���ʹSnO2/Ni���ϲ��ϵ缫���״ο���Ч�ʼ�ѭ�����ܵõ���Ч��ߡ�
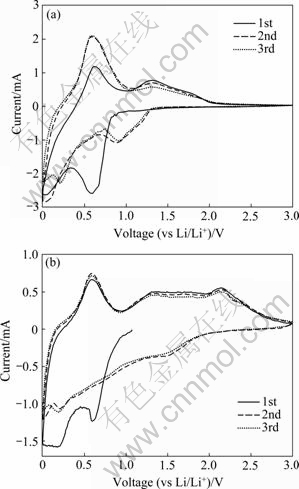
ͼ8 ������SnO2�缫(a)��SnO2/Ni���ϲ��ϵ缫(��ĥ 20 h)(b)ǰ����ѭ����CV����
Fig. 8 CV curves of 1st three cycles of anodes of commercial SnO2(a) and SnO2/Ni composites prepared from 20 h of ball- milling(b)
������ĥ������Ni����ĥ��ĥ���е�Fe��Cr�Ͻ�Ԫ�ط�����һ���̶ȵĹ��ܣ������ɵ�Ni���������С��SnO2��ѭ�������з�����������ͣ�����Ч�ֽ�SnO2���״�ѭ�����������ɵIJ���Li2O����СSnO2�缫���״β������������������ѭ��������ʹ����Li-O��������п������Ƕ����ԣ���ߵ缫��ѭ���ȶ��ԡ�
3 ����
1) ����SnO2�������Ni����ĥ�����У�����ĥʱ����ӳ����侧������ϸ�������Ǿ�������10~20 h��ĥ��SnO2������������Ч��ϣ�����Ni�����о��ȷֲ���������SnO2/Ni���������žۡ�����ĥʱ���ӳ���40 h��SnO2/Ni��������ϸ���;��Ȼ�������һ���ӳ���ĥʱ�䣬��SnO2/Ni�����������ž۳�����ĥ������������ĥ��ĥ���е�Fe��Cr���������ܣ���ʼ��Ni��һ���̶��ϳ�ΪNi�������塣
2) SnO2��Ni����ĥ�����γɵ�SnO2/Ni(Ni��������)���ϵ缫���״ο���Ч���������ĥǰ������SnO2�缫(56%)��������ߡ�������ĥʱ����ӳ������ֳ��������ټ�С�ı仯������ĥʱ��Ϊ10~20 hʱ����Ʒ���״ο���Ч�ʵõ�������ߣ�Ϊ76%~78%��SnO2��Ni���Ϻ���ѭ���ȶ���Ҳ�õ�������ߣ�������ĥʱ����ӳ�����ѭ���ȶ������ӡ��Ե缫��CV�������ŵ����ߵķ����о�������SnO2/Ni���ϵ缫�״ηŵ��������Li2O�IJ������Ա�SnO2�缫��Ҫ���ö࣬Ni��Ч�ٽ���Li2O�ķֽ⣬��������ѭ�����Բ�ͬ��Li2O��Li-O���������ʽʵ�ֲ��ֿ�����Ƕ﮷�Ӧ��
REFERENCES
[1] BEATTIE S D, LARCHER D, MORCRETTE M, SIMON B, TARASCON J M. Si electrodes for Li-ion batteries��A new way to look at an old problem[J]. Journal of The Electrochemical Society, 2008, 155(2): A158-A163.
[2] WANG K, HE X M, WANG L, REN J G, JIANG C Y, WAN C R. Si, Si/Cu core in carbon shell composite as anode material in lithium-ion batteries[J]. Solid State Ionics, 2007, 178: 115-118.
[3] ���Ǿ�, ԭ��ϼ, ���Ϸ�, ������, ������. ��ĥ���ն�̿������(CA)-SiO���ϲ��Ͻṹ�͵绯ѧ���ܵ�Ӱ��[J]. ������ѧ��, 2008, 23(5): 917-922.
CHAO Ya-jun, YUAN Xian-xia, MA Zi-feng, DENG Xiao-yan, YU Wen-li. Effects of ball-milling on structure and electrochemical property of CA-SiO composite[J]. Journal of Inorganic Materials, 2008, 23(5): 917-922.
[4] KANG Y M, KIM K T, KIM J H, KIM H S, LEE P S, LEE J Y, LIU H K, DOU S X. Electrochemical properties of Co3O4, Ni-Co3O4 mixture and Ni-Co3O4 composite as anode materials for Li ion secondary batteries[J]. Journal of Power Sources, 2004, 133(2): 252-259.
[5] NEEDHAM S A, WANG G X, LIU H K. Synthesis of NiO nanotubes for use as negative electrodes in lithium ion batteries[J]. Journal of Power Sources, 2006, 159: 254-257.
[6] XIANG J Y, TU J P, HUANG X H, YANG Y Z. A comparison of anodically grown CuO nanotube film and Cu2O film as anodes for lithium ion batteries[J]. Journal of Solid State Electrochemistry, 2008, 12: 941-945.
[7] ����ǿ, ������, ����֥, ����Ƽ, �� ��, ������, �ƿ���. ���ȳ������Ʊ�NiO��ϸ��ĩ����绯ѧ����[J]. �й���ɫ����ѧ��, 2008, 18(S1): s301-s305.
HE Ze-qiang, SUN Xin-yang, XIONG Li-zhi, LIU Wen-ping, CHEN Shang, WU Xian-ming, HUANG Ke-1ong. Preparation and electrochemical properties of superfine NiO powders by homogeneous precipitation method[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(S1): s301-s305.
[8] PARK M S, KANG Y M, KIM J H, WANG G X, DOU S X, LIU H K. Effects of low-temperature carbon encapsulation on the electrochemical performance of SnO2 nanopowders[J]. Carbon, 2008, 46: 35-40.
[9] HASSOUN J, PANERO S, SIMON P, TABERNA P L, SCROSATI B. High-rate, long-life Ni-Sn nanostructured electrodes for lithium-ion batteries[J]. Advanced Materials, 2007, 19: 1632-1635.
[10] SHIN N R, KANG Y M, SONG M S, KIM D Y, KWON H S. Effects of Cu substrate morphology and phase control on electrochemical performance of Sn-Ni alloys for Li-ion battery[J]. Journal of Power Sources, 2009, 186: 201-205.
[11] ������, ����ǿ, ����֥, ���º�, Ф��, ������, ����Ƽ. ���ȳ������Ʊ�SnO2-ʯī���Ϸۼ���绯ѧ����[J]. �й���ɫ����ѧ��, 2005, 15(5): 793-798.
MA Ming-you, HE Ze-qiang��XIONG Li-zhi, LI Xin-hai, XIAO Zhuo-bing, WU Xian-ming, LIU Wen-ping. Preparation and electrochemical properties of SnO2-graphite composites by homogeneous precipitation technique[J]. The Chinese Journal of Nonferrous Metals, 2005, 15(5): 793-798.
[12] COURTNEY I A, DAHN J R. Electrochemical and in situ X-ray diffraction studies of the reaction of lithium with tin oxide composites[J]. Journal of the Electrochemical Society, 1997, 144(6): 2045-2052.
[13] YUAN L, GUO Z P, KONSTANTINOV K, LIU H K, DOU S X. Nano-structured spherical porous SnO2 anodes for lithium-ion batteries[J]. Journal of Power Sources, 2006, 159: 345-348.
[14] WANG Y, LEE J Y. Molten salt synthesis of tin oxide nanorods: Morphological and electrochemical features[J]. Journal of Physical Chemistry B, 2004, 108: 17832-17837.
[15] CHEN Y C, CHEN J M, HUANG Y H, LEE Y R, SHIH H C. Size effect of tin oxide nanoparticles on high capacity lithium battery anode materials[J]. Surface & Coatings Technology, 2007, 202: 1313-1318.
[16] PARK M S, KANG Y M, WANG G X, DOU S X, LIU H K. The effect of morphological modification on the electrochemical properties of SnO2 nanomaterials[J]. Advanced Functional Materials, 2008, 18: 455-461.
[17] WEN Z H, WANG Q, ZHANG Q, LI J H. In situ growth of mesoporous SnO2 on multiwalled carbon nanotubes: A novel composite with porous-tube structure an anode for lithium batteries[J]. Advanced Functional Materials, 2007, 17: 2772-2778.
[18] YU Y, CHEN C H, SHI Y. A tin-based amorphous oxide composite with a porous, spherical, multideck-cage morphology as a highly reversible anode materials for lithium-ion batteries[J]. Advanced Materials, 2007, 19: 993-997.
[19] KONISHI T, HAYASHI A, TADANAGA K, MINAMI T, TATSUMISAGO M. Electrochemical performance and structural change during charge-discharge reaction of SnO-P2O5 glassy electrodes in rechargeable lithium batteries[J]. Journal of Non-Crystalline Solids, 2008, 354: 380-385.
[20] POIZOT P, LARUELLE S, GRUGEON S, DUPONT L, TARASCON J M. Nano-sized transition-metal oxides as negative-electrode materials for lithium-ion batteries[J]. Nature, 2000, 407: 496-500.
[21] XUE M Z, FU Z W. The reinvestigation on electrochemical reaction mechanism of stannic oxide thin film with lithium[J]. Electrochemical and Solid State Letters, 2006, 9(10): A468-A470.
(�༭ ������)
������Ŀ���㽭ʡ��Ȼ��ѧ����������Ŀ(Y4080190)
�ո����ڣ�2010-05-20�������ڣ�2011-12-20
ͨ�����ߣ�����ϼ�������ڣ���ʿ���绰��0571-87952615�����棺0571-87952615��E-mail: gaomx@zju.edu.cn
ժ Ҫ�����û�е��ĥ��������SnO2��Ni��ĩ���ϣ���Ϊ����ӵ�ظ������ϡ�����XRD��SEM��TEM��EDS������ĥ�����в��Ͻṹ����ò�ı仯����SnO2/Ni���ϸ������ϵ��״ο���Ч�ʡ�ѭ���ȶ��Լ�CV���ߵȽ��в��Է�������������������Ϸ�ĩ��ĥ�ʵ�ʱ���SnO2��Ni���γɽ�ϳ�֡������ߴ�ϸС���ֲ����ȵĸ��ϲ��ϣ�SnO2��Ni�ĸ��Ͽ���Ч���SnO2���״ο���Ч�ʺ�ѭ���ȶ��ԣ�SnO2/Ni���ϸ������ϵ�ѭ���ȶ�������ĥʱ����ӳ������ӣ����缫���״ο���Ч������ĥʱ����ӳ��������Ӻ��½������ƣ�Ni��������Ч��С��SnO2���״γ�ŵ�ѭ������������Li2O�IJ����淴Ӧ�̶ȣ���������ѭ�������в�����Li-O���������ʽ���п��淴Ӧ��


