���±��: 1004-0609(2005)05-0817-06
�ܽ�-�������Ʊ�TiO2����������������
Ǯ ��1, 2, 3, ����ѧ1, ʯ ë1, ����Ԫ1, ¬�ܹ�1, �ƿ���1, �� ӽ2
(1. ���ϴ�ѧ ��ѧ����ѧԺ, ��ɳ 410083;
2. ���ϴ�ѧ ��ĩұ������ص�ʵ����, ��ɳ 410083;
3. �й�ʯ����������ֹ�˾, ���� 414012)
ժ Ҫ��
������ͨ���ܽ�-���������й��ɽ���(Fe3+�� Zn2+�� Co2+�� Ni2+�� Cr3+��Sn4+)��ϡ��Ԫ��(La3+�� Pr3+�� Nd3+�� Ce4+�� Sm3+�� Tb3+�� Eu3+�� Gd3+�� Y3+��Dy3+)���ӵ�TiO2�������Ĺ������, �Լ�ͨ��������������Ӧ�����е��ܽ����Ʊ��õ���TiO2�������Ĺ�����ԡ� �������: 0.5%Sn4+�� 0.5%La3+�� 0.5%Y3+��0.5%Eu3+(��������)���ӵ�TiO2�������ڽ��������Һ�ķ�Ӧ��, �����������2%~7%; �����IJ�����ʹTiO2�������Ĺ�����Խ���0.5%~25%; ��TiO2���������Ʊ�������, ���ܽ����г������տ�ʹ�����������15%����, �������TiO2������������Ե�һ����;����
�ؼ���: TiO2������; �ܽ�-������; ���ɽ���; ϡ��Ԫ��; ����; ��������; ������� ��ͼ�����: O643; TF123
���ױ�ʶ��: A
Sol-gel preparation and photocatalytic activities of TiO2 nanoparticles
QIAN Dong1, 2, 3, YAN Zao-xue1, SHI Mao1,
CHEN Qi-yuan1, LU Zhou-guang1, HUANG Ke-long1, LIU Yong2
(1. School of Chemistry and Chemical Engineering, Central South University,Changsha 410083, China;
2. State Key Laboratory of Powder Metallurgy, Central South University,Changsha 410083, China;
3. Sinopec Changling Catalyst Division, Yueyang 414012, China)
Abstract: The photocatalytic activities of TiO2 nanoparticles doped with transition metal ions (Fe3+, Zn2+, Co2+, Ni2+, Cr3+ and Sn4+) and rare-earth metal ions (La3+, Pr3+, Nd3+, Ce4+, Sm3+, Eu3+, Gd3+, Y3+ and Dy3+) by sol-gel method and the TiO2 nanoparticles obtained from the sol with ultrasonic irradiation during their sol-gel synthesis were investigated. The results show that the photocatalytic activities of TiO2 nanoparticles doped with 0.5%Sn4+, 0.5%La3+, 0.5%Y3+ and 0.5%Eu3+ (mass fraction) increase 2%-7%, while photocatalytic activities doped by others decreases 0.5%-25% in the photocatalytic degradation of methylorange. The ultrasonic irradiation of the sol produced in the sol-gel synthesis of TiO2 nanoparticles can enhance their photocatalytic activity above 15%, which is a novel way to improve the photocatalytic activities of TiO2 nanoparticles.
Key words: TiO2 nanoparticles; sol-gel; transition metal; rare-earth metal; doping; ultrasonic irradiation; photocatalytic activity
��������װ뵼����ϵ�һ����Ҫ���ܡ� ���ڶ����װ뵼��������, TiO2���������Ըߡ� ���� �ȶ��Ժá� ��������ǿ�� �ɱ��͵��ص��Ϊ��ǰ�����Ӧ��DZ���İ뵼������, �������ڻ�������������չ�ֳ�������Ӧ��ǰ��, ��Ϊ��ǰ�������о����ص���ȵ㡣
TiO2���������Ʊ�������Ҫ�����ܽ���[1]�� ��ѧ���������[2]�� ȼ�շ�[3]�� ������[4]�� ˮ�ⷨ[5]�� ˮ�ȷ�[6]�� �ܽ�-������[7]������ĥ��[8]�� ��������TiO2�ܽ�-�����������Ʊ������ء� ���������� ��Ʒ���ȸߡ� ��ѧ�����Ժá� ����ϸ�� �ս��¶ȵ͵��ŵ�, �ѳ�Ϊ�Ʊ���������������õķ���[9]��
��θ������װ뵼��Ĺ������, �ǰ뵼�����о��������������֮һ�� Ŀǰͨ�����ù��ɽ�����ϡ��Ԫ�ز����Լ��ڰ뵼������������������������������ȷ����� Ȼ��һЩ�����Ľ��ȴ��һ��, ����ͬԪ�صĸ�����ʱ�ó��෴�Ľ��ۡ�
�������߿�����ͨ���ܽ�-���������й��ɽ�����ϡ��Ԫ�ز��ӵ�TiO2�������Ĺ������, �Լ�ͨ��������������Ӧ�����е��ܽ����Ʊ���TiO2�������Ĺ�����ԡ�
1 ʵ��
1.1 ��Ҫ�Լ�������
�Լ�: ���ᶡ��(C4H9O)4Ti(CP)�� ��ˮ�Ҵ�(AR)�� ����(AR)�� ���Ҵ���(AR)�� ������(AR)�� ������(AR)�� �Ȼ�����(CP)�� ����п(AR)�� ������(CP)�� ������(CP)�� ������La2O3(AR)�� ������Nd2O3(AR)�� ������Pr6O11(AR)�� ������(CP)�� ������Gd2O3(����99.9%)�� ������Y2O3(����99.99%)�� �����Tb4O7(����99.9%)�� ������(����99.9%)�� ������Sm2O3(����99.9%)�� ������Eu2O3(����99.9%)�ȡ�
����: BRANSON 8500������(Branson)�� ���ƹ����Ӧ��(��200mm, �⾶70mm, �ھ�35mm���п�Բ����)�� 8W���������ߵƹܡ� UV-1601P����-�ɼ���ֹ��ȼ�(SHIMACZU)�� SIZMENS D-500 X����������(SIZMENS)�� HITACHI H-800��羵(HITACHI)�� LD4-2���Ļ��� ���͵���¯�� POWER-2000��ҵ�����ܿ�����(���Ϲ�ҵ��ѧ��)�ȡ�
1.2 �ܽ�-�������Ʊ�TiO2������
�����½�10mL���ᶡ����������60mL��ˮ�Ҵ���, ��Ͼ��ȵ���Һ(1); �ٽ�30mL ��ˮ�Ҵ���1mL�����ھ��ҽ������������10mL��������ˮ��ֻ�ϵ���Һ(2)�� ����Һ(2)�ھ��ҽ����»���������Һ(1)��, Լ15min����, Ȼ���������15min, ����Ӧ��������ƿת��һ�ྻ�ձ���, ����15h, ����70���º����߸���10h����б��ա� ���վ������: ��������3��/min������250�� , ����1h��, ������5��/min���µ�450��, ������5.5h��ȡ���� ���պ�Ĺ��徭��ĥ����TiO2���塣
ͼ1��ͼ2��ʾ�ֱ�ΪTiO2��ĩ��X����������TEMͼ�� ����Ʒ��X����������(��ͼ1) ����, ���Ƶõķ���Ϊ������TiO2������ ��ͼ2�ɼ�, ���Ƶõ�TiO2������������Ϊ12~40nm, ƽ������ԼΪ25nm, ��ͨ��Scherrer��ʽ����TiO2��������X������������õ���ƽ������ԼΪ21nm, ��ͼ2�ǺϵñȽϺá�
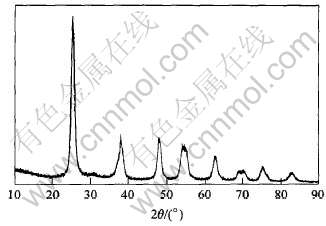
ͼ1 TiO2��������X����������
Fig.1 XRD pattern of TiO2 nanoparticles

ͼ2 TiO2��������TEMͼ
Fig.2 TEM image of TiO2 nanoparticles
1.3 �ܽ�-�������Ʊ�����TiO2������
�����½�10mL���ᶡ����������60mL��ˮ�Ҵ���, ��Ͼ��ȵ���Һ(1); �ٽ�һ��������Ԫ�� (����Ԫ�صĺ���Ϊ0.5%) ����1mL���ᡢ 30mL��ˮ�Ҵ���10mL��������ˮ�Ļ��Һ(2)�� (��һЩ�����ܽ�IJ���Ԫ��, �ʵ�����������������������ˮ)�� ����Һ(2)�ھ��ҽ����»���������Һ(1)��, Լ15min����, ��������15min, Ȼ��Ӧ��ת��һ�ྻ�ձ���, ���ó»�4d������70���º����߸���10h, �ٽ�������450����������¯������10h, ����ĥ����TiO2���ӷ��塣
1.4 ��Ʒ������ԵIJⶨ
������һ�ֽ��ѽ������ɫ������, ��ˮ��Һ��pHֵ��ͬ, ���ж���ż������ʽ�ṹȾ�ϻ����������ṹ�� ���, ������ΪȾ�Ϲ������ģ�ͻ��������һ���Ĵ�����[10, 11]�� ��Ʒ������ԵIJⶨ����: ��ȡ0.05g��TiO2����ӷ������װ��Ũ��Ϊ 20mg/L��50mL����ˮ��Һ��, ��������ɢ��, ��������ʯӢ�����Ӧ������(�����Ӧ��ԴΪ8W���������ߵƹ�), �����Ӧ20min��, ���ķ���, ȡ�ϲ���ҹ, ͨ������-�ɼ��ֹ��ȼƷ����ⶨ��465nm������ȵ�ֵ��
������ҺŨ��Ϊ0~45mg/L, ������ȳ����õ����Թ�ϵ[10, 11], ���, ������������ֵ�ı仯��������ͬTiO2���������Ի��ԡ�
2 ���������
2.1 �����������ļ�����������ʱ���Ӱ��
ͨ����Ϊ[7, 12], ���ܽ�-�������Ʊ�����TiO2������, ���ᶡ����ˮ���ȷ���ˮ�ⷴӦ:
![]()
Ti(C4H9O)4-n(OH)nһ�γ�, ���žͷ������۷�Ӧ:
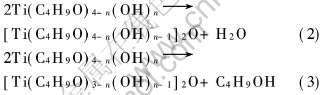
��ˮ������۵���ʼ�οɵõ��ܽ�, ��һ�����۾Ϳɵõ�����, �پ����Ȼ�����������ȥ�ܼ���ɵõ�����TiO2������
�����ɵ�[13]�Ƚ�ϵͳ�ض��ܽ�-�������Ʊ�����TiO2�����в�ͬ�ļ�ˮ��ʽ�� ��ˮ���� pHֵ�� �Ҵ����� ˮ���¶ȶԽ���ʱ���Ӱ��������о�, ���Ա����������ļ�����ȴû�н��о�����о�, ���о��Դ˽����˽�һ�����о���
��ʵ����, �������������ļ���������1��, ����ʵ���������������� ʵ���н���ʱ��ļ����Ǵ���Һ(2)����Һ(1)�Ӵ���ʼ, ���õ��Ľ�����бʱʧȥ������Ϊֹ�� �����������ļ�������TiO2�������Ʊ������н���ʱ���Ӱ�����1���С�
��1 �ܽ�-�������Ʊ�TiO2��������ԭ�ϵ����Խ���ʱ���Ӱ��
Table 1 Influence of volume for different initial materials on gel time during ol-gel synthesis of TiO2 nanoparticles
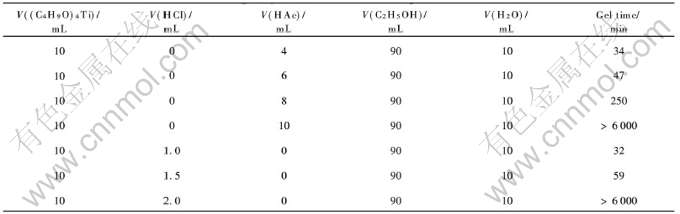
���ܽ�-�������Ʊ�TiO2�Ĺ�����, �������������������, ���ᶡ����ˮ������ˮ�����۷�Ӧ˲�����, ���ɳ����� �ӱ�1�ɿ���, �����������ļ���, ���������ᶡ��ˮ�����۷�Ӧ�Ľ���, �����������������, ����ʱ���Խ��, �����Ӱ��Ч���ȱ�����Ҫ����, ���, �ñ��������������ᶡ����ˮ������۷�ӦҪ����Щ�� �½���[14]ͨ��ʵ�鷢��, ����������Ƶ�TiO2�������Ĺ�����Աȼ��������Ҫ�ߡ�
2.2 ϡ�����Ӷ�TiO2������������Ե�Ӱ��
�����������Ʊ��˺���Ϊ0.5%(��������)��ϡ��Ԫ��La3+�� Pr3+�� Nd3+�� Ce4+�� Sm3+�� Tb3+�� Eu3+�� Gd3+�� Y3+��Dy3+���ӵ�TiO2������, �������������Һ�ķ�Ӧ�������2���С�
��2 ϡ������TiO2�������Ĺ������
Table 2 Photocatalytic activities of TiO2
nanoparticles doped with rare earth ions

�ӱ�2�ɿ���, �ڱ��о���, ϡ�����Ӳ����ܴ�������TiO2������������������Һ�Ĺ�����ԡ� ����La3+�� Y3+��Eu3+��ʹTiO2�������Ĺ���������5%~7%, ������ʹTiO2�������Ĺ�����Խ���0.5%~7%�� ����ϡ�����Ӷ�TiO2������������Ե�Ӱ�����, �����о���[14-16]����Ϊ����ϡ��Ԫ�ؿ����ƻ�ٽ�TiO2�������͵����ʯ�͵����, �����ƻ�ٽ�TiO2������������, �Ӷ�Ӱ���������ԡ�
2.3 ���ɽ������Ӷ�TiO2������������Ե�Ӱ��
�����������Ʊ��˺���Ϊ0.5%(��������)�Ĺ��ɽ�������Fe3+�� Zn2+�� Co2+�� Ni2+�� Cr3+��Sn4+���ӵ�TiO2������, �������������Һ�ķ�Ӧ������3���С�
��3 ���ɽ�������TiO2�������Ĺ������
Table 3 Photocatalytic activities of TiO2
nanoparticles doped with transition metal ions

�ӱ�3�ɿ���, �ڱ��о���, ��Sn4+���ӵ�TiO2������������������Һ�Ĺ�����������2.6%��, Fe3+�� Zn2+�� Co2+�� Ni2+��Cr3+�IJ�����ʹ�������Խ�����12%~25%�� ��һ�����½���[14]��ʵ����������ͬ�� �½�����Ϊ: Sn4+���������TiO2�������Ĺ������������Sn4+����������TiO2��ϸ��, ���ڽϵ��¶��¿��ӳٻ��谭TiO2�������͵����ʯ�͵����, ͬʱ��Sn4+���ӵ�TiO2�����������ǻ��ܶ�����, ����λ����, �ڹⷴӦ�����������˷�Ӧ���ġ�
����[14-16]�������Ĺ��ɽ�����ϡ��Ԫ�ز��Ӷ�TiO2������������Ե�Ӱ����ɲ�һ��, �Ҷ���Ӱ�����������Ҳ�Ƚϴ� �����������TiO2��������û����������൱����, �漰��ܹ�, ���ɽ�����ϡ��Ԫ�ز��Ӷ�TiO2������������Ե�Ӱ������Ҳ�ܶ�, ����TiO2���������Ʊ������� ��ѡ������۹�����ܵ�ģ�ͷ�Ӧ�����IJ�ͬ, �ó��Ľ���������һ��, �ⷽ�滹��Ҫ���д���������Ļ����о�, ��̽��TiO2��������û����� ���ɽ�����ϡ��Ԫ�ز��ӵ�Ӱ����ɡ� �л���ṹ��TiO2������ԵĹ�ϵ�ȡ�
2.4 �����������Ʊ��õ���TiO2�������Ĺ������
��TiO2���������Ʊ�������, ����Һ(2)������Һ(1)�õ����ܽ�����ͬʱ��ij��������Ʊ�TiO2������, �����������4���С�
��4 �����������Ʊ��õ�TiO2�������Ĺ������
Table 4 Photocatalytic activities of TiO2
nanoparticles prepared by ultrasonic irradiation

�ӱ�4�ɿ���, ��TiO2���������Ʊ�������, ���ܽ����г������տ���Ч�������������, ����Yu��[17]��ʵ����һ�¡� ����������ڳ��������ܴٽ����л����ε�ˮ���TiO2�������õĿ������� �ӱ�4���ɿ���, ���ܽ���������40min����, ���Ʊ��õ����������Ĺ���������, �����ŷ���ʱ����ӳ�, ���Ʊ��õ����������Ĺ�����Է������½����ơ� ������������ڳ������յij�ʼ��, ��ջ����ü���ؼ����м����ˮ��;ۺ�, �����γɴ����ľ��˶��õ���С�Ŀ����� �����Ž�һ���ij�������, ���ڿջ����ò����ľֲ���ʹ��������, �Ӷ�ʹ���Ʊ��õ��������Ĺ�����������½���
3 ����
1) ���ܽ�-�������Ʊ�TiO2������, �����������ļ���, ���������ᶡ��ˮ�����۷�Ӧ�Ľ��̡� �����������������, ����ʱ��Ҳ��֮�ӳ�, �������Ӱ��Ч���ȱ������������
2) ϡ�����ɽ������Ӳ��Ӳ����ܴ�������TiO2������������������Һ�Ĺ�����ԡ� ��Sn4+�� La3+�� Y3+��Eu3+���ӵ�TiO2�������Ĺ���������������, �����ľ���ͬ�̶ȵ�ʹTiO2�������Ĺ�������������͡�
3) ��TiO2���������Ʊ�������, ���ܽ����г������տ���Ч�������������, �������TiO2������������Ե�һ����;����
REFERENCES
[1]ʩ����, ���, �°�ƽ, ��. �������ܽ���Ӧ�����Ʊ�����TiO2��������̬�ͽṹ[J]. ����������ѧѧ��, 1999, 25(2): 151-155.
SHI Li-yi, LI Chun-zhong, CHEN Ai-ping, et al. Morphology and structure of nanosized TiO2 particles synthesized in high temperature aerosol reactor[J]. J East Chinese Univ Sci Technol, 1999, 25(2): 151-155.
[2]���Ի�, �°�ƽ, ���, ��. ��ѧ����ϳ�TiO2�����е�����������[J]. ����������ѧѧ��, 1999, 25(4): 382-385.
ZHU Yi-hua, CHEN Ai-ping, LI Chun-zhong, et al. Mechanism of powder deposition on cool wall during the process of chemical synthesis of TiO2 in vapor phase[J]. J East Chinese Univ Sci Technol, 1999, 25(4): 382-385.
[3]������, ���㾲, ����, ��. ����TiO2��ȼ�պϳɼ���������[J]. �й���ɫ����ѧ��, 2004, 14(5): 831-835.
YU Yong-li, ZHAI Xiu-jing, FU Yan, et al. Combustion synthesis of nanosized titania and its photocatalytic activity[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(5): 831-835.
[4]�Ծ���, ���ӳ�, ����, ��. Һ��һ���ϳɽ��ʯ�ͳ�ϸTiO2[J]. �ߵ�ѧУ��ѧѧ��, 1999, 20(3): 467-469.
ZHAO Jing-zhe, WANG Zi-chen, LIU Yan-hua, et al. Preparation of ultrafine rutile titania crystals by liquid method[J]. Chem J Chinese Univ, 1999, 20(3): 467-469.
[5]�ֽ���, �ƿ���, ˾ʿ��, ��. ����ɢ����TiO2�������ˮ���ܽ��Ʊ���[J]. �й���ɫ����ѧ��, 2003, 13(3): 788-792.
YAN Jian-hui, HUANG Ke-long, SI Shi-hui, et al. Preparation of photocatalytic activity nanosized TiO2 by hydrolysis-sol method[J]. The Chinese Journal of Nonferrous Metals, 2003, 13(3): 788-792.
[6]����. ���ʯ��TiO2���۵�ˮ�Ⱥϳ�[J]. ���ս�����ҵѧԺѧ��, 1997, 5(3): 54-56.
LI Yan. Hydrothermal preparation of rutile-type TiO2 nanopowder[J]. J Anhui Inst Architect, 1997, 5(3): 54-56.
[7]Haro P E, Rodigue T. Crystallization of nanosized titania particles prepared by the sol-gel process[J]. J Mater Res, 1994, 9(8): 2102-2108.
[8]Qian D, Gerward L, Jiang J Z. Deformation-induced reactions in ZnO and TiO2[J]. J Mater Sci, 2004, 39(16-17): 5389-5392.
[9]Qian D, Jiang J Z, Hansen P L. Preparation of ZnO nanocrystals via ultrasonic irradiation[J]. Chem Commun, 2003(9): 1078-1079.
[10]������, ����, ������. ������Һ����������[J]. ������ѧ, 1998, 19(1): 1-4.
WANG Yi-zhong, FU Yuan, TANG Hong-xiao. Photocatalytic degradation of methyl orange in TiO2 suspension[J]. Environ Sci, 1998, 19(1): 1-4.
[11]��ΰ��, �ط�, ���Ŀ�, ��. TiO2��������Ʊ����������[J]. �人��ѧѧ��, 1999, 45(4): 389-392.
SHEN Wei-ren, HE Fei, ZHAO Wen-kuan, et al. Preparation and photocatalytic activities of nanocrystal titania[J]. J Wuhan Univ, 1999, 45(4): 389-392.
[12]Ding X Z. Effect of hydrolysis water on the preparation of nano-crystalline titania powders via a sol-gel process[J]. J Mater Sci Lett, 1995, 14(1): 21-22.
[13]������, ���緢, ���¹�, ��. �ܽ�-�������Ʊ�����TiO2�Ľ������̻����о�[J]. ���ܲ���, 1999, 30(4): 407-409.
YIN Li-song, ZHOU Qi-fa, TANG Xin-gui, et al. The mechanism of nanocrystalline TiO2 derived by sol-gel process[J]. Funct Mater, 1999, 30(4): 407-409.
[14]�½���. ����TiO2��������Ʊ��� ���Լ���Ӧ���о�[D]. ��ɳ: ���ϴ�ѧ, 2001.
CHEN Jian-jun. Studies on the preparation, modification and applications of nanosized TiO2 photocatalyst[D]. Changsha: Central South University, 2001.
[15]���ֺ�, ˮ��, ������, ��. ϡ�����Ӷ������ѵ����������[J]. �㽭��ѧѧ��, 2000, 27(1): 69-74.
YUE Ling-hai, SHUI Miao, XU Zhu-de, et al. The A-R transformation and photocatalytic activities of mixed TiO2 rare earth oxides[J]. J Zhejiang Univ, 2000, 27(1): 69-74.
[16]������, ����, �̻���, ��. ���ӹ��ɽ������ӵ�TiO2�����������ӹ����-����B�Ĺ������[J]. �ߵ�ѧУ��ѧѧ��, 2000, 21(6): 958-960.
WANG Yan-qin, ZHANG Li, CHENG Hu-min, et al. The photocatalytic properties of transition metal ion-doped TiO2 nanoparticles-photocatalytic degradation of rhodamine B[J]. Chem J Chinese Univ, 2000, 21(6): 958-960.
[17]Yu J C, Yu J, Ho W, et al. Preparation of highly photocatalytic active nano-sized TiO2 particles via ultrasonic irradiation[J]. Chem Commun, 2001, 19: 1942-1943.
������Ŀ: ���Ҹ����о���չ�ƻ�������Ŀ(2001AA2180041); ���ϴ�ѧ��ĩұ������ص�ʵ���ҿ��ſ���
�ո�����: 2004-10-25; ������: 2005-03-04
�����: Ǯ ��(1967-), ��, ������, ��ʿ.
ͨѶ����: Ǯ ��; �绰: 0731-8830886; ����: 0731-8879616; E-mail: qiandong6@vip.sina.com
[2]���Ի�, �°�ƽ, ���, ��. ��ѧ����ϳ�TiO2�����е�����������[J]. ����������ѧѧ��, 1999, 25(4): 382-385.
[3]������, ���㾲, ����, ��. ����TiO2��ȼ�պϳɼ���������[J]. �й���ɫ����ѧ��, 2004, 14(5): 831-835.
[4]�Ծ���, ���ӳ�, ����, ��. Һ��һ���ϳɽ��ʯ�ͳ�ϸTiO2[J]. �ߵ�ѧУ��ѧѧ��, 1999, 20(3): 467-469.
[5]�ֽ���, �ƿ���, ˾ʿ��, ��. ����ɢ����TiO2�������ˮ���ܽ��Ʊ���[J]. �й���ɫ����ѧ��, 2003, 13(3): 788-792.
[6]����. ���ʯ��TiO2���۵�ˮ�Ⱥϳ�[J]. ���ս�����ҵѧԺѧ��, 1997, 5(3): 54-56.
[10]������, ����, ������. ������Һ����������[J]. ������ѧ, 1998, 19(1): 1-4.
[11]��ΰ��, �ط�, ���Ŀ�, ��. TiO2��������Ʊ����������[J]. �人��ѧѧ��, 1999, 45(4): 389-392.
[13]������, ���緢, ���¹�, ��. �ܽ�-�������Ʊ�����TiO2�Ľ������̻����о�[J]. ���ܲ���, 1999, 30(4): 407-409.
[14]�½���. ����TiO2��������Ʊ��� ���Լ���Ӧ���о�[D]. ��ɳ: ���ϴ�ѧ, 2001.
[15]���ֺ�, ˮ��, ������, ��. ϡ�����Ӷ������ѵ����������[J]. �㽭��ѧѧ��, 2000, 27(1): 69-74.


