���±�ţ�1004-0609(2015)-01-0203-08
�������պ��ڸ�����������
������1, 2��������1���� ƽ2��֣ʫ��2������3����С��1���� ܲ2
(1. ������ɫ�����о���Ժ ϡ�н���ұ��������о��������� 100008��
2. �й���ѧԺ ���̹����о��� ʪ��ұ����������������ҹ���ʵ���ң�����100190��
3. ������ɷ�����˾������ 473003)
ժ Ҫ��
��Ը������������պ��ڸ�ת�����ʽ������⣬�Ը������չ��̸�ת����70%�ĸ���Ϊԭ�ϣ���������������ͻ�ѧ�ɷ֣������о��������չ������¶ȡ�ʱ�䡢Na2CO3��CaCO3 �ȶԸ����и�ת���ʵ�Ӱ�죬̽����߸������������պ��ڸ�ת���ʵĻ����������������������ΪMgCr0.4Fe1.6O4�⾧ʯ������ΪNaSiAlO4��Mg1.5Na9Si12Al12O48���ƹ����Ρ����������ࣻ����Na2CO3�����������շ�Ӧ�����и�ת���ʽ�Ϊ50%~60%���ƹ����Ρ��������ε���Ĵ��ڵ���Na+�������ʽ��ͣ���ɸ����еĸ�ת�����ѣ�Ca�������û��˸����и����Na����ת������ߵ�84.7%�������˸��۵��Ca2Fe1.2Mg0.4Si0.4O5������ε��࣬�����˱��չ�����Na+Ũ�ȣ��ٽ��˸���ת��������˱��պ��ڸ���ת���ʡ�
�ؼ��ʣ�
�������������û���Na+Ũ������������
��ͼ����ţ�TQ136.1���� ���ױ�־�룺A
Re-oxidation mechanism of chromite roasting in late stages
CHEN Yong-an1, 2, WANG Wu-yu1, LI Ping2, ZHENG Shi-li2, ZHANG Xiang-dong3, CHE Xiao-kui1, ZHANG Yi2
(1. Division of Rare Metal Materials and Metallurgy, General Research Institute for Non-Ferrous Metals, Beijing 100008, China;
2. National Engineering Laboratory for Hydrometallurgical Cleaner Production Technology,
Institute of Process Engineering, Chinese Academy of Sciences, Beijing 100190, China;
3. Lida Photoelectric Co., Ltd., Nanyang 473003, China)
Abstract: Based on the conversion rate of trivalent chromium at the late stages of the chromite lime-free roasting, Na2CO3 roasting of the chromium residues obtained by roasting the chromite ore with Na2CO3 with the conversion rate of 70% was used as raw materials. The phases and chemical composition of chromium residues were analyzed firstly, the effects of roasting process conditions such as roasting time, roasting temperature and the amount of Na2CO3 and CaCO3 addition, on the Cr conversion rate were further investigated. The mechanism of reoxidation of trivalent chromium at the late stages of roasting process was studied. The results show that the main phase of the chromium residues is MgCr0.4Fe1.6O4 spinel, and some sodium silicate and silicon aluminate phases, such as NaSiAlO4 and Mg1.5Na9Si12Al12O48 also exist in the chromium residues. During the roasting process of chromium residues reacting with Na2CO3, the conversion rate of trivalent chromium of chromium residues is only 50%-60%, due to low utilization of Na+ that resulted from the formation of sodium silicate and sodium silicon aluminate phases. The conversion rate of trivalent chromium increases to 84.7% when the CaCO3 is added into the roasting process of chromium residues, the sodium silicate and silicon aluminate reacts with Ca to generate high melting point calcium silicate salt phases, such as Ca2Fe1.2Mg0.4Si0.4O5. Therefore, the concentration of Na+ is improved and the chromium transformation is promoted, and the conversion rate of trivalent chromium increases at the late stages of roasting process.
Key words: chromium residue; roasting; replacement; Na+ concentration; re-oxidation
����������Ϊ�ҹ��ص㷢չ��������ԭ�ϣ��ڵ�ơ����ӡȾ��ҽҩ�����ϡ���������������������ʴ���ȷ������Ź㷺����;[1]������������������������ҪΪ�Ʊ��շ�[2-3]��Һ��������[4-5]��Һ���������Dz��÷dz�����ʺ�������Һ���з���������Ӧ���÷�����ת���ʸߣ������ڲ�Ʒ��һ���dz��������Ҫ�������õ����⣬Ŀǰ���ģ��ҵ������ؽ��������Ʊ��շ��Dz��ø�������Na2CO3ֱ�ӱ��գ�ÿ�ֲ�Ʒ(��Na2Cr2O7��)����0.6~0.8 t������������С�������ȷ�չ�ĸ������������������[6-8]��Ȼ�����������Ʊ��շ�Ӧ���ڸ�ת�����ѣ���ת���ʽ�Ϊ70%~80%[9]�����պ����и��ĺ����ߣ����¸���Դ�����ʵͺ�DZ�ڵĶ�����Ⱦ����[10]��������ѧ�߶Ը������Ʊ��յķ�Ӧ������������Ӧ���ڸ�ת�����ѵ�ԭ��չ�˴������о���SASTRI��[11]��GARBERS��[12]�����ȷ����ֶ��о���Cr2O3- Na2CO3-O2��ϵ�еĸ��������ɣ���Ϊ��Cr2O3���������п��γ�CrO3��CrO4x-(x=2, 3, 4)�Ȳ�ͬ��̬�ĸ��м仯��������м仯�����ڽϸ��¶��·ֽ⣬����Cr2O3�ڸ�������������ȫ��BROWN��[13]��Ϊ����SiO2����ʱ��SiO2�Ⱥ�Na2CO3����Na2O��SiO2��Na2O��SiO2��һ����Cr2O3��Ӧ����Na2CrO4�����¶ȴ���900 ��ʱ��SiO2��ʹ���ֵ�Na2CrO4ת��ΪCr2O3��Na2O��SiO2����ɸ���������ȫ��������[14]�о��˸������Ʊ��ն���ѧ�����ָ�ת������80%~90%����ת�ۣ���Ϊ��Ӧ�����в����γɵ�Һ��Ĥ�����˶�������ɢ���������Ӷ���ɸ��������ѡ���С���[3]�о��˸������ն���ѧ����Ϊ���������շ�Ӧ���ڣ�NaFeO2����Na2CO3����⾧ʯ����������Ӧ���˷�Ӧ��������Ҫ�ϸߵ��¶Ȳ���ʹ����ȫ��������������[15]�о���Fe��Al���ʶԸ������ʵ�Ӱ�죬��Ϊ�ڷ�Ӧ���ڣ�NaFeO2��ȫ���Դ���Na2CO3�����������Ӧ��
�����������������չ���Ӱ�����ض࣬������ǿ�����й����Ը������շ�Ӧ�����������DZ��պ��ڸ�������������ʶ��������������о��������պ��ڸ�������������߸���Դ�����ʡ���������ɵĻ�����Ⱦ������Ҫ���塣���������Ը������չ���ת����Ϊ70%���õ��ĸ���Ϊԭ�ϣ�����������������ѧ���ԣ������о��¶ȡ�ʱ�䡢���������������ȶԸ����и�ת���ʵ�Ӱ�죬̽����������������
1 ʵ��
�ϷǸ������Na2CO3���գ�����ת����70%�����ղ��ᆳϴ�ӡ�������ڸ�������ĥ����ĥϸ��ѡ��ͨ����Ϊ74 ��m����ɸ�ĸ�����Ϊ��һ���о���ԭ�ϡ�
Ϊ����ʱ����¶ȶԸ�ת���ʵ�Ӱ�죬ÿ��ȡ����50 g���̶�������������Na2CO3���ڻ���Ͳ�л���10 min����б��ա�������ɺѸ��������Ͻ�����ĥ��ˮ�������ˣ���ȥ����Na2CrO4��NaAlO2�ȵ���Һ������Cr6+����������������ռ������ܸ������������ࡣ�ٷֱ�����ʵ�鲽�裬�̶��¶Ⱥ�ʱ��������Na2CO3�Ը�ת���ʵ�Ӱ�죻�̶��¶ȡ�ʱ�估Na2CO3������������CaCO3�Ը�ת���ʵ�Ӱ�졣
����������������������������������е����۸����ܸ�������������������ʡ�����AXIOS��Xӫ�������(XRF)���Ը����ɷ֡�Ϊ���⺬����������ӫ��ЧӦ�ĸ��źͱ�֤���Ծ������ú������ɿ�XPert Pro MPD��XRD(CoK��)��ɨ���ٶ�0.01 (��)/s�����Ծ��Ȧ���=0.0004�㣬�������������ϼ�ˮϴ���������ࡣ����FEI MLA250��SEM/EDS�ڸ����ģʽ�·���ˮϴ����������ò�����ס�
2 ��������
2.1 ��������������
����������Ҫ����Ϊ������þ�⾧ʯ��([Fe,Mg][Cr,Fe]2O4)����Ҫ����Fe��Cr��Mg��Al��Si��O��Ԫ�أ�ʵ���и������Na2CO3�ڿ����б��գ���ת����Ϊ70%ʱ�õ��ĸ���������������Ļ�ѧ�ɷ����1���С�
��1 �ϷǸ���������Ļ�ѧ�ɷַ���
Table 1 Elemental composition of South Africa chromite and chromite residue obtained by XRF analysis
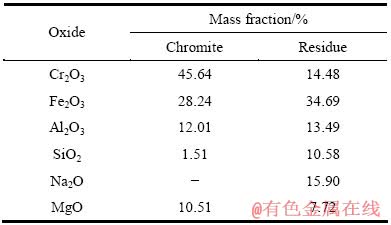
�ɱ�1��֪����������Na2CO3�������գ��������ɸ������е�45.64%���������е�14.48%����������28.24%������34.69%��Na��Si�����л� �ۣ��������ƺ���ռ�������Ľ�16%���ɴ˿ɼ����������գ�����Ӧʹ����Na�Բ���ˮ�����������У����ø���Ϊ������(Cr��Fe��Na�ĺ��������������)������������ͼ����ͼ1��ʾ��ͼ1�У�������Ҫ���ɸ���þ�⾧ʯ������Ρ������εȸ��Ӹ�����ɵģ����У��⾧ʯ��ΪMgCr0.4Fe1.6O4������ΪMg1.5Na9Si12Al12O48��NaSiAlO4��[9]��
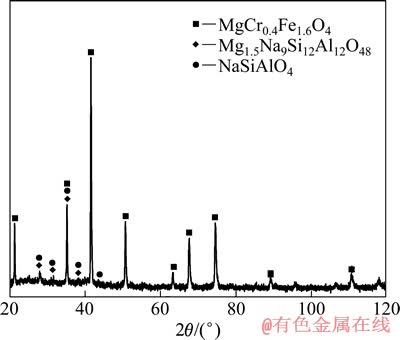
ͼ1 ������Na2CO3�����������ø�����XRD��
Fig. 1 XRD pattern of chromium residue obtained by roasting chromite with Na2CO3
Ϊ��һ��ȷ�������е���ͳɷ֣��Ը����������б�ɢ��ɨ��羵������(SEM/EDS)������ͼ2��ʾΪ��������͵���������ò����ͼ2��֪�����������������ս��壬��ò������������治����(��ͼ2(a))��ͼ2(b)��ʾΪ�����������Ķ���ͼ��ͼ����ʾ��������������ɫ��Ͱ���ɫ����ɣ�������������������ݿ����лҶ�ֵ�IJ�ͬ���Ը����������д����Ե�A��B��C������EDS�������������2���С��������ʾ��A��Mg��Cr��Fe ��Ħ����Ϊ1:0.4:1.60��C��Mg��Na��Al��Si��Ħ����Ϊ2.2:9.4:12.84:12.29������ƥ����XRD�Ը������м⾧ʯMgCr0.4Fe1.6O4��������Mg1.5Na9Al12Si12O48�ķ�����B��Ϊ���������ڲ���ߴ����Ե�����λ����ɫ��Ͱ���ɫ��Ľ�ϲ�λ���ɷָ��ӣ����ڼ⾧ʯ�����λ������εĻ������Ͽ�֪���������о�Na2CO3�������գ�������Fe��Cr������Mg��Al�γ�MgCr0.4Fe1.6O4�⾧ʯ�࣬Na��Si������Al��Mg���γ�Mg1.5Na9Al12Si12O48��NaAlSiO4�������ࡣ
��2 ���������ɷַ���
Table 2 Composition analysis of chromium residue
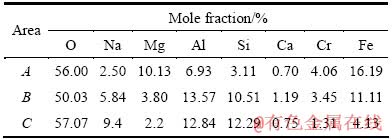

ͼ2 ������Na2CO3�����������ø�������ò
Fig. 2 SEM images of chromium residue obtained by roasting chromite with Na2CO3
2.2 ���������е�Ӱ������
2.2.1 �����¶ȵ�Ӱ��
�¶��DZ��չ��̵���Ҫ���أ�Ϊ������Ը����и�ת���ʵ�Ӱ�죬������Na2CO3������������ʱ��30 min�������¶Ը������б��գ�������ͼ3(a)��ʾ����ͼ3(a)��֪�����ű����¶ȵ����ߣ���ת���ʲ������ߣ��������¶ȳ���1150 ��ʱ����ת���ʼ������䣬��߸�ת���ʽ�Ϊ52.68%���ڽϵ͵ı����¶��£�Na2CO3�ֽ⡢Na+��ɢ����MgCr0.4Fe1.6O4�⾧ʯ�ķ�Ӧ�̶ȶ���Խϵͣ��Ӷ�Ӱ���ת���ʡ��ڸ����£���ת������ߣ����������¶ȣ�����Na��Si��Al��Ԫ�������ɲ�����ˮ�Ķ�Ԫ���ƹ����Ρ��������࣬��Ч��Na+Ũ�Ƚ��ͣ����¸����и�ת�������߲����ԡ�
2.2.2 ����ʱ���Ӱ��
ѡ�����¶�1150 �棬������Na2CO3�������¿��첻ͬ����ʱ��Ը����и�ת���ʵ�Ӱ�죬������ͼ3(b)��ʾ����ͼ3(b)���Կ�����20 min�ڸ�ת���ʼ������ߣ�����������ƷŻ���40 min��ת���ʻ������ֺ㶨����ת�������Ϊ56.05%���ڷ�Ӧ��ʼ�Σ�Na+Ũ�Ƚϸߣ����������е�CrѸ��ת�������ŷ�Ӧ�Ľ��У�Na+��⾧ʯ��MgFe1.6Cr0.4O4��Ӧ����Na2CrO4��ͬʱ��Ҳ�����˺��ƹ����Ρ������εȸ��࣬��������Na2CrO4��Na+���٣���������ɻ��δ��Ӧ�ĸ����⾧ʯ�ṹ�γɰ������谭���뷴Ӧ�ĸ������ڼ⾧ʯ�ṹ�е���ɢ����ˣ�һ����Ӧʱ��͵� Na+Ũ�Ⱥ���ɢЧӦ��ͬ���õ����˸�ת���ʵ����߷Ż���
2.2.3 Na��������Ӱ��
�ڱ����¶�1150 �棬����ʱ��20 min�������£�����Na������(�����)�Ը�ת���ʵ�Ӱ�죬�����ͼ3(c)��ʾ����ͼ3(c)���Կ�����Na2CO3����������������0.8�����ӵ�1.1���������и�ת���ʱ仯�����ԣ�������ڸ�����Ӧ���ڸ��ӵĸ�������ṹʹ��ҵ���й��������õ���������ԶԸ�ת���ʲ������Ե�Ӱ�죬������Ԫ˫��[16]�о����շ�������Ը�ת����Ӱ��ó��Ľ���һ�¡�
2.2.4 ����������Ӱ��
ѡ�����¶�1150 �棬����ʱ��20 min��������Na2CO3�������������¿�����������Ը����и�ת���ʵ�Ӱ�죬������ͼ3(d)��ʾ����ͼ3(d)��֪���ڲ�����CaCO3�������£���ת����ֻ��50%���ң�����Ca�ļ��룬��ת���ʲ������ߣ���CaCO3������������ȴﵽ20%ʱ����ת���ʴﵽ84.7%���� CaCO3�ļ���������20%ʱ����ת���ʳ��½����ơ�
��ͬ���������������ø���������ͼ��ͼ4��ʾ��ͼ4(a)��ʾΪֱ�ӱ���(1150 �棬20 min)������������������ͼ����XRD�����ʾΪ�⾧ʯMgFe1.6Cr0.4O4�����������ǰ�еļ⾧ʯ����һ�£������ֱ�ӱ��ռ���û�жԸ���������仯����Ӱ�졣�����м�������Na2CO3���������б���ʱ��ˮϴ����������ΪMg1.5Na9Si12Al12O48��NaSiAlO4��Na3MgAlSi2O8��Na(Fe0.75Al0.25)O2�Ⱥ��Ƶĸ����Fe2O3��(��ͼ4(b))�������������������Na2CO3����ʱ��MgFe1.6Cr0.4O4�⾧ʯ�����˷ֽ⣬NaCO3�ͼ⾧ʯ������Ӧ����Na2CrO4��ͬʱ���������������ࡣ������������Na2CO3��ͬʱ����CaCO3���������ʱ���ڼ���2%��CaCO3ʱ��ˮϴ����������仯��������(��ͼ4(c))������CaCO3�ļ��룬�����к��Ƶĸ���������٣���CaCO3������Ϊ��������20%ʱ����Na������ʧ��ת��ΪCa2Fe1.2Mg0.4Si0.4O5�ȹ��������(��ͼ4(d))��
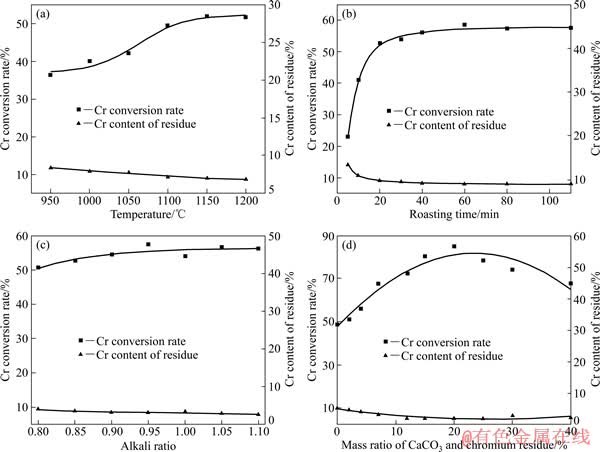
ͼ3 �����¶ȡ�����ʱ�䡢��������������ʶԸ����и�ת���ʵ�Ӱ��
Fig. 3 Effects of roasting temperatures (a), times (b), CaCO3 addition (c) and alkali addition (d) Cr conversion rate of chromium residue
�ڱ��չ����У���ֻ��Na2CO3ʱ�����չ�����Na2CO3�ֽ�⾧ʯʹ����Cr3+��������Cr6+�ܳ���ͬʱNa+����Fe��Al��Mg�ȷ�Ӧ����Na(Fe0.75Al0.25)O2��Na3MgAlSi2O8�ȸ��ࣻ����Ca2+����ʱ��Ca2+������й����Ρ������εȸ����γ����۵���ߵĹ�������࣬Na+���û�����������Ca2Fe1.2Mg0.4Si0.4O5�����������и��ߵ��ȶ��ԣ��뱻�û�������Na+һ��ٽ��˸����и���ת�������⣬���۵�������������ɼ����˸�����Na2CO3 ��Ӧ���̲�����Һ��������������������ɢ��ͬ���ٽ��˸�������������CaCO3���ӵ�20%����ʱ����ͼ3(d)�б���Ϊת���ʽ��ͣ������������Ca2+�����ת�����CrO42-�γ�CaCrO4����������������С����XRD����û�з���������塣
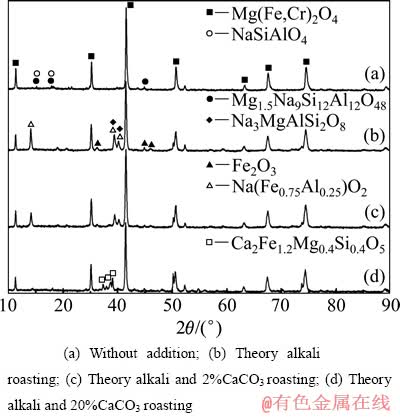
ͼ4 ��ͬ���������Ը����������Ӱ��
Fig. 4 Effect of CaCO3 addition on Cr conversion rate of chromium residue
�������չ����У�Ca�������û��˸����и����Na�������˱��չ�����Na+Ũ�ȣ��ٽ��˸�����Crת���ʵ���ߡ�������Һ�������������������Ҳ֤ʵ�˸��������(Na+��K+)Ũ���ǻ�ø������нϸ߸�ת���ʵĹؼ�����[17-18]��
2.3 �����������о�
Ϊ��һ���о�Na+�Ը����к����⾧ʯ�����û��ƣ�����1 mol/L������Һ��80 ���¶Ը������3 h�����ˡ���������ϴ���ijɷ֡����ࡢ��ò���������3���У�ͼ5(a)��6(a)��ʾ��
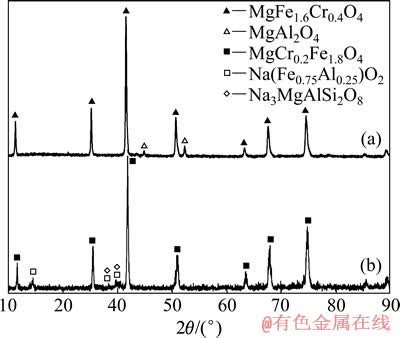
ͼ5 HCl��ϴ������������ۼ��ˮϴ�������XRD��
Fig. 5 XRD patterns of chromium residue pretreated by HCl solution (a) and its residue washed with stoichiometric alkali ratio roasting (b)
�ɱ�3��֪������ϴ������е�Na2O������15.96%���͵�0.65%��Al2O3������13.49%���͵�4.88%��SiO2������10.58%���͵�1.68%��CaO������0.93%���͵�0.28%��������NaSiAlO4��Mg1.5Na9Si12Al12O48�ȸ�����������ܽ��ȥ��ʣ��ɷ�ΪMgCr0.4Fe1.6O4��������MgAl2O4�⾧ʯ��(��ͼ5(a))��SEM����ʾ��ϴ����òΪ��ṹ(��ͼ6(a))������ϴ������������Na2CO3�����б��յó���Crת����Ϊ56.95%����ԭ��ֱ�ӱ��ո�ת���ʵ�51.86%��5%���ң��ɼ�������ԭ�е�Mg1.5Na9Si12Al12O48��NaSiAlO4�ȸ����MgCr0.4Fe1.6O4�⾧ʯ��İ�����һ���̶����谭����Cr��������
��3 HCl��ϴ�����ɷ�
Table 3 Composition of chromium residue washed with HCl
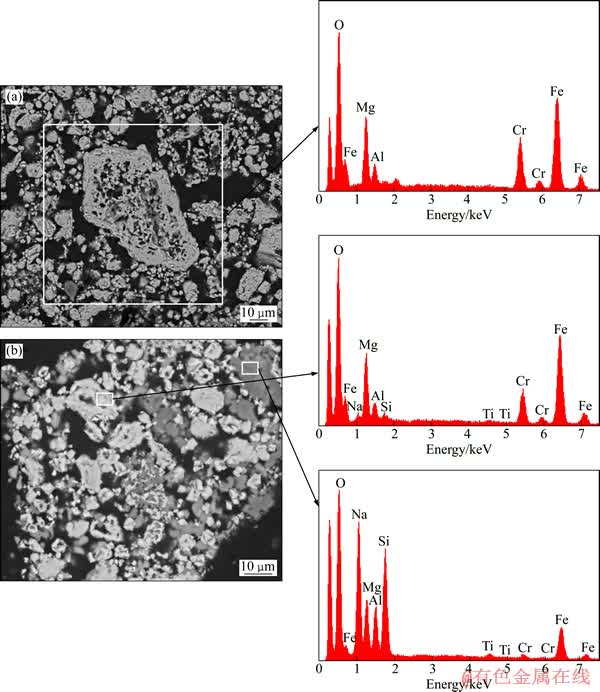
ͼ6 HCl��ϴ������������ۼ��ˮϴ�������SEM���EDS��
Fig. 6 SEM images and EDS spectra of chromium residue pretreated by HCl solution (a) and its residue washed by stoichiometric alkali ratio roasting (b)
����ϴ������������Na2CO3���պ��ˮϴ���������XRD��SEM/EDS������������ͼ5(b)��6(b)��ʾ����ͼ5(b)��֪��ˮϴ��������Ҫ������Ȼ�Ǽ⾧ʯ�࣬���չ����и����������ܳ�����ʱ������⾧ʯΪMgFe1.8Cr0.2O4��Na+��Ӽ⾧ʯ�ֽ�����IJ���Fe��Al��Mg�������˲�����ˮ�ĸ���Na(Fe0.75Al0.25)O2��Na3MgAlSi2O8�Ȳ��������С���ͼ6(b)�п��Կ�����Na+�ͼ⾧ʯ���õĽ���������������������ļ⾧ʯ��(��ɫ����)��������������(��ɫ����)�����д�����A��B�����������Ӧ����ͼ����ͼ6(b)����ķֲ�״̬���Կ�����Na+�ڱ��չ����в����ڴӿ�϶�������ܶԼ⾧ʯ�Ľ��зֽ⣬�γ��ƵĻ����Ȼ���һ��ʹ���۸������ܳ���
��������ϴ�����⾧ʯ�ĸ��༸������ȫ�ܽ��ȥ����Na2CO3���չ����У��⾧ʯ������ܻ��϶��������Na2CO3������Ӧ�������ȥ��������O2-�ͽ������ӵ���ɢ��һ���̶�������˸�ת���ʡ����Na��Al��Si��Ԫ�ؼ������ɰ����⾧ʯ�����������θ��࣬����Na+������Ӧ���ġ��ʸ���İ���ֻ����һ���̶���Ӱ���ת���ʣ�Na+����ЧŨ�Ȳ������Ʊ��պ��ڸ�ת���ʵ�����
3 ����
1) ��������ת����Ϊ70%��õ��ĸ�������MgCr0.4Fe1.6O4�⾧ʯΪ���࣬NaSiAlO4��Mg1.5Na9Si12Al12O48Ϊ���ࡣ
2) �������շ�Ӧ���ڣ����ڹ����Ρ������εȸ���Ļ����Լ���ЧNa+Ũ�ȵĽ��ͣ����º��ڸ��������ѣ����ۼ����½����������ո���ת����ֻ��50%~60%��
3) �������չ����У�Ca�������û��˸��������е�Na�������˸��۵��Ca2Fe1.2Mg0.4Si0.4O5������ε��࣬�����˸�����Al��Si��Fe����Na�ĸ���Ӧ�������˷�Ӧ������Na+Ũ�ȣ��ٽ��˸����и�����������
4) ��ϴ��������ȫ��ȥ�����еĹ����Ρ������εȸ��࣬����Լ⾧ʯ�İ�����һ���̶���Ӱ���ת���ʣ�Na+����ЧŨ�Ȳ������Ʊ��պ��ڸ�ת���ʵ�����
REFERENCES
[1] �� ��, �� ��. ��������������Ӧ��[M]. ����: ��ѧ��ҵ������, 2003.
DING Yi, JI Zhu. Production and application of chromium compounds[M]. Beijing: Chemical Industry Press, 2003.
[2] �� ��. �������Ʊ��յķ�Ӧ����[J]. ���ι�ҵ, 1997(1): 18-21.
JI Zhu. Reaction mechanism of chromite non-calcium roasting method[J]. Inorganic Chemicals Industry, 1997(1): 18-21.
[3] ��С��, �����, ��־��, ����, ������. �������������ն���ѧ[J]. �й���ɫ����ѧ��, 2010, 20(9): 1822-1828.
LI Xiao-bin, QI Tian-gui, PENG Zhi-hong, LIU Gui-hua, ZHOU Qiu-sheng. Kinetics of chromite ore in oxidation roasting process[J]. The Chinese Journal of Nonferrous Metals, 2010, 20(9): 1822-1828.
[4] SUN Zhi, ZHANG Yang, ZHENG Shi-li, ZHANG Yi. A new method of potassium chromate production from chromite and KOH-KNO3-H2O binary sub-molten salt system[J]. AIChE Journal, 2009, 55(10): 2646-2656.
[5] ZHANG Yang, ZHENG Shi-li, DU Hao, XU Hong-bin,ZHANG Yi. Effect of mechanical activation on alkali leaching of chromite ore[J]. Transactions of Nonferrous Metals Society of China, 2010, 20(5): 888-891.
[6] ÷����, �� ϼ, �Ŵ���, �����, ������, ����Ԫ. dz��������������������Ʊ��շ���������[J]. ���ι�ҵ, 2005, 37(3): 5-7.
MEI Hai-jun, LI Xia, ZHANG Da-wei, MA Guang-hui, HAN Deng-lun, ZHANG Zhong-yuan. The advantages of cleaning production technology-��non-calcium roasting method�� for chromium salt[J]. Inorganic Chemicals Industry, 2005, 37(3): 5-7.
[7] ������, ����Ԫ, ��Ԫ��, �� ��, ��ϲ��, ������, �ź��, ����ɽ. �Ʊ������������ƹ���: �й�, CN 1579947[P]. 2005-02-16.
HAN Deng-lun, ZHANG Zhong-yuan, LI Yuan-kui, YANG Hai, HE Xi-shan, DENG Zhen-lan, ZHANG Hong-jun, YANG Kun-shan. Lime-free roasting method for production of sodium chromates: China, CN 1579947[P]. 2005-02-16.
[8] BROADWAY A, CAVE M R, WRAGG J, FORDYCE F M, BEWLEY R J F, GRAHAM M C, NGWENYA B T, FARMER J G. Determination of the bioaccessibility of chromium in Glasgow soil and the implications for human health risk assessment[J]. Science of the Total Environment, 2010, 409(2): 267-277.
[9] �����. ������ǿ�������������뼼���о�[D]. ��ɳ: ���ϴ�ѧ, 2011.
QI Tian-gui. Theory and technology for intensified oxidative roasting of chromite ore[D]. Changsha: Central South University, 2011.
[10] JAGUPILLA S C, MOON D H, WAZNE M. Effects of particle size and acid addition on the remediation of chromite ore processing residue using ferrous sulfate[J]. Journal of Hazardous Materials, 2009, 168(1): 121-128.
[11] SASTRI M N, HILL J O. Reaction between chromium (III) oxide and oxygen in the presence of sodium carbonate-A DTA study[J]. Journal of Thermal Analysis, 1977, 11(2): 323-326.
[12] GARBERS A M, VANVUUREN C P J. A thermoanalytical study of the solid state reactions in the Cr2O3-Na2CO3-O2 system[J]. Thermochimica Acta, 1987, 120(15): 9-17.
[13] BROWN D H, FERGUSON D A. Thermal analysis of chromium (��) and chromium (��) systems with silica and sodium silicate[J]. Journal of Thermal Analysis, 1976, 9(12): 79-82.
[14] ������. ���������������������������¹��ռ���Ӧ�����Ͷ���ѧ�о�[D]. ���: ����ѧ, 2002.
WANG Kai-yu. The study of dynamics and reaction machanism of the new technology that chromite lime-free oxidation roasting producing sodium chromate[D]. Tianjin: TianJin University, 2002.
[15] ������, ţ ��, ������, �����, ����, ��־��, ��С��. �������������������Ը������ʵ�Ӱ�켰�����[J]. �й���ɫ����ѧ��, 2012, 22(5): 1503-1508.
ZHOU Qiu-sheng, NIU Fei, WANG Jun-e, QI Tian-gui, LIU Gui-hua, PENG Zhi-hong, LI Xiao-bin. Influences of impurities of ferrous oxide and aluminum oxide on oxidation rate of trivalent chromium and its mechanism[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(5): 1503-1508.
[16] ��Ԫ˫, ����, ������. ������ı��չ����о�[J]. ����ұ��, 2000, 29(6): 15-18.
LIAO Yuan-shuang, YANG Da-jin, PENG Jian-rong. Study on the roasting of chromium concentrate[J]. Yunnan Metallurgy, 2000, 29(6): 15-18.
[17] ZHANG Yang,LI Zuo-hu,QI Tao,ZHENG Shi-li,LI Hui-quan, XU Hong-bin. Green manufacturing process of chromium compounds[J]. Environmental Progress, 2005, 24(1): 44-50.
[18] LI Ping, XU Hong-bin, ZHANG Yi, LI Zuo-hu, ZHENG Shi-li, BAI Yu-lan. The effect of Al and Ba on the color performance of chromic oxide green pigment[J]. Dyes and Pigments, 2009, 80(3): 287-291.
(�༭ ����)
������Ŀ��������Ȼ��ѧ����������Ŀ(51204154)
�ո����ڣ�2014-06-24�������ڣ�2014-10-17
ͨ�����ߣ��� ƽ�����о�Ա����ʿ��E-mail��lipinggnipil@ipe.ac.cn��chyan1102@126.com
ժ Ҫ����Ը������������պ��ڸ�ת�����ʽ������⣬�Ը������չ��̸�ת����70%�ĸ���Ϊԭ�ϣ���������������ͻ�ѧ�ɷ֣������о��������չ������¶ȡ�ʱ�䡢Na2CO3��CaCO3 �ȶԸ����и�ת���ʵ�Ӱ�죬̽����߸������������պ��ڸ�ת���ʵĻ����������������������ΪMgCr0.4Fe1.6O4�⾧ʯ������ΪNaSiAlO4��Mg1.5Na9Si12Al12O48���ƹ����Ρ����������ࣻ����Na2CO3�����������շ�Ӧ�����и�ת���ʽ�Ϊ50%~60%���ƹ����Ρ��������ε���Ĵ��ڵ���Na+�������ʽ��ͣ���ɸ����еĸ�ת�����ѣ�Ca�������û��˸����и����Na����ת������ߵ�84.7%�������˸��۵��Ca2Fe1.2Mg0.4Si0.4O5������ε��࣬�����˱��չ�����Na+Ũ�ȣ��ٽ��˸���ת��������˱��պ��ڸ���ת���ʡ�
[1] �� ��, �� ��. ��������������Ӧ��[M]. ����: ��ѧ��ҵ������, 2003.
[2] �� ��. �������Ʊ��յķ�Ӧ����[J]. ���ι�ҵ, 1997(1): 18-21.
[3] ��С��, �����, ��־��, ����, ������. �������������ն���ѧ[J]. �й���ɫ����ѧ��, 2010, 20(9): 1822-1828.
[9] �����. ������ǿ�������������뼼���о�[D]. ��ɳ: ���ϴ�ѧ, 2011.
[14] ������. ���������������������������¹��ռ���Ӧ�����Ͷ���ѧ�о�[D]. ���: ����ѧ, 2002.
[16] ��Ԫ˫, ����, ������. ������ı��չ����о�[J]. ����ұ��, 2000, 29(6): 15-18.


