���±�ţ�1004-0609(2010)01-0143-06
�⻯����巢�ݷ��Ʊ�С����ĭ��
�����1���� ͦ1��Ҧ�㴺2����С��2���� ��1
(1. ������ѧ ��ѧԺ������ 110004��
2. ������ѧ ������ұ��ѧԺ������ 110004)
ժ Ҫ��
��ZrH2Ϊ���ݼ����������巢�ݷ��Ʊ�����С����ĭ�����������Ʊ����̼�Ӱ��ṹ�����أ��Ż�ʵ�����Ʊ���ĭ���Ĺ�������������ͼ�η�������������ĭ���Ŀ��ֲ�������TiH2�Ʊ�����ĭ�������˶Աȣ����øĽ�����װ���о����Ͻ����⻯�����ʪ��Ϊ�����������ZrH2���ʺ��Ʊ�С����ĭ�����Ż���������Ϊ��Al 650 g����ճ��Ca �ļ�����2.5%�����ݼ�ZrH2�ļ�����1.0%�������¶�680 �棬����ʱ��1.5 min������ʱ��2.5 min���Ʊ�����ĭ�������ȣ�ƽ����С��1.5 mm��ZrH2�����Ͻ��е���ʪ�ص��ǵ�����ĭ������С����Ҫԭ��
�ؼ��ʣ�
��ͼ����ţ�TG 146.2���� ���ױ�ʶ�룺A
Preparation of foam aluminum with small pores by
melt-based route of ZrH2
LI Da-wu1, SUN Ting1, YAO Guang-chun2, ZHANG Xiao-ming2, LI Jie1
(1. College of Sciences, Northeastern University, Shenyang 110004, China;
2. School of Materials and Metallurgy, Northeastern University, Shenyang 110004, China)
Abstract: Foam aluminum with small pore diameters was prepared by the melt-based route using ZrH2 as foaming agent. The relationship between the foaming process parameters and the cell structures of foam aluminum was studied. The foaming process conditions were optimized. The pore diameter distribution of the foam aluminum was characterized by the graphical analysis method and the foaming agent TiH2 was commonly used for the comparison. The improved sessile drop device was used to research the wetting behaviors of Al alloy on the surface of hydride. The results indicate that the foaming agent ZrH2 is suitable for preparation of the small pore diameter foam aluminum and the optimized process conditions are obtained (650 g of Al; addition of Ca 2.5%; ZrH2 1.0%; temperature 680 ��; stirring time 1.5 min; holding time 2.5 min). The average pore diameter is uniform and below 1.5 mm. The wetting behaviors are the main factor of influencing the pore diameter.
Key words: foam aluminum; melt-based route; zirconium hydride; wettability
��ĭ����һ���ɽ����Ǽܺ��ݿ���ɵ����Ͷ�ܲ��ϣ��������ᡢ������������������Ρ����ܻ��塢���ȡ��ͻ���������ԣ��㷺Ӧ���ڽ�����������������µ�����[1]��
���巢�ݷ�����ĭ����������Ҫ��ʽ֮һ�������ڽ����У����ݼ��ֽ�������壬����Ѹ����ȴ�����������������ڲ��γ���ĭ����(�տ���ĭ)����ˣ����ݼ�����ĭ���ķ���Ч������϶�ʺͿ������Ծ��кܴ�Ӱ�죬ѡ����ʵķ��ݼ�������Ҫ[2]���������о���Ҫ���������÷��ݼ�TiH2��CaCO3[3?5]���Ʊ���ĭ��������ѧ�����TiH2������������µ����ڿ������⣬��TiH2�����˻�ѧ����[6?8]����������[9]�����ϳɳ�һ�ַֽ��¶ȷ�Χ�����ֽ�����ƽ���������κ�Ԥ�����ĸ��Ϸ��ݼ����Ʊ���ĭ�����ϸ�ѧ��[10]���Ƴ����ͷ��ݼ��⻯ϡ�����������۵��⻯ϡ������������ʹҺ̬�����ݡ�ʵ����������ͬ���͵ķ��ݼ���ֽ���Ϊ�в�������в�ͬ�ķ���Ч��������ĭ���������нϴ��Ӱ��[11]��������ʹ��ZrH2�����ݼ������巢�ݷ��Ʊ���ĭ�����о�����������о�ZrH2��Ϊ���ݼ���һ�������������ĭ�������ķ��ݼ���ѡ��Χ��ͬʱ���Խ�һ���˽ⷢ�ݼ��ķ��ݻ�����Ӱ�����ء�
1 ʵ��
ʵ�����õ���Ҫ����Ϊ��ZrH2��((74 ?m�����ȣ�99.6%�����ݽ������ϳ�)��TiH2��(74 ?m�����ȣ�99.0%����˳���ػ��²���Ӧ�ü����о���)����ҵ����(���ȣ�99.0%����˳��ҵ����˾)������Ca(���ȣ�98%������ʡ�ױ����λ�þҵ����˾)���ߴ���� (99.999%���п�Ժ�����о���)��ʵ���豸Ϊ��ʽSRJG?5?10����������¯(�����г��ǹ�ҵ��¯��)��������ƽ(�Ϻ����շ�����������˾)���������(������������˾)��D120?2F�͵綯������(�����DZ��������˾)��DRZ?4���¶ȿ�����(��������ʵ���¯��)��SDTQ600V8.1���ط�����(����TA��˾)�����������ʵ��װ��(������ѧ����)��
1) ��ĭ�����Ʊ�
���������ۻ�Ԥ�����õĹ�ҵ����������Һ�¶�Ϊ860 ��ʱ����������������Ca�������ٽ���(500~700 r/min)ʹCa���ȷ�ɢ��Ȼ������ʵ���趨�¶ȣ��������¶Ⱥ㶨30 min�����转��Ԥ�Ⱥ���0.6%��0.8%��1.0%��1.2%��1.4% (��������)�ķ��ݼ�ZrH2�����ٽ���ʹ֮���ȷ�ɢ(�����ٶ�Ϊ800~ 1 000 r/min)�������������1~3 min�������¯��Ȼ��ȴ�����и���ĭ����۲����ò��
2) ZrH2�ȷֽ�
ʵ���������TA������˾������SDTQ600V8.1���ط����ǣ�Al2O3������αȣ���Ʒ����Լ17 mg������Ϊ100 mL/min�ĸߴ��������������10 ��/min������Ϊ900 �档
3) ������
�����Ʊ�����ĭ���и��4 cm��6 cm�ij����ο飬���б���Ⱦɫ��������ǿɫ�ʶԱȶȣ���ʹ��IMAGIN 5.0��������ͼƬ���п�ͳ�Ʒ�����
4) ���Ͻ����⻯����ʪ���о�
���ǵ��⻯����600 ������ʱ�ֽ���죬������õ��۵�(500 �棬Ge 30.1%)������Ͻ����⻯�Ѻ��⻯���Ϊ������壬����Ͻ�ΪҺ�Σ��������η��ⶨ����ʪ�ǣ���������ʪ���ܡ�ʵ���趨�¶�Ϊ545 �棬��ն�Ϊ2��10?3 Pa���⻯��ѡȡ�ϴ���壬����ϸɰֽ����档
2 ���������
ͼ1��ʾΪZrH2��ĩ�IJ�������(DTA)����ͼ1���Կ�����540 ���730 ��ʱ�����������ȷ壬��540 �渽�������ȷ��С��������730 �����ҵ����ȷ�������ԡ�ZrH2��540 ��ʱ�Ѿ���ʼ�ֽ⣻�ﵽ730 ��ʱ���ֽ���ҡ����巢�ݷ��Ʊ���ĭ���Ĺ����У������¶�һ��Ҫ���ںϽ��۵㣬ͬʱ��Ҫ���Ƿ����¶��뷢�ݼ����ֽ��¶ȵ�ƥ������[6]��ԭ���Ϸ����¶�Ҫ�������ֽ��¶ȣ����ܿ����ֽ��¶ȣ����ܵõ��Ϻõķ���Ч�������ѡ�������ֽ��¶��·��ݣ������ڴ��¶��·��ݼ��ֽ���Ϊ���ң����ʵ��������Կ��ơ���ˣ�����ZrH2�����¶���������660~720 ��֮�䣬�����ܿ��˷��ݼ���540 ���730 ��ʱ�����ֽ��¶ȣ��ڷ��ݼ�δ�ﵽ���ֽ�����ǰ�����ݼ�������������Һ�У�����ʵ�������ͬʱ���ԽϺõؿ��ƽ���ʱ��Ϳ�������ʵ����Ҳ��������һ�㡣
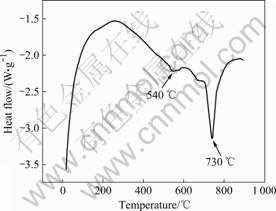
ͼ1��ZrH2�IJ��ȷ���
Fig.1 Differential thermal analysis of ZrH2
���巢�ݷ��Ʊ���ĭ���Ĺ�����Ҫ���������ۻ���������ճ��Ca�����ӷ��ݼ����������Լ����ݺ���ȴ�Ȳ��衣���н����Ƶ������������¶ȡ�ZrH2�ļ������������ٶȡ�����ʱ�䡢�Լ�����ʱ�����ȴ��������������ĭ����Ʒ���������кܴ��Ӱ�죬�κ�һ�����ض��ܸı��ݿĽṹ��������Щ���ղ���֮���ƥ���ϵʮ�ָ��ӣ�����ڿ�����ĭ��Ŀ�϶���Լ����ijߴ��Ϊ���ѡ�
��Һ�����������Ʊ���ĭ����������Ҫ�IJ��衣���ݼ��ֽ���������徭�����ٽ�����ȵط�ɢ�������У����������ݡ��������ճ�ȹ��ͣ��γɵ����ݾͻ�ϲ��ϸ����ݳ�������浼�·���ʧ�ܣ���ճ�ȹ������½������ѣ����ݼ������ȷ�ɢ������������ճ��Ca���������������Ƶĸ���������[12]����CaAl2��CaAl4�ȣ���Щ�����仯������Al2O3��ͬ�������ճ�ȣ��������γɵ�˲���ṩ������κ˽��ʣ�ͬʱճ�ȵ�����Ҳֱ��Ӱ�쵽����Һ��ı�������������������Һ��ı��������ܣ�ʹ���ɵ������ܹ��ȶ����ڡ�������߹�С��ճ�ȶ���Ӿ���IJ������ԡ�
ʵ����õ����ؿ��Ʒ������Ż����Ʊ���ĭ����ʵ��������ͼ2��ʾΪ�Ʊ�����ĭ���ĺ����ò����ͼ2�ɼ�����ĭ���Ŀ���С�����ȡ�ʵ�����Ż���������Ϊ��Al 650 g����ճ��Ca �ļ�����2.5%�����ݼ�ZrH2������1.0%�������¶�680 �棬����ʱ��1.5 min������ʱ��2.5 min���Ʊ���������ĭ�������ܶ�Ϊ0.29~0.50 g/cm3��Ϊ������TiH2�Ʊ�����ĭ���Աȣ�ͬʱҲ���õ����ؿ��Ʒ������Ʊ���ĭ�������������������[13]��

ͼ2 ��ĭ���ĺ����ò
Fig.2 Macroscopical morphology of foam aluminum
��ZrH2��TiH2�Ʊ�����ĭ���и��4 cm��6 cm�����ο飬Ϊ����ǿ����������ȣ����ڿ�����������ĭ����Ʒ�����˱��滯ѧ��ɫ����������������������ʵ��ķ���ø߷ֱ�����������࣬���ü�������Matlab��im2bw������������õ�ͼƬ��ֵ�����������ͼ�η�������imagin5.0����ͳ�ƣ�����ƽ����(D��mm)�����ۻ�����(%)��������1��ͼ3��ʾ��ZrH2��TiH2�Ʊ�����ĭ����
��1 ���������
Table 1 Analytical results of pore diameter

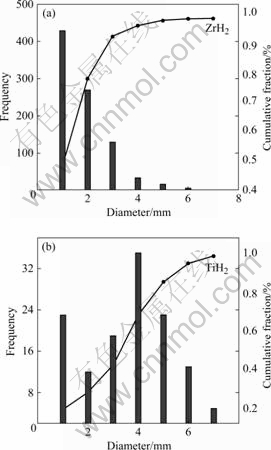
ͼ3 ��ͬ���ݼ��Ʊ�����ĭ���Ŀ��ֲ�ͼ
Fig.3 Diameter distribution diagrams of foam aluminum prepared by different foaming agents: (a) ZrH2; (b) TiH2
ƽ��ֱ���ֱ�Ϊ1.35��3.18 mm����С����(��1 mm)�ֱ�Ϊ48.52%��17.69%�������(��5 mm)�ֱ�Ϊ2.5%��31.53%��ÿƽ��������(N/A)ZrH2(32)��TiH2(6.6)��5������TiH2�Ʊ�����ĭ����ȣ�ZrH2�Ʊ�����ĭ�����������ҿ���С��
ͨ���Ż�ʵ�������ZrH2���Ʊ�����С���Ҿ��ȵ���ĭ����Ʒ����������ͬ������������������TiH2�Ʊ�����ĭ���Ŀ���ϴ�[13]���ɴ˿ɼ���ZrH2���ݼ��ʺ��Ʊ�����С����ĭ����
SUN��[14]��Ϊ��ĭ������С��ԭ���뷢�ݼ���������ķ�ɢ��Ϊ�йأ�����������ʪ��Ϊ����ĭ�ķ�ɢ���ȶ��Ծ��нϴ��Ӱ�졣������Ϊ����ʪ����ȫ��ʪʱ��������ǿ�����ȵ����ݳ���������ƣ��������������ž۳��Ŷ�Ӱ���ɢ����е�����ɢ����ͨ����е���跽ʽ����Һ��ǿ�����˶���ʹ�����ž�������������ɢ�ı�Ҫ�����ǻ�е��(����ļ�������ѹӦ��)Ӧ���ڿ������ճ����[15]��ͬʱ���ٽ��跽ʽҲ������ʵ����ƵIJ��ȶ��ԡ�
�����塢���塢Һ�������ʱ���������Ľ����洦����һ�����ܵ㣬�ɺ�ʱ����������ܵ���Ϊͻ�ƿڷ�����䡣��Һ̬�����г������ݺ�ʱ��ϵͳ�������ܱ仯?GΪ

ʽ�У�VbΪ���ݺ˵������?PΪ���ݺ���������ѹ��������ݺ�Ϊ����ʱ������rΪ���ݺ˰뾶��AlvΪ���ݱ��������lvΪ���������ݽ���ı���������f(��)Ϊ�����κ����ӣ�?GhomΪ�κ˵��ٽ�Gibbs�����ܡ�
�ɼ�����ʪ��ΪӰ�����κ������ܵı仯����ʪ�ǹ������ӷ�ɢ���������������Ҫ�ѹ������Ӿ��ȵط�ɢ�ڽ����У����ȱ���ʹÿ�����������������ܱ����ʳ�ֵ���ʪ��ʽ(5)������ʪ�Ƕ���ĭ�κ������нϴ��Ӱ�죬����ʪ��Ϊ0?ʱ����ζ�ŷǾ���ɺ�����˷��κ��������ݣ�������ӿ�ֱ���ɸ���̬�����̬�������ɺˡ��Ǿ���ɺ��У�ͨ������0?~180?֮��[16]�������������ڿ�������Ϊ��ʼ״̬�������뷢�ݼ�����ʪ��Ϊ����ĭ���Ŀ�Ӱ��ܴ�����б�Ҫ�Է��ݼ����������ʪ��Ϊ�����о���
ʵ����õĸ��������װ����ͼ4��ʾ���Ӵ��ǵIJ��������μ�����[17]��Ϊ�����ͳ���η��н���Һ�������¹����������������⣬ʵ���в���������ձó�����5��10?3 Pa��ͨ��10 min�ߴ�������д�ɨ��Ȼ������ձó�����2��10?3 Pa���Լ���������������Ϊ�˾������ٷ��ݼ������µĹ����ֽ⣬ʵ���趨�¶���550 �����£�ͬʱ���õ��۵������Ͻ�(��Ge 30.1%)��Ϊ��ֹ����¶��������������һ�ּ��������������Բ������ʵ����Ͻ�Һ�Σ��ںܴ�̶��ϼ�����������Ĥ�Բ�����ʪ�ǵ�Ӱ�죬ͬʱ����1 mm���ĵιܣ��ܹ��ε�����Ĥ������[18]��
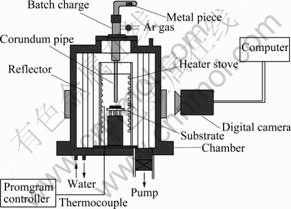
ͼ4 ����ʵ��װ��ʾ��ͼ
Fig.4 Schematic diagram of sessile drop experimental apparatus
�봫ͳ�����η���ȣ���������η��������ŵ㣺
1) ������������Ӧ�ķ���������Һ�ε���������Ϊ�Ϲ������Բ�Σ�
2) ���ø�������װ�ý����������㣬��¼ʵ���ȫ���̡�
ͼ5��ʾΪҺ���ڲ�ͬ�����µ�ƽ��״̬�����Կ���ZrH2��TiH2�Ļ����ϣ���ʪ��Ҳ�������졣��ʵ���пɷ��֣���������ڻ�Ƭ��50 s��Һ�λ����ﵽ��ѧƽ�⣬ƽ��Ӵ��Dz��ٷ����仯�������������Һ�εı���״̬��û����ʱ����ӳ��������仯���������������ԭ���������ۡ����ߵĹ�ͬ�ص��������ʪ�����Դ���90?����ZrH2����ʪ��ҪС��TiH2����ʪ�ǣ�����ZrH2���������еķ�ɢ������TiH2�ķ�ɢ�����á�
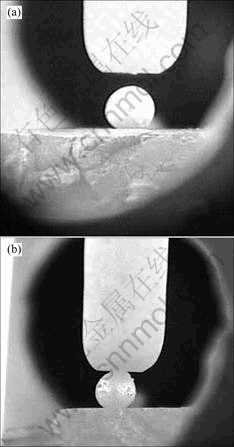
ͼ5��Һ���ڲ�ͬ�����µ�ƽ��״̬
Fig.5 Equilibrium contact angles of liquid droplet at different interfaces: (a) ZrH2; (b) TiH2
��2����Ϊ��ͬʵ���¶��µ���ʪʵ�������ɱ�2���Կ���ƽ����ʪ�������¶ȵı仯�������ֽϴ�ı仯�����ֳ������¶����������ӵ����ơ�TiH2��ƽ����ʪ�Ǵ�142?���ӵ�153?����ZrH2��ƽ����ʪ�����142?���ӵ�148?��
��2 �⻯��������Ͻ����ʪ��
Table 2 Contact angles between hydride and Al-Ge alloy

��2 ���������Կ����������¶ȵ����ӣ�ZrH2��TiH2��ƽ����ʪ�Ǿ����ֳ��������Ƶ�ͬʱ�����ߵIJ�ֵ?��Ҳ��������������Ԥ�����Ʊ���ĭ���ķ����¶���(680~720 ��)��ZrH2����ʪ����Ҫ��������TiH2�ġ���ʪ�ԶԷ�ĩ��ɢ�кܴ��Ӱ�죬�ڷ���
�����н����ݼ����뵽Al����ʱ��TiH2�ͻ���ֳ���Ϊǿ�ҵ��ž�����ʹ��ɢ������ѣ�����ֻ�ܲ��ø�ǿ�Ȼ�е����ķ���ʹ���ɢ����Ϊ��ĭ�����Ʊ������˲�������������ɵĽ���ǿ����ֽ��������Ҫ���Դ���ZrH2�ֽ����������ͬʱ�����ʵ��IJ��ɿ����ԣ�������������ͨ��ѹ����ϳ���������ĭ�����������γɵ���ĭ�����Ӵ��෴��ZrH2���ֳ���Խ�С���ž���Ϊ������������Ծ��ȵط�ɢ���������У������TiH2��ȣ�ZrH2�ķ�����Ϊ���ֳ��Ϻõ�Ч�����ʺ��Ʊ�С����ĭ����Ʒ��
3 ����
1) ZrH2�ֽ�ʱ�����������ȷ壬�ֱ�Ϊ540 �渽����һ��С���ȷ��730 �����ҳ��ֵĽϴ�����ȷ塣Ϊ�˻�ýϺõķ���Ч���������¶�Ӧ������660~730 ��֮�䡣
2) �Ż�����ZrH2Ϊ���ݼ����������巢�ݷ��Ʊ���ĭ���Ĺ�������������650 g Al����ճ��Ca �ļ�����Ϊ2.5%�����ݼ�ZrH2������Ϊ1.0%�������¶�680 �棬����ʱ��1.5 min������ʱ��2.5 min���Ʊ���������ĭ�������ܶ�Ϊ0.29~0.50 g/cm3��
3) �ڸ��Ե��Ż����������£��ֱ�ʹ�÷��ݼ�TiH2��ZrH2�Ʊ�����ĭ�����в�ͬ�ı�����ò����ƽ�����ֱ�Ϊ3.18 mm��1.35 mm��С����(��1 mm)Ϊ17.69%��48.52%�������(��5 mm)Ϊ31.53%��2.5%��ZrH2�ʺ��Ʊ���С�����ȵ���ĭ����
4) ���Ͻ����⻯�����ʪ���о�������ZrH2��TiH2�����Ͻ�����ֳ�����ʪ��Ϊ����ʵ���¶�(��680 ��)�£�ZrH2����ʪ��������TiH2�����ǵ�����ĭ����С�Ҿ��ȵ���Ҫ���ء�
[1] BANHART J. Manufacture, characterisation and application of cellular metals and metal foams[J]. Progress in Materials Science, 2001, 46 (6): 559?632.
[2] ZEPPELIN F V, HIRSCHER M, STANZICK H, BANHART J. Desorption of hydrogen from blowing agents used for foaming metals[J]. Composites Science and Technology, 2003, 63(16): 2293?2300.
[3] DUARTE I, BANHART J. A study of aluminum foam formation kinetics and microstructure[J]. Acta Materialia, 2000, 48(9): 2349?2362.
[4] GERGELY V, CURRAN D C, CLYNE T W. The FOAMCARP process: foaming of aluminium MMCs by the chalk-aluminium reaction in precursors[J]. Composites Science and Technology, 2003, 63(16): 2301?2310.
[5] SONG Zhen-lun, ZHU Jin-song, MA Li-qun, HE De-ping. Evolution of foamed aluminum structure in foaming process[J]. Mater Sci Eng A, 2001, 298(1/2): 137?143.
[6] MATIJASEVIC-LUX B, BANHART J, FIECHTER, S, GO��RKE O, WANDERKA N. Modification of titanium hydride for improved aluminium foam manufacture[J]. Acta Materialia, 2006, 54: 1887?1900.
[7] KENNEDY A R. The effect of TiH2 heat treatment on gas release and foaming in Al-TiH2 performs[J]. Scripta Materialia, 2002, 47(11): 763?767.
[8] ������, ��־��, ������. SiO2/TiH2����������Ʊ�������������[J]. �ߵ�ѧУ��ѧѧ��, 2005, 26(7): 1225?1227.
FANG Ji-xiang, YANG Zhi-mao, DING Bing-ju. Coating process of silica film on TiH2 particles and hydrogen release characteristics[J]. Chemical Journal of Chinese Universities, 2005, 26(7): 1225?1227.
[9] ������, �� ��, ��ϣȪ, ����ר. ��ĭ���������Ʊ����������ͷ��ݼ����ȷֽ���Ϊ[J]. �й���ɫ����ѧ��, 2008, 18(12): 2265?2269.
ZHOU Xiang-yang, ZHANG Hua, LIU Xi-quan, LIU Hong-zhuan. Thermal decomposition behavior of novel gas-generating agent used for two steps foaming process of aluminum[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(12): 2265?2269.
[10] �ϸ�ѧ, �� ��, �ȳ���. �����ͷ��ݼ�-�⻯���ϡ���Ʊ���ĭ�����о�[J]. �й�ϡ��ѧ��, 2005, 23(2): 186?189.
YAN Fu-xue, ZHAO Kang, GU Chen-qing. Fabrication of foamed aluminum by a new vesicant-mixed rare earths hydride [J]. Journal of the Chinese Rare Earth Society, 2005, 23(2): 186?189.
[11] MUKAI T, MIYOSHI T, NAKANO S, SOMEKAWA H, HIGASHI K. Compressive response of a closed-cell aluminum foam at high strain rate[J]. Scripta Materialia, 2006, 54(4): 533?537.
[12] UENO H, AKIYAMA S. Effects of calcium addition on the foamability of molten aluminum[J]. Light Metals, 1987, 37(1): 42?47. (in Japanese)
[13] �� ��, Ҧ�㴺, �� ��, ���. ��������ĭ�����ϵ��Ʊ�����[J]. ������ѧѧ��: ��Ȼ��ѧ��, 2007, 28(8): 1159?1162.
LI Bing, YAO Guang-chun, WANG Yong, LUO Hong-jie. On the preparation process of foamed pure aluminum[J]. Journal of Northeastern University: Natural Science, 2007, 28(8): 1159?1162.
[14] SUN Y Q, GAO T. The optimum wetting angle for the stabilization of liquid-metal foams by ceramic particles: experimental simulations[J]. Metallurgical and Materials Transactions A, 2002, 33(10): 3285?3292.
[15] �� ��, �� ��, ¬�ٴ�. ������ɢ��ѧ�뼼��[M]. ����: ��ѧ��ҵ������, 2005: 204?207.
REN Jun, SHEN Jian, LU Shou-ci. Particles dispersion technology and scientific[M]. Beijing: Chemical Industry Press, 2005: 204?207.
[16] �μ���. ���;ۺ���ݲ��ϼ�����[M]. ����: ��ѧ��ҵ������, 2008: 9?12.
HE Ji-min. A new foaming polymer materials and technology [M]. Beijing: Chemical Industry Press, 2008: 9?12.
[17] ������, Ҧ�㴺, ���콾, ������. þ�������ú����ʪ�Ե�Ӱ��[J]. �й���ɫ����ѧ��, 2004, 14(10): 1700?1704.
WU Lin-li, YAO Guang-chun, LUO Tian-jiao, ZHANG Xiao-ming. Effect of magnesium on wettability of aluminium melt on fly ash[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(10): 1700?1704.
[18] PING S, HIDETOSHI F, KIYOSHI N. Wettability of polycrystalline rutile TiO2 by molten Al in different atmospheres [J]. Acta Materialia, 2006, 54(6): 1559?1569.
������Ŀ�����Ҹ����о���չ�ƻ�������Ŀ(2004AA33G060)������ʡ�Ƽ����ؼƻ�������Ŀ(2003221004)
�ո����ڣ�2009-04-16�������ڣ�2009-07-25
ͨ�����ߣ���ͦ�����ڣ���ʿ��024-83684786��E-mail: sun1th@163.com
(�༭ ����Ⱥ)


