���±�ţ�1004-0609(2008)05-0923-06
Pb/Znұ���������м۽���������������Ż�
������1, 2���� ��2�������1����ѧ��1���˷↑2
(1. ���ϴ�ѧ ��Դ�ӹ������﹤��ѧԺ����ɳ 410083��
2. ���ϴ�ѧ ұ���ѧ�빤��ѧԺ����ɳ 410083)
ժ Ҫ��
ժ Ҫ��Ϊ����������Pb/Znұ���������м۽����Ľ����ʣ�����������ƣ�ͨ��ҡƿʵ�飬�о��������ijPb/Znұ�������������¶ȡ�pHֵ������Ũ�ȼ�����ʱ��ȶԷ�����Cu��Zn��In��Ga��Pb��Ag���м۽���������Ӱ�졣�����������pHֵΪ1.5������Ũ��Ϊ5%���¶�Ϊ65 ����Ż������������������4d��Pb/Znұ���������м۽���Cu��Zn��In��Ga�Ľ����ʷֱ�ﵽ95.5%��93.5%��85.0%��80.2%����Pb��Ag����Ҫ������Ǧ���Ƽ����������ʻ�������ʽ�����������С�
�ؼ��ʣ�
Pb/Znұ���������м۽�����������������������Ż���
��ͼ����ţ�TF 18; X 705���� ���ױ�ʶ�룺A
Optimization on bioleaching of metal values from
Pb/Zn smelting slag
GUO Zhao-hui1, 2, CHENG Yi2, QIU Guan-zhou1, LIU Xue-duan1, PAN Feng-kai2
(1. School of Resources Processing and Bio-engineering, Central South University, Changsha 410083, China;
2. School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: In this study, the main variables involved in the bioleaching process include temperature, pH, pulp density and leaching time. These variables were studied through a shaking flask experiment by orthogonal design in order to improve the leaching rate of metal values, including Cu, Zn, In, Ga, Pb and Ag, from the Pb/Zn smelting slag. The results show that bioleaching rate of Cu, Zn, In and Ga in the Pb/Zn smelting slag under optimized conditions (pH 1.5, temperature 65 ��, 5% pulp density and a leaching time of 4 d) is 95.5%, 93.5%, 85.0% and 80.2% respectively. Lead and silver, however, are mostly deposited in the leached residues with the forms of lead sulfate, argentojarosite-type or silver sulfide compounds, respectively.
Key words: Pb/Zn smelting slag; metal values; bioleaching; optimization of bioleaching variables
���Ź��õĿ��ٷ�չ����ɫұ����ҵ��չѸ��[1]���ҹ���ɫұ��������Ҫ�Ի�Ϊ��������ɫұ�������в����˴�����ұ������������ȱ����Ч�����á������Ѻõ��м۽������ռ��������´�����ɫұ���������á���Щ���õ���ɫұ�������к��д���As��Cd��Cr��Cu��Ni��Pb��Zn�Ⱦ��и߶�Ǩ���Ե��ؽ������ж�Ԫ�أ����ڶ��ò������´����м۽�������ʧ�����Ҷ�����������ˮ����̬�������DZ����Ⱦ��Σ��[2]����ͳ����ɫұ����������������Ҫ�������ô�������������ϵ�[3]�������ô�ѡ����ѡ��ʪ������ͱ��յȼ���������ɫұ���������м۽�����Ҫ��������Щ���нϸ�Ʒλ��Al��Co��Cu��Ni��Pb��Zn�Ƚ����ͺ�Au��Ag��In��Nb��Pt��Ta�ȹ������ұ������[4]������Щ���մ��ھ���Ч��͡��ײ���������Ⱦ���ȱ�㡣��ˣ��о���Ӧ�þ��ú����������Ѻò��ܴ�����Ʒλ��ɫұ�������Ĵ������ղ��������ڱ�����̬��������������������м۽������ۺϻ����ʺ������ʡ�
���������������д�������Χ�㡢���̼��ܺĵ͡������Ѻõ��ŵ�õ��˹㷺��ע��Ŀǰ���ü��������ɹ���Ӧ���ڴӵ�Ʒλ���β���л���Au��Cu��Co[5-6]��U[7]]���м۽��������Ҵӵ�Ʒλ���л���Ag��Cd��Ga��Mo��Ni��Pb��Pd��Pt��Rh��Ru��Sb��Zn�Ƚ���Ҳ����һ����ǰ��[5]������������������������ⶾ�����ؽ���������[8-9]������[10]�����������ٻ�¯�ɻ�[11]���ܵ��˻��������ߵĹ�ע����ɫұ�������ɷָ��ӣ�������ͨ�����д������ͽ������Ϊ���þ��������ͼ���������������շ������м۽�����ʵ�ַ�����Դ���������ṩ�˿���[12]��Ŀǰ���������\������ɫұ������������Դ�����������о����������ࡣGUPTA��[13]�о�������������˾�(Thiobacillus ferrooxidans)���������ա��������������ұ��п�����в����Ľ�����(��Zn 11%~18%��Pb 4%~6%��Fe 18%~29%��Ag 200~ 500 mg/kg��Cu 0.15%~0.3%��Cd 0.12%~0.25%��Ni 100~140 mg/kg��Co 80~100 mg/kg)����pHֵΪ1.2���¶�Ϊ35 �棬��Ũ��Ϊ1%�������½���30 d��Zn�Ľ����ʿɸߴ�27.5%����������������˾��ܴٽ�����Zn�Ľ����������ڽ����ʵ͡�����ʱ�䳤��Ŀǰ���Զ����������м۽��������ۺϻ��ա����ø����¾��и�������ԺͿ����Ե��е����Ⱦ���ɴ����߽����Ľ�����[14]������ͬ�¶�[9, 13]��pHֵ[13]����Ũ��[13, 15]�ͽ���ʱ��[16]�ȶ����н����Ľ�����Ӱ�����ԡ���ˣ�Ѱ�Һ��ʵ���Դ�������������������Dz��������������������ɫұ������ؽ������Ĺؼ����⡣���о�����������ƣ�ͨ��ҡƿ���飬�о����¶ȡ�pHֵ������Ũ�ȼ�����ʱ����е����Ⱦ�������ɫұ���������м۽����������ɵ�Ӱ�죬Ϊѡ���������������ɫұ������������Դ����ѡ�����������ĸ�Ч�������ղ����ṩ��ѧ���ݡ�
1 ʵ��
1.1 �����;���
ʵ�����÷�������ij����Ǧпұ���������ѳ�������Ȼ��ɣ���ĥ��ĥϸ����0.1 mmɸ����105 ���ɣ����к�����Լ35%��Ϊ�������еIJ�������Դ��ĥϸ��ķ���������������װ������ʵ���á���Fe���������Ҫ�м۽���Ԫ��ΪZn��Cu��Pb��Ag��In��Ga�ȣ��京���ֱ�Ϊ2.57%��1.03%��0.41%��92 g/t��100 g/t��916 g/t����Ҫ�к�Ԫ��ΪAs��Cd��Pb�ȣ�As��Cd�����ֱ�Ϊ0.42%��24 g/t��
���о����ñ�������ѱ�����е����Ȼ�Ͼ�Ⱥ�������Ϊ�������������ԡ����£���55~65 ����Ժ�ǿ��ʵ�������þ���ͨ��8 000 r/min���ķ������ȥ����Һ�����µľ���������ˮƯϴ�����ģ��ظ�2�κ���pHֵΪ2.0��������������Һϡ����2��107��ϸ��/mL���á�
1.2 ����ʵ�����
��ȡ����ʵ����ƣ�����ҡƿ(��ƿ�ݻ�Ϊ250 mL)ʵ�鿼��pHֵ���¶ȡ�����(��)Ũ�ȼ�����ʱ��Է������м۽��������ʵ�Ӱ�졣����������L9(34)[17]��ÿ�������ظ�3�Ρ����У�pHֵ��Ϊ0.5��1.5��2.5���¶���Ϊ45��55��65 �棬����Ũ����Ϊ5%��10%��15%������ʱ����Ϊ4 d��8 d��12 d��Ϊʹ������ϵpHֵ�����ȶ���������1.5 mol/L������ҺԤ��1 d���������е���ʯ������ƿ�м���90 mL������������Һ���ϸ����pHֵ���趨ֵ���������1?10�����������ֺ����ں���ˮԡҡ���У�ת��Ϊ120 r/min�������������趨�¶����������ֱ��ڵ�4 d��8 d��12 dȡ����������ϵpHֵ����pH��(420 ĄʽpH/mV)ÿ��24 h�ⶨ1�Σ��ⶨ��μ�2 mol/Lϡ���������Ϊʵ���趨pHֵ�����ú�����������ˮ������������е�ˮ����ʧ��ͬʱ��������ʵ����ƻ����ϣ������Ż�����������֤ʵ�顣
1.3 �����뷽��
����Ʒȫ��ת����100 mL���Ĺ�����5 000 r/min������5 min��ȡ����Һ2.5 mL������2.5 mL������ö���ȥ����ˮ������50 mL�����˺�����100 mL����ϩƿ����4 ����ء�ȡ�Ż������½���������105 ���ɺ����X�����������(SIMENS2500X��X������)������Һ��Cu��Zn��Pb��Ag��In��Ga��Ũ�Ȳ��õ����ϵ������巢�������(�����ȵ�Ԫ�ع�˾Intrepid��XSP��)�ⶨ��ʵ��������������ϴ����12%���ϵ�������Һ����24 h�����ö���ȥ����ˮ��ϴ���ɱ��á�
2 ���������
2.1 ��������м۽��������Ż�����
2.1.1 pHֵ
�ӱ�1��ʾ��������������Կ�����pHֵ��Ӱ�������������Ҫ������֮һ��PHֵ�Է�����Cu��Zn��Ag��In�м�����Ӱ��(F��F0.01)����Է�����Cu��Zn��Ag��In������Ӱ��Ĺ����ʷֱ�Ϊ37.9%��21.1%��94.8%��89.1%����ˣ�pHֵ�Է�����Ag��In�Ľ�������������ã�ͬʱ��Ӱ�������Cu��Zn��������ҪӰ������֮һ(��B����E)��
��1 L9(34)����ʵ�鷽�����
Table 1 Variance analysis of L9(34) orthogonal experiments

Cu��Ga��Zn�Ľ�������pHֵΪ1.5ʱ���(ͼ1)���о���������������ϵpHֵΪ1.5ʱ���е����Ⱦ����нϸ��ԣ��ܼӿ�Fe2+��Fe3+֮���ת����ѭ��[18]������ϵpHֵΪ0.5��2.5ʱ�������ڷ�����Cu��Zn�������������[18]��������Ag��In��Ҫ������ͬ����ʽ��Ƕ������п��ͭ�Ƚ�������ľ�����[12]����ˣ���Fe��Zn��Cu�Ƚ������ﱻ����������Ag��In���ܱ�������Ȼ����Ag��In�ڽ�����ϵpHֵ����1.5ʱ�����ʶ��dz���(ͼ1)�������������ϵ�У���pHֵ����1.5ʱ����ϵ�н����Ĵ��������ӿ�ʼˮ�⣬�����Ƽ�����������(ͼ5)[18]���谭�����������֮��Ĵ��ʣ��������ͳ����ѽ����Ľ������ӣ�����Ӱ���������Ľ�һ���� ��[18]��Ag+�Ƚ����ۼ��ڻƼ����������ж�����������[19]���³��������У���ˣ�������Ag�ڽ�����ϵpHֵ����1.5ʱ�����ʵ���10%�����⣬����Ag+����ȡ�����н���Ԫ������Ag2S(ͼ5)(Ksp = 5.5�� 10-51)��������������ı��棬����������������ɴ���С��ԭ��أ��Ӷ��ٽ����������Ľ���[6]����Һ��InҲ����Ƽ�����һ���������������[20]����������ϵpHֵ����1.5ʱ��In������Ҳ���Խ��͡���ˣ��ۺϿ��Ƿ�������Ҫ�м۽���Ԫ��Cu��Zn�Ľ������Լ�Ag�ܸ����ڻƼ������е����أ�ѡ��ϸ�������˷������Ż�pHֵΪ1.5��
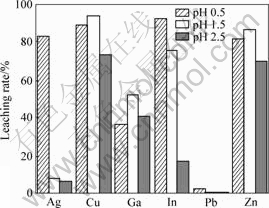
ͼ1 pHֵ�Է������м۽��������ʵ�Ӱ��
Fig.1 Influences of pH value of solution on leaching rate of metal values from smelting slag
2.1.2 ����Ũ��
�ӱ�1��ʾ��������������Կ���������Ũ�ȶԷ�����Cu��Zn��In�Ľ����м�����Ӱ��(F��F0.01)����Ag������Ӱ��(F��F0.05)��������ʵ�������£�����Ũ�ȶԷ�����Cu��Zn��In�����ʵĹ����ʷֱ�Ϊ28.0%��24.8%��5.8%����������Ũ��Ҳ��Ӱ�������Cu��Zn��������Ҫ����֮һ(��D����E)��������Cu��Zn���������ŷ���Ũ�ȵ����߶����½�����(ͼ2)������Ũ�ȶ�Ag��In������Ӱ���С(��D����E)�����о��������������ʱ��Ũ����5%���ڲ�����Ӱ�����Ͷ�����̼�Ĵ����ٶȣ�����Ũ�ȹ��ߣ���������������ĺ������ʽ�������Һ�������ʣ��Ӷ���ɽ�����ϵȱ��[21]��ͬʱ����Ũ�ȵ����߽��Ӿ�������֮���Ħ����Һ��ļ��������Ӷ��������ϸ���Ļ�е����[22]������Ӱ��������м۽�����������������⣬��Ũ�����Ӻ���Һ��Fe3+Ũ�ȴ��ӿ������ڻƼ�����������[18, 23]����Ҳ������Cu��Zn��Ag��In�����ʽ��͡���ˣ�����Ũ��Ϊ5%Ӧ�Ƿ����������Ż�Ũ�ȡ�
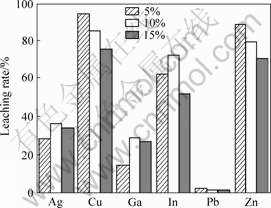
ͼ2 ����Ũ�ȶԷ������м۽��������ʵ�Ӱ��
Fig.2 Influence of pulp density on leaching rate of metal values from smelting slag
2.1.3 �¶�
�ӱ�1��ʾ��������������Կ������¶ȶ�Cu��Zn��In��Ag�Ľ������ż�������Ӱ��(F��F0.01)���¶ȶԷ�����Cu��Zn��Ag��In������Ӱ��Ĺ����ʷֱ�Ϊ15.4%��25.2%��0.6% ��1.0%����ˣ��¶�Ҳ��Ӱ�������Cu�� Zn��������Ҫ����֮һ(��A����E)����ͼ3���Կ������¶�Ϊ65 ��ʱCu��Ga��Zn��������ߣ���Ag��In������Ҳ�ϸߡ������������Ļ����¶ȷ�Χ�ڣ��ڽϸ��¶��²�������Ч��ߴ���Ч�ʣ��������̽���ʱ��[14]�����ٷ����в����ѽ�����������Ľ���[12]�����һ�������Ч���ƶۻ���(�Ƽ����������� ��)���γ�[14]����ˣ������е����Ⱦ������������м۽������Ż��¶�Ϊ65 �档
2.1.4 ����ʱ��
�ӱ�1��ʾ��������������Կ���������ʱ��Է�����Cu��Zn��Ag��In�Ľ����м�����Ӱ��(F��F0.01)��������ʱ��Է�����Cu��Zn��Ag��In�����ʵ�Ӱ�칱���ʽ�С����Ϊ4.7%��11.4%��1.2%��1.6%����ͼ4��֪���������м۽�����ǰ4 d���ܴﵽ�ܸߵĽ����ʣ��������ʱ���һ���ӳ����������м۽��������ʲ�����������ߡ����ڽ���ʱ��ȡ���ڽ������ʣ�Ӱ��������ʵ����ذ���������ɼ��ṹ[5]����ͬ������ּ����������ȣ���ˣ��ڷ����ɷֺ�ϸ������ȷ�������£�������ϵ������(pHֵ���¶Ⱥͷ���Ũ�ȵ�)���Ż��ܴ�̶ȵ�����м۽����Ľ������ʡ������������������������Ż���pHֵ���¶Ⱥͷ���Ũ�ȵĽ��������£�����4d������Cu��Zn��Ag��In��Ga��Pb�Ľ����������Ͽ��Էֱ�ﵽ(92.6��5.2)%��(88.6��6.0)%��(6.8��0.6)%��(74.3��5.0)%��(87.6��7.0)%��(1.1��0.1)%��������8 dʱ��Cu��Zn��Ag��In��Ga��Pb�Ľ����������Ͽ��Էֱ��(93��5.3)%��(89��5.8)%��(15��6.2)%��(64.2��5.0)%��(73��6.5)%��(1��0.1)%����˵������������ϵ�����Ż��������м۽�����4 d��������Դﵽ�ܸߵĽ����ʣ�������Ϊ�Ƚ�����Ľ���ʱ�䡣
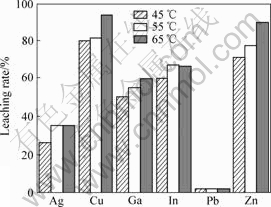
ͼ3 �¶ȶԷ������м۽��������ʵ�Ӱ��
Fig.3 Influence of temperature on leaching rate of metal values from smelting slag
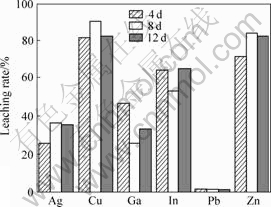
ͼ4 ����ʱ��Է������м۽��������ʵ�Ӱ��
Fig.4 Influence of leaching time on leaching rate of metal values from smelting slag
�����о�������pHֵ������Ũ�ȡ��¶Ⱦ���Cu��Zn�������ŷdz�������Ӱ�졣pHֵ��Ӱ�������Cu����������Ҫ���أ�����Ƿ���Ũ�ȣ��ٴ����¶ȣ�������ʱ��Է�����Cu�Ľ���Ӱ����Խ�С���¶ȡ�pHֵ������Ũ����Ӱ�������Zn��������Ҫ����(��A����B�ͦ�D�����ڦ�E)�����߶�Zn�Ľ���Ӱ���൱ (��A����B�ͦ�D�ֱ�Ϊ25.2%��21.1%��24.8%)�����������������֪���������������Cu��Zn���Ż���������ӦΪ��pHֵΪ1.5���¶�Ϊ65 �棬��Ũ��Ϊ5%���ڴ������½���4 d��������Ag��In�Ľ�������Ҫ������pH(�Ƿֱ�Ϊ94.8%��89.1%)���¶ȡ�����Ũ�ȼ�����ʱ����Ӱ��Ƚ�С��In��pHֵΪ1.5���¶�Ϊ65 �桢����Ũ��Ϊ5%�Ľ�����ϵ�У������ʿ��Դﵽ74.3%����Ag�����ʺܵͣ���Ҫ�ԻƼ����������ʺ�����(ͼ5)����ʽ�����ڽ���������[19]��pHֵ������Ũ�ȡ��¶ȼ�����ʱ��Է�����Pb�����ʾ��м�������Ӱ��(F��F0.01)����������Ǧ�ܽ��(Ksp=1.62��10-8)�Ͷ����Գ���(ͼ5)��������[24]����ˣ�������Ǧ�����ʺܵ�(��5%)��pH���¶ȡ�����Ũ�ȼ�����ʱ�����Ga�����м�����Ӱ�죬pH�ͷ���Ũ����Ӱ�������Ga��������Ҫ����(�Ƿֱ�Ϊ31.5%��23.6%)�����¶Ⱥͽ���ʱ��Ĺ����ʽ� С������������������������pHֵΪ1.5���ҡ�����Ũ��Ϊ5%���¶�Ϊ65 ��������½���4 d������Ҳ�ɴﵽ87.6%���ҡ���Ga�ڷ����еĴ�����̬���ӣ���Ҫ���������������������ͬ����ʽ��Ƕ���ڻ�������[12]��Ŀǰ��Ga��������������о�����[5]��Ga�ڷ����еĽ������ɼ���������д���һ���о���������������������������յ��Ż�����ѡȡ���£�pHֵΪ1.5������Ũ��Ϊ5%���¶�Ϊ65 �棬����ʱ��Ϊ4 d�����Ż����������£�ͨ��������� (��1)��������Cu��Zn�Ľ����������Ͽɷֱ�ﵽ(92.6��5.2)%��(88.6��6.0)%��In��Ga�ֱ�ﵽ(74.3��5.0)%��(87.6��7.0)%��Ag��Pb�Ľ����ʺܵͣ�Ϊ(6.8��0.6)%��(1.1��0.1)%��
2.2 �Ż������·������м۽����Ľ�������
��������ʵ���Ż���������(pHֵΪ1.5���¶�Ϊ65 �棬����Ũ��Ϊ5%������ʱ��Ϊ4 d)����չʵ����֤�����������Cu��Zn��In��Ga������ʵ�ʷֱ�ﵽ95.5%��93.5%��85.0%��80.2%����Ag��Pb�Ľ����ʽ�Ϊ7.2%��0.8%������������ʵ�鷽���������Ǻϡ���ˣ��������м۽���Ԫ��Cu��Zn��In��Ga��Ag��Pb���Է�Ϊ�����ࣺһ���Ƿ����е�Cu��Zn��In��Ga���нϸߵĽ����ʣ�����ͨ���������������Һ�У���ͨ����ȡ�����ȹ��ջ��գ�����һ��ΪAg��Pb�Ⱦ�ϸ������������Ҫ�ԻƼ����������ʡ�����������Ǧ����ʽ������������(ͼ5)����ҪѰ������;������������������л���Pb��Ag[25-26]��
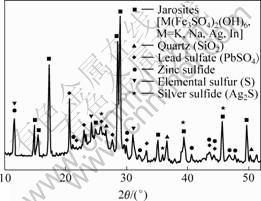
ͼ5 �Ż����������������������XRD��
Fig.5 XRD pattern of residues from bioleaching process under optimization variables
3 ����
1) ����ʵ���о����������������ϵ��pHֵ������Ũ�ȡ������¶Ⱥ�ʱ���Pb/Znұ���������м۽�������Ӱ��dz����ԡ��������м۽�������������Ż�����Ϊ��pH 1.5����Ũ��5%���¶�65 �棬����ʱ��4 d��
2) �ڴ��Ż������£������е�Cu��Zn��In��Ga��ʵ�ʽ����ʷֱ���Դﵽ95.5%��93.5%��85%��80.2%������ͨ����������ӽ���Һ�л��շ����е�Zn��Cu��In��Ga��Ag��Pb����Ҫ�ԻƼ����������ʡ�����������Ǧ����ʽ�����������С�
REFERENCES
[1] ��ҵ��. ��ɫ����ұ������о�����״���Խ��Ľ���[J]. �й���ɫ����ѧ��, 2004, 14(1): 21-24.
LIU Ye-xiang. Current status and future proposals of fundamental research in nonferrous metallurgy[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(1): 21-24.
[2] MANZ M, CASTRO L J. The environmental hazard caused by smelter slags from the STA. Maria De La PAZ mining district in mexico[J]. Environmental Pollution, 1997, 98(1): 7-13.
[3] AGRAWAL A, SAHU K K, PANDEY B D. Solid waste management in non-ferrous industries in India[J]. Resources Conservation and Recycling, 2004, 42(2): 99-120.
[4] GBOR P K, HOQUE S, JIA C Q. Dissolution behavior of Fe, Co, and Ni from non-ferrous smelter slag in aqueous sulphur dioxide[J]. Hydrometallurgy, 2006, 81(2): 130-141.
[5] ������, �����, ����ϼ. ����ʪ��ұ��[M]. ����: ұ��ҵ������, 2003: 106-244.
YANG Xian-wan, SHEN Qing-feng, GUO Yu-xia. Bio-hydrometallurgy[M]. Beijing: Metallurgical Industry Press, 2003: 106-244.
[6] ������, �����, ������, л��Ԫ. �����Ѵ������ʯ���������������ռ�Ӧ��[M]. ����: ұ��ҵ������, 2006: 133-137.
YANG Song-rong, QIU Guan-zhou, HU Yue-hua, XIE Ji-yuan. The application of biooxidation of arsenic-bearing refractory gold ore[M]. Beijing: Metallurgical Industry Press, 2006: 133-137.
[7] MUFIOZ J A, GONZBLEZ F, BLIZQUEZ M L, BALLESTER A. A study of the bioleaching of a Spanish uranium ore, Part I: A review of the bacterial leaching in the treatment of uranium ores[J]. Hydrometallurgy, 1995, 38(1): 39-57.
[8] CHEN S Y, LIN J G. Bioleaching of heavy metals from sediment significance of pH[J]. Chemosphere, 2001, 44(5): 1093-1102.
[9] TSAIA L J, YU K C, CHEN S F, KUNG P Y. Effect of temperature on removal of heavy metals from contaminated river sediments via bioleaching[J]. Water Research, 2003, 37(10): 2449-2457.
[10] BABEL S, DACERA M D. Heavy metal removal from contaminated sludge for land application: A review[J]. Waste Management, 2006, 26(9): 988-1004.
[11] ISHIGAKI T, NAKANISHI A, TATEDA M, IKE M, FUJITA M. Bioleaching of metal from municipal waste incineration fly ash using a mixed culture of sulfur-oxidizing and iron-oxidizing bacteria[J]. Chemosphere, 2005, 60(8): 1087-1094.
[12] ������, �� ��, ����Ԫ, �� ��. ��ɫұ�������Ŀ���ѧ�������价�������о�[J]. ���ϴ�ѧѧ��: ��Ȼ��ѧ��, 2007, 38(6): 1100-1105.
GUO Zhao-hui, CHENG Yi, CHAI Li-yuan, SONG Jie. Mineralogical characteristics and environmental availability of the non-ferrous slag[J]. Journal of Central South University: Natural Sciences, 2007, 38(6): 1100-1105.
[13] GUPTA A, BIRENDRA K, MISHRA R. Study on the recovery of zinc from Moore cake: a biotechnological approach[J]. Minerals Engineering, 2003, 16(1): 41-43.
[14] ROD?GUEZ Y, BALLESTER A, BL?ZQUEZ M L, GONZ?LEZ F, MU?OZ J A. New information on the chalcopyrite bioleaching mechanism at low and high temperature[J]. Hydrometallurgy, 2003, 71(1/2): 47-56.
[15] LIU Yun-guo, ZHOU Ming, ZENG Guang-ming, LI Xin, XU Wei-hua, FAN Ting. Effect of solids concentration on removal of heavy metals from mine tailings via bioleaching[J]. Journal of Hazardous Materials, 2007, 141(1): 202-208.
[16] POWELL N, JORDAN M A. Batch Leaching data analysis: Eradication of time dependency prior to statistical analysis[J]. Minerals Engineering,1997, 10(8): 859-870.
[17] ������, ������. ������������ݴ���[M]. ����: ��ѧ��ҵ������, 2005. 208-215.
LI Yun-yan, HU Chuan-rong. Experiment design and analysis[M]. Beijing: Chemical Industry Press, 2005: 208-215.
[18] DAOUD J, KARAMANEV D. Formation of jarosite during Fe2+ oxidation by Acidithiobacillus ferrooxidans[J]. Minerals Engineering, 2006, 19(9): 960-967.
[19] BOLORUNDURO S A, DREISINGER D B, WEERT V G. Zinc and silver recoveries from zinc-lead-iron complex sulphides by pressure oxidation[J]. Minerals Engineering, 2003, 16(4): 375-389.
[20] ������. ��ұ��[M]. ����: ұ��ҵ������, 2006: 82-88.
WANG Shu-kai. Indium metallurgy[M]. Beijing: Metallurgical Industry Press, 2006: 82-88.
[21] TIPRE D R, DAVE S R. Bioleaching process for Cu-Pb-Zn bulk concentrate at high pulp density[J]. Hydrometallurgy, 2004, 75(1/4): 37-43.
[22] DEVECI H. Effect of solids on viability of acidophilic bacteria[J]. Minerals Engineering, 2002, 15(15): 1181-1189.
[23] ���г�, ë����, ���, ��־��. ���ຮɽ������Ƽ��������γɻ��Ƽ����������[J]. ���ʵ���ѧ, 1999, 27(1): 33-37.
ZHANG Zhao-chong, MAO Jing-wen, YANG Jian-min, WANG Zhi-liang. Genesis of jarosite in the Hanshan gold mine of Gansu province and its geological significance[J]. Geology- Geochemistry, 1999, 27(1): 33-37.
[24] SILVA D G. Kinetics and mechanism of the bacterial and ferric sulphate oxidation of galena[J]. Hydrometallurgy, 2004, 75(1/4): 99-110.
[25] LIAO M X, DENG T L. Zinc and lead extraction from complex raw sulfides by sequential bioleaching and acidic brine leach[J]. Minerals Engineering, 2004, 17(1): 17-22.
[26] FR?AS C, D?AZ G, OCA?A N, LOZANO J I. Silver, gold and lead recovery from bioleaching residues using the PLINT process[J]. Minerals Engineering, 2002, 15(11): 877-878.
������Ŀ��������Ȼ��ѧ����������Ŀ(20507022)�����ϴ�ѧ��ʿ�����������Ŀ(1339-811640000)
�ո����ڣ�2007-08-10�������ڣ�2008-03-04
ͨѶ���ߣ������ͣ������ڣ���ʿ���绰��0731-8836442�����棺0731-8710171��E-mail: zhguo@mail.csu.edu.cn


