H-A-O����ǿ���ѵ���ϵͳ������������о�
������1��������1���ž���1������Ө1��������1, 2
(1. ������ˮ�ʿ�ѧ��ˮ�����ָ������ص�ʵ���ң����� 100124��
2. ������������ѧԺ ��������Դ����ѧԺ������ 100044)
ժҪ��Ϊ���������ˮ��ͳ�������շ������ѵ���������ϵͳ�ڲ�ʵ��������������ˮ���ữ-ȱ��-����(H-A-O)�����ѵ������������Ϲ��ա���������������з�ʽ����ʵ��������ˮΪ����ˮ��ѧ������(COD)Ϊ220~410 mg/L����ˮNH4+-N����Ũ��Ϊ36~58 mg/L������Һ������(r)Ϊ300%��������������ˮ���ữ����ʹԭˮ�Ŀ����������60%��ϵͳ�������̼Դ�ͼ�������£�COD��NH4+-N��TN��ȥ���ʷֱ�ﵽ90%��95%��74%�������ܵ�(TN)ȥ��Ч�����12%����������ˮ���ữ��ˮ��������ˮ��Ϊ������̼Դʱ�����NO3--N���������ʷֱ�Ϊ0.75 mg/min��0.66 mg/min��H-A-Oϵͳ����ˮ���ữ����ʵ��ʣ���������Ϊ37%��ͬʱ���ϵͳ���ѵ�Ч����
�ؼ��ʣ�
��ͼ����ţ�X703.1 ���ױ�־�룺A ���±�ţ�1672-7207(2011)06-1813-06
Enhanced nitrogen removal and internal sludge reduction by H-A-O technology
PENG Yong-zhen1, GAO Yong-qing1, ZHANG Jing-yu1, WANG Shu-ying, WANG Jian-long1, 2
(1. Key Laboratory of Beijing for Water Quality Science and Water Environment Recovery Engineering,
Beijing University of Technology, Beijing 100124, China;
2. Beijing University of Civil Engineering and Architecture,
School of Environmental and Energy Engineering, Beijing 100044, China)
Abstract: A hydrolysis-anoxic-oxidation (H-A-O) combined system for enhanced nitrogen removal and waste activated sludge (WAS) reduction within the process was designed. This combined system was conducted continuously, and domestic wastewater was treated. Influent chemical oxygen demand (COD) and NH4+-N concentration were 220-410 mg/L and 36-58 mg/L, and the ratio of nitrification liquid return (r) was 300%. Experiment results indicate that domestic wastewater biodegradability increases by 60% under the function of hydrolysis and acidification. Without external C-source and alkalinity addition, COD, NH4+-N and TN removal efficiency in this system reach 90%, 95% and 74%, where total nitrogen (TN) removal efficiency increases by 12%. When WAS hydrolysis effluent and domestic wastewater are used as denitrifiction C-source respectively, the average maximum NO3--N denitrification rate reaches 0.75 mg/min and 0.66 mg/min. Finally, sludge reduction rate by hydrolysis and acidification technology in H-A-O system reaches 37%. It can be concluded that nitrogen removal efficiency is enhanced.
Key words: hydrolysis and acidification; nitrogen removal; sludge reduction
���ڶ�����ˮ���������ô�ͳ�Ļ������෨��ˮ�����ʽӽ�70%�����ǣ���һ����ߴ�ͳ���յ��ѵ�����Ч��ȴ��Ϊ�˶�����ˮ���������е�ƿ����ͬʱ�������л���ȥ��Ч�ʵ�����ߣ�ʣ���������Ҳ�ڴ����������ʣ������Ĵ����봦�����Ϊ������ˮ������ؽ���������һ���ص����⡣����ɷָ��ӣ����д����ж��к����ʣ���������ɶ�����Ⱦ�������������еĴ����л�̼Դ���ܹ������о��ߵĹ� ע[1-4]�������е��л��ɷֺܸߣ�̼ˮ������ռ50.2%��������ռ26.7%��֬��ռ20.0%[5]��ˮ���ữ��������ʹ�����е��л�̼Դת��Ϊ����ˮ��С������̬����Ҫ����ˮ��[6]���ˮ��[7]���ᷨˮ��[8]��Ͷ�ӻ�ѧ�Լ���ˮ��[9]����������ˮ��[10]�ȡ�ˮ���ữ����������߷�ˮ�Ŀ������ԣ�����������ʣ���ʡ�� ��[11-14]������ˮ���ữ�������Խ������������ܳ����л�̼Դ��������Ϊ��һ������ѵ�����Ч�ʵIJ���̼Դ[15-17]��Kampas��[18]��Ũ�����ʣ��������л�е�����õ��ӷ����л���(VFA)�ͻ�ѧ��Ҫ��(COD)�������Ũ�ȿɴ�850 mg/L��6 530 mg/L��Ϊ��ǿ���ѵ������գ�һЩ��ˮ���Ѿ����ó�������ˮ���ữ��������COD̼Դ[19]��Cecchi��[20]��Ϊ���������п����オ����л����ַ��Ͳ������л����������ǿ�������ѵ�����ϵͳ�����һ����о������ơ�Biradar��[21]�ڲ��������е���������COD���з������о�ʱ���֣���COD���ܵ�(TN)��������Ϊ7ʱ�������η�����ȥ���ʿɴﵽ100%��A-O������Ŀǰ������ˮ������Ӧ����㷺��һ���ѵ�����[22]��Ȼ����������ˮC/N�ϵͣ�ʹ��A-O���շ�����������̼Դ���㣬�����������ס���ˣ��������߽�ˮ���ữ����(H)�ʹ�ͳA-O�������Ϊ�µ�H-A-O���գ����ڸ����ϵͳ�ڿ�����ʵ��������ˮǿ���ѵ���ϵͳ�����������������С�Թ�ģ����ˮ�����о������ϣ���������ýϴ��͵�����ˮ���ữ��Ӧ������������̼Դֱ��Ӧ���ڴ�ͳA-O��Ӧ����ʵ����������ˮһ�廯������Ϊˮ���ữ�������������������̼Դ���������ʵ��Ӧ���ṩ�ο���
1 �����뷽��
1.1 �������
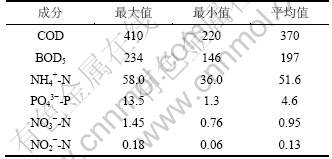
ͼ1��ʾΪ�������̡���ͼ1��ʾ��ˮ���ữ��Ϊ����ʽ���Ϸ�Ӧ��(ͼ2)�����¶��Ϸ�Ϊ������(7 L)��������(4 L)��ǿ����(13 L)�������Ϊ24 L��A-O����Ч���Ϊ54 L��A1~A3Ϊȱ������O1~O6Ϊ���������������Ϊ1:4��A-O��Ӧ����������������Ũ��(MLSS)ά����3 000 mg/L���ҡ�����Һ�Ͳ���ʣ�����������A1ȱ��������ʵ��������ˮΪ������ҵ��ѧ��ְ����������������ˮ����ʵ��������ˮˮ�����1��ʾ��
1.2 ���鷽��
���������Ϊ2�����нΣ���1�Σ�������ˮ���ữ���ײ�����ϵͳ������ˮ��ͣ��ʱ��(tHRT)Ϊ3.5 h������ͣ��ʱ��(tSRT)Ϊ40 d����MLSSΪ3.0~3.5 g/L��A-O��tHRTΪ8 h��tSRTΪ12 d��rΪ300%�����������(R)Ϊ50%�����������ܽ�������Ũ�Ȧ�DO��0.7~3.0 mg/L֮�䣻�ڵ�2�Σ���ʣ�������������ˮͬʱ�����ữ����������ˮ��ˮ�������1��ͬ������tHRTΪ2.4 h��tSRTΪ20 d�����Ц�MLSSΪ8.5~10.0 g/L��A-O�Ц�DO��0.7~4.2 mg/L֮�䡣�����ڼ�ϵͳ�����̼Դ�ͼ�ȡ�
���������ʲⶨ����Ϊ��ʽ���飬����Ч�ݻ���Ϊ1 L�ķ�Ӧ���ڽ��У��¶�Ϊ(25��1) �棬����pH�����ô������������衣��������ȡ��A-O��Ӧ��ȱ������������ˮΪʵ��������ˮ�������ữҺΪ�����������ữ����2�εij�ˮ��

ͼ1 H-A-O��������
Fig.1 H-A-O system schematic layout
��1 ������ˮ��������
Table 1 Characteristics of domestic wastewater mg?L-1
1.3 ��������
ˮ�������˺������ⶨ����������Ϊ��βⶨ��ƽ��ֵ�������ظ���ط��ⶨCOD����Ũ�ȣ����������Լ��ֹ��ȷ��ⶨNH4+-N����Ũ�ȣ�����N-(1-����)-�Ҷ�����ȷ��ⶨNO2--N����Ũ�ȣ���������ݷӷֹ��ȷ��ⶨNO3--N����Ũ�ȣ�������ֽ�������ⶨMLSS����Ũ�ȣ�����WTW DO pH�ⶨ�DzⶨpH��DO���¶ȣ�����BOD5�ⶨ�DzⶨBOD5����Ũ�ȣ��������л�̼(TOC)������(Multi NC3100)�ⶨ���л�̼����Ũ�ȡ�
2 ������������
2.1 ������ˮ�������Ե����
��ˮ�Ŀ����������Լ���������һ����5��������������(BOD5)���(COD)����ӷ�ӳ������������ˮ�����Ѿ��п������ԽϺõ��ص㣬��(BOD5)/��(COD)һ����0.3~0.5֮�䡣�ڱ������1�Σ�������ˮ����ˮ���ữ�������������������ߡ�ͼ2��ʾΪ������ˮˮ���ữ�����еĿ������Ա仯����ͼ2�ɼ���������ˮ��(BOD5)/��(COD)�ɽ�ˮ����0.5������ữ����ˮʱ��0.8��������ˮ����������ˮ���ữ������߶ȵ����߶���������ߡ���˵���������ォ�����ԵĴ�����л�����ͨ��ˮ������ת�����ܽ��Եġ������オ���С���������ͷŵ���ˮ����[23]��
ˮ���ữ��Ӧ���ײ�Ϊ��ˮ��������в�Ϊ��������ͨ����Ӧ����ֱ�����ð���ʵ����ˮ���룻��Ӧ���ϲ�������Ĥ��ά���ϣ�����ˮ�����ˮ���ữЧ������ǿ������ˣ�������ˮ���������ط�Ӧ���߶ȶ�����ǿ����ˮ���ữ��Ӧ���ײ��Ļ�������в��ij�������(TOC)/��(COD)������������0.47������0.74����˵�������е��л����������ܽ����л�̼��ʽ�ܳ������л����ܳ����ʴ����������ʡ��ڷ�Ӧ���ϲ��ͳ�ˮλ�æ�(TOC)/��(COD)�����½�������ά����0.7���ҡ���(TOC)/��(COD)�½�����������������Ĥǿ��������ˮ�����Ũ���Ѿ��ܵͣ�����Ĥ��������õ�������Q����٣����´�ʱ�л�����ܳ�����С������������л�����������ʡ��ڳ�ˮλ�ã���������Ũ�Ⱥܵͣ�����û���л�����ܳ����������������ữ����ˮ��(BOD5)/��(COD)�ͦ�(TOC)/��(COD)��ԭ������ˮ�ֱ�������60%��48.9%��
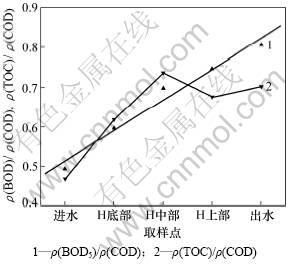
ͼ2 ������ˮˮ���ữ�����еĿ������Ա仯
Fig.2 Variation of wastewater biodegradability during hydrolysis procedure
2.2 H-A-Oϵͳ���л����ȥ��
�������������ڴ����ѽ����ˮ����Ũ�ȷ�ˮ�е��л����H-A-Oϵͳ�У�ˮ���ữ��Ӧ����BOD5��TOC��ȥ���ʵ���10%��A-O��Ӧ�����л����ȥ��Ч����ͼ3��ʾ����2����ͬ���нε��ȶ�״���£�A-O��Ӧ����CODȥ����û�����Ա仯����������������У�����ˮ��(COD)��220~410 mg/L��Χ�ڲ���ʱ��CODȥ�����ȶ���90%���ң���ˮ��(COD)��31~67 mg/L��Χ�ڡ���ͼ3�ɼ�������ˮˮ����ͬʱ��A-O��Ӧ���ڵ�2�����ʱ�ij�ˮˮ���ܽ�ˮ����Ӱ���С(60 d�Ժ�)�����ڵ�1�γ�ˮ�����ϴ�(60 dǰ)����˵��H-A-O��Ϲ�����Ȼû���������CODȥ���ʣ�ȴ��ǿ��ϵͳ���е��ȶ��Լ���������������������������2�Σ�����ʣ������ˮ���ữΪ����A-O��Ӧ���ѵ������˼����������õ�̼Դ������ԭ������ˮ�е�С�����ѽ����л���Ҳ��ˮ���ữΪ������̼Դ����ˣ���ˮˮ�ʸ����ȶ���

ͼ3 CODȥ������ʱ��ı仯
Fig.3 Variation of COD removal efficiency on time
2.3 H-A-Oϵͳ�ѵ�Ч������
ͼ4��ʾΪNH4+-N��TN��ȥ���ʡ���ͼ4�ɼ�����2�ν�ʣ���������ˮ���ữ��Ӧ����δͶ�Ӽ�Ⱥ�������̼Դ��ϵͳ�ѵ�Ч��������ߡ�����ˮ���ữ�������ܳ�COD�������ͷų���������ϸ���еIJ���N��P��ϵͳ��ǰ��2�����н���NH4+-Nȥ����һֱ����95%����ˮNH4+-N����Ũ�ȵ���3 mg/L��A-O��Ӧ��û���ܵ�NH4+-N���������Ӱ�졣�����1�Σ�����������ˮ��û��������ʽ̼Դ��Ϊ���䣬����TNƽ��ȥ����ֻ��62%���ң�TNȥ��Ч�������ܴ�(60 d��ǰ)���ڵ�2�Σ�ʣ������ˮ���ữ������̼ԴΪA-O��Ӧ���ѵ����̲�����̼Դ������ʣ��������Я��������NO3--N�����ữ����Ѹ�ٱ�����������Ҳ�ٽ����ѵ�Ч�ʵ���ߡ���2��TNƽ��ȥ���������74%���ң�ȥ��Ч���ȶ�(60 d�Ժ�)��˵��ͨ�����������ˮ���ữ���������NH4+-N��TN��ȥ���ʣ���ǿ����ϵͳ�ѵ����� ���ԡ�
Ϊ��һ���˽�����ˮ���ữ̼Դǿ��H-A-Oϵͳ�ѵ�Ч����ԭ�ֱ���������ˮ�͵ڶ��ε�ˮ���ữ��Ӧ����ˮΪ̼Դ������ͬ�����½����˷��������顣��ʼ��(COD)��Ϊ270 mg/L��NO3--N����Ũ�Ⱦ�Ϊ35 mg/L��������ˮ��ˮ���ữ��Ӧ����ˮˮ�������ͼ5��ʾ����ͼ5�ɼ���2��ˮ���о���VFA�͵�������ռ������ߣ������ữ��ˮ��VFA����ռ��TOC��47.2%����������ˮ�е�VFA�����߳�14%���ң��������ʺͶ��DZ����ֱ��������ˮ�е�15%��5%���ҡ��ữ��ˮ�������л�̼���(��֬������֬�����)���Ա�������ˮ�жࡣ
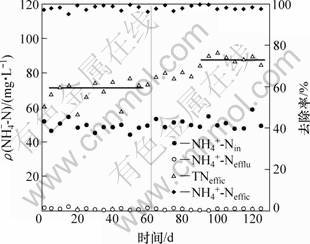
ͼ4 NH4+-N��TN��ȥ����
Fig.4 Removal efficiency of NH4+-N and TN
��ͬˮ����Ϊ̼Դʱ�ķ�����������ͼ6��ʾ����ͼ6�ɼ���������ˮ�ij�ʼNO3--N����������Ϊ0.79 mg/min���ữ��ˮ�ij�ʼNO3--N����������Ϊ0.75 mg/min���ڷ�Ӧǰ40 min���ữ��ˮ�ķ��������ʺ㶨Ϊ0.73 mg/min��40 min���������ʿ�ʼ��0.018 mg/min2���ٶȳ������½���ֱ��60 minһֱ��0.012 mg/min2���ٶȳ������½���90 min��ʱ��Ӧ���ڽ�������������ˮ������������ǰ60 minһֱ��0.012 mg/min2���ٶȳ������½���60 min���������ʵ���0.1 mg/min��ֱ��150 minʱ��Ӧ���ڽ������ɴ�˵�����ữ��ˮ�����ױ����������õ��л������ԭ������ˮ��Ҫ�ḻ�ö࣬��ǰ40 min�ڣ����ŷ������Ľ��У��ữ��ˮ���Դ��ڳ��������������̼Դ����������ˮ�е�����������̼Դȴ�ڼ�����ٲ����ѷ��������ڷ���������һֱ�����Լ�С��H-A-Oϵͳͨ��ˮ���ữ����Ϊ�������ṩ�˽ϴ����������������̼Դ��ʹ�ѵ�����������ߡ�

ͼ5 ��ͬˮ�����л��������
Fig.5 Proportion of organic materials in domestic wastewater and hydrolysis effluent

ͼ6 ��̼ͬԴ��Դʱ�ķ���������
Fig.6 Denitrification rate with different C-source origins
2.4 ʣ�������������
�����2�Σ�ˮ���ữ��Ӧ�����������仯��ͼ7��ʾ����ͼ7�ɼ����������ز���ʣ����������ữ����������������������ӣ�ˮ���ữϵͳ�������������ӣ���ʱˮ���ữ��������Ĵ���������Խϵ͡�ǰ 21 d��������������٣�ÿ�첻��1 g�������������ϵͳ��m(�ӷ��Թ���)/m(�ܹ���)������28 dʱ��ˮ���ữ��Ӧ��������ļ�����������ǿ��ÿ����������������࣬��49 dʱÿ���������������8 g���ң������Ż���������������룬m(�ӷ��Թ���)/m(�ܹ���)�ڵ�49 d���������ֵ70.5%��49 d֮��ˮ���ữ��Ӧ��������ļ������������ȶ�������������������㶨ʱ��ÿ������������㶨��11.1 g���ң�����m(�ӷ��Թ���)/m(�ܹ���)��ʼ��С���ڵ�105 dʱ�Ѽ�С��63.5%�������H-A-Oϵͳ����ʵ��ʣ�������ڲ�ѭ��������ϵͳ�ȶ�����������ʴﵽ37%���ҡ�

ͼ7 ˮ���ữ��Ӧ�����������仯
Fig.7 Changes of sludge quantity in hydrolysis reactor
3 ����
(1) H-A-Oϵͳ�е�ˮ���ữ���ý�������ˮ�Ŀ���������0.5��ߵ�0.8���ҡ�
(2) H-A-Oϵͳ��COD��NH4+-Nȥ����һֱ����90%��95%��ˮ���ữ���������A-O��Ӧ���л���ȥ��Ч�����ȶ��Լ����������������
(3) H-A-Oϵͳͨ���Բ���ʣ�������ˮ���ữ����ΪA-O��Ӧ���ṩ�˷�����̼Դ��TNȥ���ʴﵽ��74%���벻��������̼Դʱ��������12%���������ữ��ˮΪ̼Դʱ��ƽ�����NO3--N���������ʴﵽ0.75 mg/min����������ˮֻ��0.66 mg/min��
(4) ͨ��ˮ���ữ����ʣ����������ﵽ37%��ʵ����ʣ������ϵͳ�ڼ��������á�
�ο����ף�
[1] Bouzas A, Ribes J, Ferrer J, et al. Fermentation and elutriation of primary sludge: Effect of SRT on process performance[J]. Water Research, 2007, 41(4): 747-756.
[2] Mahmoud N, Zeeman G, Gijzen H, et al. Anaerobic stabilisation and conversion of biopolymers in primary sludge-effect of temperature and sludge retention time[J]. Water Research, 2004, 38(4): 983-991.
[3] Ucisik A S, Henze M. Biological hydrolysis and acidi?cation of sludge under anaerobic conditions: The effect of sludge type and origin on the production and composition of volatile fatty acids[J]. Water Research, 2008, 42(14): 3729-3738.
[4] Feng L, Wang H, Chen Y, et al. Effect of solids retention time and temperature on waste activated sludge hydrolysis and short-chain fatty acids accumulation under alkaline conditions in continuous-?ow reactors[J]. Bioresource Technology, 2009, 100(1): 44-49.
[5] Djafer M, Luck F, Rose J, et al. Transforming sludge into a recyclable and valuable carbon source by wet air oxidation[J]. Water Sci Technol, 2002, 41(8): 77-83.
[6] Fisher R A, Swanwick S J. High temperature treatment of sewage sludges[J]. Water Pollut Control, 1971, 71(3): 355-370.
[7] Lin J G, Chang C N, Chang S C. Enhancement of anaerobic digestion of waste activated sludge by alkaline solubilization[J]. Bioresource Technol, 1997, 62(3): 85-90.
[8] Neyens E, Baeyens J, Weemaes M, et al. Hot acid hydrolysis as a potential treatment of thickened sewage sludge[J]. Journal of Hazardous Materials B, 2003, 98: 275-293.
[9] Jiang S, Chen Y G, Zhou Q. Effect of sodium dodecyl sulfate on waste activated sludge hydrolysis and acidification[J]. Chemical Engineering Journal, 2007, 132(1/3): 311-317.
[10] Do?an I, Dilek-Sanin F. Alkaline solubilization and microwave irradiation as a combined sludge disintegration and minimization method[J]. Water Research, 2009, 43(8): 2139-2148.
[11] Coulter J B. Anaerobic process for sewage disposal[J]. Sewage and Industrial Waste, 1991, 29(4): 468-472.
[12] ��ҫ��, ������. ˮ���ữ���ռ���Ӧ���о�[J]. ������������ѧѧ��, 1999, 32(6): 35-38.
SHEN Yao-liang, WANG Bao-zhen. Hydrolysis-acidogenosis process and its application and study[J]. Journal of Harbin University of Civil Engineering and Architecture, 1999, 32(6): 35-38.
[13] �Դ�, ������, �����. ������ˮˮ���ữ���о�[J]. ɽ����������ѧԺѧ��, 2006, 21(2): 154-158.
ZHAO Da-chuan, NI Tao-qing, CUI Qing-jie. Research on domestic sewage treatment by hydrolysis-acidification reactor[J]. Journal of Shandong Jianzhu University, 2006, 21(2): 154-158.
[14] ������, ���. ˮ���ữ/ǰ�÷����������������˳ع��մ���������ˮ[J]. �й���ˮ��ˮ, 2006, 22(12): 63-66.
LI Yong-ze, CHENG Wei. Hydrolysis acidification/pre- denitrification up-flow biological filter used in town wastewater treatment[J]. China Water & Wastewater, 2006, 22(12): 63-66.
[15] Moser-Engeler R, Udert K M, Wild D, et al. Products from primary sludge fermentation and their suitability for nutrient removal[J]. Water Sci Technol, 1998, 38(1): 265-273.
[16] Cokgor E U, Oktay S, Tas D O, et al. Influence of pH and temperature on soluble substrate generation with primary sludge fermentation[J]. Bioresource Technology, 2009, 100(1): 380-386.
[17] Tong J, Chen Y. Recovery of nitrogen and phosphorus from alkaline fermentation liquid of waste activated sludge and application of the fermentation liquid to promote biological municipal wastewater treatment[J]. Water Research, 2009, 43(12): 2969-2976.
[18] Kampas P, Parsons S A, Pearce P, et al. Mechanical sludge disintegration for the production of carbon source for biological nutrient removal[J]. Water Research, 2007, 41: 1734-1742.
[19] Llabres P, Pavan P, Battistioni P, et al. The use of organic fraction of municipal solid waste hydrolysis products for biological nutrient removal in wastewater treatment plants[J]. Water Research, 1999, 33(1): 214-222.
[20] Cecchi F, Battistoni P, Pavan P, et al. Anaerobic digestion of OFMSW and BNR processes: a possible integration: preliminary results[J]. Water Sci Technol, 1994, 30(8): 65-72.
[21] Biradar P M, Roy S B, D��Souza S F, et al. Excess cell mass as an internal carbon source for biological denitrification[J]. Bioresource Technology, 2009, 101(6): 1787-1791.
[22] ������, ������, ����Ө. A/O�ѵ�����Ӱ�����ؼ�����Ʋ��Ե��о�[J]. ��������ҵ��ѧѧ��, 2005, 37(8): 1053-1057.
PENG Yong-zhen, WANG Xiao-lian, WANG Shu-ying. Study on influence factors and control strategies of A/O nitrogen removal process[J]. Journal of Harbin Institute of Technology, 2005, 37(8): 1053-1057.
[23] Kuhn E P. Microbial transformation of substituted benzenes during infiltration of river water to ground water[J]. Environ Sci Technol, 1985(6): 961-968.
(�༭ �°���)
�ո����ڣ�2010-05-25�������ڣ�2010-07-15
������Ŀ��������Ȼ��ѧ����������Ŀ(50808128)��������У�˲�ǿ�̼ƻ��߲���˲�������Ŀ(PHR20090502)�������н�ί�Ƽ�����ƽ̨��Ŀ(PXM2008_014204_050843)
ͨ�����ߣ�������(1949-)���У��������������ˣ����ڣ�������ˮ�����ѵ���������̿��Ʒ�����о����绰��010-67392627��E-mail��pyz@bjut.edu.cn


