DOI��10.19476/j.ysxb.1004.0609.2018.01.25
��������ʪ��ѡ���Խ�����
��ΰ��1, 2���ƿ˺�1��������1���Ŷų�1���� ��1
(1. ���ϴ�ѧ ұ���뻷��ѧԺ����ɳ 410083��
2. ����ԥ���Ǧ�����������ι�˾����Դ 459000)
ժ Ҫ��
��Ը������������Ѷȴ�����⣬������������ڼ���������ϵѡ���Խ�����ķ�������������ض�������ʵ�Ӱ�첢ȷ�������Ž���������ͬʱ�����������Ž��������½����Ľ����ʡ�������������ƹ���ϵ������������Ũ�Ⱥ��¶ȵ����߾������������Ľ����ʣ������ӳ���Ӧʱ���ʹ�����ܽ����������������߽����ٶȿ���ǿ����������������֮�����ɢ���̣�����ϴˮ�ȿ���ʵ�������ȫ�ѳ��������������£���Ľ����ʴﵽ99.0%���ϣ������Ľ����ʷֱ�Ϊ1.50%��0.06%���������������н������ܽ���ʧ��С������Һ���ú������ij��������ʽΪNaSbO��
�ؼ��ʣ�
���±�ţ�1004-0609(2018)-01-0205-07���� ��ͼ����ţ�TF831��TF818���� ���ױ�־�룺A
�����Ѵ�������ǻƽ���ȡ����Ҫ��Դ֮һ[1]�������ຬ���ߵͷ�Ϊ�����Ѵ������(�ຬ��С��15%)������(�ຬ������15%)����[2]�������Ѵ������ͨ����Ϊֱ����ȡ���ԭ�ϣ���������Ϊֱ����ȡ���ԭ�ϡ�
Ŀǰ�����������ҹ��Ĺķ�¯�ӷ����պͶ���˹�ĵ�¯��������[3]���ķ�¯��������[4]�������ڹķ�¯�лӷ�������ʹ����ӷ������������������������˽�Ĺ��࣬�ù����ڹ�������ɽ������ҵ�������ι�˾[5]�ͺ��ϳ��ݿ�ҵ�ɷ�����˾[6]���ص���ұ����ҵ��ù㷺Ӧ�á�����˹�ĵ�¯������ ��[7]���������ڵ�¯�л�ԭ����ʹ��ͽ�ԭ��������У������һ����������������ͬʱʹ���ڵϽ��С�����������Ļ��ն��ǽ���ӷ�����������ʽ�����������ڷ���¯�����ξ�����ԭ��������������;�����Ǧ���̲����ට�����ǣ������е���Ҳ��ӷ����������������ڴ�����Ծ��������������[8]����ʽ�������麬�������Ӳ���ʹ�þ���ʱ���ӳ������ҵ�����ļ�����ʧ���ӣ����ԣ�ұ����ҵͨ���ϸ�����������麬��(ͨ��С��2.0%)[9]��������ʹ�ø�����������ұ����ҵ�ġ����ߡ���
��������[10]������������;������һ���Ǹ��������ѳ�����ùķ�¯�������ջ�����ͽ𣻵ڶ����Ǹ��������ѳ������Ԥ����-�軯����ջ��ս�[11]��ͨ�����õڶ��������Ӹ���������ѡ�����ܽ��࣬�����Լ���ͬ��Ϊ����������ϵ�������Ȼ�����ϵ���֣����Ƕ��������ӻ����[12-13]������Ǧ���[14]������ͭ��[15]���Ѵ������[16]���ѳ��࣬������ϵ������ȱ�㣬���Ǿ���ѡ�ú���ʪ��ұ����ϵ������Ҫ��ֿ��Ǻ����������պ���Һ�������õ�����[17]��
���ڴˣ�������������Ӹ���������ȡ�������������գ�����������������Һ�н������������Һ�ٲ��ü�ѹ������ʽʹ�����Ϊ�������Ʋ� Ʒ[18]����������Һ�����к;�����Ũ���ᾧ�������������Ʋ�Ʒ[19]���ڴˣ��ص��о������������������ϵ�������̵�����Ӱ�죬ͬʱ���������������½������ܽ���Ϊ��Ϊ����������Դ�ĺ����������ṩ�����ָ����
1 ʵ��
1.1 ԭ��
ʵ��ԭ�����Ĵ�ʡ������ɽʢ��ҵ����˾�����ĸ������ý��110 ������ɸ�֣��Ա�֤100%����74 ��m��ɸ�������������Ҫ��ѧ�ɷּ���1��
��ʵ���������ƺ��������ƾ�Ϊ�����������������XRD��ͼ1����ͼ1���Կ������ø���������Ҫ�л���������������Ͷ������裬�����жϣ������ֱ��Ի��������������̬���ڡ�
��1 �����������Ҫ��ѧ�ɷ�
Table 1 Main chemical composition of high-arsenic antimony-gold concentrate (mass fraction, %)


ͼ1 ���������XRD��
Fig. 1 XRD pattern of high-arsenic antimony-gold concentrate
1.2 ����ԭ����ʵ�鷽��
1.2.1 ����ԭ��
�����������������Sb2S3��Na2S������Ӧ��ʹ����Na3SbS3��ʽ������Һ������NaOH��������Na2S��ˮ�⣬�������̷����Ļ�ѧ��Ӧ���£�
Sb2S3+3Na2S=2Na3SbS3 (1)
Na2S+H2O=NaOH+NaHS (2)
1.2.2 ʵ�鷽��
������������ƽ���ʵ������250 mL�������ձ��н��С��������ձ������䱸�д����������ĺ���ˮԡ�У�����Ҫ��Ũ�ȵ����ƺ��������ƻ����Һ�������¶���Ҫ����ֵʱ����50 g����������Ҫ�����ǿ���·�Ӧһ��ʱ�䣬��Ӧ��ɺ���չ��ˣ�ȡ����Һ���������������ϴ��ˮ�������㵹ϴ�ӣ��˱���110 ���ɺ�����������������Ǹ��������ܽ���ռ�ܽ������ķ������䰴ʽ(3)���㣺
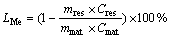 (3)
(3)
ʽ�У�LMeΪ����������(%)��mmat��mres�ֱ�Ϊԭ�Ϻͽ�����������(g)��Cmat��Cres�ֱ�Ϊԭ�Ϻͽ������н�������(%)��
1.3 ������������
��Ʒ�н�����������ICP-AES�����Dzⶨ(�����ȵ繫˾IRIS Interprid �� XRS�͵����ϵ������巢�������)��������Ʒ���������XRD�����Dzⶨ(�ձ���ѧTTRAX-3�ͣ���Ӧ�IJ��Ե�ѹΪ50 kV�����Ե���Ϊ300 mA��ɨ������Ϊ10 (��)/min)��������Ʒ����ò����SEM����(Japan Jeol JSM-6360LV��20 kV)��
2 ���������
�ڼ���������ϵ����������������е��࣬��ϸ�о������ƹ���ϵ������������Ũ�ȡ��¶ȡ�Һ�̱�(Һ�����(L)���������(kg)֮��)��ʱ�䡢�����ٶȺ�ϴˮ��(ˮ���(L)���������(kg)֮��)�����ض����ƽ������̵�Ӱ�졣
2.1 ���ƹ���ϵ����������ʵ�Ӱ��
���ʵ��������������������Ľ����ʣ����ǹ��ߵĹ���ϵ��������Һ��������������ѡ���ʼ�������£�Һ�̱�L/S=4.0��NaOHŨ��20 g/L����Ӧ�¶�50 �桢ʱ��2 h�������ٶ�180 r/min��ϴˮ��2.0���������ƹ���ϵ����������ʵ�Ӱ�죬�����ͼ2��

ͼ2 ���ƹ���ϵ����������ʵ�Ӱ��
Fig. 2 Effect of Na2S excess coefficient on Sb leaching rate
��ͼ2���Կ������������ƹ���ϵ�������ӣ���Ľ����������Ӻֲ��䣬�����ƹ���ϵ����0.90������1.0ʱ�����������ຬ����1.4%������0.50%����Ľ�������98.0%�����99.2%�������������ƹ���ϵ������Ľ����ʻ������䡣�����Ǧ���[14]������ͭ��[15]�����ƽ��������������𣬸�����������������̬���ڵ������������Ϊ�������Ľ����ʺͼ������Ƶ����ģ�ѡ�����ƹ���ϵ��Ϊ1.0�ȽϺ�����
2.2 ��������Ũ�ȶ�������ʵ�Ӱ��
����NaOH�������������Ƶ�ˮ�ⷴӦ��������ʼ���������ƹ���ϵ��1.0��Һ�̱�L/S=4.0����Ӧ�¶�50 �桢ʱ��2 h�������ٶ�180 r/min��ϴˮ��2.0�������������Ƴ�ʼŨ�ȶ�������ʵ�Ӱ�죬�����ͼ3��

ͼ3 �������Ƴ�ʼŨ�ȶ�������ʵ�Ӱ��
Fig. 3 Effect of NaOH concentration on Sb leaching rate
��ͼ3���Կ�����������������Ũ����ߣ���Ľ������������ӣ����������ຬ�����ͱȽ����ԣ�����������Ũ�������20.0 g/Lʱ����Ľ�����������99.0%���ϣ����������������Ũ�ȣ�����������Ӳ����ԡ����ߵ���������Ũ�Ȼᵼ�º����Ѵ�����������Կ�����ܽ�(����������)������ѡ����������Ũ��Ϊ20.0 g/L�ȽϺ�����
2.3 �¶ȶ�������ʵ�Ӱ��
��߷�Ӧ�¶������ڴٽ���ѧ��Ӧ���С���ʼ�������£����ƹ���ϵ��1.0����������Ũ��20 g/L��Һ�̱�L/S=4.0��ʱ��2 h�������ٶ�180 r/min��ϴˮ��2.0�������¶ȶ�������ʵ�Ӱ�죬�����ͼ4��
��ͼ4���Կ������¶ȶ�������ʵ�Ӱ����ֽ��Ա仯������Ӧ�¶Ȳ�����35 ��ʱ�����������ຬ��ֻ�ܽ�����0.80%���ң���Ľ�����Ϊ98.80%���ң������¶�������50�漰����ʱ�����������ຬ��������0.50%���ң���Ľ����ʴﵽ99.27%��ͬʱ�������¶���������߹����ٶȣ�˵����߷�Ӧ�¶ȶ������ƽ��������������ģ����Ƿ�Ӧ�¶ȵ�����������Һ�ӷ���ʹ�����������ۺϿ���������ʡ������ٶȺͲ������������أ�ѡ������¶�Ϊ50 �档

ͼ4 �¶ȶ�������ʵ�Ӱ��
Fig. 4 Effect of temperature on Sb leaching rate
2.4 Һ�̱ȶ�������ʵ�Ӱ��
��ʼ�������£����ƹ���ϵ��1.0����������Ũ��20 g/L���¶�50 �桢ʱ��2 h�������ٶ�180 r/min��ϴˮ��2.0������Һ�̱ȶ�������ʵ�Ӱ�죬�����ͼ5��
��ͼ5���Կ���������Һ�̱ȵ������������ຬ��ʼ��ά����0.50%���ң���Ľ����ʱ�����99.2%���ң���Һ�̱ȶ�������ʵ�Ӱ���С�����ǣ�Һ�̱ȵ���С�������ᵼ�½���Һ����Ũ�ȵ������С������Һ��Ũ�ȹ���������������������ʱ���ӳ�����Һ��Ũ��̫����������Ч�ʣ�Ϊ�˱��ں����������������Һ��ѹ�����Ʊ��������Ʋ�Ʒ��������Һ��Ũ�Ȳ�����150 g/L�ȽϺ��ʣ����ԣ�ѡ��Һ�̱�Ϊ3.0�ȽϺ�����
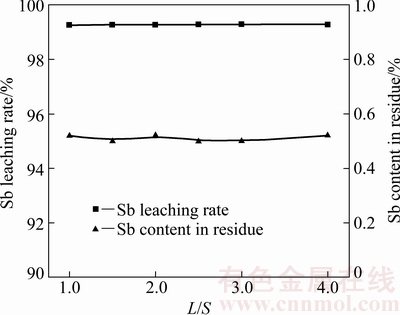
ͼ5 Һ�̱ȶ�������ʵ�Ӱ��
Fig. 5 Effect of L/S on Sb leaching rate
2.5 ʱ���������ʵ�Ӱ��
��ʼ���������ƹ���ϵ��1.0����������Ũ��20 g/L���¶�50 �桢Һ�̱�L/S=3.0�������ٶ�180 r/min��ϴˮ��2.0������ʱ���������ʵ�Ӱ�죬�����ͼ6��
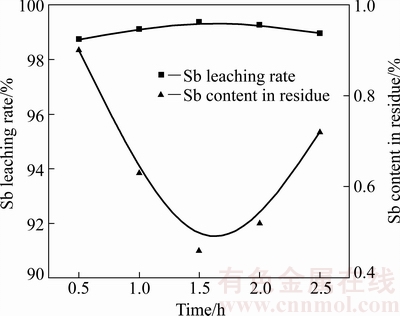
ͼ6 ʱ���������ʵ�Ӱ��
Fig. 6 Effect of time on Sb leaching rate
��ͼ6���Կ������ʶȵ��ӳ���Ӧʱ�������������Ľ����ʣ�����Ӧʱ��Ϊ1.5 hʱ���������е��ຬ��������0.46%����Ľ����ʴﵽ99.34%�������ӳ���Ӧʱ�䣬���������ຬ�������ߣ����Ӧ��Ľ����ʻ������͡���ԭ����������ڷ�Ӧʱ����ӳ���������Һ���������������������������ʽ������Һ�е��౻�����е�������������[20]���������Խ���������ʽ�����������У�����ʹ��������ʽ��ͣ������Ļ�ѧ��Ӧ��ʽ(4)��
2Na3SbS3+7O2+2NaOH+5H2O=2NaSb(OH)6+3Na2S2O3 (4)
��ѡ��Ӧʱ��Ϊ1.5 hΪ�ˡ�
2.6 �����ٶȶ�������ʵ�Ӱ��
��ʼ�������£����ƹ���ϵ��1.0����������Ũ��20 g/L���¶�50 �桢Һ�̱�L/S=3.0����Ӧʱ��1.5 h��ϴˮ��2.0����������ٶȶԽ������̵�Ӱ�죬�����ͼ7��
��ͼ7���Կ��������Ž����ٶȵ���������
���ຬ�����罵�ͣ���Ľ�������Ѹ�����ӣ��������ٶ���0�����180 r/minʱ�����������ຬ����25.66%������0.52%����Ľ�������40.94%��ߵ�99.26%��˵�������ٶȶ�������ʵ�Ӱ��ϴ�����������ڸ���������ܶȽϴ�(���������ܶ�3.50 g/cm3)�����������費���ʱ����������������Һ��ֽӴ���������Ľ����ʱȽϵ͡����ǣ������ٶȹ�������ʹ��Һ����Ŀ���������Һ���������������������Һ���������µĽ������ຬ�����ӡ����ԣ�ѡ������ٶ�Ϊ180 r/min�ȽϺ��ʡ�
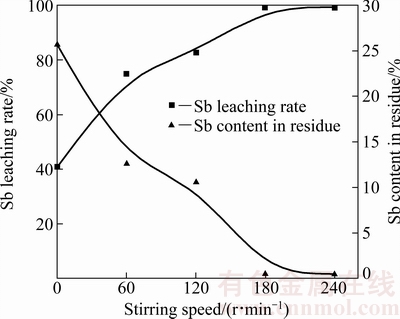
ͼ7 �����ٶȶ�������ʵ�Ӱ��
Fig. 7 Effect of stirring speed on Sb leaching rate
2.7 ϴˮ�ȶ�������ʵ�Ӱ��
��ʼ�������£����ƹ���ϵ��1.0����������Ũ��20 g/L���¶�50 �桢Һ�̱�L/S=3.0����Ӧʱ��1.5 h�ͽ����ٶ�180 r/min������ϴˮ�ȶԽ������̵�Ӱ�죬�����ͼ8��
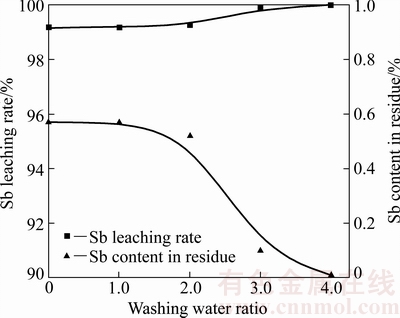
ͼ8 ϴˮ�ȶ�������ʵ�Ӱ��
Fig. 8 Effect of washing water ratio on Sb leaching rate
��ͼ8���Կ���������ϴˮ�ȵ����ӣ����Ƚ��������ຬ�����н��ͣ���ϴˮ����1.0�����2.0ʱ�����������ຬ������0.57%������0.52%����Ľ�������Ȼ��99.20%���ң�����������ϴˮ�ȣ����������ຬ����Ѹ�ٽ��ͣ���ϴˮ��������4.0ʱ�����������ຬ��������0.01%���ң���Ľ����ʴﵽ99.99%��������ϴˮ�������������ȫ�ѳ���������ĺ�������0.50%���ҽ�����0.01%��˵�������ܶȴ�ĸ�������Խ���Һ�ļ����������ԣ�������ϵͳˮѭ�����ýǶȿ��ǣ������ʵ�ϴˮ�����б�Ҫ�ģ�ѡ�����ϴˮ��Ϊ2.0��ϴ��ˮ���Ժ���������һ�ν���ʹ�á�
2.8 ��������
ͨ���о�ȷ�������������ƽ������������������£����ƹ���ϵ��1.0����������Ũ��20 g/L���¶�50 �桢Һ�̱�L/S=3.0����Ӧʱ��1.5 h�������ٶ�180 r/min��ϴˮ��2.0�������������½���1000 g�����������飬����������Ϊ50.0%���ң����������ຬ��Ϊ0.50%���ң���Ľ����ʴﵽ99.0%���ϣ�����������Ҫ��ѧ�ɷּ���2��
���������������XRD���������ͼ9����ͼ9���Կ�������������ֻ�л������������Ͷ�����������࣬������������ȫ��ʧ��˵�����ƽ�������ʵ���˸��������������Ч�ѳ���
��2 ����������Ҫ��ѧ�ɷ�
Table 2 Main chemical composition of leach residue (mass fraction��%)


ͼ9 �����������ƽ�������XRD��
Fig. 9 XRD pattern of leaching residue
2.9 �������ܽ���Ϊ
�о��˸����������ƽ����������������½������ܽ���Ϊ�����������û��Խ��ⶨ����������Һ����ICP-MS�ⶨ��Һ�н����ĺ��������ݽ����������ͽ���Һ����ֱ��������Ľ����ʣ��������3��
��3 ���ƽ������̽����Ľ�����
Table 3 Leaching rates of gold and arsenic during leaching process of sodium sulfide

�ɱ�3���Կ���������������Ũ��Ϊ125.0 g/L��������Һ�н���ʱ�����ݽ���Һ�н����Ũ�ȼ��㣬��������߽����ʷֱ�Ϊ1.50%��0.06%���Խ������н���麬�����㣬��������߽����ʷֱ�Ϊ0.31%��0.05%��˵���ڴ������¸����������ƽ������̣��������ܽ���ʧ�dz�С���������Ժ��Բ��ơ�
2.10 ����Һ������
�����������ƽ������̵��Ͻ�����Һ�̷������Һ����48 h����Һ������һ�ֺ�ɫ�������ó�����100 mLˮϴ�Ӻ���110 ���ɣ�ͨ��X����ӫ�����(XRF)�����Ϊ(%)��Sb74.52��Na14.05��O10.75���ó������SEM��EDS��ͼ10��
��ͼ10���Կ������ó�������ֲ�������״����Ҫ�����ࡢ�ƺ���3��Ԫ�أ�����XRF����������жϣ��ó�����ķ���ʽΪNaSbO����˵�������Ѵ�������д�������һ��̬�����ÿ��������ܽ��ڽ���Һ�У��������Һ���ù����ֻ�ᾧ������
3 ����
1) �о���ȷ���˸����������ƽ��������������������ƹ���ϵ��1.0����������Ũ��20 g/L���¶�50 �桢Һ�̱�L/S=3.0����Ӧʱ��1.5 h�������ٶ�180 r/min��ϴˮ��2.0������������Ϊ50.0%���ң����������ຬ��Ϊ0.50%���ң���Ľ����ʴﵽ99.0%���ϡ�
2) �������ƹ���ϵ���������������Ũ�������ڽ��ͽ��������ຬ���������¶Ȳ������Խ��ͽ��������ຬ�������ҿ�����߹����ٶȣ�Һ�̱ȶԴ����ܶȴ�ĸ����������ƽ������̵�Ӱ���С�������ӳ���Ӧʱ���ʹ�����ܽ����������������������ٶ�������ǿ����������������֮�����ɢ���̣����������Ľ����ʣ�����ϴˮ����ʵ�ָ��������������ȫ�ѳ���
3) ������������ƽ������������������£��Խ���Һ�н���Ũ�ȼƽ�������߽����ʷֱ�Ϊ1.50%��0.06%���Խ������н��������ƽ�������߽����ʷֱ�Ϊ0.31%��0.05%��˵�����������н������ܽ���ʧ��С������Һ�������ú������ĺ�ɫ���������ʽΪNaSbO��
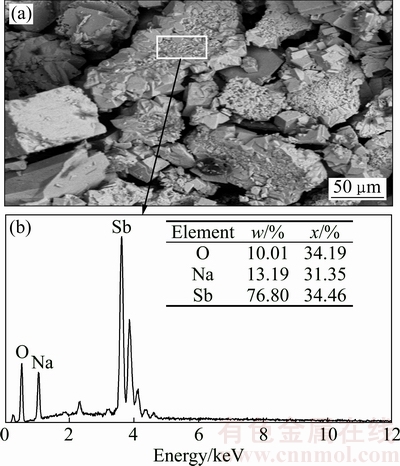
ͼ10 ����Һ�������SEM��EDS��
Fig. 10 SEM image and EDS spectrum of precipitate from leaching solution
REFERENCES
[1] GEORGE M W. Gold[J]. U. S. Geological Survey Mineral Yearbook, 2014(5): 1-18.
[2] ������. �����ұ��Ʒ��ӹ�[M]. ��ɳ: ���ϴ�ѧ������, 2005: 210-248.
YANG Tian-zu. Metallurgy and product of precious metals[M]. Changsha: Central South University Press, 2005: 210-248.
[3] LIU Wei-feng, YANG Tian-zu, ZHANG Du-chao, CHEN Lin, Liu Yun- feng. A new pyrometallurgical process for producing antimony white from by-product of lead smelting[J]. JOM, 2014, 66(9): 1694-1700.
[4] LIU Wei-feng, YANG Tian-zu, JIANG Ming-xi , LIU Wei, DOU Ai-chun. Improvements on the process of gold-antimony concentrate smelting in China[C]//HOWARD S M. Extraction & Processing Division. New Orleans: TMS, 2008: 121-128.
[5] ��С��, ���, ������, �� ��, �Ƴ���, ������, ������. �ɻ������¹���������ȡ����[J]. �й���ɫ����ѧ��, 2012, 22(10): 2896-2901.
LIU Xiao-wen, YANG Jian guang, WU Yong tian, LI Jing, TANG Chao bo, CHEN Yong ming, TANG Mong tang. Separationofneedle antimony from stibnite through low- temperature sulfur fixing smelting process[J].The Chinese Journal of Nonferrous Metals, 2012, 22(10): 2896-2901.
[6] ������, ������, ������. ��ұ��������״���о���չ�뽨��[J]. ������ɫ����, 2015, 31(3): 45-50.
LI Liang-bin, XU Xing-liang, CHEN Xiao-chen. Present situation and development of atimony metallurgical process[J]. Hunan Nonferrous Metals. 2015, 31(3): 45-50.
[7] MYZENKOV F A, TARAOV A V. Development and creation of modern metallurgical technology for antimony production with gold recovery from domestic gold-antimony concentrates in Russia[C]//KONGOLI F, REDDY R G. Proceedings of Sohn International Symposium. San Diego: TMS, 2006: 121-128.
[8] ������, ����Ԫ, ������. ��ұ��������м���Դ�ۺϻ��չ�ҵ�����о�[J].������ɫ����,2014, 30(3): 24-27.
DENG Wei-hua, CHAI Li-yuan, DAI Yong-jun. Industrial experimental study on comprehensive recoverying valuable resources from antimony smelting arsenic alkali residue[J]. Hunan Nonferrous Metals, 2014, 30(3): 24-27.
[9] �� ��, ʯ ��, ���컪, ��ѧ��. �����̳�������Ʊ��������Ƶ��¹���[J]. �й���ɫ����ѧ��, 2015, 25(1): 241-249.
YI Yu, SHI Jing, TIAN Qing-hua, GUO Xue-yi. Novel technology for preparation of sodium pyroantimonate from alkali leaching residue of high arsenic dust[J]. The Chinese Journal of Nonferrous Metals, 2015, 25(1): 241-249.
[10] ������, ������. ��ѡұ���ʯ����[M]. ����: ���ʳ�����, 1997: 20-48.
NIE Shu-ren, SUO You-rui. Leaching of gold from refractory gold ore[M]. Beijing: Geology Publishing House, 1997: 20-48.
[11] CELEP O, ALP I, DEVECI H. Improved gold and silver extraction from a refractory antimony ore by pretreatment with alkaline sulphide leach[J]. Hydrometallurgy, 2011, 105: 234-239.
[12] UBADINI S, VEGLIO F, FORNARI P, ABBRUZZESE C. Process of flow-sheet for gold and antimony recovery from stibnite[J]. Hydrometallurgy, 2000, 57(5/6): 187-199.
[13] ZHAO Tian-cong. Metallurgy of antimony[M].Changsha: Central South University of Technology Press, 1987: 358-462.
[14] YANG Tian-zu, JIANG Ming-xi, LAI Qiong-gen, CHEN Jin-zhong. Sodium sulfide leaching of low-grade jamesonite concentrates in production of sodium pyroantimoniate[J]. Journal of Central South University Technology, 2005, 12(3): 290-294.
[15] CURRELI L, GARBARINO C, GHIANI M, ORRU G. Arsenic leaching from a gold bearing enargite flotation concentrate[J]. Hydrometallurgy, 2009, 96: 258-263.
[16] ��Ƚ��, �� ��, �� ��, ������. �������ƽ������������н�����Ϊ[J].��ɫ����(ұ������), 2014(7): 38-41.
JIN Ran-gong, WANG Yun, LI Yun, SUN Liu-gen. Behavior of gold and antimony during leaching of Sb-bearing gold concentrate with sodium sulfide[J]. Nonferrous Metals (Metallurgy Part), 2014(7): 38-41.
[17] RUIZ M C, GRANDON L, PADILLA R. Selective arsenic removal from enargite by alkaline digestion and water leaching[J]. Hydrometallurgy, 2014, 150: 20-26.
[18] ZHANG Du-chao, XIAO Qing-kai, LIU Wei-feng, CHEN Lin, YANG Tian-zu . Pressure oxidation of sodium thioantimonite solution to prepare sodium pyroantimonate[J]. Hydrometallurgy, 2015, 151: 91-97.
[19] ������, �� ��, ��͢ʡ. �������������軯β������ͭп�����Ļ����[J].�й���ɫ����ѧ��, 2016, 26(9): 1982-1989.
YANG Xiu-li, HUANG Xiong, QIU Ting-sheng. Activation of sodium metabisulfite on surfaces of copper-zinc sulfide ore in cyanidation tailings[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(9): 1982-1989.
[20] YANG Tian-zu, LAI Qiong-lin, TANG Jian-jun, Chu-guang. Precipitation of antimony from the solution of sodium thioantimonite by air oxidation in the presence of catalytic agents[J]. Journal of Central South University of Technology, 2002, 9(2): 107-111.
Selective leaching of antimony from high-arsenic antimony-gold concentrate
LIU Wei-feng1, 2, HUANG Ke-hong1, YANG Tian-zu1, ZHANG Du-chao1, CHEN Lin1
(1. School of Metallurgy and Environment, Central South University, Changsha 410083, China;
2. Henan Yuguang Gold and Lead Group Co., Ltd., Jiyuan 459000, China)
Abstract: Aiming at solving the problem of difficult utilization, a novel method for selective leaching of antimony from high-arsenic antimony-gold concentrate in alkaline sulfide solution was proposed. The effect of various factors on the leaching rates of antimony was investigated, and these leaching rates of gold and arsenic were also studied at the optimum conditions. The results show that the Na2S excess coefficients, NaOH concentration and temperature increase are beneficial to promote the leaching rate of antimony. Antimony content in the leaching residue can be decreased with increasing the temperature. Antimony dissolved in the leaching solution will be oxidized and precipitated in the residue with excessive prolonging time. Increasing stirring speed can improve the diffusion between sodium sulfide and concentrate. Antimony will be removed completely by increasing washing water ratio. Under the optimum conditions, the leaching rate of antimony reaches more than 99.0%, and the leaching rates of gold and arsenic are 1.50% and 0.06%, respectively. It indicates that antimony can be removed efficiently from antimony-gold concentrate, meanwhile, the dissolved losses of gold and arsenic are negligible. A black deposit of NaSbO can be precipitated from leaching solution.
Key words: antimony-gold concentrate; leaching; antimony; arsenic; sodium sulfide
Foundation item: Project(51404296) supported by the Young Scientists Fund of National Natural Science Foundation of China; Project(2016M60247) supported by China Postdoctoral Science Foundation
Received date: 2016-11-09; Accepted date: 2017-03-22
Corresponding author: ZHANG Du-chao; Tel: +86-13787003744; E-mail: zdc015@sina.com
(�༭ ������)
������Ŀ��������Ȼ��ѧ�������������Ŀ(51404296)���й���ʿ���ѧ��������������Ŀ(2016M602427)
�ո����ڣ�2016-11-09�������ڣ�2017-03-22
ͨ�����ߣ��Ŷų�����ʦ����ʿ���绰��13787003744��E-mail��zdc015@sina.com
ժ Ҫ����Ը������������Ѷȴ�����⣬������������ڼ���������ϵѡ���Խ�����ķ�������������ض�������ʵ�Ӱ�첢ȷ�������Ž���������ͬʱ�����������Ž��������½����Ľ����ʡ�������������ƹ���ϵ������������Ũ�Ⱥ��¶ȵ����߾������������Ľ����ʣ������ӳ���Ӧʱ���ʹ�����ܽ����������������߽����ٶȿ���ǿ����������������֮�����ɢ���̣�����ϴˮ�ȿ���ʵ�������ȫ�ѳ��������������£���Ľ����ʴﵽ99.0%���ϣ������Ľ����ʷֱ�Ϊ1.50%��0.06%���������������н������ܽ���ʧ��С������Һ���ú������ij��������ʽΪNaSbO��
[1] GEORGE M W. Gold[J]. U. S. Geological Survey Mineral Yearbook, 2014(5): 1-18.
[2] ������. �����ұ��Ʒ��ӹ�[M]. ��ɳ: ���ϴ�ѧ������, 2005: 210-248.
[6] ������, ������, ������. ��ұ��������״���о���չ�뽨��[J]. ������ɫ����, 2015, 31(3): 45-50.
[8] ������, ����Ԫ, ������. ��ұ��������м���Դ�ۺϻ��չ�ҵ�����о�[J].������ɫ����,2014, 30(3): 24-27.
[9] �� ��, ʯ ��, ���컪, ��ѧ��. �����̳�������Ʊ��������Ƶ��¹���[J]. �й���ɫ����ѧ��, 2015, 25(1): 241-249.
[10] ������, ������. ��ѡұ���ʯ����[M]. ����: ���ʳ�����, 1997: 20-48.
[16] ��Ƚ��, �� ��, �� ��, ������. �������ƽ������������н�����Ϊ[J].��ɫ����(ұ������), 2014(7): 38-41.


