DOI: 10.11817/j.ysxb.1004.0609.2020-37570
���ڸ�Ĥ���������Ǧ��ʪ����Ǧ�¹��ռ��绯ѧ����
�� ������㣬�����裬���곿�����ij���������
(���ϴ�ѧ ұ���뻷��ѧԺ����ɳ 410083)
ժ Ҫ��
��������ƽ��͵��ƽ��ԭ������Pb(��)-Ac--H+-H2O��ϵ��������ѧ������������������ڽӽ���ʵ�ʽ���Һ��pHֵ��Χ�ڣ���Һ��PbAc+ƽ��Ũ����ߡ���ʪ����п����������Ǧ��Ϊԭ�ϣ����õ�����ʵ�鷨�Ż�����������λ����-��Ĥ�����ȡǦ������Ҫ�������������õ��������鷨�Ż�����Ǧ��Һ��Ĥ���������������������ɨ�衢ѭ�������ȵ绯ѧ�����ֶ��о�Pb(��)-Ac--H2O��ϵǦ��������������绯ѧ��Ϊ������������ڷ�Ӧʱ��1 h�������¶�70 �桢�����Ũ��4 mol/L��Һ�̱�4:1���Ż������½�������Ǧ����Ǧ������93.28%���ڵ���¶�30 �桢Pb2+Ũ��50 g/L�������ܶ�100 A/m2����������������Ч��98%���ң�ÿ��Pbֱ�����Լ700 kW��h���ڴ�������������Ǧ������Һֱ����Ϊ���Һ��Ĥ���8 h���������Ի�ô���99.2%��Ϊ����ƽ���ĵ�Ǧ����������Ч��96.16%��Ǧ�Ļ�ԭ����������һ����������̣�Ǧ�ڵ����������ѭ��ά�����ɺ������������ƣ������¶Ⱥ��������ҺPb2+Ũ�ȿ��Դٽ���Һ������ɢ����ߵ���Ч�ʡ�
�ؼ��ʣ�
����Ǧ������������ϵ����λ��������Ĥ��������绯ѧ������
���±�ţ�1004-0609(2020)-07-1677-14���� ��ͼ����ţ�TF81���� ���ױ�־�룺A
��ͳʪ����п�����У���������������Ǧ�������⣬�������̳�����ͭ���̳��Ⱦ���ԭ�ӷ������õ����̳���ͬ������Ǧ�����ֺ�Ǧ�̳�������������γ�����Ǧ���������ڽ�������[1]����Щ����Ǧ���е�Ǧ����PbSO4��������ڣ�Ǧ����һ��Ϊ10%~50%[2]��ʵ������Դ�����������������þ�����Ҫ���塣
Ŀǰ�������Ǧ���Ĵ������տɷ�Ϊ��ʪ�����ࡣ������Ҫ�ǽ�����Ϊ��Ǧԭ�ϣ���Ǧ����һͬ�������Ǧұ��ϵͳ����Ǧ[3]������������Ǧ����Ǧ������Խϵͣ�����PbS����������ȣ�����Ǧ�ķֽⴿ�����ȷ�Ӧ���Ӷ���Ҫ�ⲿ���Դ��������ܡ���ˣ����������¯��PbS����һ������ʱ������������ޣ���������ά��Ǧұ��ϵͳ����ƽ��[4]�����⣬���մ�������Ǧ�������ܺĸߣ������ײ�����Ũ��SO2���ӷ���Ǧ���ȴ�����Ⱦ��������������ɱ���Ը���[5]��ʪ��������Ŀǰ���������Ǧ��������������Ҫ�������ν����û���Ǧ[6]���Ȼ���-�����Ͻ�����Ǧ[7]�Լ�̼��ת�ͽ�����Ǧ[8]�ȡ�̼��ת�ͺ�������ֽν���õ���Ǧ��ʽ����Na2CO3��NaHCO3Ϊ�����������Һǿ���������½�����Ǧ����PbSO4ת��ΪPbCO3���ٽ�PbCO3���ջ��������������������ϵ���õ�Ǧ��[9-10]����ʵ��֤��������Ǧ��ʪ���������մ���ת���ʵ͡���ˮ�ŷ����������ϵ���ʱ���ͷ�HF���ж��к����������[11]�����Ź��ҶԻ����������ȵIJ��ϼӴ�����һ����ࡢ��Ч������Ǧ�������¹��վ����ش���ʵ���塣����������⣬����������������ڴ�ͳ������ʽ���������λ������������Ǧ������ʵ��Ǧ�ĸ�Ч���պ�����������÷������кܺõĻ��������ü�ֵ��
�����������Ŷ��з���һ�ֻ��ڸ�Ĥ�������[12-13]��ʪ��ұ���¹��գ��ù����ѳɹ�ʵ�ִӺ������ࡢ�����ɫ������Դ����ࡢ��Ч��ȡ��[14]����[15]����[16]�Ƚ������¹��վ������̶̡�����Ч���ŵ㡣���о���Ŀ�IJ����dz��Խ���Ĥ�����������չӦ����Ǧ����Դ��������[17]��ͬʱҲ��Ϊ�˽��Ǧ��Ϊ��۽����ڴ�ͳ����������ж�������������������ɵĶۻ����⣬���ø�Ĥ��������ܹ���Ч�����������������������ɢ���Ӷ�������������������������Ӧ[18-19]��ͨ���Ż����ղ������Ӷ���û��ڸ�Ĥ�������������Ǧ����ദ��������Ϊʵ�ִ�������������Ǧ��������Ч����Ǧ�ṩ�ο���
1 ʵ��
1.1 ����ԭ��
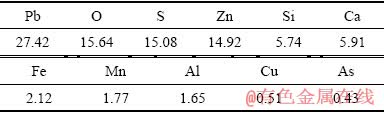
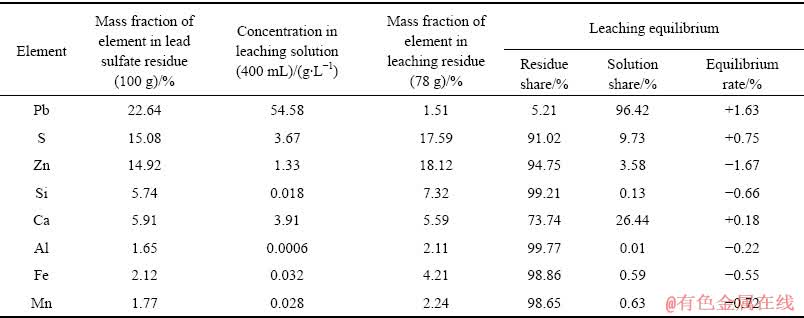
���������õ�ԭ��Ϊ����ij��п��ҵпұ������������������Ǧ����������Ҫ��ѧ�ɷ־�XRF������±�1���У�������ɾ�XRD��������ͼ1��ʾ������Ǧ�����༰��ɲ��û�ѧ�������������±�2���С�
��������������������õ�ԭ��������PbSO4Ϊ����Ҳ��������ZnS��PbS�Լ�CaSO4�ȣ����ϴ�ͳʪ����п���̲�������Ǧ���ĵ���������ԭ����Ǧ�Ķ���������������������Ǧ����PbSO4���ำ���Ǧ����Ϊ22.64%�����о���Ҫ�������������λ�������ֵ�Ǧ����˱����м�������Ǧ����Ǧ�Ľ�����ʱ�Կ���λ�ܽ��PbSO4Ϊ��
�о����õ���������ѧ�Լ��������Ϊ����ͷ����¤��������˾���ã���Ϊ����������
��1 ����Ǧ����Ҫ��ѧ�ɷ�
Table 1 Main element content of lead sulfate residue (mass fraction, %)
��2 ����Ǧ���и����ຬǦ��
Table 2 Lead content of different phase in lead sulfate residue (mass fraction, %)

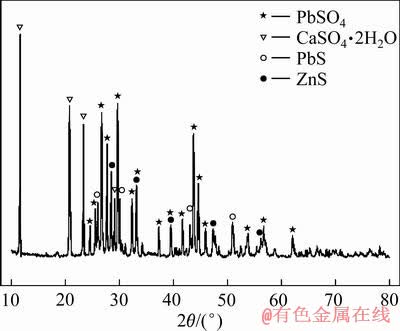
ͼ1 ����Ǧ��ԭ��XRD��
Fig. 1 XRD pattens of lead sulfate residue
1.2 ��������
�������о���������ʾ��ͼ��ͼ2��ʾ������Ǧ��ͨ����������λ��������һ��Ũ�ȵ��������ҺΪ����Һ����������λ����Һ��Ϊ����Һ���и�Ĥ�������������������õ���Ǧ�����������Һ����������ʹ�ã��������Һ������Ⱥ������Ϊ����Һʹ�á�
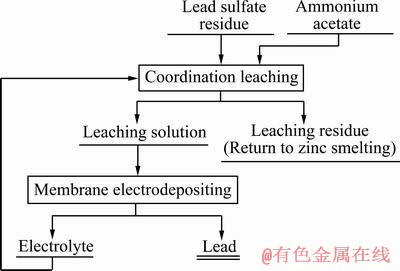
ͼ2 ���鹤������ͼ
Fig. 2 Test flow chart
1.3 ����ԭ��
1.3.1 ������������ѧ����
��������ƽ��͵��ƽ���˫ƽ��ԭ������Ա����о���Ҫ���������Ϻͽ��������ۺϿ���Pb(��)-Ac--H+-H2O��ϵ��Pb2+��Ac-�ļ�����λ��ʽ����ʽ(1)~(4)��ʾ�������ƽ������ѧ�������۷���������ϵ����Ҫ���ڵ�������Pb2+��PbAc+��PbAc2�� ��
��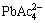 ��Ac-��H+��OH- (Ϊ���ڼ�������ʵ������ϵ��H+Ũ�Ƚϵͣ���Ac-ˮ��̶�С���ʲ�����Ac-ˮ�������)�����б�״̬��Pb2+�������(Ac-)�γ��������ۻ����ɳ���[20]���3���С���������ƽ��ԭ�������г�Ǧ��������������̷ֱ�����ʽ(5)��(6)�����ݵ��ƽ����з�������ʽ(7)��
��Ac-��H+��OH- (Ϊ���ڼ�������ʵ������ϵ��H+Ũ�Ƚϵͣ���Ac-ˮ��̶�С���ʲ�����Ac-ˮ�������)�����б�״̬��Pb2+�������(Ac-)�γ��������ۻ����ɳ���[20]���3���С���������ƽ��ԭ�������г�Ǧ��������������̷ֱ�����ʽ(5)��(6)�����ݵ��ƽ����з�������ʽ(7)��
PbSO4+2NH4Ac=(NH4)2SO4+Ac-+Pb(Ac)+ (1)
PbSO4+2NH4Ac=(NH4)2SO4+Pb(Ac)2 (2)
PbSO4+3NH4Ac=(NH4)2SO4+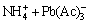 (3)
(3)
PbSO4+4NH4Ac=(NH4)2SO4+2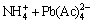 (4)
(4)
��3 �¶�25 ��ʱPb2+�������(Ac-)�γ��������ۻ����ɳ���
Table 3 Cumulative formation constant of complex formed by Pb2+ and Ac- in 25 ��

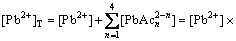
 (5)
(5)
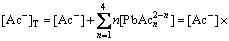
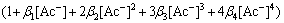 (6)
(6)
 (7)
(7)
����Matlab�����е�fsolve����������Է�����ķ��������ʵ�������ģ����ȷ����[Pb2+]T��[Ac-]T��[H+]���е�һ��Ũ�Ⱥ��������ϵ�ڸ������ֵ�ƽ��Ũ��������һ��������Ũ�ȱ仯���仯�����[21-22]�������ͼ3��ʾ��
��ͼ3��֪����[Pb2+]TŨ��Ϊ30~60 g/L��pHֵ�ϵ�(0~2)ʱ����ϵ�� Ũ������pHֵ���������½�����ϵ��Pb2+��PbAc+��Pb(Ac)2��
Ũ������pHֵ���������½�����ϵ��Pb2+��PbAc+��Pb(Ac)2��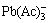 ��Ũ��������pHֵ�����������ӣ���pHֵΪ2~7ʱ����ϵ�к�Ǧ���ֵ�ƽ��Ũ�������ȶ����ڴ���������ϵ��PbAc+Ũ����ߣ���ηֱ�Ϊ
��Ũ��������pHֵ�����������ӣ���pHֵΪ2~7ʱ����ϵ�к�Ǧ���ֵ�ƽ��Ũ�������ȶ����ڴ���������ϵ��PbAc+Ũ����ߣ���ηֱ�Ϊ ��
��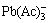 ��Pb2+��Pb(Ac)2��������Щ���ֵ�Ũ�ȶ���[Pb2+]TŨ�ȵ����߶����ӡ�����ʵ�ʽ�����ϵ����Һ��pHֵ�ӽ���7������ʵ����������Ϊ��Ũ��Ϊ30~60 g/Lʱ������Һ��Ũ����ߵ�����ΪPbAc+��
��Pb2+��Pb(Ac)2��������Щ���ֵ�Ũ�ȶ���[Pb2+]TŨ�ȵ����߶����ӡ�����ʵ�ʽ�����ϵ����Һ��pHֵ�ӽ���7������ʵ����������Ϊ��Ũ��Ϊ30~60 g/Lʱ������Һ��Ũ����ߵ�����ΪPbAc+��
1.3.2 ��Ĥ�������
��λ������õ�Pb2+��Ac-������Ϊ����Һ������һ��Ũ�ȵ��������Һ��Ϊ����Һ���и�Ĥ�����Ǧ��ֵ��һ����ǣ�����ڷǸ�Ĥ�������Pb2+������������������������PbO/PbO2��Ǧ�����ﲢ�������������棬��������ۻ������⣬ʹ��������������У���Ĥ�����Ǧ���ղ�����������Ĥ�����Pb2+��������ɢ��;�����Ӷ�������������Pb2+�����IJ�����Ӧ��
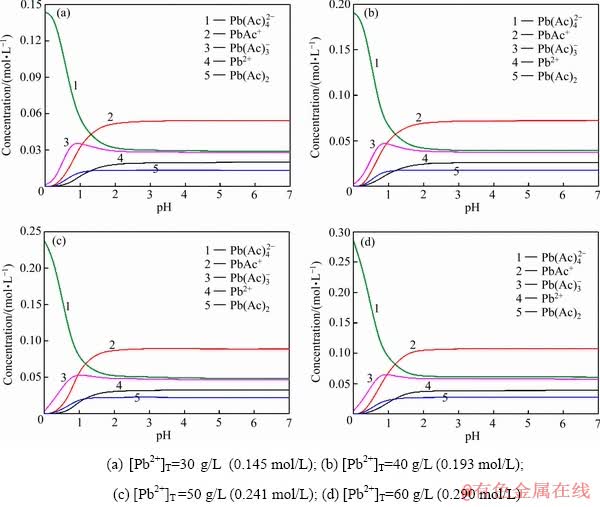
ͼ3 ��ͬ[Pb2+]TŨ����Ǧ�����ֲַ���pHֵ�Ĺ�ϵ
Fig. 3 Relationship between species distribution of lead and pH value at different concentrations of [Pb2+]T
�������淢������Ҫ��ӦΪ
2H2O-4e-��O2+4H+ (8)
�������淢������Ҫ��ӦΪ
Pb2++2e��Pb (9)
�ܷ�ӦΪ
2Pb(Ac)2+2H2O��2Pb+O2��+4HAc (10)
��ʽ(8)~(10)��֪���������������ڷ���Pb������Ӧ��ͬʱͨ��Ac-���������ݵ��ӣ��������ڷ���O2������Ӧ���ͷ�H+����Ac-��Ϊ����pH���ͼ���ʹ��ҺpH�����ȶ���һ����Χ�ڡ��������������ƶ��Һ����Ϊ���������ؼ�����������Ǧ����������Һͨ���ʵ�������ȿɼ�����Ϊ���Һʹ�á�
2 ���������
2.1 ����Ǧ����λ��������
���õ��������鷨�о�����Ǧ��λ�����������������ֱ������Ũ�ȡ��¶ȡ�����ʱ���Һ�̱ȶԽ����ʵ�Ӱ�졣��λ���������ģ25 g/�Σ������ۺ���֤�����ģ50 g/�Σ�����ѭ��������ʽ����2�Ρ�
2.1.1 ������Ũ�ȶ�Ǧ�����ʵ�Ӱ��
��Һ�̱�4:1(mL/g)���¶�70 �桢����ʱ��2 h�������·ֱ�����������Ũ�ȷֱ�Ϊ1��2��3��4��5 mol/Lʱ����Ǧ��Ǧ�Ľ����ʣ���������ͼ4��ʾ��
��ͼ4��֪�����Ž���ʱ����淋�Ũ�ȴ�1 mol/L���ӵ�5 mol/L������Ǧ�Ľ���������ߡ��������Ũ��Ϊ1 mol/Lʱ������Ǧ�Ľ����ʽ���30%���ң��������Ũ�����ӵ�4 mol/L������ʼ���������������ʱ������Ϊ94.05%�����о�ѡ�������Ũ��4 mol/LΪ��ѽ�����Ũ�ȡ�
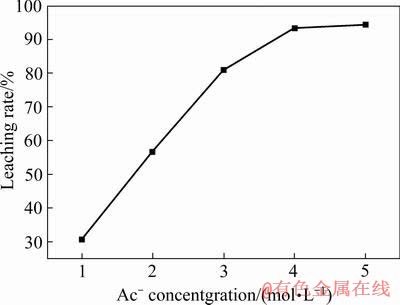
ͼ4 �����Ũ�ȶ�Ǧ�����ʵ�Ӱ��
Fig. 4 Effect of ammonium acetate concentration on lead leaching rate
2.1.2 �¶ȶ�Ǧ�����ʵ�Ӱ��
��Һ�̱�4:1(mL/g)�������Ũ��4 mol/L������ʱ��2 h�������¿��������Ӧ�¶ȷֱ�Ϊ30��50��70��90 ��ʱ����Ǧ��Ǧ�Ľ����ʣ���������ͼ5��ʾ��
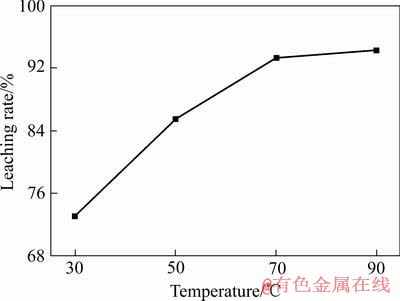
ͼ5 �¶ȶ�Ǧ�����ʵ�Ӱ��
Fig. 5 Effect of temperature on lead leaching rate
��ͼ5��֪�����Ž����¶ȵ����ӣ�����Ǧ�Ľ���������ߡ��ڷ�Ӧ�¶�Ϊ30 ��ʱ������Ǧ�Ľ�����ֻ��73%���ҡ��¶����ߵ�70 ��ʱ�������ʴﵽ94%���ң���������ʱ��Ǧ�����ʼ������ٱ仯���������¶ȴﵽ90�� ʱ������Һ���������������ӣ�������Ч��δ�������ı��������ܺģ��ʱ��о�ѡ����ѽ����¶�Ϊ70 �档
2.1.3 ����ʱ���Ǧ�����ʵ�Ӱ��
��Һ�̱�4:1(mL/g)�������Ũ��4 mol/L�������¶�70 ��������¿������ʱ��ֱ�Ϊ0.5��1.0��1.5��2.0 hʱ����Ǧ��Ǧ�Ľ����ʣ���������ͼ6��ʾ��
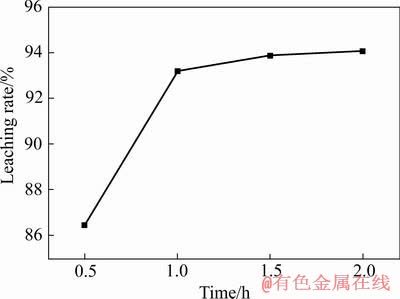
ͼ6 ��Ӧʱ���Ǧ�����ʵ�Ӱ��
Fig. 6 Effect of reaction time on lead leaching rate
��ͼ6��֪�����ŷ�Ӧʱ������ӣ��������ȿ�������Ȼ�����ӻ�������ƽ�ȣ�����Ӧʱ��Ϊ0.5 hʱ��������ԼΪ86%����Ӧʱ�����ӵ�1 hʱ��������ߵ�93%���ң���1 h�ټ����ӳ���Ӧʱ��ʱ�������ʵ��������������ӷ�Ӧʱ�������Ч��Ӱ�첻���ҽ���Ч�ʣ��ʱ��о�ѡ����ѽ�����Ӧʱ��Ϊ1 h��
2.1.4 Һ�̱ȶ�Ǧ�����ʵ�Ӱ��
�������Ũ��4 mol/L�������¶�70 �桢��Ӧʱ��1 h�������¿������Һ�̱ȷֱ�Ϊ3:1��4:1��5:1��6:1(mL/g)ʱ����Ǧ��Ǧ�Ľ����ʣ���������ͼ7��ʾ��
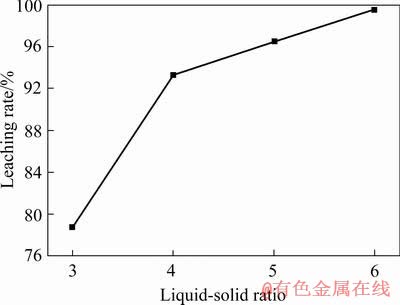
ͼ7 Һ�̱ȶ�Ǧ�����ʵ�Ӱ��
Fig. 7 Effect of liquid-solid ratio on lead leaching rate
��ͼ7��֪�����Ž���Һ�̱ȴ�3:1���ӵ�6:1������Ǧ����������ߡ���Һ�̱�Ϊ3:1ʱ��������ԼΪ79%���ҡ���Һ�̱����ӵ�6:1ʱ�������ʴﵽ99%���ϣ���ʱ�����ﵽ��ȫ������ֵ��һ����ǣ�Һ�̱ȵ�������Ȼ��ʹǦ���������ӣ�������Һ������Ũ��������Һ�̱ȵ����Ӷ����ͣ���ʱ���ܲ������ں���������ա��ۺϿ��ǣ����о�ѡ��������Һ�̱�Ϊ6:1��
2.1.5 ���������ۺ���������
�ڸ����������¼������Ũ��4 mol/L�������¶�70 �桢Һ�̱�6:1������ʱ��1 h�����ۺ��������飬ѭ������2�κ������������Ԫ��ƽ��������4���У����������������ͼ8��ʾ��
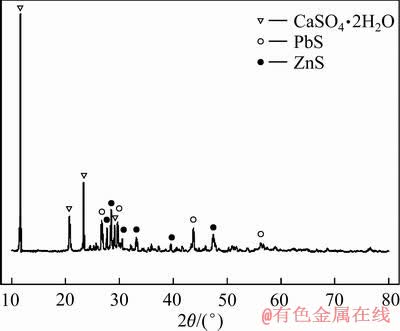
�ɱ�4��֪����������������£�Ǧ�����ʴﵽ96.42%����Ǧ���������Zn��Ca��S������Һ��������ΪAc-��Ϊһ����λ����ǿ���������������λ���������Ժ�Pb2+�γ������ͬ��������Ca2+��Zn2+�γ���Ӧ������S��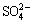 ����ʽ������Һ�С����Ǻ���������ն���Һ��һ��Ҫ�����Կ���ͨ���ڽ��������м���Ca(Ac)2��������ӹ�����������Ҫ�Խ������������֪������Ǧ�����ѻ�����ʧ����������Ҫ��CaSO4��PbS��ZnSΪ����������Ǧпԭ����߶�����Դ���Ϻ���Ϊ����Ǧ/пԭ�Ϸ���ұ��ϵͳ���߽�����ѡ����[23-25]��
����ʽ������Һ�С����Ǻ���������ն���Һ��һ��Ҫ�����Կ���ͨ���ڽ��������м���Ca(Ac)2��������ӹ�����������Ҫ�Խ������������֪������Ǧ�����ѻ�����ʧ����������Ҫ��CaSO4��PbS��ZnSΪ����������Ǧпԭ����߶�����Դ���Ϻ���Ϊ����Ǧ/пԭ�Ϸ���ұ��ϵͳ���߽�����ѡ����[23-25]��
2.2 Ǧ��Ĥ�������
���õ��������鷨�о�Ǧ��Ĥ��������������������������Ϊʯī�����������Ϊ����֡��ֱ����¶ȡ���ҺPb2+Ũ���Լ����������ܶȶ���������Ч�ʡ�������ò����ĵ�Ӱ�졣������������������Һ��������Ǧ����Һ���ۺ�������������Һ������ʵ����Һ�����е���Ч�ʼ��ܺļ�����ʽ(11)��(12)��ʾ��
��4 �ۺ��������������е�Ԫ��ƽ�����
Table 4 Analysis of element equilibrium during leaching under comprehensive conditions
ͼ8 �ۺ������½�����XRD��
Fig. 8 XRD pattern of leaching slag under comprehensive conditions
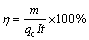 (11)
(11)
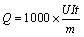 (12)
(12)
ʽ�У���Ϊ�����ܶ�(%)��mΪ��������Ǧ����(g)��qcΪPb2+��ԭ��Pb�ĵ绯������3.866 (g/(A��h))��IΪ������С(A)��tΪ���ʱ��(h)��UΪ����۵�ѹ(V)��QΪֱ�����ܺ�(kW��h/t)��
2.2.1 �¶ȶԵ������Ӱ��
��Pb2+Ũ��50 g/L�������ܶ�150 A/m2�����ʱ��4 h�������¿������¶ȷֱ�Ϊ20��30��40��50 ��ʱ����������Ч�ʡ��ܺ��Լ�������ò��Ӱ�졣��������ͼ9��10��ʾ��
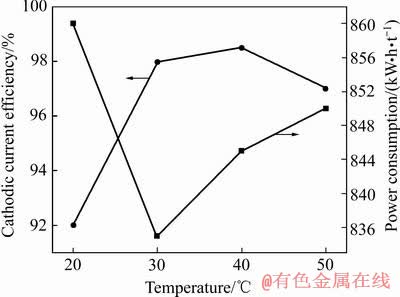
ͼ9 �¶ȶ�Ǧ��Ĥ�����������Ч�ʺ�ֱ����ĵ�Ӱ��
Fig. 9 Effect of temperature on cathodic current efficiency and power consumption of lead membrane electrodeposition

ͼ10 ��ͬ�¶�����������Ǧ�ĺ����ò
Fig. 10 Macroscopic morphologies of cathode lead at different temperatures
��ͼ9��10��֪���¶�Ϊ20 ��ʱ����Ч�ʽϵͣ�ֻ��92%�����¶����ߵ�30 ��ʱ������Ч��Ѹ���������ﵽ98%���ϣ����������¶�ʱ����Ч�ʲ��ټ������ߣ����¶Ƚϸ�ʱ����Ч�ʷ������½�����20~30 ��ʱ����Ǧ�����ò�Ϻá�ƽ���⻬����û��֦�����������Ҵ�ʱ�ܺ���ͣ����¶ȹ���ʱ���������������������������Ϊ�¶ȹ���ʱ�绯ѧ�����������ҽᾧ���ܲ����ɵ���Ч�ʵͣ�Ҳ��Ӱ����Һ�����ӵ�Ǩ�ƣ�ʹ��Һ�������ֱ��Ӱ�쵽ֱ���ܺġ������¶ȿ�����ǿ���Һ��������ɢ���ʣ��ٽ��������Ӧ�Ľ��У���ߵ���Ч�ʣ����ǵ��¶ȹ���ʱ����Һ�и����ӵ����˶��Ӿ磬��ʱ�����帽����Ϊ�����ṩ�ȶ������������Ӷ�������Ǧ�ɰ�;����ȶ��������ʱ��о�ѡ����ѵ���¶�Ϊ30 �档
2.2.2 Pb2+Ũ�ȶԵ������Ӱ��
���¶�30 �桢�����ܶ�150 A/m2�����ʱ��4 h�������¿���Pb2+Ũ�ȷֱ�Ϊ30��40��50��60 g/Lʱ����������Ч�ʡ��ܺ��Լ�������ò��Ӱ�졣��������ͼ11��12��ʾ��
��ͼ11��12��֪��������Һ��ʼPb2+Ũ�ȴ�30 g/L���ӵ�60 g/LʱǦ����Ч��Ҳ��90%�������ӵ�98%���ϣ�����Pb2+Ũ�Ƚϵ�(30~40 g/L)ʱ�����������Ϊ��ĩ״����Ǧ�ɰ�Ч�����Pb2+Ũ�����ӵ�50 g/L����ʱ������Ǧ��ò���ƽ���⻬�����Һ��Pb2+Ũ�������ܴٽ��������Ӧ�Ľ��У�������Ϊ����Һ��Pb2+Ũ�Ƚϵ�ʱH+������Pb2+һ��������ӣ������ⷴӦ���������ƽϴ���H2����ʱ������Pb�ľ����γɺͳ��Ӷ���������ɰ�Ч�������Ч�ʵ͵�һϵ�����⡣�ʱ��о��������������ҺǦŨ��Ӧ����50 g/L��
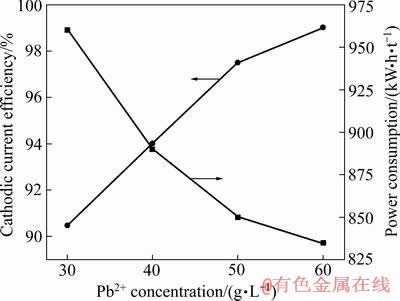
ͼ11 ����Һ[Pb2+]Ũ�ȶ�Ǧ��Ĥ�����������Ч�ʺ�ֱ����ĵ�Ӱ��
Fig. 11 Effect of Pb2+ concentration on cathode current efficiency and power consumption of lead membrane electrodeposition

ͼ12 ��ͬ����Һ[Pb2+]Ũ��������Ǧ�ĺ����ò
Fig. 12 Macroscopic morphologies of cathode lead at different Pb2+ concentrations
2.2.3 ���������ܶȶԵ������Ӱ��
���¶�30 �桢����ҺPb2+Ũ��50 g/L�����ʱ��4 h�������¿������������ܶȷֱ�Ϊ100��150��180��210��250 A/m2ʱ����������Ч�ʡ��ܺ��Լ�������ò��Ӱ�졣��������ͼ13��14��ʾ��
��ͼ13��14��֪���������ܶ�Ϊ100 A/m2ʱ����Ч�ʴ�98%���ϣ������ܶ�Ϊ250 A/m2ʱ������Ч�ʽ���86%���ڽϵ͵ĵ����ܶ��²�����������Ч�ʸߣ������ܺ�Ҳ�ϵͣ��ڵ͵���Ч��������(100~150 A/m2)ʱ�����õ��ĵ�Ǧƽ���⻬���ɰ�Ч���ã��������ܶȽϸ�180 A/m2����ʱ����Ǧ�ɰ�Ч����ʼ��������֦����������Ϊ�����������ܶ�������ʱ���缫�����ʵ�ʵ����ܶȴ�����ɢ���Ƶ����ܶȣ��Ӿ��˼�˷ŵ�ЧӦ���Ӷ��������������κ˲����ȶ��γ�֦������Ȼ�ϵ͵ĵ����ܶȻή������Ч�ʣ�����Ϊά�ֵ����������ƽ�Ƚ��У����о�ѡ����ѵ����ܶ�Ϊ100~150 A/m2��
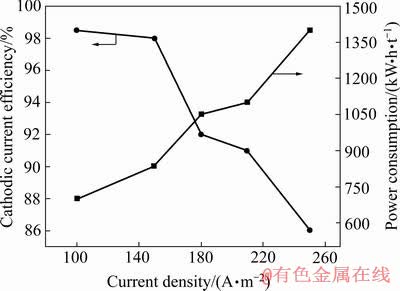
ͼ13 �����ܶȶ�Ǧ��Ĥ�����������Ч�ʺ�ֱ����ĵ�Ӱ��
Fig. 13 Effect of current density on cathode current efficiency and power consumption of lead membrane electrodeposition

ͼ14 ��ͬ�����ܶ��µ����Ǧ��ĺ����òͼ
Fig. 14 Macroscopic morphologies of cathode lead at different current densities
2.2.4 �ۺ�����ѭ������Һ��Ĥ�����֤ʵ��
�Ա�4��ʾ�ɷֽ���Һ��Ϊ����Һ����1 mol/L�������ҺΪ����Һ���ڸ����������¼�����¶�30 �桢Pb2+Ũ��50 g/L�����������ܶ�130 A/m2�������½����ۺ���������8 h��������������Ǧ�ĺ����ò��SEM���XRD����ͼ15��16��17��ʾ�����õ�Ǧ��ѧ�ɷּ�����������5���С�
�ۺ�������֤�������������Ż������µ�����Եõ����ܡ���Ϊƽ��������Ǧ�壬����������Ч��Ϊ96.16%����������Ǧ����99.2%��ͨ��Ǧ��SEM����Կ���Ǧ���������������������ж��ɣ����ҳ����˽�Ϊƽ���ı��棬�����ߴ��С���ȡ�XRD��ͬ��֤������������ijɷ֣����������г���PbO2�������壬������Ϊ����������������Ǧ�Ӵ��������Ѹ�ٷ���������Ӧ���Ӷ���������PbO2��

ͼ15 �ۺ����������µ����Ǧ��ĺ����òͼ
Fig. 15 Macroscopic morphology of cathode lead at comprehensive conditions

ͼ16 �ۺ����������µ����Ǧ���SEM��
Fig. 16 SEM images of cathode lead at comprehensive conditions
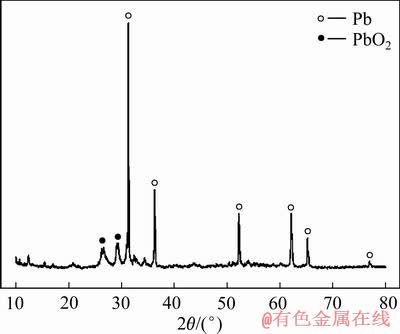
ͼ17 �ۺ����������µ����Ǧ��XRD��
Fig. 17 XRD patterns of cathode lead at comprehensive conditions
2.3 �����绯ѧ��Ӧ��������
�������缫��Ĥ���ۣ����缫�ֱ�Ϊ�������缫��316L����ֵ缫(��Ч���7.065 mm2)�������缫���ߴ���Ƭ�缫(��Ч���1 cm2)���αȵ缫�����ʹ��缫(SCE)������ѭ���������߲�����20 ���½��У�ͨ���ı䲻ͬɨ�����ʣ������Ӧ���ߣ�����ɨ�������������20 �桢50 mV/s�������½��У���ò�ͬ�¶�(20~50 ��)����ͬ����ҺPb2+Ũ��(20~50 g/L)�������������ߣ���ʱ�������Է���20 �桢50 mV/s�½��У���ú���ƽ�Ծ���ߣ��о�����ϵ�µ�������̾��˳ɺ˻�����
2.3.1 ����ѭ����������
���¶�20 �桢������Һ�����Ũ��1 mol/L������Pb2+Ũ��50 g/L�������·ֱ����ɨ������5��10��20��30��40��50 mV/sʱ����ѭ���������ߣ���ͼ18��ʾ��
��ͼ18��֪����������ѭ���������߳������Ƶı仯���ƣ����ŵ�λ����ɨ�裬�����ܶȿ�ʼѸ�����ӣ�������ʱ������ʼ����Ǧ������Ӧ�������ܶȴﵽ��ֵ�������½���������ʱ����������Pb2+�Ѿ�����������ϣ�����Һ��Pb2+��ɢ���������������ʱ�Pb2+��������������ʱ��ɢ��Ϊ���Ʋ���[26]����λ������ɨ�������ܶȿ�ʼ�������ӣ�ͬʱ�۲������������������������ʱ�������ⷴӦ������ɨ��ʱ���������壬�˹���Ϊ����Ǧ���ܡ�
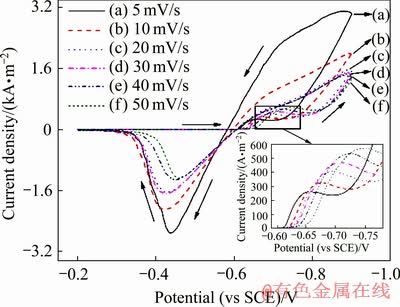
ͼ18 ��ͬɨ�������µ�ѭ����������
Fig. 18 Cyclic voltammetry curves at different scanning rates
�ı�ɨ�����ʺ�����ɨ��������5 mV/s������50 mV/s��Ǧ�Ŀ�ʼ������λ��-0.610 V������-0.660 V��ͬʱǦ�������ֵ�����ܶ�Ҳ��265 A/m2������550 A/m2������Ӧ��λ��-0.635 V������-0.744 V�����ڿ�����ת�ƹ���������ֵ��λ����ɨ�ٱ仯���仯��ͬʱ����������ֵ��λ��Զ��������ֵ�������ڸ���ϵ�£�Ǧ�ij��������Dz����淴Ӧ��һ�����˫����ת��[27-28]��
2.3.2 ��������ɨ�����
1) ��ͬPb2+Ũ����������������
���¶�20 �桢������Һ�����Ũ��1 mol/L��ɨ������50 mV/s�������·ֱ��������Pb2+Ũ��20��30��40��50 g/Lʱ��������ɨ�����ߣ���ͼ19��ʾ��
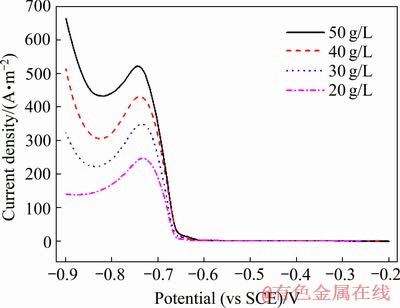
ͼ19 ��ͬ����ҺPb2+Ũ���µ�������������
Fig. 19 Cathode polarization curves of different Pb2+ concentration
��ͼ19��֪����������Pb2+Ũ�ȵ����ӣ�����Ǧ��ʼ������λ���������ƶ������仯�������ԣ�˵��Pb2+Ũ�ȵ����Ӵٽ���Ǧ������Ӧ�ķ����������ܶȷ�ֵҲ����Pb2+Ũ�ȵ����Ӷ������ӣ�˵��Pb2+Ũ�ȵ����Ӽӿ��˷�Ӧ�Ľ��̣�������Ϊ����Һ��Ǧ����Ũ��Խ�ߣ���Һ�ĵ�������Խ�ã�ͬʱ��������Һ��Ũ������ٽ�����Һ����ɢ�������ӿ������Ӧ�Ľ��С�
2) ��ͬ�¶��µ�������������
������Pb2+Ũ��50 g/L��������Һ�����Ũ��1 mol/L��ɨ������50 mV/s�������·ֱ�����¶�Ϊ20��30��40��50 ��ʱ��������ɨ�����ߣ���ͼ20��ʾ��
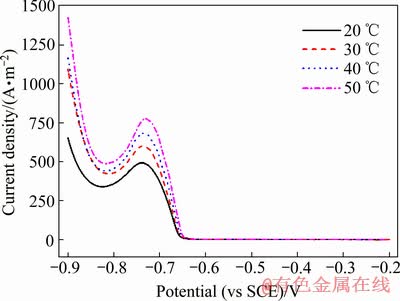
ͼ20 ��ͬ�¶��µ�������������
Fig. 20 Cathode polarization curves at different temperatures
��ͼ20��֪�������¶ȵ����ӣ�����Ǧ��ʼ�����ĵ�λ����û�б仯��˵���¶Ȳ���ı䷴Ӧ��������ʼ��λ�������ܶȷ�ֵ�����¶ȵ����Ӷ������ӣ�˵���¶ȵ����Ӽӿ��˷�Ӧ�Ľ��̣�������Ϊ�¶����ߣ���Һ��������ɢ���ʼӿ죬ʹ��Һ��������ǿ������ʹ��Ӧ�������ӡ������¶����ߺ�Ҳͬ���ӿ������ⷴӦ�Ľ��У�������ʵ�ʵ������������Ӧѡ���Ϊ���ʵĵ���¶��Դﵽ�ٽ���Ǧ�ͷ�ֹ�����ƽ�⡣
2.3.3 ������ʱ��������
��20 �桢����Pb2+Ũ��50 g/L�������£����ú��λ��Ծ���ⶨ����ϵ������Ǧ�������̵ĵ���-ʱ����̬���ߣ���ͼ21��ʾ��
��ͼ21��ʾ���ڸտ�ʼ�ļ����ڣ������ܶ�Ѹ�����ߴﵽһ����ֵ������֮������ܶ��ֿ�ʼ�½���������ȶ������������ڽᾧ�����д����ľ����γ�������������ɵ��µ���Ѹ���������ﵽ���ֵ������DZ���ƽ�Ȼ������½������������ȶ�����ʱ��Һ������ɢ��绯ѧ��Ӧ���ڶ�̬ƽ�⡣
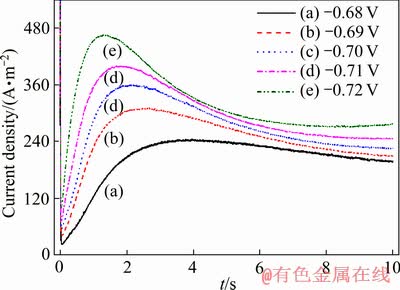
ͼ21 ��ͬ��Ծ��λ�µĵ���-ʱ����̬����
Fig. 21 Current-time transient curves at different step potentials
����Ǧ�ĵ�������̳�������ɢ���ƣ�����ѭ���͵���ά�����ͳɺ˺;���������ơ�����SCHARIFKER��[29]����������ģ�ͣ�����ͨ��ʱ��������Ĺ�ϵȷ���ɺ˷�ʽ��˲ʱ�ɺ˻��������ɺˡ�˲ʱ�ɺ˺������ɺ˹�ϵʽ��(13)��(14)��ʾ��
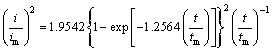 (13)
(13)
 (14)
(14)
ʽ�У�im��tm�ֱ�Ϊ����-ʱ����̬���ߵ������������Ӧʱ�䡣
ͼ22��ʾΪ(i/im)2��(t/tm)�������ٹ�ϵ���ߣ���ͼ��֪�������ʵ�������������ɺ������������Ǻϣ��ҽ�Ծ��λԽ����ʵ�ʲ������Խ�ӽ����������ߣ��ɴ�˵������ϵ������Ǧ��ԭ���ڷ��������ɺ˹��ɡ�
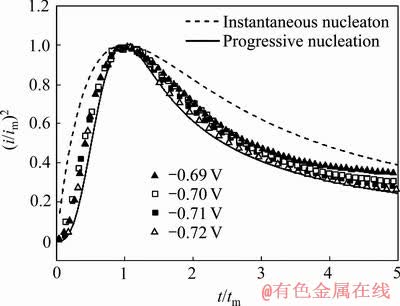
ͼ22 ��ͬ��λ������(i/im)2-(t/tm)����
Fig. 22 Nondimensional curves (i/im)2-(t/tm) in different potentials
3 ����
1) ��������λ��������Ǧ�����Ż���������Ϊ�������Ũ��4 mol/L����Ӧʱ��1 h�������¶�70 �桢Һ�̱�6:1���ڴ˹��������½�������Ǧ����Ǧ������93.28%����������Ҫ��ZnS��PbS��ɣ�������Ϊ��Ǧ/пԭ�Ϸ���ұ��ϵͳ������Ǧ����Һ��Ĥ������Ż�����Ϊ�������ܶ�130 A/m2��Pb2+Ũ��54.58 g/L���¶�30 �档�ڴ�������������Ǧ������Һֱ�Ӹ�Ĥ���8h,���Ի�ñ����Ϊ����ƽ��������Ǧ���䴿����99.2%���ϣ���������Ч��96.16%��
2) ��Ĥ�����Ǧ��������ԭ������һ�������������һ�����˫����ת�ơ������¶Ⱥ��������ҺPb2+Ũ�ȿ��Դٽ���Һ������ɢ���ӿ췴Ӧ���̣���ߵ���Ч�ʡ�Ǧ�ڵ����������ѭ��ά�����ɺ��뾧��������ơ�
3) �������������λ����-��Ĥ�����ʪ����������Ǧ�����¹��գ�����Ч��������Ǧ���е�Ǧ���ù��ո����̲�����ʵ����Һ��·ѭ����ͬʱ���ɱ���Ǧ������̶��������ۻ���������ʹ�ø�Ĥ�����������ɲ۵�ѹ��������������ӣ��Ӷ������������ɱ��������价��ѹ��С����������Ч���ص㣬ʹ�øù����Ծ��нϴ��ǰ���;�������
REFERENCES
[1] ������. �ؽ���ұ��ѧ[M]. ��ɳ: ���ϴ�ѧ������, 2003.
PENG Rong-qiu. Heavy metal metallurgy[M]. Changsha: Central South University Press, 2003.
[2] ������. �ҹ�Ǧпұ����״�������չ[J]. �й���ɫ����ѧ��, 2004, 14(S1): s52-s62.
JIANG Ji-mu. Status and sustainable development of lead and zinc smelting industry in China[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(S1): s52-s62.
[3] ������. QSL����Ǧ���յ��½�չ[J]. ������ɫ����, 1997, 13(1): 34-38.
HUANG Zuo-ren. New progress in the lead-smelting process of QSL method [J]. Hunan Nonferrous Metals, 1997, 13(1): 34-38.
[4] �ΰ�ƽ, κ ��, �� ��, ��Ʋ�, ̷����. ����21�����ҹ�Ǧұ�������ĸ���ͷ�չ˼��[J]. ��ɫ����(ұ������), 2000(6): 2-6.
HE Ai-ping, WEI Chang, HUANG Bo, WU Hao-bo, TAN Chun-e. Thoughts on the reform and development of China��s lead smelting technology in the 21st century[J]. Nonferrous Metals (Smelting Part), 2000(6): 2-6.
[5] �¼���. ʪ��ұ����о��뷢չ[M]. ����: ұ��ҵ������, 1998.
CHEN Jia-yong. Research and development of hydrometallurgy[M]. Beijing: Metallurgical Industry Press, 1998.
[6] ͯ־Ȩ. ���ν���-�����û���������Ǧ���л���Ǧ[J]. ��̶��ѧ��Ȼ��ѧѧ��, 1991, 13(3): 70-76.
TONG Zhi-quan. Lead recovery from residue containing lead sulphate by means of metal chloride leaching-ferrous power replacing[J]. Natural Science Journal of Xiangtan University, 1991, 13(3): 70-76.
[7] �Ŵ���, ���ı�, �� ��, �� ��, �� ��. �Ѵ���Ǧп���������������Ǧ�Ĺ����о�[J]. Ӧ�û�ѧ, 2012, 41(7): 1188-1192.
ZHANG Chuan-bao, YAN Wen-bin, XU Hui, GAO Feng, HUA Jun. Study on recovery lead sulfate from complex acid leaching residue of lead-zinc mine[J]. Applied Chemical Industry, 2012, 41(7): 1188-1192.
[8] ���Ͻ�, ������, ������. ��Ǧ���ؼ����ĩʪʽ��������Ǧ[J]. ���̹���ѧ��, 2009, 9(S2): 71-75.
CHEN Meng-jie, SHIU Yan-jang, LIN Cheng-hsiung. Recovery of lead from spent lead batteries by hydrometallurgical method[J]. The Chinese Journal of Process Engineering, 2009, 9(S2): 71-75.
[9] ��άƽ, ����ɭ, �·���. PbSiF6-H2SiF6��ϵ�����Ǧ�ĵ绯ѧ[J]. �й���ɫ����ѧ��, 1996, 6(3): 43-46.
CHEN Wei-ping, Gong Jian-sen, Chen Fan-cai. Electrochemistry of electrodepositing Pb in PbSiF6-H2SiF6 system[J]. The Chinese Journal of Nonferrous Metals, 1996, 6(3): 43-46.
[10] �ɳ���, �¹���, �ɺ�, �����, ����ǿ. ��Ǧ��������Ӳ֬��Ǧ���о�[J]. �㶫����, 2001(6): 44-46.
XI Chang-sheng, CHEN Go-xie, YI Fei-hong, PENG Cui-hong, ZOU Xian-qiang. Study on the production of lead stearate using waste material containing lead[J]. Guangdong Chemical Industry, 2001(6): 44-46.
[11] ���IJ�, �� ��. ��Ǧ������Դ�����õ��о�[J]. ��ҵ�о��뿪��, 2010, 30(3): 58-59.
DAI Wen-can, CHEN Tao. Study on utilization of a residue containing lead as resource[J]. Mining Research and Development, 2010, 30(3): 58-59.
[12] ���, ��aԴ, �� ��, ������, �� ��, �Ƴ���, ������. һ�ֻ�������-������ϵ������ˮ���ӷ�����ˮ�л������ķ���: �й�, CN103741142A[P]. 2014-04-23.
YANG Jian-guang, LI Jun-yuan, LEI Jie, YANG Sheng-hai, HE Jing, TANG Chao-bo, CHEN Yong-ming. A kind of tin-fading liquid based on the hydrochloric acid-tin salt system and the process of recycling tin from the spent tin-fading liquid: China, CN103741142A[P]. 2014-04-23.
[13] ���, �� ��, ��˼Ң, ��aԴ, �� ��, ������, �Ƴ���, ������. һ�ִ����������л������Ĺ���: �й�, CN104630826[P]. 2015-05-20.
YANG Jian-guang, LEI Jie, PENG Si-yao, LI Jun-yuan, HE Jing, YANG Sheng-hai, TANG Chao-bo, CHEN Yong-ming. A process of tin recovery from the tin anode slime: China, CN103741142A[P]. 2015-05-20.
[14] ��˼Ң, ���, �� ��, ������, �� ��, ��aԴ. ����������Դ��Ĥ����������¹�������[J]. �й���ɫ����ѧ��, 2016, 26(12): 2656-2667.
PENG Si-yao, YANG Jian-guang, CHEN Bing, LI Shu-chao, LEI Jie, LI Jun-yuan. Novel process for tin recovery from stannous secondary resources based on membrane electrodeposition[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(12): 2656-2667.
[15] YANG Jian-guang, YANG Sheng-hai, TANG Chao-bo. The membrane electrowinning separation of antimony from a stibnite concentrate[J]. Metallurgical & Materials Transactions B, 2013, 44(2): 479-481.
[16] ���̷�, �� ��, ���. �ø�Ĥ������ӻ�����л�����[J]. ʪ��ұ��, 2012, 31(1): 45-48.
WANG Ji-feng, LI Jing, YANG Jian-guang. Recovery of bismuth from a bismuthinite concentrate by membrane- electrowinning[J]. Hydrometallurgy of China, 2012, 31(1): 45-48.
[17] NEDWED T, CLIFFORD D A. Feasibility of extracting lead from lead battery recycling site soil using high- concentration chloride solutions[J]. Environmental Progress, 2000, 19(3): 197-206.
[18] ������, ������, ����ΰ, �� ��, �Ƴ���, ���, ������. ��������ϵ�����Ǧ������������Ӧ�ĵ绯ѧ�о�[J]. ʪ��ұ��, 2018, 37(5): 356-361.
YANG Sheng-hai, WU Yan-zeng, SUN Yan-wei, HE Jing, TANG Chao-bo, YANG Jian-guang, CHEN Yong-ming. Electrochemistry of anodic reactions in MSA system during electrowinning of lead[J]. Hydrometallurgy of China, 2018, 37(5): 356-361.
[19] ���ı�, ������, ��ΰ��. ������Һ��Ǧ����Ĥ�о��ļ�������(һ)[J]. �绯ѧ, 1995, 1(3): 259-262.
CAI Wen-bin, LIU Hou-tian, ZHOU Wei-fang. Problems on the study of anodic films on Pb in sulfuric acid solution (��)[J]. Electrochemistry, 1995, 1(3): 259-262.
[20] DEAN J A. Lange��s handbook of chemistry[M]. New York: McGraw-Hill, 1999.
[21] ������, ������, ���, ������, ���ĺ�, �Ƴ���, �� ��. Zn(��)-NH3-Cl--CO32--H2O��ϵ��Zn(��)���ƽ��[J]. �й���ɫ����ѧ��, 2008, 18(S1): s192-s198.
WANG Rui-xiang, TANG Mo-tang, YANG Jian-guang, YANG Sheng-hai, ZHANG Wen-hai��TANG Chao-bao, HE Jing. Thermodynamics of Zn(��) complex equilibrium in system of Zn(��)-NH3-Cl--CO32--H2O[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(S1): s192-s198.
[22] TANG Mo-tang, YANG Jian-guang, YANG Sheng-hai, TANG Chao-bo. Thermodynamic calculation of Sn(��)- NH4+-Cl--H2O system[J]. Transactions of Nonferrous Metals Society of China, 2004, 14(4): 802-806.
[23] �Ƴ���. Ǧ���ԭ��������·����о�[D]. ��ɳ: ���ϴ�ѧ, 2003.
TANG Chao-bo. New process studies on reducing-making matte smelting of lead and antimony[D]. Changsha: Central South University, 2003.
[24] Ҧά��, �Ƴ���, ������, ������, �����. ��Ǧ������SO2�ŷŷ���¯һ����Ǧ�빤ҵ����[J]. �й���ɫ����ѧ��, 2001, 11(6): 1127-1130.
YAO Wei-yi, TANG Chao-bo, TANG Mo-tang, LI Zeng-rong, LIU Feng-cheng. One-stage smelting lead from lead sulfide concentrates in reverberatory furnace without sulfur dioxide[J]. The Chinese Journal of Nonferrous Metals, 2001, 11(6): 1127-1130.
[25] �̴�֦. ��Ǧпѡ����̽��[J]. ������ɫ����, 2019(4): 69-70.
CHENG Chun-zhi. Discussion on beneficiation technology of lead and zinc sulfide[J]. The World Nonferrous Metals, 2019(4): 69-70.
[26] WEN S X, SZPUNAR J A. Nucleation and growth of tin on low carbon steel[J]. Electrochimica Acta, 2005, 50(12): 2393-2399.
[27] LEI Jie, YANG Jian-guang. Electrochemical mechanism of tin membrane electro-deposition in chloride solutions[J]. Journal of Chemical Technology & Biotechnology, 2017, 92: 861-867.
[28] NAN Tian-xiang, YANG Jian-guang, CHEN bing. Electrochemical mechanism of tin membrane electrodeposition under ultrasonic waves[J]. Ultrasonics- Sonochemistry, 2018, 42: 731-737.
[29] SCHARIFKER B R, MOSTANY J. Three-dimensional nucleation with diffusion controlled growth: Part ��. Number density of active sites and nucleation per site[J]. Journal of Electroanalytical Chemistry and Interfacial Electrochemistry, 1984, 177: 13-23.
New technology and mechanism for extracting lead from lead sulfate residue by membrane electrodeposition
DING Long, YANG Jian-guang, NAN Tian-xiang, LI Ling-chen, WANG wen-chao, YAN wan-peng
(School of Metallurgy and Environmental, Central South University, Changsha 410083, China)
Abstract: According to the theory of material balance and charge balance, the thermodynamic analysis of Pb(��)-Ac--H+-H2O system was carried out. The conclusion is that the equilibrium concentration of PbAc+ in solution is the highest in the range of pH value close to the real leach solution. Using lead sulfate residue as raw material, the optimum conditions of this process were obtained by single factor experiment. The optimum conditions and experimental results of leaching are finally determined as follows: temperature of 70 ��, reaction time of 1 h, ammonium acetate concentration of 4 mol/L, the ratio of liquid to solid of 4:1. The leaching efficiency of lead is 93.28%. The optimum conditions and experimental results of membrane electrodeposition are finally determined as follows: temperature of 30 ��, Pb2+ concentration of 50 g/L, current density of 100 A/m2. The cathode current efficiency could reach 98%, the DC power consumption is 700 kW��h per ton Pb. When electrowinning with selective leaching solution under the optimal process conditions, and a relatively compact and flat lead can be obtained at the cathode with a purity of 99.2%, and the current efficiency of the cathode is 96.16%. The electrochemical behavior of lead electrodeposition was investigated. It is an irreversible reaction of lead membrane electrodeposition; the initial process of lead electrodeposition follows the diffusion controlled three-dimensional nucleation and grain growth mechanism; ion diffusion rate and current efficiency are improved by the increase of temperature and concentration of Pb2+.
Key words: lead sulfate residual; coordination leaching; membrane electrodeposition; acetate system; electrochemical mechanism
Foundation item: Project(51574294) supported by the National Natural Science Foundation of China
Received date: 2019-12-02; Accepted date: 2020-06-11
Corresponding author: YANG Jian-guang; Tel: +86-731-88830470; E-mail: jianguang_y@163.com
(�༭ �� ��)
������Ŀ��������Ȼ��ѧ����������Ŀ(51574294);
�ո����ڣ�2019-12-02�������ڣ�2020-06-11
ͨ�����ߣ���㣬���ڣ���ʿ���绰��0731-88830470��E-mail��jianguang_y@163.com
ժ Ҫ����������ƽ��͵��ƽ��ԭ������Pb(��)-Ac--H+-H2O��ϵ��������ѧ������������������ڽӽ���ʵ�ʽ���Һ��pHֵ��Χ�ڣ���Һ��PbAc+ƽ��Ũ����ߡ���ʪ����п����������Ǧ��Ϊԭ�ϣ����õ�����ʵ�鷨�Ż�����������λ����-��Ĥ�����ȡǦ������Ҫ�������������õ��������鷨�Ż�����Ǧ��Һ��Ĥ���������������������ɨ�衢ѭ�������ȵ绯ѧ�����ֶ��о�Pb(��)-Ac--H2O��ϵǦ��������������绯ѧ��Ϊ������������ڷ�Ӧʱ��1 h�������¶�70 �桢�����Ũ��4 mol/L��Һ�̱�4:1���Ż������½�������Ǧ����Ǧ������93.28%���ڵ���¶�30 �桢Pb2+Ũ��50 g/L�������ܶ�100 A/m2����������������Ч��98%���ң�ÿ��Pbֱ�����Լ700 kW��h���ڴ�������������Ǧ������Һֱ����Ϊ���Һ��Ĥ���8 h���������Ի�ô���99.2%��Ϊ����ƽ���ĵ�Ǧ����������Ч��96.16%��Ǧ�Ļ�ԭ����������һ����������̣�Ǧ�ڵ����������ѭ��ά�����ɺ������������ƣ������¶Ⱥ��������ҺPb2+Ũ�ȿ��Դٽ���Һ������ɢ����ߵ���Ч�ʡ�
[1] ������. �ؽ���ұ��ѧ[M]. ��ɳ: ���ϴ�ѧ������, 2003.
PENG Rong-qiu. Heavy metal metallurgy[M]. Changsha: Central South University Press, 2003.
[2] ������. �ҹ�Ǧпұ����״�������չ[J]. �й���ɫ����ѧ��, 2004, 14(S1): s52-s62.
[3] ������. QSL����Ǧ���յ��½�չ[J]. ������ɫ����, 1997, 13(1): 34-38.
[5] �¼���. ʪ��ұ����о��뷢չ[M]. ����: ұ��ҵ������, 1998.
[6] ͯ־Ȩ. ���ν���-�����û���������Ǧ���л���Ǧ[J]. ��̶��ѧ��Ȼ��ѧѧ��, 1991, 13(3): 70-76.
[8] ���Ͻ�, ������, ������. ��Ǧ���ؼ����ĩʪʽ��������Ǧ[J]. ���̹���ѧ��, 2009, 9(S2): 71-75.
[9] ��άƽ, ����ɭ, �·���. PbSiF6-H2SiF6��ϵ�����Ǧ�ĵ绯ѧ[J]. �й���ɫ����ѧ��, 1996, 6(3): 43-46.
[10] �ɳ���, �¹���, �ɺ�, �����, ����ǿ. ��Ǧ��������Ӳ֬��Ǧ���о�[J]. �㶫����, 2001(6): 44-46.
[11] ���IJ�, �� ��. ��Ǧ������Դ�����õ��о�[J]. ��ҵ�о��뿪��, 2010, 30(3): 58-59.
[16] ���̷�, �� ��, ���. �ø�Ĥ������ӻ�����л�����[J]. ʪ��ұ��, 2012, 31(1): 45-48.
[19] ���ı�, ������, ��ΰ��. ������Һ��Ǧ����Ĥ�о��ļ�������(һ)[J]. �绯ѧ, 1995, 1(3): 259-262.
[20] DEAN J A. Lange��s handbook of chemistry[M]. New York: McGraw-Hill, 1999.
[23] �Ƴ���. Ǧ���ԭ��������·����о�[D]. ��ɳ: ���ϴ�ѧ, 2003.


