����SO2��ԭ-��ɢ������������ͭ�����ˮ
�� ��1���żѷ�1��������1, 2����ʤ��3
(1. ���ϴ�ѧ ұ���ѧ�빤��ѧԺ������ ��ɳ��410083��
2. ��ͭ���Ź�Ϫ�²�������˾������ ��Ϫ��335424��
3. ���ֹ�ѧԺ �����뻯ѧϵ������ ���֣�541004)
ժ Ҫ��
ժ Ҫ������SO2��ԭ-��ɢ�������Ը�ͭ�����ˮ����ͭ����룬�о�SO2��������Ӧʱ�䡢��Ӧ�¶Ⱥͽ����ٶ��Լ���ɢ�������̽�ˮ��ȡ�ˮ���١������ٶ�ͭ������Ӱ�졣�����������20 L��ͭ�����ˮ�����£���SO2����Ϊ3 kg/h����Ӧʱ��Ϊ1 h����Ӧ�¶�Ϊ���£������ٶ�Ϊ800 r/min����ˮ���Ϊ5 g/L��ˮ����Ϊ400 mL/h��������Ϊ400 mL/hʱ��ͭ������ۺ�Ч����ã�ͭ�ķ����ʴ�94.71%����ķ����ʴ�95.63%��
�ؼ��ʣ�
��ͭ�����ˮ��ͭ������������SO2��ԭ����ɢ������
��ͼ����ţ�TQ085.41 ���ױ�ʶ�룺A ���±�ţ�1672-7207(2009)04-0863-05
Treatment of wastewater containing high concentration of copper and arsenic by sulphur dioxide reduction-diffusion dialysis
ZHANG Bao1, ZHANG Jia-feng1, YANG Xing-wen1, 2, ZHONG Sheng-kui3
(1. School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China;
2. Jiangxi Copper Company (Guixi) New Materials Company, Guixi 335424, China;
3. Department of Materials and Chemistry, Guilin University of Technology, Guilin 541004, China)
Abstract: Sulphur dioxide reduction combined diffusion dialysis experiment was used for separation of copper and arsenic in wastewater containing high concentration of copper and arsenic. The effects of the flow of sulphur dioxide, reaction time, reaction temperature and stirring speed and the diffusion dialysis process of the influent acidity, water flow rate and material flow rate on the ratio of separation of arsenic and copper were studied. The results show that under the conditions of the flow of sulphur dioxide of 3 kg/h, reaction time of 1 h, at room temperature, stirring speed of 800 r/min, and the inlet water acidity of 5 g/L, water flow rate of 400 mL/h, material flow rate of 400 mL/h, the effect of separation is the best. The ratio of copper reaches 94.71% and arsenic 95.63%.
Key words: wastewater containing high concentration of copper and arsenic; copper; arsenic; separation; sulphur dioxide reduction; diffusion dialysis
����һ���ж����°����ʣ��Ի�������Ⱦ��Ҫ�Ƕ�ˮ�����Ⱦ���Ը�ͭ�����ˮ���з��룬���۴���Դ���ջ��ǻ�������������˵������ʮ����Ҫ�� ���塣Ŀǰ����������Ҫ����ʯ��-���γ����������������кͳ��������������鷨����ȡ�����ӽ������ȷ������������ˮ������ʯ��-���γ��� ��[1-2]���������ˮ�ɱ��ͣ����ռ��ֲ�����Ч��������������������������ɻ���������Ⱦ����ȫ�������øߣ�������������S2-�����γ�����ij��������乤�����̳����������øߣ�������������Ĵ���Ч���ã��Ա�����ұ����ҵ�㷺���ã��кͳ�����[3-4]��Ҫ��ͨ�����ˮ�������������ƣ���߷�ˮpHֵ��ʹ����������ƺ��������ʽ���������ø÷��ɳ�ȥ���飬�ҷ������������������������Խ���ˮ�����������ŷű����������鷨���������ˮ��ͨ�������ʵ�����������3��������Ϊ5�������Fe3+����Ũ�ȴ����£�ʹ֮����FeAsO4�������Ӷ��ﵽ����Ŀ�ġ��÷����ռ��ɱ��ͣ����÷�������ͭ�����ˮʱͭ������ͭ��������ͭ��ʽ������������Ч�ػ��ա���ȡ[5]�����ӽ�����[6]����Ч���ã������ո��ӣ�Ͷ�ʽϴ���ɢ������[7-12]������ˮ����Ͷ��С���ܺĵͣ��������㣬������ȾС���ŵ㣬�ڴˣ��������߲���SO2��ԭ-��ɢ��������ͨ��SO2��ԭ�������ɢ�������գ�ʹͭ����õ���Ч�ط���ͻ��ա�
1 ʵ ��
1.1 ԭ ��
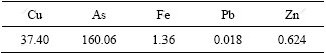
��ͭ�����ˮ��Դ������ijұ����ҵ���������в���������ͭ�ᾧĸҺ����Ҫ����Cu2+��AsO43-��H+��������������Fe��Zn��Pb�ȡ���ѧ����������1��ʾ��
��1 ��ͭ�����ˮ����Ҫ�ɷ�
Table 1 Chemical composition of wastewater containing high
concentration of copper and arsenic ��/(g?L-1)
1.2 �Լ�������
�Լ�������(������)��Ũ����(������)�ȡ�
������������������������(810)������������Ĥ��ɢ������(HKY-001)������װ�õȡ�
1.3 ʵ��ԭ��
SO2��ԭ��ͭ�����ˮ����������SO2����������H3AsO4��ԭ����˪�����ڳ���ǿ���������£�SO2��������Cu2+������Ӧ���Ӷ��ﵽ���ͷ�ˮ���麬����Ŀ�ġ����巴ӦʽΪ��
2SO2+2H3AsO4 ![]() As2O3��+2H2SO4+H2O��
As2O3��+2H2SO4+H2O��
��ɢ����������������ҺŨ�Ȳ�Ϊ������������һ���ⲿ����ֻ����H+����������ˮ��Ǩ��(�������ӽ���Ĥ��ѡ����������)�Խ������������ӣ�ʹ������������H+�������ӷֿ�������ʹCu2+��AsO43-�ﵽ��Ч�ط��롣
1.4 SO2��ԭ-��ɢ������������
SO2��ԭ-��ɢ������������ͭ�����ˮ����������ͼ1��ʾ��

ͼ1 SO2��ԭ-��ɢ������������ͭ�����ˮ��������
Fig.1 Flowsheet of sulphur dioxide reduction combined diffusion dialysis treating wastewater containing high concentration of copper and arsenic
1.5 ��������
ͭ�����Ũ����ԭ�����չ������з���(ԭ�����չ�����ΪAvanta Ultr Z)��
2 ���������
2.1 SO2������SO2�����ʵ�Ӱ��
ͼ2��ʾΪ20 L��ͭ�����ˮ�����£��ڷ�Ӧ�¶�Ϊ���£������ٶ�Ϊ800 r/min����Ӧ����Һ�ﵽƽ��ʱSO2������SO2�����ʵ�Ӱ�졣��ͼ2�ɿ�����SO2��������SO2������������͡���SO2����������3 kg/hʱ����Ӧ�����ʻ���������43%���ң���SO2��������������ʱ��SO2�����ʿ��ټ�С����ԭ�����������SO2����������SO2����Һ�Ӵ���ʱ���̣���������Һ�Ĵ���Ч����

��Ӧ�¶�Ϊ���£������ٶ�Ϊ800 r/min
ͼ2 SO2������SO2�����ʵ�Ӱ��
Fig.2 Effect of sulphur dioxide flow on ratio of sulphur dioxide utilization
2.2 SO2�������黹ԭ�ʵ�Ӱ��
ͼ3��ʾΪ20 L��ͭ�����ˮ�����£�����Ӧ�¶�Ϊ���£���Ӧʱ��Ϊ1 h�������ٶ�Ϊ800 r/minʱ��SO2�������黹ԭ�ʵ�Ӱ�졣��ͼ3�ɿ�������ˮ���������Ũ����SO2�������������С��Ȼ�ֻ������䡣��SO2����Ϊ3 kg/hʱ����Ļ�ԭЧ����á���ʵ������SO2��ԭ���̷�Ӧʽ���Կ�������SO2����Ϊ3 kg/hʱ��������ת������˪����Һ����ƽ��״̬���˺���Һ���麬���������ֲ��䡣

��Ӧʱ��Ϊ1 h����Ӧ�¶�Ϊ���£������ٶ�Ϊ800 r/min
ͼ3 SO2�������黹ԭ�ʵ�Ӱ��
Fig.3 Effect of sulphur dioxide flow on ratio of arsenic reduction
2.3 ��Ӧʱ����黹ԭ�ʵ�Ӱ��
ͼ4��ʾΪ20 L��ͭ�����ˮ�����£���SO2����Ϊ3 kg/h����Ӧ�¶�Ϊ���£������ٶ�Ϊ800 r/minʱ����Ӧʱ����黹ԭ�ʵ�Ӱ�졣�ɼ�����ˮ���������Ũ���淴Ӧʱ����ӳ�����С��Ȼ�ֻ������䡣����Ӧʱ��Ϊ1 hʱ����Ļ�ԭЧ���Ѵ���á���Ϊ����Ӧʱ��Ϊ1 hʱ��SO2�ѽ����黹ԭ����˪��ʹ��Ӧ����һ��ƽ��״̬����Һ��������Ũ�ȴ���͡�
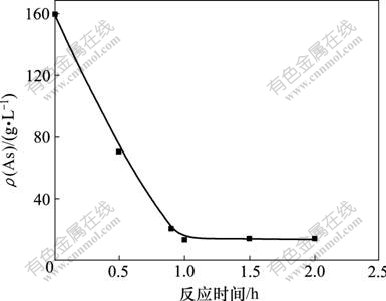
SO2����Ϊ3 kg/h����Ӧ�¶�Ϊ���£������ٶ�Ϊ800 r/min
ͼ4 ��Ӧʱ����黹ԭ�ʵ�Ӱ��
Fig.4 Effect of reaction time on ratio of arsenic reduction
2.4 ��Ӧ�¶ȶ��黹ԭ�ʵ�Ӱ��
ͼ5��ʾΪ20 L��ͭ�����ˮ�����£���SO2����Ϊ3 kg/h����Ӧʱ��Ϊ1 h�������ٶ�Ϊ800 r/minʱ����Ӧ�¶ȶ��黹ԭ�ʵ�Ӱ�졣�ɼ�����Ӧ�¶ȵı仯�Է�ˮ��������Ũ�ȵ�Ӱ�첻����Ӧ�¶���20~40 ��֮��ʱ����ˮ���������Ũ�Ȼ������䡣��ˣ��÷�Ӧ�����������¼��ɽ��С�

SO2����Ϊ3 kg/h����Ӧʱ��Ϊ1 h�������ٶ�Ϊ800 r/min
ͼ5 ��Ӧ�¶ȶ��黹ԭ�ʵ�Ӱ��
Fig.5 Effect of reaction temperature on ratio of
arsenic reduction
2.5 �����ٶȶ��黹ԭ�ʵ�Ӱ��
ͼ6��ʾΪ20 L��ͭ�����ˮ�����£���SO2����Ϊ3 kg/h����Ӧ�¶�Ϊ���£���Ӧʱ��Ϊ1 hʱ�������ٶȶ��黹ԭ�ʵ�Ӱ�졣�ɼ�����ˮ���������Ũ��������ٶȵ��������С���������ٶȳ���800 r/minʱ����ˮ�е�������Ũ���ֿ�ʼ����������Ϊ�������ٶȽϵ�ʱ��SO2���岻������Һ��ֽӴ�����Ӧ���ܳ�ֽ��У����������٣����������ٶȹ���ʱ��SO2���������ֱ�Ӵ���Һ��������������ٶ�Ϊ800 r/minʱ����ԭ��Һ���������Ũ�ȴ�14.05 g/L����ˣ������ٶ�Ϊ800 r/minʱ�黹ԭЧ����á�
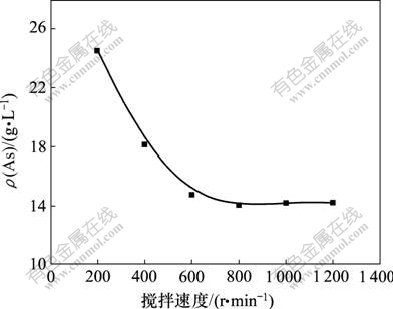
SO2����Ϊ3 kg/h����Ӧʱ��Ϊ1 h����Ӧ�¶�Ϊ����
ͼ6 �����ٶȶ��黹ԭ�ʵ�Ӱ��
Fig.6 Effect of stirring speed on ratio of arsenic reduction
�о�������SO2��ԭ20 L��ͭ�����ˮ���Ż��������£�SO2����Ϊ3 kg/h����Ӧʱ��Ϊ1 h����Ӧ�¶�Ϊ���£������ٶ�Ϊ800 r/min���ڸ��Ż������£�SO2��ԭ���ˮ���������Ũ�ȴ�160.06 g/L����14.05 g/L����Ļ�ԭ�ʴ�91.25%��
2.6 ��ˮ��ȶ�ͭ������Ӱ��
ͼ7��ʾ�ǵ�����ʱ��Ϊ2 h��ˮ����Ϊ400 mL/h��������Ϊ400 mL/hʱ��ˮ��ȶ�ͭ������Ӱ�졣��ͼ7�ɿ���������ˮ���Ϊ5 g/Lʱ��ͭ�ķ�����Ϊ95.18%����ķ�����Ϊ50.05%��ͭ����ۺϷ���Ч����á�������Ϊ���Ž�ˮ��ȵ����ӣ���ˮ��H+��Ũ����������С����Ļ������½����������ڷ�Һ�е������ӣ���һ���̶���������H3AsO4�ĵ��룬�Ӷ�AsO43-��ɢ��������������С����ķ����ʼ�С��
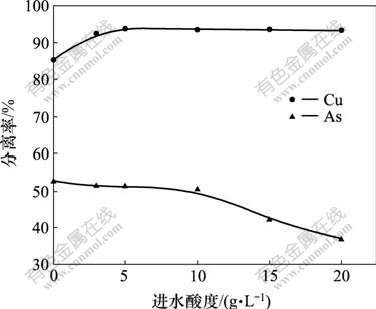
Fig.7 Effect of influent acidity on separation of
copper and arsenic
2.7 ˮ���ٶ�ͭ������Ӱ��
ͼ8��ʾ�ǵ�����ʱ��Ϊ2 h����ˮ���Ϊ5 g/L��������Ϊ400 mL/hʱˮ���ٶ�ͭ������Ӱ�졣�ɼ���ͭ�ķ���������ˮ���ٵ����Ӷ����ͣ�����ķ�����������ˮ���ٵ����Ӷ����ӣ���ˮ����Ϊ400 mL/hʱ, ͭ�ķ����ʴ�95.12%����ķ����ʴ�50.02%��ͭ����ۺϷ���Ч����á�������Ϊ����ˮ���ٵ����ӣ�Ĥ�����Ũ�Ȳ������ɷƿ˵�һ����J=-DAs��dc/dx[13](���У�JΪ��ɢͨ����DΪ��ɢϵ����AsΪ��ɢ��������dc/dxΪŨ��仯)���Եõ���Ũ��Խ����ɢͨ����Խ����ɢ���̽���Խ�죬ʹ��ͭ�����ˮ�е�ͭ�����������һ����ɢ��Խ�ࡣ��ˣ�����ˮ���ٵ����ӣ�ͭ������������Ҳ���������ӣ�����ͭ���ڲ�Һ�е�����С��ͭ�ķ����ʼ�С��������ɢ���������������ӣ�������ķ���������

ͼ8 ˮ���ٶ�ͭ������Ӱ��
Fig.8 Effects of water flow rate on separation of
copper and arsenic
2.8 �����ٶ�ͭ������Ӱ��
ͼ9��ʾ�ǵ�����ʱ��Ϊ2 h����ˮ���Ϊ5 g/L��ˮ����Ϊ400 mL/hʱ�����ٶ�ͭ������Ӱ�졣�ɼ���ͭ�ķ��������������ٵ����Ӷ�������ķ������������ٵ����Ӷ���С����������Ϊ400 mL/hʱ��ͭ�ķ�����Ϊ94.96%����ķ�����Ϊ49.95%��ͭ����ۺϷ���Ч����á�������Ϊ���������ٵ����ӣ���Һ��Ĥ�Ӵ���ʱ���̣�ͭ���������������٣����ڲ�Һ�е������ӣ�ͭ�ķ��������ӡ�ͬʱ����ˮ��ɢ��������������С����ˮ�������������H3AsO4�ĵ��룬���AsO43-��ɢ��������������С��ʹ��ķ������½���
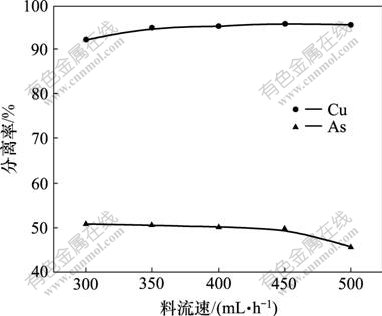
ͼ9 �����ٶ�ͭ������Ӱ��
Fig.9 Effect of material flow rate on separation of
copper and arsenic
3 �� ��
a. SO2��ԭ20 L��ͭ�����ˮ���Ż��������£�SO2����Ϊ3 kg/h����Ӧʱ��Ϊ1 h����Ӧ�¶�Ϊ���£������ٶ�Ϊ800 r/min���������£��������Ũ�ȴ�160.06 g/L������14.05 g/L����Ļ�ԭ�ʴ�91.25%��
b. ��ɢ�������̵��Ż��������£���ˮ���Ϊ 5 g/L��ˮ����Ϊ400 mL/h��������Ϊ400 mL/h���������µõ���������ͭ������Ũ��Ϊ1.76 g/L���������Ũ��Ϊ6.86 g/L����Һ��ͭ������Ũ��Ϊ34.86 g/L���������Ũ��Ϊ6.58 g/L��ͭ�ķ�����Ϊ95.12%����ķ�����Ϊ50.02%��
c. ����SO2��ԭ-��ɢ�������Ը�ͭ�����ˮ����ͭ����룬�������Ũ�ȴ�160.06 g/L������Һ�е�6.58 g/L��ͭ������Ũ�ȴӸ�ͭ�����ˮ�е�37.4 g/L�����������е�1.76 g/L��ͭ����õ�����Ч���룬ͭ���ܷ����ʴ�94.71%������ܷ����ʴ�95.63%��
d. �������е�ͭ������Ũ�����ͭ�����ˮ�е�ͭ������Ũ����ȴ���Ƚ��ͣ��ɿ��Ƿ�������ͭ����ʹ�ã���ɢ������Һ���鼰�������Ũ�ȴ���Ƚ��ͣ��ɲ���ˮ�����������ͭ��
�ο����ף�
[1] �� ��. �������Է�ˮ�����¹���[J]. ������ҵ�ߵ�ר��ѧУѧ��, 2005, 15(1): 10-11.
LIU Qi. A new techniques for high concentration arsenic acid waste water[J]. Journal of Luoyang Technology College, 2005, 15(1): 10-11.
[2] �� ��, �� ��, �ܻ�ǿ. �������Է�ˮ������о�[J]. ƽ��ɽʦרѧ��, 2004, 19(5): 37-40.
LIU Qi, WANG Bin, ZHOU Hua-qiang. A study of the high concentration of arsenic acid waste water[J]. Journal of Pingdingshan Teachers College, 2004, 19(5): 37-40.
[3] ������, ���ǿ, л����, ��. ͭұ������¯�̳������������к�����[J]. ���ϴ�ѧѧ��: ��Ȼ��ѧ��, 2006, 37(1): 73-78.
ZHANG Rong-liang, QIU Ke-qiang, XIE Yong-jin, et al. Treatment process of dust from flash smelting furnace at copper smelter by oxidative leaching and dearsenifying process from leaching solution[J]. Journal of Central South University: Science and Technology, 2006, 37(1): 73-78.
[4] ׯ����, ����Ԫ, ��С��, ��. �����ˮ�����о���չ[J]. ��ҵˮ����, 2004, 24(7): 13-17.
ZHUANG Ming-long, CHAI Li-yuan, MIN Xiao-bo, et al. Process of the research on the treatment of As-containing wastewater[J]. Industrial Water Treatment, 2004, 24(7): 13-17.
[5] Dapaah A R K, Ayame A. Solvent extraction of arsenic from acid medium using zinc hexamethylenedithiocarbamate as an extractant[J]. Analytica Chimica Acta, 1998, 360(1/3): 43-52.
[6] Jay J A, Blute N K, Hemond H F, et al. Arsenic-sulfides confound anion exchange resin speciation of aqueous arsenic[J]. Water Research, 2004, 38(5): 1155-1158.
[7] Nagarale R K, Gohil G S, Shahi V K, et al. Recent developments on ion-exchange membranes and electro-membrane processes[J]. Advances in Colloid and Interface Science, 2006, 119: 97-130.
[8] Strathmann H. Ion-exchange membrane separation processes[J]. Membrane Science and Technology, 2004, 9: .
[9] Kentish S E, Stevens G W. Innovations in separations technology for the recycling and re-use of liquid waste streams[J]. Chemical Engineering Journal, 2001, 84(2): 149-159.
[10] ���־, �� ��, �۽�ӱ, ��. Ĥ�����ڹ�ҵ��ˮ�����е�Ӧ���о���չ[J]. ��ҵˮ����, 2006, 26(4): 1-4.
XU De-zhi, XIANG Bo, SHAO Jian-ying, et al. Application of membrane technology to the industrial wastewater treatment[J]. Industrial Water Treatment, 2006, 26(4): 1-4.
[11] ̷�¾�, ��ΰ�, ������. Ĥ��ˮ�����������о���Ӧ����״[J]. ����������ѧ, 2006, 32(6): 27-30.
TAN De-jun, L? Wei-ya, WANG Ya-qin. Research and application status of membrane separation for water treatment[J]. Environmental Protection Science, 2006, 32(6): 27-30.
[12] �ν���. Ĥ���뼼������Ӧ��[M]. ����: ��ѧ��ҵ������, 2003.
REN Jian-xin. Membrane separation technology and its applications[M]. Beijing: Chemical Industry Press, 2003.
[13] ������. ұ������ѧ�빤��[M]. ����: ��ѧ������, 2004.
ZHANG Qi-xiu. Metallurgical separation science and engineering[M]. Beijing: Science Press, 2004.
�ո����ڣ�2008-05-26�������ڣ�2008-09-23
������Ŀ��������Ȼ��ѧ����������Ŀ(50774100)
ͨ�����ߣ��� ��(1971-)���У����������ˣ���ʿ�������ڣ�������Դѭ�������о����绰��0731-88877655��E-mail��csuzb@vip.163.com


