���±�ţ�1004-0609(2008)08-1555-05
���ε�ⷨ�Ʊ�����м�Ͻ�
��̶��������ܣ���͢������ ������
(������ѧ ������ұ��ѧԺ������ 110004)
ժ Ҫ��
�о���LiCl-LiF-Li2CO3�������ϵ���³�ʽ��Һ�����۽ṹ�����������м�Ͻ�Ĺ��չ��̣���������Li2CO3Ϊԭ�ϴ���LiCl�ĵ����̡��������ε�����Dz����������еķ��綯�ơ��۵�ѹ�������ȹ��ղ�������Ⲩ��ͼ��ͨ����λ���Ʒ�����Li2CO3�ļ������ڣ�ͬʱ���ݵõ��ĺϽ��Ʒ�е�﮺���̽��Ӱ�����Ч�ʵ����ء�������������綯��������ܶ����Ӷ�������2%��Li2CO3��ʹ���綯�ƽ���0.5 V��ͨ�����Ƶ�λ����ü�������Ϊ15 min����680 �桢�����ܶ�Ϊ0.62 A/cm2�������³������3 h�������Ƶ���﮺����ߴ�7.93%����﮺Ͻ𣬵���Ч�ʿɴ�74.1%��
�ؼ��ʣ�
��﮺Ͻ������ε�������綯��������Ч����
��ͼ����ţ�TF 827.2 ���ױ�ʶ�룺A
Preparation of Al-Li master alloys by molten salt electrolysis
LI Ji-dong, ZHANG Ming-jie, ZHANG Ting-an, LI Dan, ZHANG Zhuo
(School of Materials and Metallurgy, Northeastern University, Shenyang 110004, China)
Abstract: Al-Li master alloys were prepared using sinking-mode aluminum liquid as cathode and a mixture of LiCl-LiF-Li2CO3 as molten salt electrolyte in a laboratory cell. The electrolysis process with Li2CO3 as raw material instead of LiCl was studied in detail. The technological parameters such as back electromotive force, cell voltage, current and electrolysis waveform were measured by testing device of molten salt electrolysis. The period of Li2CO3 feeding was adjusted by the method of electric potential control. At the same time, the factor that affects current efficiency was discussed according to the lithium content of alloys obtained. The results indicate that back electromotive force increases with increasing current density and decreases by 0.5 V after adding 2% Li2CO3, the feeding period is 15 min measured by the method of electric potential control. Finally, the Al-Li alloy with the lithium content of 7.93%(mass fraction) can be obtained by electrolyzing for 3 h at the current density of 0.62 A/cm2 and at 680 ��, and the current efficiency can reach 74.1%.
Key words: Al-Li alloy; molten salt electrolysis; back electromotive force; current density
�����Ȼ��������Ľ���Ԫ�أ��ܶȽ�Ϊ0.534 g/cm3���������в���1%(��������)��﮿�ʹ�Ͻ��ܶȽ���3%������ģ������Լ6%��������泣������Ͻ𣬿�ʹ������������10%~15%���ն����15%~20%[1?3]����ˣ���﮺Ͻ���Ϊһ�ֵ��ܶȡ��ߵ���ģ������ǿ�Ⱥ߱ȸնȵ�����ṹ���϶��㷺Ӧ���ں��պ��켰����̫�յ�����[4?5]��
Ŀǰ��������﮺Ͻ�ķ�����Ϊ�Բ���,�������м���������������������һ��Ũ�ȵ���﮺Ͻ����ε�ⷨ������Һ��������������ɵĽ��������������������ɢ����Һ�У�һ��ֱ�ӺϽ���Բ���������﮺Ͻ���ȣ����ε�ⷨ����Ũ�Ⱦ��ȡ�﮵�������С���������������ƺ͵ͳɱ����ŵ㣬������������ǵĹ㷺�о�[6?11]��ͬʱ���һ���Ͻ�ҲӦ�������������Ͻ���Ʊ����̣������ε�ⷨ��ȡ���ȺϽ����ֺϽ��[12?13]����Li2CO3Ϊԭ�ϴ���LiCl���е�ⲻ����������������Ի�������Ⱦ�����������ܺĺ������ɱ����������߲����������壭��������о���LiF-LiCl�������ϵ�У���Li2CO3Ϊԭ�ϣ���ʯī����������Һ�����������ε�ⷨ��ȡ��﮺Ͻ�Ĺ��չ��̣�ͬʱ���ضԵ����̵�Ӱ�������練�綯�ơ�����Ч�ʺͺϽ�Ũ�ȵȽ���������̽�֡�
1 ʵ��
ʵ�������õ��۽ṹ��ͼ1��ʾ��Ϊʹ��ھ�Ե�����ײ����ĸ����ڳ�����ʯī�����У��Դ��дɱ����ܵ�ʯī������������ס����Һ��Ϊ�������¶���DWT?702�����¶��Զ�����װ�ÿ��ƣ������ڡ�0.5 �棬���·�Χ��0~1 000 �档
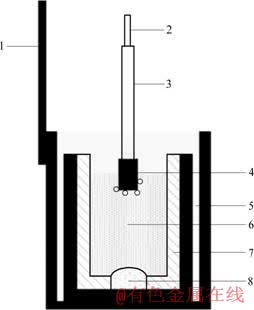
ͼ1 ���ۼ�ͼ
Fig.1 Configuration of electrolytic bath: 1�� Iron outer with guide rod; 2��Anode guide rod; 3��Ceramic protection sleeve; 4��Graphite anode; 5��Graphite crucible; 6��Electrolyte; 7��Insulated sleeve; 8��Aluminum liquid
1.2 ������װ�á����ε������
�����������Ƶ����ε�����Dz����������еķ��綯�ƣ���ԭ��������[14?15]���ƣ�����������ʾ�������Ļ����ϣ�ʹ������汸��ʾ�����Ĺ��ܡ�ͨ��������IJ����ܾ�ȷ��ʾ�����ε������е��¶ȡ����綯�ơ��۵�ѹ����������Ҫ��������ȷָʾ���ֻ�����ֽ��������ر������ڵ����кϽ���Ʊ���
ʵ���������Ȼ��Ϊ���������������ķ�������ˮLiCl��LiF��Li2CO3��Ϊ�Ϻ��Լ����������ķ������Լ������е�ҩƷ����300 ��ĺ��µ������к��2 h������á�
2 ���������
Ҫ�ӵ�����е���������������Һ�γ���﮺Ͻ���ѡ֧�ֵ����Ӧ�нϸߵķֽ��ѹ������Li+��������λ�ϸ��������ҵ�������������������Ϊ﮵���֧�ֵ���ʡ�ͬʱ��Ϊ���ڵ������в������������ʣ���ѡ��LiCl-LiF�������Ϊ����ʣ������ڵ������н���Li+�ŵ���������֤�˺Ͻȡ�����Li2CO3����LiCl��Ϊ���ԭ�ϣ��������CO2��������Ⱦ�ҽ����˲۵�ѹ���������ܺġ����ڸ���ϵ���������ܽ��������ޣ�����ģ������������������ڼ��ϡ��ټ���ԭ�����Li2CO3�ĺ������ڱ��о���ѡ��LiCl60%-LiF40%��Ϊ�����������ϵ������LiCl�ӷ�������ڼ�Ҫע�ⲻ�ϲ������ʡ���ͼ2��ʾ��LiCl-LiF�Ķ�Ԫ��ͼ��֪���õ��������µij����¶���650 �����ң�ͬʱ���ǵ�����¶Ȳ��ɵ��������۵�660�棬���ǹ��ߵ��¶���ʹ�õ���ʻӷ����ؼ�����Ч�ʽ��ͣ�����ڱ��о��н�����¶ȶ�Ϊ680 �档
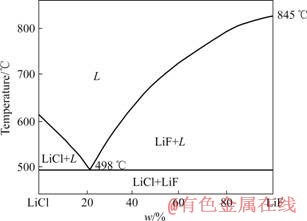
ͼ2 LiCl-LiF������ϵ��ͼ
Fig.2 Phase diagram of LiCl-LiF system
2.2.1 LiCl-LiF��ϵ�еķ��綯��
��ν�����綯�ơ���ָ�ڵ������е�ʵ�ʷֽ��ѹ���������۷ֽ��ѹ����������ѹ����������ѹ��ɡ�
![]()
��680 ����LiF-LiCl��ϵ���ı�����ܶȣ���÷��綯����ͼ3������A��ʾ�����綯�������������ܶ����Ӷ����ӡ�������Ϊ��ʱ����ʱ������ͨ������������֮������һ����λ�Լ1.5~1.6 V֮�䣬��ʱ�൱�ڵ�����ⷴ�����ĵ綯�ƣ����������ڲ����������Ҳ������[15]������ӳ��̿������������ʱ�����ĵ�λ���ڵ�����ҪԤ�ȵ��15 min��ʹ��������̿�缫�ϵ��������IJ�ʹ̿�缫��ȫʪ��
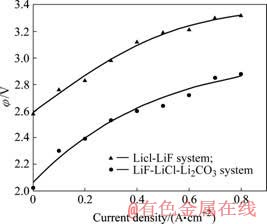
ͼ3 �����ܶ��뷴�綯�ƵĹ�ϵ
Fig.3 Relationships between current and back EMF (60%LiCl- 40%LiF, t = 680 ��)
2.2.2 �ٽ�����ܶ�
�����Ӵ�����ܶ�,�����������ܶȼӴ�1.0 A/cm2���ϱ㷢���������������е�����ЧӦ����ʱ�۵�ѹ�������ߣ�����ͻȻ������С�������������������ܱ߳��ֻ���ŵ������Ҳ��ڷ����������죬��˱�ʵ���е����ٽ�����ܶ�Ϊ1.0 A/cm2���ٽ�����ܶȴ�С��Ҫ���Ȼ����Ũ���йأ�����LiCl���IJ������ĺͻӷ�ʹ����ϵ�е��Ȼ����Ũ�Ƚ��ͣ������Һ�治�Ͻ��ͣ�����Һ���µ�����������ٵ������������ܶȽӽ��ٽ�����ܶ�ֵ������ϵ���Ȼ����Ũ�Ƚ��͵�һ���̶�ʱ���������ӷŵ磬��ʱ������������С�Ϊ�˱�������ЧӦ��Ƶ�����������������趨�ڲ�������������LiCl����֤Һ��߶Ⱥͼ����С��
2.2.3 LiF-LiCl-Li2CO3ϵ�еķ��綯��
����LiF-LiCl��Ϊ֧�ֵ���ʲ�����ϵ����Li2CO3ʱ�������ܶȶԷ��綯�Ƶ�Ӱ����ͼ3������B��ʾ��
����LiF-LiCl��ϵ������Li2CO3֮��,����ͬ�ĵ����ܶ��£����綯�ƽ�����0.5 V���ҡ���˵����ʱ���������Ѳ�����Cl?�ŵ�������¼����Li2CO3�����O2?�ŵ��ˡ�����O2?������λ����Cl?��������λ����˷��綯������֮���͡�
�ڵ���¶�Ϊ680 �桢���������ܶ�Ϊ0.4 A/cm2�����£����15 min�ȶ���ÿ�ΰ���������2%��Li2CO3�����ʱ���뷴�綯�Ʊ仯�ļ�������������ͼ4��ʾ��
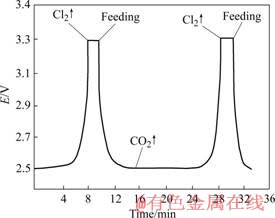
ͼ4 ��������������
Fig.4 Period curve of material feeding
Ϊ�˱�֤Li2CO3������⣬��ֹ����Li2CO3�������ܽⲻ�˶�ʹ����ʷ�ճ��������Li2CO3��Ũ�Ȳ���������������ӷŵ磬��ˣ�ʵ���в����˵�λ���Ʒ���ط��綯�Ƶı仯�������ڼ��ϡ��ټ��ϵ�ԭ��ʱ����Li2CO3����Li2CO3�ֽ�����Li2O��CO2ʱ������O2?��������λ����Cl?��������λ�����������Ϸų�����CO2��
![]()
��ʱ���綯���½�����λ������Li2CO3����������ģ�O2?��Ũ�Ȳ��Ͻ��ͣ������ں���������µ�⣬��缫�Ϸ�Ӧ�ٶ��Ǻ㶨�ġ���O2?���ٵ�һ���̶Ⱥ�����ɢ���缫������ٶȲ����Թ����缫��Ӧʱ�����λ������Cl?�ŵ�����Cl2�����綯����缫��λ���߲�����������ǰ�����ֵ����ʱ�貹�����Li2CO3��Cl2���綯�ƵĹ��ɱ仯������һ���������ڡ��ڱ�ʵ�������£���������ԼΪ15 min��
��680 ���£���ȡ30 g��������������̿��������������1 cm�ʹ������ﵽ12.5 cm2���ֱ��ڲ�ͬ�ĵ����͵��ʱ�����������ȡһ��Ũ�ȵ���﮺Ͻ��Ҹ���ʽ(2)������Եĵ���Ч�ʣ�ʵ�������1���С�

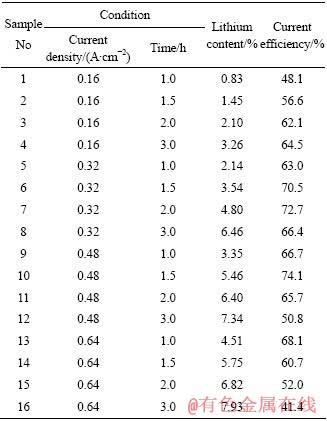
��1 ��ͬʵ�������µ����﮺Ͻ��ʵ����
Table1 Results of preparation of Al-Li alloy by electrolysis under different conditions
1) ����Ч�ʵ��о�
�ӱ�1��֪�������������ܶ�Ϊ0.16 A/cm2ʱ������Ч����ʱ����ӳ�����ߣ��ڵ����ܶ�Ϊ0.48 A/cm2ʱ�����1.5 h�����Ч�ʴﵽ���ֵ74.1%�������ӳ����ʱ�䣬����Ч���������͡����ʱ�������Ч�ʵĹ�ϵ��ͼ5��ʾ��
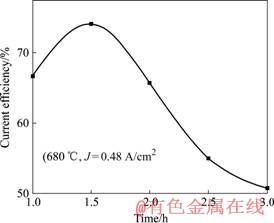
ͼ5 ���ʱ�������Ч�ʵĹ�ϵ
Fig.5 Relationship between electrolysis time and current efficiency
�����ݵı仯�п��Կ�������Ч�ʡ��Ͻ�Ũ�Ⱥ͵��ʱ�������Ĺ�ϵ��һ�������ܶ��£��ڵ��ij��ڣ�����Ч���������ӣ������ŵ��ʱ����ӳ����Ͻ����Ũ��Խ��Խ�ߣ����Ͻ�Ũ�Ƚӽ�5.0%~5.4%ʱ������Ч����ʱ����ӳ������͡���ʱ������﮵������ٶȴ��������������ɢ�ٶȣ�����ﮱ��������Һ���档������Һ���ڵ��۵ײ���������﮵��ܶȺ��ᣬ��˴�����������Һ�ϱ�������������ɢ����Һ���ϸ�������������ȼ����ģ�����һ�������ܽ�������У���Щ�������﮵���ʧ���µ���Ч�ʽ��͡�
��ʵ�����л����Կ�������һ�����ʱ�������£��ı����������ܶ�Ҳ��Ӱ�����Ч�ʵı仯�������ܶ������Ч�ʵĹ�ϵ��ͼ6��ʾ��
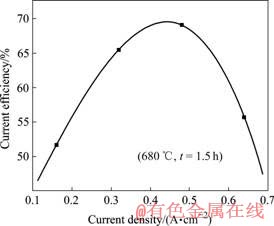
ͼ6 �����ܶ������Ч�ʵĹ�ϵ
Fig.6 Relationship between current density and current efficiency
������ӵ����ܶȣ���Ӧ�ٶȼӿ죬����Ч�ʲ�����ߣ��ﵽһ���̶��Ժ�����Ӵ�����ܶȣ�����Ч�����͡���Ϊ��ʱ�������������ܶȳ������ӣ����������ŷ�������ʹ����ʵ�ѭ��������ǿ�����ڴ˽ṹ���۵���������û�б�������������������IJ��ֽ�����ױ����������������������¶��η�Ӧ�ķ������Ӷ��������Ч�ʵĽ��͡�
����ߵ���Ч�������ϣ���Ȼ�������Ҫ������Ľ����۽ṹʹ���������ָ��������Ӵࡢ�Ͻ���﮺�������̫�ߡ����ⷢ������ЧӦ�ȷ��档
2) ���ʱ����Ͻ�Ũ��
�ɹ�ʽ(2)��ʵ�������Կ�������ߵ����ܶȡ��ӳ����ʱ�䶼�������ӺϽ��е�﮺�������ʵ���У�﮵�����������߿ɴ�7.93%��
3 ����
1) ���LiCl-LiF��ϵ�����綯�������������ܶ����Ӷ������ٽ�����ܶȾ�����Ϊ1.0 A/cm2������2%��Li2CO3��ʹ���綯�ƽ���0.5 V���ң�ͨ�����Ƶ�λ����ü�������Ϊ15 min��
2) ����Ч���ܵ��ʱ��͵����ܶȵ�Ӱ����߿ɴ�74.1%�������͡�
3) ��680 �棬�����ܶ�Ϊ0.64 A/cm2�������£����3 h����ȡ﮵����������ߴ�7.93%��﮺Ͻ���Li2CO3Ϊԭ�ϴ���LiCl���е���������������Ի�������Ⱦ�����������ܺĺ������ɱ�����ˣ�����������ǽ�����Ʊ������Ͻ�ķ�չ����
[1] �ܲ���, ������, �쳯��, ���˱�, ��־��. ������﮺Ͻ���о��ͷ�չ[J]. ���ϵ���, 2004, 18(5): 30?32.
ZHOU Chang-rong, PAN Qing-lin, ZHU Chao-ming, HE Yun-bin, YIN Zhi-min. Development and study of new types aluminum-lithium alloys[J]. Material Review, 2004, 18(5): 30?32.
[2] ����Ƽ, ֣����, ����ƽ. 2197���-�Ͻ����֯������[J]. �й���ɫ����ѧ��, 2004, 14(12): 2066?2072.
HUANG Lan-ping, DENG Zi-qiao, HUANG Yong-ping. Microstructure and properties of 2197 Al-Li alloy[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(12): 2066?2072.
[3] ���Ƿ�, ֣����. ��﮺Ͻ��о���������ʷ����״[J]. ���ϵ���, 2003, 17(2): 18?20.
YIN Deng-feng, ZHENG Zi-qiao. History and current status of aluminum-lithium alloys research and development[J]. Material Review, 2003, 17(2): 18?20.
[4] FRIDLYANDER I N. Current-technology aluminum alloys for aerospace applications[J]. Metal Science and Heat Treatment, 2001, 7(7): 7?8.
[5] GUPTA R K, NIRAJ N, NAGASIREESHA G, SHARMA S C. Development and characterization of Al-Li alloys[J]. Mater Sci & Eng A, 2006, 420(2): 228?234.
[6] �����, ʯ����, ������. ���ε�ⷨ��ȡAl-Liĸ�Ͻ�[J]. ��ұ����, 2004, 24(3): 56?57.
XU Jun-li, SHI Zhong-ning, QIU Zhu-xian. Preparation of Al-Li master alloy by molten salt electrolysis[J]. Mining and Metallurgical Engineering, 2004, 24(3): 56?57.
[7] ���˸�, ������, ̷�Ǿ�. ���ε�ⷨ��ȡ��Ũ�ȵ���﮺Ͻ�[J]. �����, 1998, 12(1): 38?40.
DAI Xing-fu, ZHANG Ming-jie, TAN Ya-ju. Preparation of Al-Li alloy with high concentration by molten salt electrolysis[J]. Light Metals, 1998, 12(1): 38?40.
[8] SATO Y, SAITO S, ARAIKE E, SUZUKI T, YAMAMURA T. Electrode behavior for the electrolytic production of Al-Li alloy by using molten chlorides[J]. Journal of Japan Institute of Light Metals, 1993, 43(1): 33?39.
[9] SATO Y, KARIYA H, SUZUKI T, SAITO S, YAMAMURA T. High efficient electrolytic production of Al-Li alloy by using Li2CO3 as a source of lithium[J]. Journal of Japan Institute of Light Metals, 1998, 48(3): 138?142.
[10] ������, ��̶�, ��ҫ��. Li2CO3��KCl-LiCl�����еĵ绯ѧ��Ϊ[J]. ������ѧѧ��: ��Ȼ��ѧ��, 2005, 26(6): 570?573.
ZHANG Ming-jie, LI Ji-dong, WANG Yao-wu. Electrochemical behavior of lithium carbonate in KCl-LiCl melt[J]. Journal of Northeast University: Natural Science, 2005, 26(6): 570?573.
[11] COX A, MORRIS J W. Improving energy efficiency of electrowinning of lithium[J]. Light Metal, 1998, 11(6): 1295?1298.
[12] YANG Shao-hua, GAO Bing-liang, WANG Zhao-wen, SHI Zhong-ning, BAN Yun-gang, KAN Hong-min, CAO Xiao-zhou, QIU Zhu-xian. Preparation of Al-Sc alloys by molten salts electrolysis[C]// Powell A. Innovation in Eleotrometallurgy. Orland: TMS, 2007: 1?4.
[13] ��̶�, ������, ��͢��, ���ٻ�. ���ε�ⷨ����Al-Sr�Ͻ��з��綯�ƺ͵���Ч�ʵ��о�[J]. ϡ�н���, 2007, 31(4): 577?580.
LI Ji-dong, ZHANG Ming-jie, ZHANG Ting-an, YANG Shao-hua. Research on the EMF and current efficiency in the process of Al-Sr alloy preparation by molten salt electrolysis[J]. Chinese Journal of Rare Metals, 2007, 31(4): 577?580.
[14] ������, ������. ���ε绯ѧԭ����Ӧ��[M]. ����: ��ѧ��ҵ������, 2006: 162?163.
ZHANG Ming-jie, WANG Zhao-wen. Principle and application of electrochemistry of fused salts[M]. Beijing: Chemical Industry Press, 2006: 162?163.
[15] QIU Z X, ZHANG M J. Studies on anode effect in molten salts electrolysis[J]. Electrochemical Acta, 1987, 16(4): 607?609.
������Ŀ��������Ȼ��ѧ�����ص�������Ŀ(50574024)
�ո����ڣ�2007-11-30�������ڣ�2008-04-15
ͨѶ���ߣ���̶�����ʿ�о������绰��13840413898��E-mail: lijidong1980@tom.com
(�༭ ��ѧ��)


