���ڶ��ǻ���Ƥ��������ø��ӫ�����ߴ���ϵͳ
�ⶨ���ϸ˾�����
տѩ�ԣ����氲������������ɣ��ܷң�����
(��ɳ������ѧ ��ѧ����������ѧԺ������ ��ɳ��410076)
ժ Ҫ��
ժ Ҫ����һ�ִ���Ȼ������ǻ���Ƥ��(4-hydroxycinnamic alcohol, HCA)Ϊ������������ø(HRP)����������ǻ���Ƥ��-������������ø-������������ϵ�����ǻ���Ƥ������ֻ�м�����ӫ�⣬��HRP���¿ɱ�H2O2�����ɶ��������ö�������315 nm�ļ��������ܷ��䲨��Ϊ467 nm��ǿӫ�⣬���ҷ�Ӧ��ϵӫ��ǿ������ֵ��HRP����һ��Ũ�ȷ�Χ�ڳ�������ء����ݴ˹�ϵ�;��������߶���ԭ���������ò��ϸ˾�����ⶨ��ӫ��ø�����ߴ�����ϵ���������߲ⶨ������pHֵ��HRP-BrAb������BSA�����ٵȽ����Ż��������Ʊ�������ϵ�ⶨ�ò��ϸ˾����������Ũ�����Է�ΧΪ2.7~90 ��g/L�������Ϊ2.7 ��g/L����Ա�ƫ��Ϊ4.6%�����ǻ���Ƥ���ڿ����н��ȶ������������������ٴ��Ͽɴ��洫ͳHRP���
�ؼ��ʣ�
���ǻ���Ƥ����HRP ӫ����������ϸ˾����������ߴ�����ϵ��
��ͼ����ţ�O656.2 ���ױ�־�룺A ���±�ţ�1672-7207(2010)03-0890-06
An enzyme-linked fluoroimmunosensing system for Brucella melitensis antibody detection based on a novel substrate 4-hydroxycinnamic alcohol for HRP
ZHAN Xue-hui, ZHOU Sui-an, GONG Fu-chun, LI Fei, CAO Fen, LI Xia
(School of Chemical and Biological Engineering, Changsha University of Science and Technology,
Changsha 410076, China)
Abstract: A natural product, 4-hydroxycinnamic alcohol (HCA) was used as a substrate for HRP in enzyme-linked fluoroimmunoassay. In enzymatic reaction procedure, HRP-Brucella melitensis antibody conjugate (HRP-BrAb) catalyze the polymerization of HCA by H2O2, and the HCA is partly converted to polymers, a fluorescent species. The fluorescence increase of the HRP-enzymatic product at emission of 467 nm (excitation at 315 nm) is proportional to the concentration of HRP-BrAb binding to the Brucella melitensis antigens, which were entrapped in cellulose-paraffin matrix. The linear range of determination for BrAb is 2.7-90 ��g/L with the relative standard deviation of 4.6%. The detection limit is 2.7 ��g/L. HCA is stable in air and non-toxic to human health. The proposed method can be used for analysis of commercial formulation and plasma sample with satisfactory results.
Key words: 4-hydroxycinnamic alcohol; HRP fluorogenic substrate; Brucella melitensis antibody; immunosensing system
����ø�����߷������������ø�Ĵ��Ŵ�����߷�Ӧ�������ԣ����з��������ȸߺ�ѡ���Ժõ��ص㣬��ʵ���еõ��˹㷺Ӧ�á�����������������ø(HRP)��ø�����߷���������Ӧ����ɹ��ķ���֮һ[1-5]���÷���ͨ������HRP��ǿ���/��ԭ��ͨ��HRP��H2O2����ø������ɲ�ͬ���ۻ��۲�������ʽ��ż�������ʵȡ�Ȼ���÷ֹ��ȡ��绯ѧ��ѧ/�绯ѧ����ȷ����ⶨø������Ĺ�/���źţ���Ӳⶨ����/��ԭ��뿹ԭ����ˣ�HRPø������ϵ��������ѡ���������ԡ�������ȶ��Ե����ܡ�Ŀǰ��HRP��Ҫ�����б�������[6]����������[7]����������[8]�Լ��ɱ���������������һЩż��Ⱦ��[9]�ȣ����ǣ���Щ����������²��㣺(1) �ȶ��Բ����������ڿ����м��ױ����������ﱣ�����ѣ�һ��ֻ���������ã�(2) H2O2 ��������������ź�ǿ����ϵ�����źŽ�ǿ��(3) �еĵ����Ӧ��������������ж�������[10-11]����ż��Ⱦ�ϡ������ͱ������ȡ�����������⣬�������߶�HRP ��������о������ò��ϸ˾�����Ϊ�������������Զ��ǻ���Ƥ��ΪHRP �����ø��ӫ�����߷����������÷������ڽ�ELISA������ø�Ļ��۷Ŵ�������ӫ������ż������绯ѧ����������-�ɼ���ȷ�����������нϴ���ߡ����ַ�����������Ѫ����Ʒ�ⶨ������������������ý�����Ǻϣ����������ٴ�������Ҫ��
1 ʵ��
1.1 ����
HITACHI F4500ӫ������ǣ�����ӫ��ⶨ�����ղ��䶯�ã����ڲ���ˮ���������CSS501�ͺ���ˮԡ�ۣ����ڿ��������¶ȡ�
1.2 �Լ�
������������ø(HRP�����ΪEC 1.11.1.7, �Ȼ���RZ��3)�Ͷ��ǻ���Ƥ��(4-hydroxylcinnamic alcohol��HCA)������Sigma��˾������ά�غ�ʯ���������Ϻ���ѧ�Լ���˾�����ϸ˾���ԭ(BrAg)�Ͳ��ϸ˾�����(BrAb)���ɺ���ʡ���������ְҵ����ѧԺ�ṩ��1.00 mmol/L ���ǻ���Ƥ������Һ����2.31 mg���ǻ���Ƥ��(Sigma��˾)����100 mL��ˮ�Ҵ��У��ܹⱣ�棬ʹ��ʱ��pH=6.8��B-R ����Һϡ�͡���ʵ�����õ�������Һ�ö�������ˮ�Ʊ���
1.3 ø�꿹��(HRP-BrAb)���Ʊ�
��10 mL pHֵΪ6.8�����Ỻ����Һ(PBS)�м���������HRP(3.5 mg)��2 mL �������Ϊ1%�����ȩ����ֻ�ϣ�������������12 h�����õ�����Һ���¶�Ϊ4 �桢Ũ��Ϊ10 mmol/L PBS��0.15 mol/L NaCl��Һ(pHΪ7.2)������ҹ�����ܽ���1 mL pHֵΪ9.6����0.15 mol/L NaCl��0.1 mol/L Na2CO3��ɵ���Һ�е�BrAb(5 mg)����������HRP-���ȩ��Һ��ϣ���4 ������24 h���õ�����Һ��10 mmol/L��pHֵΪ7.2��PBS��������Sephadose G-200���������˽�һ������������HRP-BrAb������(0.48 g/L)����4 �洢�汸�á�
1.4 ���ϸ˾���ԭ�Ĺ̶�
ȡ5.5 mg BrAg��12 mgţѪ�����(BSA)�ܽ���1.5 mL pHֵΪ7.0����PBS��(4 ��)������Һ��0.9 g����ά�ط۳�ֻ�ϣ�Ȼ����������ڸ���������4 ������������BrAg-BSA�ĸɷ���ʯ����������1?1���(ʯ�������ܽ���������)�������ѻӷ���(Լ5 min)�����õ��ĺ�״�Wѹ��ֱ��Ϊ6 mm�ľ�����ϩ(PVC)���У�����һ������ת��ñ��������֡���ά�ء�ʯ��֧����Ľṹ��ͼ1(a)��ʾ��
1.5 ������֡���ά�ء�ʯ��֧���������
ͨ����ת��ñʹ��ά�ء�ʯ����������ָ�����㼷��Լ0.1 mm����ˮ��ʪ��������������ɰֽ(0.05 mm)���⣬�ö�������ˮ��ϴ���ɻ�ø��µı��档
1.6 �ⶨ����
ø��ӫ�����߷���������ͼ1(b)��ʾ�������������£���1���������º��֧����A����5 mL����100 mL HRP-BrAb(0.48 mg/L)�Ͳ�ͬ�����BrAb (������)��ɵĻ�����Һ(��������Ϊ 0.1% ��BSA��pH=7.5��0.1 mmol/L Tris-HCl)������30 min����2�����������֧�����û���Һ(0.1 mol/L Tris-HCl-KCl��pH=7.5)��ֳ�ϴ��ӫ��ⶨǰ��������ͬ�Ļ���Һ�У��������õ�֧���尲װ����ͨ��Ӧ���С�

1��PVC ��ñ��2��PVC�ܣ�3��PVC���壻4���ܽ�����-ʯī���ʣ�5�����ϸ˾���ԭ(BrAg)
(a) ���ϸ˾���ԭ֧����ṹ��(b) ø�����ߴ��вⶨʾ��ͼ
ͼ1 ���ϸ˾�����ⶨ������ϵ
Fig.1 Configuration of biocomposite support body and schematic diagram of injection system coupling with fluometry
����2.5��10-7 mol/L HCA������Һͨ���䶯�ñ��뷴Ӧ�أ��ⶨ�����Ⲩ��Ϊ315 nm ʱ467 nm ��HCA��ӫ�⣬����һ������5��10-7 mol/L H2O2��HCA��Һ�У�������HCA��H2O2�ĵ�����Һ����֧�������ʱ��������֧��������HRP-BrAb-BrAg�������е�HRP��H2O2����HCA��ʹһ����HCAת��Ϊǿӫ������ʡ�ͨ���ⶨHCA������Һӫ��ǿ�ȵı仯�ɶ����ⶨ��Ʒ�е�BrAb��
2 ���������
2.1 ø����Ӧ��������������
���ǻ���Ƥ��(4-hydroxycinnamic alcohol��HCA)�ǹ㷺������ֲ�����ڵ���Ȼ���Գɷ֣����������Ƥ�������ͺ����ϸߣ�����ֲ������ͨ�����������γ�ľ֬�أ�������������[12-13]�����о��н�HCA����HRP�����BrAb�ⶨ�����źŷ��ӵ����ã���HCAΪ�����ø����Ӧ����������[14-16]�б��������ƣ����Ա�ʾΪ��ͼ2��ʾ������HCAֻ�к�����ӫ�⣬��HRP��H2O2����HCAʱ���������ɻ��м��壬Ȼ��2�������ɻ����м���ת��Ϊ���������(ǿӫ������)����ϵӫ��ǿ�����ӡ�
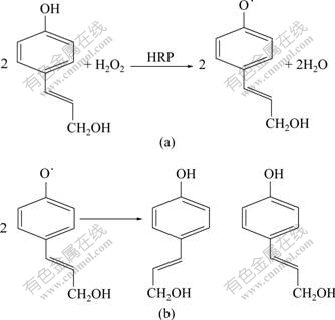
(a) ��ӫ����(b) ǿӫ�����
ͼ2 ø����Ӧ����
Fig.2 Mechanism of HRP-catalyzed reaction
�ھ������߷�Ӧ���������У�������Ʒ�е�BrAb�ͼ���ı���ҺHRP-BrAb������ϵ��̶���BrAg�ϡ����ӵ�֧��������ֱ����HRP-BrAb�����������Ʒ��BrAb�����ɷ��ȣ���ˣ���Ʒ��BrAb(������)Ũ����HCA��Һӫ��ǿ�����ӳɷ��ȡ�����DZ������������߷����ⶨBrAb�Ļ�����
��HCA-HRP-H2O2��Ӧ��ϵ��ӫ�����Խ����о����������������HCA��312 nm������1��������ӫ�ⷢ���(������Ϊ299 nm)��ͼ3��ʾ��HRP-BrAb��H2O2����HCA��ӫ�����ͼ�����Կ������ڵ���HCA��Һ�м���HRP-BrAb��H2O2��ø������467 nm����1���ϴ��ӫ�ⷢ���(��������Ϊ315 nm)������һ����Χ��ӫ��������HRP-BrAb��������ء�

����-�����Ỻ����Һ�У���2.5��10-5 mol/L HCA��5��10-5 mol/L H2O2��pH=4.5������Ӧ1 min
HRP-BrAb������Ũ��/(mg?L-1)��1��1.9��10-6; 2��9.6��10-7;
3��4.8��10-7; 4��2.4��10-7; 5��1.2��10-7; 6��6.0��10-8
ͼ3 HRP-BrAb��H2O2����HCA��ӫ�����
Fig.3 Fluorescence spectra of HCA solution catalyzed by HRP-BrAb
2.2 ����֧����������������������
��ԭ�����Ľ������ǿ�����ߴ�����ϵʵ��Ӧ�õ���Ҫ�ϰ�֮һ�����ﷴӦ�����������ѡ�ʹ����ά��-ʯ�������Ͱ���BrAg���������ڱ��ֻ����⣬֧��������ͨ������õ����¡�Ϊ�˽���HRP-BrAb��֧�������ķ�����������������BSA����ռ����ά��-ʯ�����ʶ����λ�㡣��ά�ض�HRP-BrAb��BrAb��������������ԣ����������߷�Ӧ������ά��(Cellulose)��ʯ��(paraffin)�������Ƚ����о�����1��ʾ�Dz��ò�ͬ��������ά�غ�ʯ���Ʊ��������֧�����õ�ӫ��ǿ�ȡ��ɱ�1��֪�������︴�����м�����������Ϊ0.1% BSA�ܽ���HRP-BrAb��֧�������ķ�����������������BSA����BrAb�� HRP-BrAb����ռ�ݻ��ʱ���Ķ���λ�㡣ʵ�黹������������ά�غ������������һ����HRP-BrAb�����ӫ����Ӧ��������¼���źŲ��ȶ����ʱ��о�����ά��/ʯ����������ѡ��Ϊ1?1��
��1 BSA��ӫ��ǿ�ȵ�Ӱ��
Table 1 Effect of BSA on fluorescence intensity

2.3 ��ҺpH��Ӱ��
��HCA��Һ������ӫ��ǿ������pHӰ���⣬HRP-BrAb�Ļ��Ժ�HRP-Ab-Ag����������ֵ���ȶ���Ҳ��pH��Ӱ�졣��pH��HCA��Һ������ӫ��ǿ�ȵ�Ӱ������о��������ʾ��pH��6ʱ��ӫ��ǿ����pH���Ӷ����ӣ�pH��6ʱ�����½����ơ��������pHӰ����HCA��̬�ͼ���̬��ƽ���ԭ��
��pH��HRP-BrAb�Ĵ����ü�HRP������Ӱ��Ҳ�������о��������ͼ4��ʾ���ɼ���HCAø����Ӧ�IJ����ڿɼ���315 nm�������շ壬ͨ���ⶨ315 nm�������շ���Թ���ø����Ӧ���ԣ�HRP-BrAb�������������������pH���Ӷ����ӣ���pH=5.5ʱ�����ȶ����ڸ���pH�£����������½�����������Ӧ�����pHΪ5.5������HRPֱ�Ӵ���Ӧ�����pH���в�ͬ(pH=5.0)��������HRP�����ɵ�BrAb������ʹHRP-BrAb������������ʹ pH����ø��Ӧ��ԭʼpH��Ե�ʡ���pH̫�Ͳ�����BrAb��BrAg�Ľ��ܽ�ϣ���������Һ�������︴����ı���ʱ��������HRP-BrAb��ʧ����ˣ����о��в��õ�pHΪ5.5��
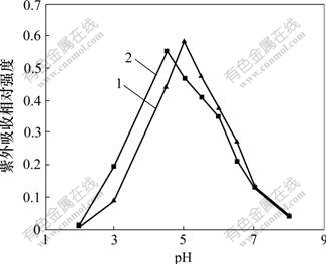
1��������������ø��2������-������������ø������
����ⶨ����Ϊ315 nm
ͼ4 pH��ø���Ե�Ӱ��
Fig.4 Effect of pH on activity of HRP
2.4 ���ٶ�ӫ��ǿ�ȵ�Ӱ��
��HCA��H2O2���������͵���ͨ��Ӧ����ʱ��HCA��H2O2��HRP-BrAb�Ӵ���������Ӧ��ʹ������ϵӫ���źŷ����仯������������ٶ�ֱ��Ӱ��HCA��H2O2��HRP-BrA�Ӵ����ᡣ��ͼ5��ʾ��������Һ����Խ�ͣ�ӫ���ź�����Խ�����ٹ��ͻ�ʹ����ʱ���ӳ�����ʵ���в��õ�����Ϊ30 mL/h��

ͼ5 ������Һ���ٶ�ӫ���Ӱ��
Fig.5 Effect of flow rate of substrate carrier solution on fluorescence
2.5 ʵ��������Ż�
ͼ6��ʾΪHRP-BrAb��������ӫ��ǿ�ȵ�Ӱ�졣�ɼ�����5 mL�����в�ͬŨ�ȵ�HRP-BrAb������Һ�У���Ӧ��HRP-BrAb���������Ӷ����ӣ���100 mL HRP-BrAb(0.48 mg/L)�����ڱ��͡�������Ϊ���ߴ��������濹ԭ���λ����������ġ���ˣ���ʵ�������5 mL����Һ�м���100 mL HRP-BrAbΪ��������Һ��ʵ���������������¶�Ϊ27 �棬�������ʱ��Ϊ30 min��
2.6 ����װ�õ�Ӧ��
ͼ7Ϊ�ⶨBrAb��У�����ߡ���ͼ7��֪��������Һӫ��ǿ�Ⱥ�����Һ�е�BrAb������ԣ����Է�ΧΪ2.7~90 ��g/L�������Ϊ2.7 ��g/L���˷����ļ��������ѹ�����ߴ��з����ļ����(7.2 ��g/L)��

HRP-BrAb������Ũ��Ϊ0.48 mg/L
ͼ6 HRP-BrAb������ӫ��ǿ�ȵ�Ӱ��
Fig.6 Effect of amount of HRP-BrAb on
fluorescence strength

��ͼΪ���ߴ������ڰ����в�ͬŨ��BrAb���塢0.48 mg/mL BrAb-HRP�����Ũ��Ϊ0.1% BSA��0.1 mol/L Tris-HCl-1 mmol/L EDTA������Һ�вⶨ�����ߡ�ÿ�����ʾ4�βⶨ��ƽ��ֵ���ƫ��(3.5%~6.1%)
ͼ7 BrAb�ⶨ�Ĺ�������
Fig.7 Calibration curve for BrAb determination obtained by competitive immunoassay
������Ũ��Ϊ55 mg/L��BrAb������Һ�ⶨ�˷����������ԣ�����ͱ�ƫ�����2���ɱ�2��֪�������ߴ�����ϵ�������Խϸߡ�
��2 ���ߴ��з�����������
Table 2 Reproducibility of immunosensing system

��2 �����е�ÿһ����ֵ����1���������֧������澭���⡢������ӫ��ⶨ���������õ�ӫ������ֵ��������BrAb ������Ũ��Ϊ0.055 g/L����2 ����Ϊ�ò�ͬ�������֧����IJⶨֵ�����ù���֧�����ڴ��ʱ��Ϊ1.5�º�ĸ��±���IJⶨֵ��ʹ�ô���Ϊ68�Σ��ۼ�ʹ��ʱ��79 h(�¶�Ϊ27 ��)��
�Ʊ������ߴ���װ�����ڼ�ⱻ��Ⱦ����Ѫ����Ʒ(�����������ְҵ����ѧԺ�ṩ)���������3���ɱ�3��֪���ô˷����ⶨ�Ľ����ELISA���ⶨ�Ľ�����Ǻϡ����ԣ��˷������ڼ��Ѫ����Ʒ�е�BrAb��
��3 ��Ѫ����Ʒ��BrAb�����IJⶨ
Table 3 BrAb determination in rabbit serum samples ?g/L

3 ����
�����µ�����ǻ���Ƥ����ø��ӫ�����߷��������봫ͳ�ⶨBrAb�����߷���������ȣ����нϴ����ƣ�
(1) ʵ����ø��ӫ�����ߴ��вⶨBrAb����������ߣ�ʵ�鲽�����
(2) �ɽ���֧��������ֱ�����£������ɱ����͡�
(3) ��ά��-ʯ������ֱ�Ӱ�������ϸ�������������ڲ��ϸ˾���ԭ���Եı��֡�
(4) �µ���Ϊ��Ȼ����������������á����ַ��������������Լ��ⶨҲ�н�����á�
�ο����ף�
[1] Engvall E, Perlmann P. Enzyme-linked immunosorbent assay (ELSIA) quantitative assay of immunoglobulin G[J]. Immunochemistry, 1971, 8(5): 871-874.
[2] Carlo M D, Mascini M. Enzyme immunoassay with amperometric flow-injection analysis using horseradish peroxidase as a label. Application to the determination of polychlorinated biphenyls[J]. Anal Chim Acta, 1996, 33(6): 167-174.
[3] Takatoshi S, Masanori Y, Hiroya I, Kiyoshi M. Flow injection analysis of amitrole by chemiluminescent immunosensor using alkaline phosphatase and adamantyl methoxyphosphoryloxy phenyldioxetane[J]. Anal Sci, 2001, 17(5): 1407-1410.
[4] Hossein S, Martin G S, Oliver H, et al. Development of enantioselective chemiluminescece flow- and sequential injection immunoassays for ��-amino acids[J]. J Biochem Biophys Methods, 2002, 53(1): 1-14.
[5] Villarta R L, Guilbault G G, Suleiman A A. Flow injection analysis of glucose by fibre optic chemiluminescence measuremen[J]. Anal Lett, 1993, 26(4): 1493-1503.
[6] Lonergan G, Mew E, Schliephake K, et al. Phenolic substrates for fluorometric detection of laccase activity[J]. FEMS Microbiol Lett, 1997, 153(2): 485-490.
[7] Ci Y X, Chen L, Wei S. Fluorescence reaction of the system mimetic peroxidase [Mn-T(4-TAP)P]-homovanillic acid- hydrogen peroxide. Spectrofluorimetric determination of H2O2[J]. Fresenius�� J Anal Chem, 1989, 33(4): 124-129.
[8] Gong F C, Zhou Z J, Shen G L, et al. Schistosoma japonicum antibody assay by immunosensing with fluorescence detection using 3,3��,5,5��-tetramethylbenzidine as substrate[J]. Talanta, 2002, 58(2): 611-618.
[9] Chen L, Chang W B. Studies on the structure of substrate for peroxidase[J]. Chemical Research in Chinese Universities, 1995, 16(5): 683-687.
[10] Tatyana V V, Ian J R. Detection of hydrogen peroxide with Amplex Red: interference by NADH and reduced glutathione auto-oxidation[J]. Archives of Biochemistry and Biophysics, 2004, 43(1): 138-144.
[11] Michel P E, Rooij de N F, Koudelka-Hep, et al. Redox-cycling type electrochemiluminescence in aqueous medium. A new principle for the detection of proteins labeled with a ruthenium chelate[J]. J Electroanal Chem, 1999, 47(4): 192-194.
[12] Lee H S. Tyrosinase inhibitors of Pulsatilla cernua root-derived materials[J]. J Agri Food Chem, 2002, 50(6): 127-132.
[13] Zapata J M, Calder��n A A, Mu?oz R, et al. Oxidation of natural hydroxybenzoic acids by grapevine peroxidases: kinetic characteristics and substrate specificity[J]. Am J Enol Vitic, 1992, 43(1): 134-138.
[14] Beier R C, Young C R, Stanker L H. USDA agricultural research service, detection of bacteria from a cecal anaerobic competitive exclusion culture with an immunoassay electrochemi- luminescence sensor[J]. Proc SPIE, 1991, 35(44): 10-20.
[15] Tuuminen T, Palomaki P, Rakkolainen A, et al. 3-p- hydroxyphenylpropionic acid-a sensitive fluorogenic substrate for automated fluorometric enzyme immunoassays[J]. Immunoassay, 1991, 12(1): 29-46.
[16] Limoges B, Degrand C, Brossier P, et al. Homogeneous electrochemical immunoassay using a persulfonated ionomer- modified electrode as a detector for a cationic labeled hapten[J]. Anal Chem, 1993, 65(3): 1054-1060.
�ո����ڣ�2009-06-30�������ڣ�2009-09-15
������Ŀ��������Ȼ��ѧ����������Ŀ(20976017��50774016)
ͨ�����ߣ�տѩ��(1972-)���У����������ˣ���ʿ�������ڣ����¾�ϸ�������о����绰��13574813956��E-mail: zhanxueh@163.com


