������ҩ���ռ������オ��������
���ܻ�����������÷�������������۳����
(�人������ѧ ��Դ�뻷������ѧԺ������ �人��430070)
ժҪ�����������Լ����л���Ⱦ������オ����������ϵ������BOD5/CODCr����������ƿ���鷨��OECD-301B(ISO 9439)����������ҩ�����オ���Խ������ۣ�������ӽṹ�����オ��ȵ�Ӱ�죬̽��������ҩ�����オ��������о�����������һ��������������������������춡����ҩ��BOD5��CODCr����Ũ��֮�ȼ���(BOD5)/��(CODCr)��С��0.25����28 d���オ��ȷֱ�Ϊ39.54%��36.88%��34.09%��29.17%��26.79%�����オ��ָ���ֱ�Ϊ101.020 0��99.019 9��88.717 5��79.125 6��71.897 5���������ֻ�ҩ�����������ʱ��ֱ�Ϊ12��13��15��17��18 d����3�����۷����ó��Ľ�����һ�µģ����������ֻ�ҩ�������������オ��ģ������オ�������ɴ���С����Ϊ���һ���ҩ����������ҩ���������ҩ���������ҩ���춡����ҩ�������̼�����ȣ���֧�ȶԻ�ҩ�����オ���Ե�Ӱ�����������CS2��ROCSSH�͵����̼�����ǻ�ҩ���オ�����Ҫ���ͬʱ����������״Һ��˫��ҩ���ɡ�
�ؼ��ʣ�
������ҩ�����オ���������ӽṹ��������
��ͼ����ţ�X703 ���ױ�־�룺A ���±�ţ�1672-7207(2011)02-0546-09
Evaluation of biodegradability of alkyl xanthates flotation collecters
CHEN Shao-hua, GONG Wen-qi, MEI Guang-jun, CHEN Xiao-dong, YAN Heng-zhen
(School of Resources and Environmental Engineering, Wuhan University of Technology, Wuhan 430070, China)
Abstract: The biodegradability of alkyl xanthates was evaluated by the methods of BOD5/CODCr, static�Cflasks test and OECD-301B(ISO 9439) according to the testing standard for biodegradability of surfactants and other organic compounds. Meanwhile��the influence of molecular structure on biodegradability was studied. Finally, the biodegradation mechanism of alkyl xanthates was preliminarily explored. The results show that the mass concentration rate of BOD5 and CODCr of ethyl xanthate, butyl xanthate, amyl xanthate, isopropyl xanthate and isobutyl xanthate are all less than 0.25, the biodegradation extent can reach 39.54%, 36.88%, 34.09%, 29.17% and 26.79%, respectively. The index of biodegradability can reach 101.020 0, 99.019 9, 88.717 5, 79.125 6, and 71.897 5, respectively in 28 d, and they have some inhibiting effects on microorganisms, the suppressed time is 12, 13, 15, 17, 18 d, respectively. Xanthates are difficult to degrade by microorganisms, and the order from strong to weak of the magnitude of the biodegradability is as follows: ethyl xanthate, butyl xanthate, amyl xanthate, isopropyl xanthate and isobutyl xanthate. Compared to alkyl chain length, the branched chains have more significant effects on the degradability of xanthates. CS2, xanthic acid and thiocarbonate are the main product of biodegradation of xanthates, in which a small amount of oil-like droplet dixanthate is produced.
Key words: alkyl xanthates; biodegradability; molecular structure; mechanism
���ſ�ҵ�ķ�չ����ѡҩ������Խ��Խ��ҩ����õIJ��ռ������ж��Ժʹ̼��Գ�ζ������ҩ��Ⱦ��ˮ��������ᣬ�����������Ⱦ�����ԣ�Ӧ��ѡ���ˮ�е�ʣ���ҩ���д�����ʹ�����ŷţ��Ա�����ɽ��̬����[1-2]��Ŀǰ��������Ը�ѡ��ˮ����Ⱦ������Ҫ������������ѧ������Ȼ������Щ���������ԵIJ��㣬���ܺĺ�ҩ�����������ײ���������Ⱦ��[3-4]�������һ��״���Ի�ҩ�������オ�������ۣ��о������オ����ɣ��˽������オ�����׳̶ȣ�Ϊ���Ƹ�Ч���Ͷ�������Ⱦ�Ļ����Ѻ���ѡ��ҩ���ṩһ�������ݣ���ѡ���ˮ����Ч����������Ҫ�����塣����Ϊֹ�������������û���漰��ҩ�����オ�����о������������е��о��������ڶԻ�ҩ�Ĺ⽵��ͶԻ�ҩ�����к����ʵķ�����ⷽ�棬���������オ���Ժ���̬��ȫ���о����б���������������� ��[5]��������Լ�[6]��ũҩ[7]���л���Ⱦ������オ���Լ���̬��ȫ�����۽϶࣬���ѽ�����Ӧ���オ�������۱���������ȫ������ģʽ���л������オ�������۷��������࣬���У�BOD5/CODCr�����㣬����õ�һ�ַ�����������ƿ���鷨��ȫģ�⾲ֹ����Ȼˮ�壬����ӽ���Ȼ״̬��һ�ֽ��ⷽʽ��OECD-301B(ISO 9439)[8]�����ö�����̼������(PCD)��Ϊ�л������オ���Բ���ָ�꣬�����������á�����ϸ���������ú�����ԭ�����ʶԲ��Խ����Ӱ��[9]�����ҴӶԻ�����Ⱦ�ĽǶȿ����л���ת��ΪCO2��H2O��ף����Ҳ�������塣�ڴˣ��������߽��������Լ����л���Ⱦ������オ������۱�������BOD5/CODCr����������ƿ���鷨��OECD-301B(ISO 9439)����������ҩ�����オ���Խ������ۡ�
1 ʵ��
1.1 �Լ�������
�Լ�Ϊ���һ���ҩ���������ҩ����������ҩ���춡����ҩ���������ҩ(��ҵ�������ᴿ��ʹ��)������ѡ��ҩ���������������Ƽ�������ѧ�Լ�(�� ����)��
����Ϊ������ˮԡ���������������������á�UV-3000������ֹ��ȼ�(ɨ�辫ȷ��Ϊ0.1 nm)��Sartorius BS210S�͵�����ƽ��LG10-2.4A������ �Ļ���
1.2 ʵ�鷽��
1.2.1 BOD5/CODCr��
BOD5���ù��귨(GB/T 7488��1987)�ⶨ�� CODCr����Ũ�Ȧ�(CODCr)���ÿ�������ֹ��ȷ� (HJ/T 399��2007)���вⶨ��
1.2.2 ������ƿɸѡ���鷨
(1) ϡ��ˮ���Ʊ���ȡһ����������ˮ�������������Ϊ10%��������ˮ����Һ�����������������غ����������ƣ�ʹ���غ����������Ƶ�����Ũ�ȷֱ�Ϊ5.0 mg/L��1.6 mg/L�����Ⱥ�����ͨ�紦3 d�� ʹ�á�
(2) ʵ�鷽������10 mL��������������ˮ������Һ�������90 mL����5 mg��ĸ��������������BOD5ϡ��ˮΪ���ʣ�ʹ�����������Ũ��Ϊ10 mg/L���������¾���������1�ܺ�ȡ������Һ10 mL��Ϊ��һ�������Ľ������������������Һ����������������ظ�������4��[10]����ÿ�������ڵĿ�ʼ������ȡ�����������ĺ�������ֹ��ȷ��ⶨ����������������ղ������������,��������Ũ�ȣ�������ʽ���������オ��ȣ�
D=(��o-��n)/��o��100 (1)
ʽ�У�DΪn����ҩ���オ��ȣ�%����o�ͦ�n�ֱ�Ϊ�����ʼ�ͽ���n���Һ�л�ҩ������Ũ�ȣ�mg/L��
�����յ����オ����Ե�4���ٽ���ʱ�Ľ���ȱ�ʾ������2���ظ�ʵ�飬������ƽ��ֵ��ʾ��
1.2.3 OECD-301B(ISO 9439)��(PCD��)
(1) ����װ�á����オ������������ͼ1��ʾ��ʵ��װ�÷�Ϊ���¼����֣��� ����װ��A��ȥ�������е�CO2������NaOH��Һ�������գ��� CO2������װ��B����������е�CO2�Ƿ�ȥ����ȫ����Ba(OH)2��Һ���飻�� ϴ��װ��W��������ˮϴ�������еļ��Գɷ֣��� ����װ��E�����������ȶ����� ���オ�ⷴӦ�ʹ�������װ�� �� CO2������װ��D����Ba(OH)2��Һ���ս�������в�����CO2��
(2) Ӫ��Һ��Ӫ��Һ�ɷ�[8,11]��������4����Һ��
�� �����λ�����Һ��8.50 g KH2PO4��21.75 g K2HPO4��33.40 g Na2HPO4��2H2O��0.50 g NH4Cl���� 1 L����ˮ�У���ҺpHΪ7.4��
�� �Ȼ�����Һ��36.40 g CaCl2��2H2O����1 L����ˮ�С�
�� ����þ��Һ��22.5 g MgSO4��7H2O����1 L����ˮ�С�
�� �Ȼ�����Һ��0.25 g FeCl3��6H2O����1 L����ˮ�С�
�� Ӫ��Һ�ĺ�������������Һ����Ϊ10 mL/L���Ȼ�����Һ������þ��Һ���Ȼ�����Һ������Ϊ1 mL/L��
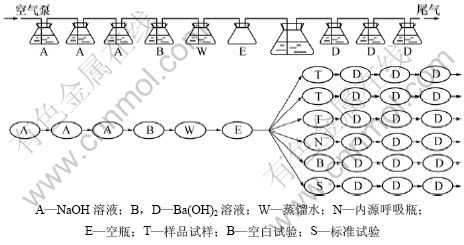
ͼ1 ���オ��������װ��ʾ��ͼ
Fig.1 Schematic diagram of equipment for evaluating biodegradation
(3) ������ͲαȻ����ʡ������T��������ȡ���人ɳ����ˮ��������ʹ��֮ǰ����5 d�Գ�ȥ��ˮ�еIJ����л���Ӷ����Ϳհ�CO2�������������ָ��Ϊ33 mL/g���ҡ���ƽ��������ⶨ�������������ϸ������ʹ�����������(4.0~8.5)��107 ��/mL��ʵ��IJαȻ���Ϊ���オ����������ķ�����������[8, 12](���オ�⼫��ֵ�ɴﵽ100%)��
(4) �������������̡�������,���������オ�ⷴӦƿ��6ֻ�����У�
�� ������Ӧƿ3ֻ(����Ӫ���Ρ������л����ҩ�ͽ�����)��Ϊ�˼�С����CO2������3�ε�ƽ��ֵ���㡣
�� ����Ӧƿ1ֻ(��Ӫ���Ρ������������ƺͽ�����)������װ�ü�����������Ч�ԡ�
�� ��Դ��Ӧƿ1ֻ(ֻ��Ӫ���Ρ����������������)��
�� �հ�Ӧƿ1ֻ(ֻ������ˮ��Ӫ����)��
Ϊ��ȥ�������е�CO2�������ﷴӦƿǰ����4������������ƿ������ǰ3������10 mol/L NaOH�������գ���4������0.05 mol/L Ba(OH)2��Һ�������գ�Ȼ��ϴ��ƿϴ���Է�ֹ���ļ�Һ���뷴Ӧƿ�������ﷴӦƿ�У���Ҫ������Ӫ��Һ����Ӧ�¶�Ϊ25 �棬ÿ����Ӧƿ����������Ϊ1~2 ��/s���ݣ������л����ʼ����Ũ��Ϊ20 mg/L(��DOC��)���������ڷ�ӦҺ�е�MLSS����Ũ��Ϊ150 mg/L[8]����Ӧʱ��Ϊ28 d��������Ӧƿ�з�ӦҺ�������Ϊ2 L(����������ͽ�����)�����з�Ӧƿ���һ���ɫ���ϴ����Է�ֹ���ϸ������CO2��
���オ�������CO2��3�������ġ��ֱ�ʢ��100 mL 0.025 mol/L Ba(OH)2����Һ����ƿ�����գ�������CO2��������Ũ����0.05 mol/L������Һ(��NaCO3��Һ�궨)�ζ���á��ζ�ʱ���Ƴ�������ƿ���������ƿ���ٽ���������ƿ������ǰ�ƶ�1��λ�ã�ͬʱ��������װ����ĩ���ټ�1���µ�װ��100 mL 0.025 mol/L Ba(OH)2����Һ������ƿ���������ʱ,Ҫ����������ƿ���еζ�����������������õ�CO2�����������۳��հ�ֵ����ÿ���CO2�������ۼӣ�����CO2����Ũ����ʱ��Ĺ�ϵ���ߡ�
2 ���������
2.1 BOD5/CODCr��
2.1.1 CODCr����������
���ڱ������������Ϊ�����ʣ��ֱ�����CODCr����Ũ��Ϊ0��25��50��150��200��250 mg/L�ı���Һ������(CODCr)������ȵı��������ߣ���ͼ 2��
2.1.2 BOD5/CODCr���オ�������۽��
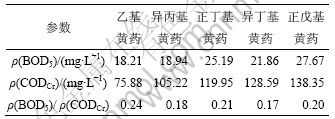
һ����˵����ˮ�Ħ�(BOD5)/��(CODCr)Խ�������オ����Խ�ã������۱�����1�����۽���� ��2��
�ɱ�2��֪���һ���ҩ���������ҩ����������ҩ���춡����ҩ���������ҩ�Ħ�(BOD5)/��(CODCr)��С��0.25���ɼ����Ƕ��������オ��ġ�
��1 ��ˮ���オ�������۲ο�ָ��
Table 1 Biodegradability evaluation indexes of wastewater

��2 ������ҩ�Ħ�(BOD5), ��(CODCr)�ͦ�(BOD5)/��(CODCr)
Table 2 ��(BOD5), ��(CODCr) and ��(BOD5)/��(CODCr) of alkyl xanthates
2.2 ������ƿɸѡ���鷨
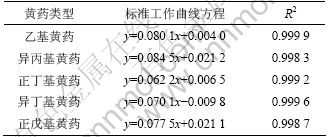
2.2.1 ������ҩ������ɨ��ͼ������������
������ҩ������ɨ��ͼ����ͼ3��ʾ����ͼ3�ɼ�����197 nm����1�����շ壬���ܼ���[13]��������ҩ��226 nm��301 nm����2�����շ壬�������֮��ԼΪ5:8��ѡ������շ岨��301 nm��Ϊ�ⶨ������ҩŨ�ȵ�����������
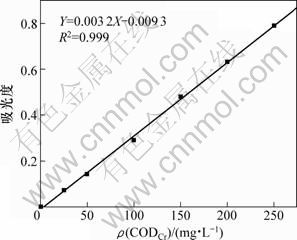
ͼ2 ��(CODCr)����������
Fig.2 Standard curve of ��(CODCr)
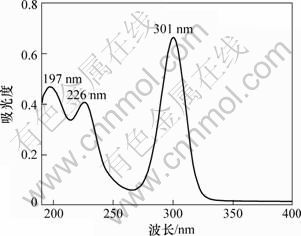
ͼ3 ��ҩ����������ͼ��
Fig.3 UV absorption spectrum of xanthate
���Ʋ�ͬ����Ũ�ȵ�������ҩ��Һ����301 nm����������ȣ�������Ũ��������ȵı��������ߣ�����������߷��̼��� 3��
��3 ������ҩ�ı���������
Table 3 Standard curve of alkyl xanthates
2.2.2 ���オ��������
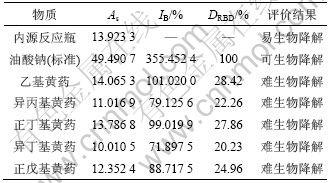
ʵ���л�ҩ�����オ�����׳̶��Ե�4�εĽ����Ϊ����[10]�������オ������۱����� 4��ʵ��ȡ2��ƽ��ʵ���ƽ��ֵ���������5��
��4 ���オ������۱�
Table 4 Evaluation standards for biodegradability

��5 ������ҩ�����オ����������
Table 5 Test results of biodegradability of alkyl xanthates
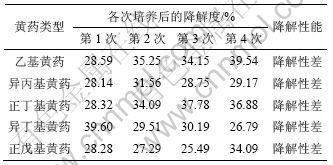
�ɱ�5��֪���һ���ҩ�����オ������Ϊ39.54%���������Ϊ��������ҩ���������ҩ���������ҩ�����ǵ����オ��ȷֱ�Ϊ36.88%��34.09%��29.17%���춡����ҩ���オ�����С����Ϊ26.79%�����ǵ����オ��Ⱦ���20%~40%֮�䣬�ɼ����ǵ����オ�����ܶ��Ƚϲ
2.3 OECD-301B��(ISO 9439��PCD��)
һ����˵���л����������オ�����ɵĶ�����̼�������オ��ʱ��Ĺ�ϵ��������ͼ4��ʾ��3�ֵ��Ͷ�����̼����Ũ������(PCD����)��������
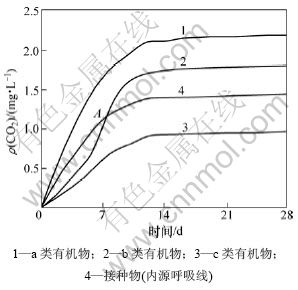
ͼ4 �л������オ������м��ֵ��͵�PCD����
Fig.4 Typical PCD curves of biodegradation of organic compounds
��ͼ4��ʾ����ͬ������PCD���߲�ͬ��a���л��ﲻ��Ҫѱ�����̣����オ�����ʺ����オ��̶Ƚϴ�PCD�����������֮������Ҳ�ϴ�b���л�����Ҫһ��ѱ�����̣����ķ�Ӧ���ʺ����オ��̶Ƚ�С��PCD�����������֮������Ҳ��С��c���л��ﲻ�����������オ�����ã������Խ�������ж��ԣ���PCD����λ�ڽ�����(��Դ��)PCD����֮����PCD�����������֮��������С���������������オ��[14]���ɴ˿ɼ���PCD�����������֮���������Ա����л������オ���ԡ���ˣ��ڶ�����̼���Է��У��л�������オ�����ܿɲ������オ����ָ��IB��ʾ[15-16]��
IB=(As/Ao)��100 (2)
ʽ�У�AsΪ�����л�������PCD�����������֮��������AoΪ��������ԴPCD�����������֮�����������������л�������オ����ָ��(IB)�ɰ��л�������オ���Ի������£�IB��200���������オ�⣻100��IB��200���������オ�⣻IB��100���������オ�⡣
��������Խ����(DRBD)Ϊ��
DRBD=(IBt/IBs)��100 (3)
ʽ�У�IBtΪ����������オ��ָ����%��IBsΪ�α��������Ƶ����オ��ָ����%��DRBDԽ��˵������������オ������Խǿ����֮��Խ����DRBD��Ϊ���オ����ָ������������Ӱ��С����ˣ����ô�ָ��ʹ������ҩ���オ�����ܵ����۸���ȫ���ֱ�ۡ�
����������ҩ��PCD����(CO2Ũ��ȡ3�ε�ƽ��ֵ)��ͼ5��ʾ��Ϊ������ط�����ͬ�ṹ��������ҩ�ڽ�������в���CO2����Ũ���Լ����������Դ������CO2����Ũ��֮��Ĺ�ϵ����ͼ5���оֲ��ŴŴ���PCD������ͼ6��ʾ���������������オ��ָ������6��
��ͼ5��ͼ6�ͱ�6��֪���������������ڿ�ʼ�ͺܿ콵�⣬�����オ����ָ��Ϊ355.452 4��Զ����200.000 0����֤����������һ�ּ���������ʣ�˵������������н��������������кܺõĻ��ԣ�������֤��ʵ�����Ч�ԡ�
5��������ҩ��PCD���߸տ�ʼ��λ����Դ���������£�������ҩ���������һ���Ķ������ã�����������Ļ��ԡ���ͼ6��֪���������ྭ��һ��ʱ�ڵ�ѱ����CO2����Ũ��������Դ��Ӧ��CO2����Ũ�ȣ���ͬ�ṹ�Ļ�ҩ�����������ʱ��Ҳ���ϴ������һ���ҩʱ����̣��������Ϊ��������ҩ���������ҩ���������ҩ�����춡����ҩ��ʱ�������ʱ��ֱ�Ϊ12��13��15��17��18 d����Origin7.5�ֱ����������֣�A0Ϊ13.923 3���һ��������������������������춡����ҩ��As�ֱ�Ϊ14.065 3��13.786 8��12.352 4��11.016 9��10.010 5���ɴ˿ɵ����ǵ����オ��ָ���ֱ�Ϊ101.020 0��99.019 9��88.717 5��79.125 6��71.897 5�������һ���ҩ���オ��ָ��101.020 0�Դ���100.000 0��������������������������ָ���֪�ǿ����オ��ģ�������������������춡�����������ҩ�����オ��ָ����С��100.000 0�������������オ�⣬���ǵ�28 d����Խ����(DRBD)�ֱ�Ϊ28.42%��27.86��24.96%��22.26%��20.23%��
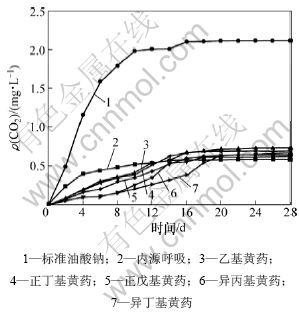
ͼ5 ������ҩCO2����Ũ����ʱ��Ĺ�ϵ
Fig.5 Relationship between mass concentration of CO2 produced of alkyl xanthates and time
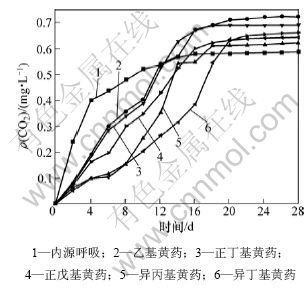
ͼ6 ͼ5�ľֲ��Ŵ�ͼ��
Fig.6 Enlarged part of Fig.5
��6 ������ҩ�����オ�����ܷ���
Table 6 Classification for biodegradability of alkyl xanthates
2.4 �������۷����ķ����ͱȽ�
�ɦ�(BOD5)/��(CODCr)�ɿ���5�ֻ�ҩ�������オ�⣻�þ�����ƿɸѡ���鷨�ó�5�ֻ�ҩ�������ܶ��Ƚϲ��OECD-301B���ó��Ľ��۳��һ���ҩ�ǿ����オ���⣬����4�ֻ�ҩҲ���������オ�⡣�ɴ˿ɼ���3�����۷����ó��Ľ�����һ�µģ������϶����������オ������オ�����ܺܲ
���æ�(BOD5)/��(CODCr)�ж��л�������オ�����ܱȽϼ����ڦ�(COD)/��(BOD5)�IJ���У����������ںϳ�ϸ�����Dz����л����������(����Ũ��)�����л�ԭ��������������Լ���(BODu)���(BOD5)�IJ����⣬������5 d��Ҳ���ܷ����������ã���ˣ��������ַ������ý�����Ȳ��ߣ������Եط�ӳ�л���Ľ������ܡ�
�þ�����ƿ���鷨�ó��һ��������������������������춡����ҩ�����オ����Դ���OECD- 301B����õ���Խ���ȣ�����Ҫ����Ϊ����̬��ƿ���Dzⶨ�������オ��ȣ�OECD-301B�Dzⶨ�������オ��ȣ��Ƿ�ӳ�л�����ȫ����Ϊ����С���ӵij̶ȣ����Ҿ�̬��ƿ�����ýϵ͵Ļ�ҩ����Ũ�ȣ�������Ķ��Բ���̫ǿ��������ϡ��ˮ֮������������Ľ�ĸ��ȡҺ�������������û�ҩ��Ψһ̼Դʱ�������ý�ĸ����Ϊ�������ʣ��п��ܷ�������л���ã�����߲��ռ������オ���ԡ�
2.5 ������ҩ�ṹ�����オ��ȵ�Ӱ��
Ϊ�˱��ڱȽϻ�ҩ�IJ�ͬ�ṹ�����オ�����ܵ�Ӱ�죬��7�г���5��������ҩ�Ħ�(COD)/��(BOD5)�����オ���D�����オ����ָ��IB���ɱ� 7��֪��
��7 ������ҩ�Ħ�(BOD5)/��(CODCr)�����オ��Ⱥ����オ��ָ��
Table 7 ��(BOD5)/��(CODCr), biodegradability and IB of alkyl xanthates
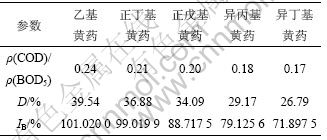
(1) ��ͬ�ṹ��ҩ�����オ��Ⱥͽ���ָ�����ϴ������オ�������ɴ���С��˳��Ϊ���һ���ҩ����������ҩ���������ҩ���������ҩ���춡����ҩ������ͬ��ʵ�������£�����ֱ��������ҩ�����һ������������������ҩ��̼�����μӳ������(COD)/��(BOD5)�����オ��ȡ����オ��ָ�������μ�С��������Ϊֱ�����̼�����������������Ӧ���ӣ������˷��Ӷ����ﷴӦ��λ��ЧӦ��������ø�ķ�Ӧ�����������л�����Ľ�ϣ��谭�����﹥��̼�˵��������Ӷ������˻�ҩ�����オ�����[17]��
(2) ��������ҩ�����オ��Ⱥͽ���ָ�����Դ����춡����ҩ�����オ��Ⱥͽ���ָ�����ɼ����������̼��Ŀ��ͬ������£�ֱ���ṹ�Ļ�ҩ��������Դ��ں�֧���Ļ�ҩ����ȡ���֧�ȶ������オ��ȵ�Ӱ��ϴ��������ڶ���ֱ���ṹ�IJ��ռ���������ӽ����ǵ�̼�˷����������ⷴӦ����֧�����ռ�������λ��ϴ������Ƚ����ڽӽ�̼�˷�����Ӧ����������オ�����ܱ�ֱ�����ռ������オ�����ܲ
(3) һЩ̼������ֱ����ҩ��̼���̵�֧����ҩ�����オ���Ի��ã�����������ҩ�����オ���Ա��������ҩ�ĺã��������ҩ�����オ���Ա��������ҩ���춡����ҩ�����オ�����ܶ��ã�˵�������̼��������˵����֧�ȶԻ�ҩ���オ���Ե�Ӱ�����
3 ��ҩ�����オ�����
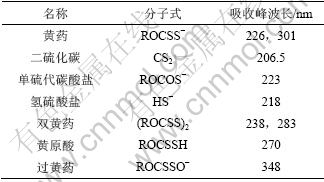
�м������γɣ�˵���л�������Ľ�����һ���dz����ӵĹ��̡���8�����˻�ҩ���䷴Ӧ������������շ岨��[18-19]��
��8 ��ҩ������Ҫ��Ӧ������������շ岨��
Table 8 Absorption peak values of butyl xanthate and main reaction products
Ϊ�˿����ҩ(�Զ�����ҩΪ��)���オ������в���ı仯������Խ�������н��ⲻͬʱ�����Һ��������ɨ�裬�����ͼ7����ͼ7�ɼ������Ž���ʱ������ӣ�����ҩ���������շ�(226 nm��301 nm)ǿ�Ȳ��Ͻ���(��190~200 nm�������շ����ܼ���)����218 nm�����������շ壬������ǽ������ɵ�CS32-���ȶ��ֽ��S2-��S2-��һ��ˮ������HS-�����շ�[20]��Ե�ʣ���ҩ�������オ��һ��ʱ�����206.5 nm����ǿ���շ壬��CS2���������շ壻����ʱ����ӳ�����ҩ���շ�ǿ�Ȳ����½�����CS2�����շ�ǿ�Ȳ������ӣ�������ҩ���ϱ������CS2��˵��CS2��Ϊ�м���ﲻ�ܺܺõر������һ�����ôӶ����ϻ��ۡ�
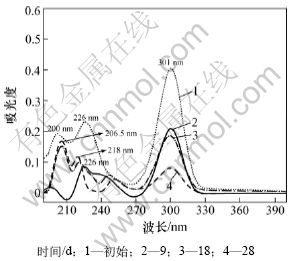
ͼ7 �����オ�ⲻͬʱ�����ҩ����������ͼ��
Fig.7 UV absorption spectra of butyl xanthate degradation by microorganisms at various reaction time
����һ��ʱ�����ƿ�г����˽������Ļ�ɫ��״Һ�Σ�����������ȡ���������ɨ�裬����������ͼ����ͼ8��ʾ�������オ���Ļ�ҩ��Һ�������������ȡ����(�հ�Ҳ������ͬ������������ȡ��Ϊ����)����ȡ���л������������ͼ����ͼ9 ��ʾ��
��ͼ8��֪����״����238 nm��283 nm�����������շ壬����˫��ҩ���������շ塣�ɼ��������ڽ����ҩʱ���в��ֻ�ҩ������������Ϊ˫��ҩ��
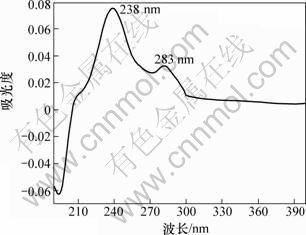
ͼ8 ��״������������ȡ�����������ͼ��
Fig.8 UV absorption spectrum of n-hexane
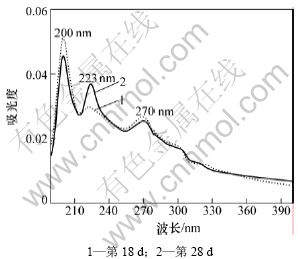
ͼ9 ���Ľ���Һ����������ȡ���л������������ͼ��
Fig.9 UV absorption spectra of organic phase in final solution
��ͼ9��֪�����オ������Һ����������ȡ��200��223��270 nm���������������շ壻200 nm���ķ���������������ˮ�����շ壻270 nm���ķ��ǻ�ԭ����������շ壬����δ�����ҩˮ��IJ����223 nm���ķ��ǵ����̼���ε��������շ壬��������ʱ����ӳ��������շ�ǿ�Ȳ������ӣ����������̼������Ϊ��ҩ������м���ﲻ�ܺܺõر������һ�����⣬�Ӷ����ϻ��ۡ������Ϸ������Ʋ��ҩ���オ��Ŀ���;�����£�
(1) 6ROCSS-+3H2O��6ROH+CO3-+3CS2+2CS32-
ROH��RCHO��RCOOH��CO2+H2O
CS32-��CS2+S2-
S2-+H2O��SH-+OH-
CS2��S2-��S��SO32-��SO42-
ROCSS-+H2O��ROCSSH+OH-
(2) 4ROCSS-+O2+2H2O��2(ROCSS)2+4OH-
(3) 2ROCSS-+O2��2ROCOS-+2S
�ɼ���CS2��ROCSSH�͵����̼�����ǻ�ҩ���オ������Ҫ���ͬʱ��������״Һ��˫��ҩ ���ɡ�
4 ����
(1) ������ҩ(�һ�������������������춡�����������ҩ)�Ħ�(COD)/��(BOD5)��С��0.25�������������オ���л��
(2) �һ���ҩ��28 d�����オ������Ϊ39.54%���������Ϊ����������������������ҩ�����ǵ����オ��ȷֱ�Ϊ36.88%��34.09%��29.17%���춡����ҩ�������С����Ϊ26.79%�����ǵ����オ��ȶ���20%~40%֮�䣬���オ�����ܶ��ϲ
(3) ��ҩ���������һ�����������ã��һ�������������������������ҩ���춡����ҩ������ʱ��ֱ�Ϊ12��13��15��17��18 d����28 d���オ��ָ���ֱ�Ϊ101.020 0��99.019 9��88.717 5��79.125 6��71.897 5�������オ��������ָ���֪���һ���ҩ�ǿ����オ�⣬�������������������������춡����ҩ�����������オ�⡣
(4) ��ҩ��̼�����Ⱥͷ�֧�ȶ����オ������Ӱ��ϴ������オ�������ɴ���С��˳��Ϊ���һ���ҩ����������ҩ���������ҩ���������ҩ���춡����ҩ�������̼��������˵����֧�ȶԻ�ҩ�����オ���Ե�Ӱ���Ϊ������
(5) CS2��ROCSSH�͵����̼�����ǻ�ҩ���オ�����Ҫ���ͬʱ��������״Һ��˫��ҩ���ɡ�
�ο����ף�
[1] 춷�, ��ǿ, ��Т��. �ҹ��������ѡҵ��ˮ��Ⱦ��������[J]. ������ɽ, 2003(9): 40-44.
YU Fang, ZHANG Qiang, GUO Xiao-min. Analysis of waste water pollution characteristics of mining and mineral processing of China��s metal mines[J]. Metal Mine, 2003(9): 40-44.
[2] ʦΰ. ������ҩ��ѡ���ռ��⻯ѧ���������о�[D]. �人: �人������ѧ��Դ�뻷������ѧԺ, 2007: 6-10.
SHI Wei. Study on photochemical degradation properties of the alkyl xanthate flotation collecters[D]. Wuhan: Wuhan University of Technology. School of Resources and Environmental Engineering, 2007: 6-10.
[3] ������, ������, л����, ��. ѡ���ˮ�л�ҩ��Ȼ�������Ե��о�[J]. ��ҵ��ȫ�뻷��, 2006, 33(6): 33-34.
ZHAO Yong-hong, CHENG Xian-xiong, XIE Ming-hui, et al. The research about the natural degradation characteristics of xanthate in beneficiation wastewater[J]. Mining Safety and Environmental Protection, 2006, 33(6): 33-34.
[4] �̽���, ���, �Ƶ���. ѡ���ˮ�в����ҩ������ɵ������о�[J]. ����������ӹ�, 2001(5): 18-22.
WENG Jian-hao, WANG Rui, HUANG Dao-yu. Study on degradation law of remaining xanthate in mineral processing waste water[J]. Industrial Minerals and Processing, 2001(5): 18-22.
[5] Beran E. Experience with evaluating biodegradability of lubricating base oils[J]. Tribology International, 2008, 41(12): 1212-1218.
[6] Adam R, Grochowalski D G, Cooper J A. Effect of surfactants on plasticizer biodegradation by bacillus subtilis ATCC 6633[J]. Biodegradation, 2007, 18(3): 283-293.
[7] Singh D K. Biodegradation and bioremediation of pesticide in soil: Concept, method and recent developments[J]. Indian J Microbiol, 2008, 48: 35-40.
[8] OECD 301B. OECD guidelines for the testing of chemicals[S].
[9] YANG Li-he, ZHU Yong, FAN Guo-chen, et al. Test on evaluation method for biodegradability of lubricants[J]. Transactions of Tianjin University, 2008, 14(1): 61-65.
[10] ���, ������, �ɵ���. ���ֻ��������ⶨ������Ⱦ�Ͽ�������[J]. ����ʦ����ѧѧ��: ��Ȼ��ѧ��, 2003, 31(1): 74-75.
WU Jie, LIU Zheng-qin, XI Da-li. Two basic methods to gauge the biodegradability of anionic dyes[J]. Journal of Henan Normal University: Natural Science, 2003, 31(1): 74-75.
[11] ���˸�, ���, ����ϼ, ��. ˮ���������オ���������۷����о�[J]. ��ҵˮ����, 2007, 27(11): 65-67.
HU Xing-gang, SUN Ji, JIN Xiao-xia, et al. Research on biodegradability evaluation method of water treatment chemicals[J]. Industrial Water Treatment, 2007, 27(11): 65-67.
[12] ����, ������, �²�ˮ, ��. �������オ���Կ��ٲⶨ�������о�[J]. ʯ��ѧ��, 2004, 20(6): 74-75.
WANG Kun, FANG Jian-hua, CHEN Bo-shui, et al. Fast method for the evaluation of biodegradability of lubricating oils[J]. Acta Petrolei Sinica, 2004, 20(6): 74-75.
[13] ������. ���ռ��Ľ�������������о�[D]. ��ɳ: ���ϴ�ѧ��ѧ����ѧԺ, 2003: 41-42.
YANG Yun-qiong. Study on the degradation properties and mechanism of sulfide flotation collectors[D]. Changsha: Central South University. School of Chemistry and Chemical Engineering, 2003: 41-42.
[14] ��չ��, ʦ����, ������, ��. �л���������オ���Զ�����̼���������Է����о�[J]. ������ѧ, 1996, 16(3): 11-14.
JIANG Zhan-peng, SHI Shao-qi, MAI Wen-ning, et al. Study on the determination of biodegradability of polluted organic substances using production of carbon dioxide test[J]. Environmental Science, 1996, 16(3): 11-14.
[15] ������, ������, ���, ��. 32�ַ��㻯����ĺ������オ���Ա���[J]. ������ѧ, 1997, 16(1): 43-45.
CHEN Yong-sheng, CHEN Li-xia, YANG Jie, et al. Study on biodegradability of 32 aromatic compounds[J]. Environmental Science, 1997, 16(1): 43-45.
[16] ���ķ�. ��ˮ�������Ӻ������オ���Լ������ѧ�о�[D].�ൺ: �й������ѧ������ѧ�빤��ѧԺ, 2006: 25-28.
TANG Gai-feng. Study on the aerobic biodegradability and degradation kinetics of nitrophenols wastewater[D]. Qingdao: Ocean University of China. College of Environmental Science and Engineering, 2006: 25-28.
[17] QIN Yong, ZHANG Gao-yong, KANG Bao-an, et al. Primary aerobic biodegradation of cationic and amphoteric surfactants[J]. Journal of Surfactants and Detergents, 2005, 8(1): 55-58.
[18] ������. ��ԭ���θ�Ч������������ձ�ѡ�����併�����Ե��о�[D]. ����: �㶫��ҵ��ѧ������ѧ�빤��ѧԺ, 2007: 38-40.
SHU Sheng-hui. Breeding of xanthate-degrading bacterial strain by ultraviolet-ray mutation and its biodegradates characteristics[D]. Guangzhou: Guangdong University of Technology. Faculty of Environment Science and Engineering, 2007: 38-40.
[19] ZHONG Xi-sun, Forsling W. The degradation kinetics of ethyl-xanthate as a function of pH in aqueous solution[J]. Minerals Engineering,1997, 10(4): 389-400.
[20] J.����. ��ĭ���渡ѡ��ѧ[M]. ����: ұ��ҵ������, 1987: 224-227.
J.Lai Ya. Surface chemistry of froth flotation[M]. Beijing: Metallurgical Industry Press, 1987: 224-227.
(�༭ �²ӻ�)
�ո����ڣ�2009-10-26�������ڣ�2010-01-10
������Ŀ�����Ҹ����о���չ�ƻ�(��863���ƻ�)��Ŀ(2007AA06Z123)���人������ѧ���������о�����������Ŀ(2010-YB-16)
ͨ�����ߣ�������(1948-)���У������人�ˣ���ʿ�����ڣ���ʿ����ʦ�����¿������\�����������\���Ϳ������ײ��ϵȷ�����о���E-mail��gongwenqi@yahoo.com.cn


