���±�ţ�1004-0609(2013)12-3387-07
B95���Ͻ���������Һ���γ�ת��Ĥ�ĵ缫��Ӧ����
�˱�ɺ��������
(�й����пƼ���������˾ �Ƚ���������Ϳ�ƹ��ҹ���ʵ���ң����� 100081)
ժ Ҫ��
���õ绯ѧ�迹��(EIS)�о�B95���Ͻ���10 mmol/L CeCl3��Һ��ת��Ĥ���γɹ��̣��ڽ���ϡ��ת��Ĥ��Ĥ�������λ��������ϣ����õ绯ѧ�迹��(EIS)�����о���Һ����������H2O2��pHֵ�ȸ��������仯��ת��Ĥ�γɹ��̵�Ӱ�졣���������O2����ķ�Ӧ����Ceת��Ĥ�γ��ٶȵľ������裬����H2O2�ӿ�Ceת��Ĥ�γ��ٶȣ��ر����γɹ��̵ĵ�һ�Σ�����������Ҫ��������;����ԭ��ʹ�ֲ�pH��������pH�ﵽ��8.05ʱ��Ce(��)ˮ����������/�����↑ʼ������Ce(��)ת��Ĥ�ﵽ�ȶ�ƽ��Σ�����Ce(OH)3�ᱻ����ԭ���м����H2O2������CeO2�������Ի���������Һ�У������Һ��pHֵ�����ճ�Ĥ������
�ؼ��ʣ�
B95���Ͻ��������迹��Ceת��Ĥ���缫��Ӧ����Ĥ������
��ͼ����ţ�O646.6��TG133.2 �� �� ���ױ�־�룺A
Electrode reaction mechanism of conversion coating forming process of B95 aluminium alloy in cerium(��) salt solution
GU Bao-shan, YANG Pei-yan
(National Engineering Laboratory for Advanced Coatings Technology of Metal Materials,
China Iron and Steel Research Institute Group, Beijing 100081, China)
Abstract: The electrochemical impedance spectroscope (EIS) was used to study the conversion coating forming process of B95 aluminum alloy in 10 mmol/L CeCl3 solution. The formation process of rare earth (RE) conversion coating can be divided into three stages. Based on the three stages formation mechanism of the rare earth conversion coatings, the influences of O2 concentration, oxidant, pH etc on the formation process of conversion film were investigated. The result shows that the reaction caused by the O2 participation is not determinate step of the Ce conversion coating formation, the addition of H2O2 speeds up the formation of Ce conversion coating, especially in the first stage. The two electric ways of cathodic reaction are formed by the conversion coating on B95 aluminum alloy in CeCl3 solution, which reasonably explains the local pH rise in micro cathode area, Ce(��) hydrous hydroxide/oxide begins to deposit when the pH reaches or exceeds 8.05. Part Ce(OH)3 can be oxidized into CeO2 by the intermediate products of H2O2 when Ce(��) conversion coating achieves stable equilibrium. In neutral or subacidity solution, improving the pH of solution will beneficial to the final formation of the coating.
Key words: B95 aluminium alloys; electrochemical impedance spectroscope (EIS); Ce conversion coating; electrode reaction; coating forming process
��������������ѧ�߶������Ͻ�ϡ��ת��Ĥ���յ��о��Ѿ�ȡ���˺ܴ�Ľ�չ�������Ĥ�������о�Ҳ�����롣HINTON��[1]���ϡ������Һ���ڽ��ݹ������������ϡ��ת��Ĥ��������Ĥ������������Ϊ�����Ͻ�������ڴ����ž��硢�������������仯�����Լ���Ȼ������Ĥ��ȱ�ݣ���һ���Ǿ��ȱ��档���������Ͻ����ϡ������Һ�У��ڱ���ֲ����ͻṹ��ԭ��أ������绯ѧ��Ӧ�����������������ܽ�(M-ze��Mz+)������������O2�Ļ�ԭ(O2+2H2O+4e��4OH-)��H2������(2H++2e��H2)�����۷������ַ�Ӧ������ʹ������OH-Ũ������pHֵ���ߣ�Ϊ��������������γɺ����Ͻ����Al2O3���ܽⴴ������[1-3]�����������˵�����Ĥʱ����ӳ���Ĥ�����ܶȺ����ߴ硢�����������к��������Ĥ��Ҳ��֮���ӵ�һЩʵ�����������ڳ�Ĥ���ʼ�ת��Ĥ����ļ�̬���⣬�������������ܸ�����͡�
DAVENPORT��[4]��HUGHES��[5]���ⷽ������һЩ�м�ֵ�Ĺ��������Dz���X�������ս��߽ṹ����(XANES)����תԲ�̵缫�����Ի�ѧ���ݷ��γ���ת��Ĥ�ij�Ĥ��Ӧ�������о������������������������Һ�γɵ���ת��Ĥ����ļ�̬��Ϊ+3�ۣ������Һ�к�O2��pHֵ����8����Һ���������ܱ��������ļ��档ALDYKIEWICZ��[6]��һ����Cu�缫ģ��Al2024�Ͻ��еĺ�Cu�࣬�о���Ĥ���γɻ��������������O2�Ļ�ԭ��Ӧ����ҺpHֵ���缫���Ƽ�����γɵ���ת��Ĥ����̬��Ӱ�졣��Ըߵĵ缫��λ��pHֵ����������ԭ��Ӧ�������Ӳ������(O2+2H2O+2e��H2O2+2OH-)���ò������в���H2O2���ɣ����ij��ֿ�ʹ��Ĥ���ʼӿ죬������Һ�м���H2O2���ٳ�Ĥ��Ӧ��һ�µ�[5, 7]�������缫��λ��pHֵ�ϵ�ʱ������ԭ��Ӧ����Ҫͨ���ĵ��Ӳ������(O2+2H2O+4e��4OH-)��
�ֲ�����[8-9]�����������Ƶ�ɨ���αȵ缫������ԭλ������CeCl3��Һ������2024-T3Al�Ͻ��������λ�ֲ��������XPS��EIS��Ceת��Ĥ�ij�Ĥ��������̽�֡������������CeCl3��Һ�У�ת��Ĥ���γɹ�����Ce3+��Cl-����������ͻ�ʴ/��ʴ���õĶ�̬���̣�����Cl-�����ľֲ���ʴʹ�þֲ�����pH�������㹻��ʱ��Ce(OH)3�ͻ�����������Ӷ����ƾֲ���ʴ�Ľ�һ����չ��������Ӧ��Oͨ�������Ӳ�����С�
��ǰ�ڹ�����[10]��ͨ��B95������10 mmol/L CeCl3ԭʼ��Һ���迹��������⣬������������Ĥ�������Ӧ��EIS�仯�������ʾĤ��ı仯�����EIS��Ч��·�Ľ�����ϡ��ת��Ĥ�ij�Ĥ���̿��Էֳ�3���Σ��γɽΡ��ɳ��κ��ȶ�ƽ��Σ������������迹��ͼ��Ч��·�����迹����ʽ�����������ڴ˻����ϣ���Ĥ��Һ��ȻΪ10 mmol/L��CeCl3���ı���Һ�е�������������������Լ��ı���ҺpHֵ��������ͨ���迹����������о������������ضԳ�Ĥ���̵�Ӱ�죬�о�B95���Ͻ���������Һ��ת��Ĥ�γɵĵ缫��Ӧ���̣�̽��ϡ��ת��Ĥ�ij�Ĥ������
1 ʵ��
�������Ϊ�������պ����ѧ�ṩ��B95��Ӳ���Ͻ𣬸úϽ�ϵAl-Zn-Mg-Cu�Ͻ𡣺Ͻ�Ļ�ѧ�ɷ�(����������%)Ϊ5.1~6.1Zn, 2.1~2.9Mg, 1.2~2.0Cu, 0.30Mn, 0.18~0.35Cr������Al��
�����迹����ʹ��EG&G Potentiostat/Galvanostat Model 273A��5210����Ŵ�����ɵĵ绯ѧ����ϵͳ���������Ҳ���λ��ֵΪ10 mV��Ƶ��ɨ�跶ΧΪ0.1Hz~10 kHz�����ʹ��缫Ϊ�αȵ缫��PtƬΪ�����缫��B95���Ͻ�Ϊ�����缫�������¶�Ϊ(22��2) �档
���Ƚ�B95���Ͻ��������ڳ�Ĥ��Һ10 mmol/L��CeCl3�У�����ҺԭʼpHֵΪ5.2~5.3�������ڳ�Ĥ��Һ���ȶ�10 min��ʼ�����迹���ԡ������������������������⡣
��Ĥ��ҺpHֵ���Բ���pH-HJ90B������ȼơ��绯ѧ�迹�IJ��Խ�����õ�Ч��·����Princeton Applied Research(EG&G)��ZSimpWin3.0�������������迹��ͼ�ס�ת��Ĥ�ĸ�ʴ��ò����S-530ɨ��羵(SEM)���й۲졣
2 ʵ����
2.1 ��Һ������������ת��Ĥ�γɹ���Ӱ��
Ϊ�о���Һ���������仯��ϡ��ת��Ĥ�γɹ��̵�Ӱ�죬��10 mmol/L CeCl3��Һͨ����30 min���������������ͨ���������迹�ף������ͼ1��ͨ���������迹ͼ��Ȼ�Ǹ�Ƶ���ּ�����һ��ֱ�ߡ���Ƶ������Ϊһ����Բ���ɴ˿�����֪[11-12]������Ȼ��һ���绯ѧ������Ũ���ͬʱ�����õĻ�Ͽ��ƣ�����Ȼ�������迹��������ơ�
��ͨ���������迹�Ľ������֣�2 min~7 h�迹��Ч��·����Ȼ״̬�µij�Ĥ�γɽ���ͬ[10]����ͨ��7 h������������Ȼ����ϡ��ת��Ĥ���γɽΡ�
2.2 H2O2���Ӷ�����ת��Ĥ�γɹ���Ӱ��
��400 mL 10 mmol/L CeCl3��Һ�м���2.5 mL 30% H2O2�����B95���������迹��������⣬�ڼ�ֱ��ڵ�24 h��28 hʱ������2.5 mL 30% H2O2���������(��ͼ2)��B95���Ͻ�������H2O2��CeCl3��Һ��ת��Ĥ�γɹ����벻��H2O2�ij�Ĥ��������[10, 13]��
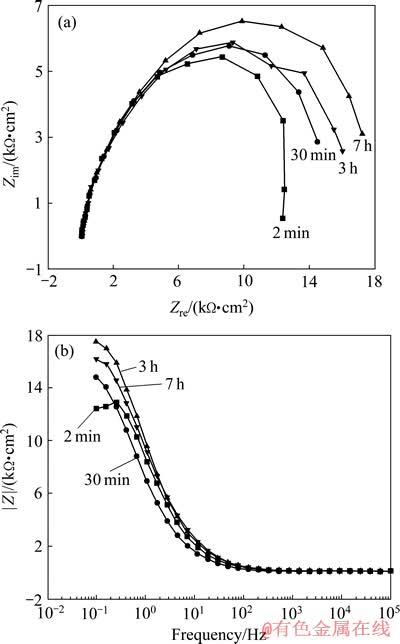
ͼ1 ��ͬͨ��ʱ��Գ�Ĥ���̵绯ѧ�迹��Ӱ��
Fig. 1 Influence of O2 flow time on Nyquist(a) and Bode(b) plots of conversion coating in aerated O2
����Ȼ����������B95���Ͻ����Ceת��Ĥ�γɹ��̵ķ�����������Ȼ�������ɵ�ת��Ĥ�������ܣ�������Һ�н���ʱ����ӳ���ת��Ĥ�����������½�[11]������H2O2��һ����ӿ�Ceת��Ĥ�γ��ٶȣ��ر��dz�Ĥ�ĵ�һ�Ρ����γɽΣ�ʹԭ��24 h�Ĺ�������Ϊ1.5 h(��ͼ2)����һ���棬H2O2��ʹB95����ת��Ĥ��������(��ͼ3)���ܹ���ֹˮ��ת��Ĥ�е�����ת��Ĥ���迹ֵ��������������ơ�
������10 mmol/L CeCl3��Һ�У�����������H2O2��10 mmol/L CeCl3��Һ�У���Ceת��Ĥ��B95���Ͻ�����γɣ���Һ��pHֵ������������(��ͼ4)��
2.3 ��Ĥ��ҺpH�仯������ת��Ĥ�γɹ���Ӱ��
Ϊ�о�pHֵ�ı仯��ת��Ĥ�γɹ��̵�Ӱ�죬����10 mmol/L CeCl3��Һ��pHֵ�ֱ�Ϊ3.0��4.0��5.0��6.0��Ȼ�����B95���������迹��������⣬���Բ��Ե��迹���з�������B95���Ͻ��ڲ�ͬ pHֵ��10 mmol/L CeCl3��Һ�в���迹ֵ��ʱ��仯��ͼ��������ͼ5����ͼ��������ʾ��pHֵ�ı仯��Ceת��Ĥ�γɹ��̵�Ӱ�졣
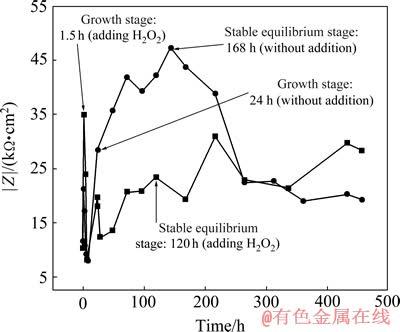
ͼ2 ����H2O2��B95���Ͻ����Ce(��)ת��Ĥ��|Z|��ʱ��仯��Ӱ��
Fig. 2 Influence of H2O2 addition on |Z| change of Ce(��) conversion coating of B95 Al alloy
1) ��ʵ�鷶Χ�ڣ�pHֵԽ�ߣ��γɵ�ת��Ĥ��ʴ��Խ�á�
2) pH=3.0��H+Ũ�ȸ���������B95���Ͻ��������Ĥ�ͻ�����ܽ���������pHֵ̫�ͣ���������ȷ�����ԣ�����Ce3+��B95���Ͻ���һ���Ļ�ʴ���ã�B95���Ͻ���10 mmol/L CeCl3��Һ����Ȼ���γ�Ceת��Ĥ�����������Ч����B95���������̣������ʱ����ӳ������Ͻ��������ܽ⡣
3) pH��4.0~6.0��Χ�ڣ�H+Ũ�Ƚϸ����������Ͻ�����ܽ����ٽ���Ĥ��һ�εĽ��У�����Ce(��)�����������������ij���ȴ�Dz����ġ���ˣ�pH=4.0ʱ����Ĥ�ٶ�Ѹ�٣�7 h�ͽ���Ĥ�ɳ��Σ����ɳ���ά�ֵ�ʱ��ܶ̾ͽ���ƽ��Σ�����Ĥ�ĺ�Ⱥ������Ծ������롣����pHֵ��ߣ����Ͻ���ܽ��ٶ��½�����Ӱ��Ĥ���γɽΣ�����������Ce(��)�����������������ij�����Ceת��Ĥ�γɹ��̵ijɳ���ʱ������ϳ�(pH=4.0��41 h��pH=5.0��48 h��pH=6.0��168 h)�����Ĥ�ĺ�ȡ�������������pH=6.0ʱ���迹ֵҪ��pHΪ3.0��4.0��5.0��ö࣬˵�������Һ��pHֵ�����ճ�Ĥ������

ͼ3 H2O2�����Ӷ�B95����Ce(��)ת��Ĥ������ò��Ӱ��
Fig. 3 Effect of H2O2 addition on surface morphologies of B95 cerium(III) conversion coating
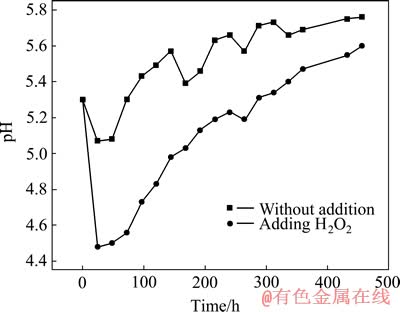
ͼ4 B95���Ͻ����ϡ��ת��Ĥ�γɹ�������ҺpHֵ��ʱ��ı仯
Fig.4 Change of pH with time in solution during cerium(��) conversion film formation processes of B95 Al alloy
ͼ5 ��Һ��ͬpHֵ��B95���Ͻ����Ce(��)ת��Ĥ��|Z|��ʱ��仯��Ӱ��
Fig. 5 Influence of pH in solution on |Z| change of Ce(��) conversion coating of B95 Al alloy with time
3 ����������
3.1 ��������ԭ��Ӧ��������
����������Ĥ����[1]����95���Ͻ����CeCl3��Һ�ڶ�������ͻ����γɾֲ���ء��ڵڶ����Ϸ���������Ӧ���������γ�Ce(OH)3������
��������ԭ��Ӧ�ĸ�����(�漰4�����Ӽ�2~4�����ӵ�ת�ƣ���O��O���Ķ���)������д�����ָ����ķ�Ӧ���������̣�����[14-15]���ж��ֱ�����������һԭ��������ԭ��Ӧ�Ļ����о��У������ڷ���������ķ�Ӧ���ͣ���������Ҫ������ν��Ӧ�ġ�ֱ���ĵ���;�����͡�������;������
1) �м����Ϊ�����������������ġ�ֱ���ĵ���;����[15-16]
�ܷ�ӦʽΪ��
O2+2H2O+4e��4OH-
��
O2+4H++4e��2H2O (1)
2) �м����ΪH2O2��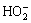 �ġ�������;����[14-15]
�ġ�������;����[14-15]
���Ի�������Һ������ԭ�Ļ������̣�
�� O2+2H2O+2e��H2O2+2OH- (�绯ѧ��Ӧ)
��
O2+2H++2e��H2O2 (�绯ѧ��Ӧ) (2)
�� H2O2+2H++2e��2H2O (�绯ѧ��Ӧ)
��
H2O2��1/2O2+H2O (���ֽ�) (3)
�ڼ�����Һ�У���Ӧ�����ղ���ΪOH-��ͬʱ�м����H2O2�ܰ���H2O2+OH-
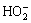 ��H2O���(pK��11.7)����ˣ���ǿ������Һ������ԭ���̰�������;������ʱ�Ļ�����Ӧ����Ϊ
��H2O���(pK��11.7)����ˣ���ǿ������Һ������ԭ���̰�������;������ʱ�Ļ�����Ӧ����Ϊ
�� O2 + 2H2O+2e��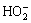 +OH- (�绯ѧ��Ӧ)
+OH- (�绯ѧ��Ӧ)
�� 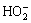 +H2O+2e��3OH- (�绯ѧ��Ӧ)
+H2O+2e��3OH- (�绯ѧ��Ӧ)
��
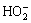 ��1/2O2+OH- (���ֽ�) (4)
��1/2O2+OH- (���ֽ�) (4)
��ʵ�ϣ���ν�������ӷ�Ӧ;�����ֿ��Է�Ϊ�����ࣺһ������H2O2���ٽ�һ����ԭ����ȫ����Ӧ���漰�ĵ�����Ϊ2����H2O2Ϊ���շ�Ӧ�����һ�������ɵ�H2O2�ɽ�һ����ԭΪˮ��OH������һ�ࡰ�����ӷ�Ӧ���ֿɳ�Ϊ�������������ӷ�Ӧ������ɵ��ĵ��ӷ�Ӧ��������Ϊ��������Ӧ����
Ҳ����˵����ֱ���ĵ���;����(��Ӧ(1))�͡�������;����(��Ӧ(2)��(3))����ʹ��������pH��ߡ�����O2�Ļ�ԭ��Ψһ����Ҫ�������̣���O2�ﵽ��ɢƽ��ʱ���ɼ�������������������ﵽ�����pHֵ����Ӧ(1)�ͷ�Ӧ(2)��Ӧ�����pHֵ�ֱ�Ϊ10.65��10.35[8]��
����������ԭ��Ӧ�ǰ���ֱ���ĵ���;�������ǡ�������;�����������Ҫ�������Ǽ�鷴Ӧ�������Ƿ����м����Ĵ��ڡ�����ڷ�Ӧ�м�鵽�м�����H2O2���ڣ���Ӧ����Ӧ���������Ӳ��裬������һ���ַ�Ӧ��ͨ�������Ӳ�����еġ�
��Һ���������仯������ת��Ĥ�γɹ���Ӱ��ĵ绯ѧ�迹��ʵ����������ͨO2��ϡ��Ceת��Ĥ���γ������Դٽ����ã�O2����ķ�Ӧ����Ceת��Ĥ�γɵľ��ٲ��裬�ɴ��ƶ�����������ԭ��Ӧ���ǰ���ֱ���ĵ���;�������С�
���⣬��H2O2���Ӷ�����ת��Ĥ�γɹ���Ӱ���У�����Ȼ����������B95���Ͻ����Ceת��Ĥ�γɹ��̵ķ�������������H2O2��һ����ӿ�Ceת��Ĥ�γ��ٶȣ��ر��dz�Ĥ�ĵ�һ�Ρ����γɽΣ�ʹԭ��24 h�Ĺ�������Ϊ1.5 h(��ͼ2)��˵����Ce��ת��Ĥ�γɹ�������H2O2�μӷ�Ӧ�����֤��������Ӧ�ǰ���������;�������С�
����H2O2��10 mmol/L��CeCl3��Һ�У����Ž���ʱ����ӳ���Ce(��)ת��Ĥ����Ҳ�����ܽ⡪�����ɵĶ�̬ƽ�⣬�ڽ���ʱ�����144 h��ת��Ĥ���迹ֵ����С�����ơ�����H2O2�����Ž���ʱ����ӳ�����ȻCe(��)ת��Ĥ����Ҳ�����ܽ⡪�����ɵĶ�̬ƽ�⣬������˵ת��Ĥ���迹ֵ��������������ƣ���ͼ2��ʾ��
3.2 ����ת��Ĥ�γɵĵ缫��Ӧ
���ֲ�pH�㹻��ʱ��Ce3+�ͻ�ˮ���Ĥ��
Ce3++3H2O��Ce(OH)3+ 3H+
��
Ce3++3OH-��Ce(OH)3 (5)
�˷�Ӧ������С�ٽ�pHcrit������ʽ����[8]��
lg[Ce3+]sat=22.15-3pHcrit (6)
���У�[Ce3+]sat��Ce3+�ı���Ũ��(�ڱ�ʵ����Ϊ10 mmol/L)������ʽ(6)����õ�pHcritΪ8.05��pHcrit��������pHֵ(10.35~10.65)С�ö࣬��ˣ���������Ce(OH)3���Գ���������
��Ӧ(2)���ܷ�Ӧʽ��������ԭ����H2O2�ķ�Ӧʽ(2)�Ŀ��Ʋ�����û��H+���Ӳμӵĵ���ת�Ʋ���[14]������־���һϵ�з�Ӧ���裬����������H2O2��ͬ��H2O2�Ļ�ԭ���̵Ŀ��Ʋ���Ϊ(H2O2+e��OH+OH-)����û��H+���Ӳμӵĵ���ת�Ʋ��衣�����Ӳ������������������ԭ���̵Ŀ��Ʋ�����H+�����ء�
�ڳ�Ĥ���γɽδ����������������ٽ��ķ�Ӧ��1) ���Ͻ��������Ĥ���ܽ�����Ͻ������ܽ���2) Ce�����������������ij�����H+����Ũ�Ƚϸ���������B95���Ͻ��������Ĥ�ͻ�����ܽ��������H+����Ũ��̫�ߣ���������ȷ�����ԣ�����Ce3+��B95���Ͻ���һ���Ļ�ʴ����[16]��B95���Ͻ���10 mmol/L CeCl3��Һ����Ȼ���γ�Ce(OH)3���������������Ч����B95���������̣������ʱ����ӳ������Ͻ��������ܽ⡣��֮��H+����Ũ�ȵͣ��䲻�������Ͻ����Ļ��������ȷ�����������ԣ�ֻ�ܼ���Ce�����������������ij����ٶȡ���Ĥ����������缫��Ӧ���̷������Ժ�����������������pH=3.0ʱ������Ĥ��pH=4.0ʱ����Ĥ�ٶ���죻pHΪ5.0��6.0ʱ���γ�ת��Ĥ�ȶ��ε�ʱ�����ӳ���
���⣬����[8, 17-18]�б���Ce(��)���յõ���ת��Ĥ��Ce(��)��Ce(��)�Ļ�����һ�������£�Ce(OH)3�ɽ�һ��������ΪCeO2��CeO2��Ce(OH)3��Ce2O3���и��õ��赲�ԣ���Ceת��Ĥ������������Ҫ�����á�Ce(OH)3��ͨ����Ӧ(7)����CeO2��
Ce(OH)3-e��CeO2+H2O+H+ (7)
��Ӧ��λΪ����0=1.559-0.059pH
��������Ӧ�ǡ��ĵ���;��������Ӧ��λΪ��0=1.229-0.059pH+0.015 lg pO2 (pO2=2.02��104 Pa)���Ƚ������������缫��λ��֪����Һ���ܽ�O2�����ܽ�Ce(OH)3����ΪCeO2����������Ӧ�ǡ�������;��������Ӧ�ĵ缫��λΪ��0=1.776-0.059pH+0.030 lg[H2O2]�������ԣ���Ce(OH)3���ڵ�pH�����£�H2O2�ܹ���Ce(OH)3����ΪCeO2���Ժ������ٽ����γɵ�B95���Ͻ�Ce(��)ת��Ĥ����XPS��ͼ����ת��Ĥ����Ҫ�ɷֺ���ļ�̬���������ת��Ĥ��Ce��Ҫ��+4��̬����������ʽ���ڡ�
4 ����
1) �绯ѧ�迹��(EIS)ʵ����������O2����ķ�Ӧ����Ceת��Ĥ�γɵľ��ٲ��裻��Ce��ת��Ĥ�γɹ�������H2O2�μӷ�Ӧ��
2) ת��Ĥ�γɽΣ������Ͻ��ܽ⣬����������Ҫ����������;������ԭʹ�ֲ�pH��������pH�ﵽ��8.05ʱ��Ce(��)ˮ����������/�����↑ʼ���ᡣ
3) Ce(��)ת��Ĥ�ﵽ�ȶ�ƽ�⣬����Ce(OH)3�ᱻ����ԭ���м����H2O2������CeO2��
4) �����Ի���������Һ�У������Һ��pHֵ�����ճ�Ĥ������
REFERENCES
[1] HINTON B R W, ARNOTT D R, RYAN N E. Cerium conversion coating for the corrosion protection of aluminum[J]. Materials Forum, 1986, 9(3): 162-173.
[2] ARNOTT D R. Cationic film forming inhibitors for the corrosion protection of AA7055 aluminum alloy in chloride solutions[J]. Materials Performance, 1987, 26(8): 42-47.
[3] ARNOTT D R. Cationic film forming inhibitors for the protection of AA7075 aluminum alloy against corrosion in aqueous chloride solution[J]. Corrosion, 1989, 45(1): 12-19.
[4] DAVENPORT A J, ISAACS H S, KENDIG M W. XANES investigation of the role of cerium compounds as corrosion inhibitors for aluminum[J]. Corrosion Science, 1991, 32(4): 635-663.
[5] HUGHES A E, TAYLOR R J, HINTON B R, WILSON L. XPS and SEM characterization of hydrated cerium oxide conversion coatings[J]. Surface and Interface Analysis, 1995, 23(7/8): 540-550.
[6] ALDYKIEWICZ A J, DAVENPORT A J, ISAACS H S. Study of the formation of cerium-rich protective films using X-ray absorption near-edge spectroscopy and rotating disk electrode methods[J]. J Electrochem Soc, 1996, 143(1): 147-153.
[7] HUGHES A E, TURNEY T W, NELSON K J H. Process and solution for providing a conversion coating on a metal surface. US Patent: US6206982[P]. 2001-03-27.
[8] ������, ����˫, �� ��, ���ڸ�, �ֲ���. Al�Ͻ����Ceת��Ĥ��Ĥ�����о�[J]. ������ѧѧ��, 2002, 18(9): 791-795.
SHAO Min-hua, HUANG Ruo-shuang, FU Yan, HU Rong-gang, LIN Chang-jian. Investigation on the formation mechanism of Ce conversion films on 2024 aluminum alloy[J]. Acta Phys-Chim Sin, 2002, 18(9): 791-795.
[9] ������, �� ��, ���ڸ�, �ֲ���. Al�Ͻ�����ת��Ĥ��ʴ�����о�[J]. �绯ѧ, 2002, 18(1): 15-21.
SHAO Min-hua, FU Yan, HU Rong-gang, LIN Chang-jian. An investigation of inhibition mechanism of cerium for aluminum alloy 2024-T3[J]. Electrochemistry, 2002, 18(1): 15-21.
[10] �˱�ɺ, ������. ���ζ����Ͻ�ij�Ĥ���̵绯ѧ�����迹�о�[J]. �й�ϡ��ѧ��, 2007, 25(2): 210-216.
GU Bao-shan, LIU Jian-hua. Cerium(��) film formation process for aluminum alloys observed with electrochemical impedance spectroscopy[J]. Journal of Chinese Rare Earth Society, 2007, 25(2): 210-216.
[11] �˱�ɺ, ������, �� ��. �绯ѧ�迹�����о�Ce(��)ת��Ĥ��3.5%NaCl��Һ�еĸ�ʴ��Ϊ[J]. �й���ɫ����ѧ��, 2013, 23(6): 1640-1643.
GU Bao-shan, YANG Pei-yan, GONG Li. Corrosion behavior of Ce(��) conversion coating in 3.5%NaCl solution by electrochemical impedance spectroscope[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(6): 1640-1647.
[12] ROCCA E, JUERS C, STEINMETZ J. Corrosion behaviour of chemical conversion treatments on as-cast Mg-Al alloys: Electrochemical and non-electrochemical methods[J]. Corrosion Science, 2010, 52: 2172-2178.
[13] �˱�ɺ, ������. �������������ת��Ĥ�γɹ���Ӱ��ĵ绯ѧ�迹�о�[J]. ��ʴ��ѧ���������, 2011, 23(2): 143-146.
GU Bao-shan, LIU Jian-hua. Effect of H2O2 on formation process cerium(��) conversion film on aluminum alloys by EIS[J]. Corrosion Science and Protection Technology, 2011, 23(2): 143-146.
[14] �� ݶ. �绯ѧԭ��[M]. ����: �������պ����ѧ������, 1999: 394-398.
LI Di. Electrochemical fundamentals[M]. Beijing: Beijing University of Aeronautics and Astronautics Press, 1999: 394-398.
[15] ��ȫ��. �缫���̶���ѧ����[M]. 3��. ����: ��ѧ������, 2002: 258-262.
CHA Quan-xing. Introduction of electrode process kinetics[M]. 3rd ed. Beijing: Science Press, 2002: 258-262.
[16] GU Bao-shan, LIU Jian-hua. Corrosion inhibition mechanism of rare earth metal (REM) on LC4 Al alloy with the spilt cell technique[J]. Journal of Rare Earths, 2006, 24(1): 89-96.
[17] ARNOTT D R. Auger and XPS studies of cerium corrosion inhibition on 7075 aluminum alloy[J]. Applications of Surface Science, 1985, 22/23: 236-251.
[18] SCHOLES F H, SOSTE C, HUGHES A E, HARDIN S G, CURTIS P R. The role of hydrogen peroxide in the deposition of cerium-based conversion coatings[J]. Applied Surface Science, 2006, 253(4): 1770-1780.
(�༭ ����)
�ո����ڣ�2013-01-22�������ڣ�2013-08-02
ͨ�����ߣ��˱�ɺ�����ڼ�������ʦ����ʿ���绰��010-62182573��13501237905��E-mail: gubs@263.net
ժ Ҫ�����õ绯ѧ�迹��(EIS)�о�B95���Ͻ���10 mmol/L CeCl3��Һ��ת��Ĥ���γɹ��̣��ڽ���ϡ��ת��Ĥ��Ĥ�������λ��������ϣ����õ绯ѧ�迹��(EIS)�����о���Һ����������H2O2��pHֵ�ȸ��������仯��ת��Ĥ�γɹ��̵�Ӱ�졣���������O2����ķ�Ӧ����Ceת��Ĥ�γ��ٶȵľ������裬����H2O2�ӿ�Ceת��Ĥ�γ��ٶȣ��ر����γɹ��̵ĵ�һ�Σ�����������Ҫ��������;����ԭ��ʹ�ֲ�pH��������pH�ﵽ��8.05ʱ��Ce(��)ˮ����������/�����↑ʼ������Ce(��)ת��Ĥ�ﵽ�ȶ�ƽ��Σ�����Ce(OH)3�ᱻ����ԭ���м����H2O2������CeO2�������Ի���������Һ�У������Һ��pHֵ�����ճ�Ĥ������
[9] ������, �� ��, ���ڸ�, �ֲ���. Al�Ͻ�����ת��Ĥ��ʴ�����о�[J]. �绯ѧ, 2002, 18(1): 15-21.
[10] �˱�ɺ, ������. ���ζ����Ͻ�ij�Ĥ���̵绯ѧ�����迹�о�[J]. �й�ϡ��ѧ��, 2007, 25(2): 210-216.
[13] �˱�ɺ, ������. �������������ת��Ĥ�γɹ���Ӱ��ĵ绯ѧ�迹�о�[J]. ��ʴ��ѧ���������, 2011, 23(2): 143-146.
[14] �� ݶ. �绯ѧԭ��[M]. ����: �������պ����ѧ������, 1999: 394-398.
[15] ��ȫ��. �缫���̶���ѧ����[M]. 3��. ����: ��ѧ������, 2002: 258-262.


