DOI: 10.11817/j.ysxb.1004.0609.2021-37670
�Ϲ���ý����̿����ʵ��
��ʢ��1���� ��2��������2���ν���1�����2����ѧ��1
(1. ���ϴ�ѧ ұ���뻷��ѧԺ����ɳ 410083��
2. ���ϴ�ѧ ��Դ��ѧ�빤��ѧԺ����ɳ 410083)
ժ Ҫ��
�Ϲ���ý�����������չ����γɴ����Ի���̿Ϊ��Ҫ��ֵķ���������������ữѧ���������������ϵķ������ԷϹ���ý����̿�����������Ƚϲ�ͬ���������µ��������ܣ���������Ũ�ȡ�����ʱ�䡢�������¶Ⱥ�������ʱ���Ӱ�졣��������Ļ���̿��Ʒ�����˱�������������ָ������Լ��̶����ѹ�ʵ�顣������������û�ѧ���������������ϵķ�������ʵ�ַϹ���ý����̿�ĸ�Ч�������Ż�����������Ϊ��Ũ��ֵ0.6 mol/L����ѧ����ʱ��0.5 h���������¶�750 �桢������ʱ��2 h����������̿������ֵ��߿ɴ�1022.12 mg/g���Ǽ�������ֵ��߿ɴ�182.34 mg/g�������ʻ���̿�൱����������̿�Ĺ�����Ч����3 h�ڿ���ά��80%���ϡ������ṩһ�ּ����á���Ч�ķϹ���ý����̿����������������ʵ�ַϹ���ý��ѭ�����á�
�ؼ��ʣ�
�Ϲ���ý������̿����ѧ������������������
���±�ţ�1004-0609(2021)-03-0715-09���� ��ͼ����ţ�TF11.31���� ���ױ�־�룺A
���ĸ�ʽ����ʢ��, �� ��, ������, ��. �Ϲ���ý����̿����ʵ��[J]. �й���ɫ����ѧ��, 2021, 31(3): 715-723. DOI: 10.11817/j.ysxb.1004.0609.2021-37670
WANG Sheng-cai, YANG Qin, ZHANG Ming-guang, et al. Regeneration of activated carbon from waste mercury catalyst[J]. The Chinese Journal of Nonferrous Metals, 2021, 31(3): 715-723. DOI: 10.11817/j.ysxb.1004.0609.2021-37670
����ý�ǵ�ʯ������������ϩ(PVC)���ɻ�ȱ�IJ��֣�����PVC��������Ȳ���Ȼ�������ϳ�����ϩ(VCM)�Ĵ���������ý���������Ի���̿�����塢�Ȼ���Ϊ�������ʣ����Ȼ��������ڻ���̿����[1-2]������ý��ʹ��һ��ʱ���������½�����и��������������ķϹ���ý��һ����Ȼ����2%���ҵ��Ȼ���[3]���Ȼ����綾�����ӷ�����������ˮ���������������Ĺ���ýֱ�ӽ��ж�����ѷţ��Ʊؽ�������صĹ���Ⱦ�������ش�ȫ������Ŀǰ����ԷϹ���ý����������������Ҫ�������������ͻ�ѧ�����������Ϊ��[4-6]������ԭ��Ϊ������ʯ�ҡ��������Ƶȣ����Ϲ���ý�и���̬�Ĺ�ת��Ϊ�ֽ⡢�ӷ����ռ��������������������ȷֽ�Ϊ���ʹ����������Ե��ʹ��������д��䣬ʵ�ַϹ���ý�й��Ļ���[7]��
��Ȼͨ������ȷ�������ʵ�ַϹ���ý�����������빯�Ļ��գ������������ҵ��û���ض��Ĺ�����������̿���Ӷ���ɻ���̿��Դ�˷��Լ�DZ�ڵĶ�����Ⱦ��Ŀǰ��������Թ��ͻ���̿ͬʱ���յĹ��ղ�����[1, 7]����������Ԥ������������������ʯ�ҡ��������Ƶ����ʣ��Ϲ���ý����������渽���˴���̼��ơ������ơ�̼���Ƶȷ�ĩ���������ܱ����ѽ�һ�������� ��[8]����Ȼ�Ϲ���ý�������չ�������������ԭ���Ͽ�����Ϊһ�������д����������ڹ������������乯������Ȼ���ܻᳬ��Σ�շ���ļ��������ˣ��Ϲ���ý����̿���������Ƿdz���Ҫ�ġ�Ŀǰʹ�õĻ���̿����������Ҫ��������������ѧ�Լ����������������������绯ѧ����������������������[9-10]�����У�����������ͨ�����ȵķ�ʽʹ����̿���������ʽ��н�����ֽ⣬��һ�ֽ�Ϊ���������������������Һ�ʱ���һ���ɴ�����̿��ʧ�������ɱ��ܸ�[9]��Ʃ�磬����������ķϹ���ý����̿�У�ͨ������̼��ơ������ƺ�̼���Ƶ����ʣ���Щ������̼���Ƶķֽ��¶ȸߴ�1744 �棬������������������������ܺĺܸߡ�̿��ʧ�ܴ�ѧ�Լ���������������Ӧ�Ļ�ѧ�Լ��Ի���̿���������ʽ����ѳ�������ʱ��϶̣�̿��ʧ��С������������Ч�ʵͣ�һ����Ѵﵽ80%[11]��
Ϊʵ�ַϹ���ý����������ϻ���̿�ĸ�ֵ���ã������ṩһ�ֵͳɱ������̼�Ч���õķϹ���ý����̿���������������ǣ��������ữѧ���������������ϵķ��������Ϲ���ý����������ķϻ���̿������ڲ����ڵ�̼��ơ�̼���ơ������ơ�����PVC�������仯����������ѳ����ָ�����̿�����������Ӷ�ʵ�ַϻ���̿�����������Ļ�������ǰ��Ļ���̿���е�����ֵ���Ǽ�������ֵ��ָ��IJ��ԣ���̽����ѵ�����������
1 ʵ��
1.1 ��Ʒ����Ҫ�Լ�
ʵ������Ϲ���ý����̿�������½�ij�Ϲ���ý������ҵ�����Ѿ��������մ��������ڶѴ���һ��ʱ�䣬����溬�д���������������еĶ�����̼��Ӧ���ɵ�̼��ơ�
����ζ���Һ(c(1/2I2)=0.1 mol/L)�������֮һ�˵�����ƽ��ȡ12.700 g�ⵥ����19.100 g�⻯������100 mL�ձ��У��ڴ��������£��ֶ�μ���ȥ����ˮֱ����Һ����ﵽ50~60 mL������������ȫ�������ܽ⣬��������Һ����1000 mL����ɫ����ƿ�У���ȥ����ˮϡ�Ͷ��ݡ�
0.1 mol/L�����������Һ����ȡ26 g��ˮ�������������0.2 g��ˮ̼��������1000 mLȥ����ˮ�У��������10 min����ȴ�����£��������ܺ���˱��á�
����ָʾ������ȡ2.00 g��������5 mLȥ����ˮ�б�ɺ�״���ڴ��������¼���90 mL��ˮ�����1~2 min���ݵ�100 mL��
����Һ����ȡ9.080 g����������������ȥ����ˮ�У���������Һת����1000 mL����ƿ�У���ȥ����ˮ���ݵõ�����ҺaҺ����ȡ29.300 gʮ��ˮ������������������ȥ����ˮ�У���������Һת����1000 mL����ƿ�У���ȥ����ˮ���ݵõ�����ҺbҺ����ʹ��ʱ��aҺ��bҺ���������1:1��ϵõ�����Һ��
0.02 g/mL�Ǽ�����Һ�����ڽ��Ǽ������и���ᷢ�����ԣ���˲���ֱ�Ӹ���ʹ�ã����Ȳⶨ��ˮ�ʣ���ȡ1.000 g�Ǽ�������105 ����������4 h����ȡ��1.5 g�������Ǽ������Ӧ��δ������Ǽ����Լ�����60~70 ��ˮԡ���������ڻ���Һ�У��ܽ���ȫ����ȴ�����£������˵�1000 mL����ƿ�У��û���Һϴ�Ӻ�ϡ�Ͷ��ݡ�
1.2 ��Ʒ��������
���о��зϻ���̿���û�ѧ�����������ϵ�����������
��ѧ��������������״�ϻ���̿(WAC)��ȥ����ˮ��ϴ����105 �������º�ɡ�ȡ����150 mL����貣����ƿ���ֱ����10 gϴ�Ӹ����ķϻ���̿����ȡ50 mL��ͬŨ�ȵ�������Һ(0.2~0.8 mol/L)���뵽������ƿ�У����������У���Ƶ��30 r/min����ʱ��ֱ�ȡ0.5 h��1 h��2 h��4 h���������Ʒ���˸������㶨�������⡣
������������ѡȡ��ѧ����������ָ��Ϻõ���Ʒ�����ǵ���ʱ�Ļ���̿���Ժ��������Ĺ���̼��ƣ�����650~850 ���¶������ڽ���������ʵ�顣ȡ2 g�ϻ���̿��Ʒ���뵽ʯӢ���У��ڹ�ʽ¯�н��м��ȴ����������¶�����Ϊ650~850 �棬ÿ��100 ��ȡһ��ʵ��㣬������ʱ��Ϊ0.5 h��1 h��2 h��4 h��
1.3 ��������̿��Ʒ����ָ�����
������Ʒ������ȡ10 g�ϻ���̿��Ʒ��105 ��������и���6 h����ȴ����ĥ��90%������Ʒ��ͨ��200Ŀɸ��װ������ܷ���б��á�
������ֵ�ⶨ����һ�������Ĵ�����������
250 mL��ƿ�У�����Һ�ܼ���10 mL������Һ(10%���������)���ڼ��Ȱ������30 s����ȴ�����¡�����Һ�ܼ���50 mL����ζ���Һ(0.1 mol/L)����������ƿ������ҡ��30 s��Ѹ����������ֽ���ˡ�ȡ50 mL��Һ����250 mL��ƿ�У��������������Һ(0.1 mol/L)�ζ������ʵ���ɫ�����2 mL����ָʾ���������ζ�ֱ����Һ����ɫ��ʧ��������ֵD(��λmg/g)�������¹�ʽ���м��㣺
 (1)
(1)
ʽ�У�c1��c2�ֱ��ʾ����ζ���Һ�������������Һ��Ũ�ȣ���λmol/L��V1��V2��V3�ֱ��ʾ����ζ���Һ��������Һ�����ĵ������������Һ���������λmL��V��ʾ��Һ�������λmL��M������Ħ��������ֵ[M(1/2I2)=126.9 g/mol]����λmol/L��
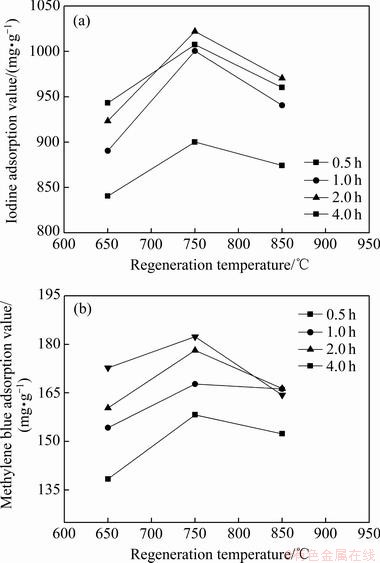
�Ǽ�������ֵ�ⶨ��ȷ��ȡһ�������Ĵ�����Ʒ����100 mL��ƿ�У����������IJ�ͬ�μ�5~15 mL�Ǽ�����Һ(1.5 g/L)������������������30 min������������ɫ����ҡ�ȡ��ù��Ϊ10 mm�ı�ɫ����665 nm�������ⶨ��Һ�����ֵ(�α�ҺΪȥ����ˮ)������������Ǽ�����Һ���ֱ����Һ�����ֵ������ͭ����Һ�������ֵ�IJ�ֵС��0.02���Ǽ�������ֵX(��λΪmg/g)�������¹�ʽ���㣺
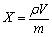 (2)
(2)
ʽ�У� ��ʾ�Ǽ���Ũ��ֵ����λΪmg/L��V��ʾ���ĵ��Ǽ�����Һ�������λΪmL��m��ʾ������������λΪg��
��ʾ�Ǽ���Ũ��ֵ����λΪmg/L��V��ʾ���ĵ��Ǽ�����Һ�������λΪmL��m��ʾ������������λΪg��
1.4 ��������
����SDT Q600��ͬ���ȷ����Ƕ�����ǰ����ѹ�����̿��Ʒ�������ط���(TGA)��ȷ������̿�������ʵ���Ҫ�Ѹ��¶���ֽ��¶ȡ�TGA�����������¶ȷ�Χ20~800 �桢��������5 ��/min����������Ϊ100 mL/min��
����QuadraSorb SI�ͱȱ�������������Ƕ�����ǰ����ѹ�����̿��Ʒ���бȱ�������������ȷ������̿����ǰ��ıȱ���������̿�ڲ����ֲ��ı仯����������������ǰ�Ƚ���Ʒ��120 �������������������3 h����77 K�����½��е�������������̿�ȱ��������Brunauer- Emmett-Teller(BET)�����㣬����t-plot���������̿��������ױȱ��������ױȱ�������������BJHģ��ȷ����
1.5 ��������̿�ѹ����ܲ���
������ǰ��Ļ���̿��Ʒ��ͼ1�еĹ̶�������ʵ��ϵͳ������̬Hg0����ʵ�飬�Ƚ�����ǰ����������ܡ�ʵ������������̿��Ʒ����0.2 g�����ڹ�Ũ��65 ��g/m3����������1 L/min�������¶�120 �档

ͼ1 ʵ��ϵͳʾ��ͼ
Fig. 1 Schematic diagram of experimental system
2 ���������
2.1 ��ѧ���������Ի���̿����ָ���Ӱ��
���û�ѧ�������Էϻ���̿������������̽��������Ũ��ֵ������ʱ��Ի���̿����Ч����Ӱ�죬�ֱ��������������̿�ĵ�����ֵ���Ǽ�������ֵ�������д����Ե�����ָ�꣬�����ͼ2��ʾ����ͼ2�п��Կ�������ѧ������ʹ�ϻ���̿�ĵ�����ֵ���Ǽ�������ֵ�������ָ���������ֵ�ɷϻ���̿��452.32 mg/g��ָ���653.21 mg/g���Ǽ�������ֵ�ɷϻ���̿��64.69 mg/g��ָ���137.78 mg/g��������ʱ����ͬʱ����������̿�ĵ�����ֵ��������Ũ�ȵ����Ӷ����ӣ�����������ʱ��϶�(0.5 h)ʱ�����н�Ϊ���Ե����ӷ��ȡ�����ʱ��ϳ�(4 h)ʱ�����ӷ��Ƚ�С������ͬ����Ũ�ȴ���ʱ����������̿�ĵ�����ֵ��������ʱ����ӳ������ӡ��Ǽ�������ֵҲ���ֳ����������ֵ���Ƶı仯���ơ�����Ҫ����������ʱ�䡢����Ũ��ֵӰ����������Ӧ�����ʡ����ڵ�����Ũ��(0.6 mol/L����)�����Ļ���̿��Ʒ��������Ӧ���ʽ�������������̿���������ܷ�Ӧʱ���Ӱ��ϴ�����ʱ��϶�ʱ��������Ӧ����ȫ����Ȼ���в���̼����������������Թ�û�б�������Һ�ܽ⣬��ʹ��϶û�еõ��Ϻõ��ͷţ����������������������ŷ�Ӧʱ������ӣ���������̿����������ߡ����ڸ�����Ũ��(0.6 mol/L����)�����Ļ���̿��Ʒ��˵����������Ũ�Ƚϸߣ���Ӧ��Ϊ���ң������˻���̿�������̣���������̿��������������Ũ�ȵ�Ӱ��ϴ�����ʱ�����Ӱ���С����ˣ�������Ũ��Ϊ0.8 mol/Lʱ����������̿�����������뷴Ӧʱ���Ѿ����ٳ��������ӵĹ�ϵ��������Ũ��Ϊ0.8 mol/L����Ӧʱ��Ϊ2 hʱ��������Ӧ�ﵽ���ͣ���������̿�������ܴﵽ��ֵ���ӳ���Ӧʱ�䵽4 h������ʹ����̿���Ũ������ĸ�ʴ��ʹ��������̿���������½���
���ǵ�ʵ��������ʱ��ɱ�������Ч����ѡȡ����Ũ��Ϊ0.6 mol/L������ʱ��0.5 h��Ϊ�Ż��Ļ�ѧ�����������ڽ�������ʵ���У����Դ������������Ļ���̿Ϊ��Ʒ������һ���������������ӻ���̿������������ȱ������

ͼ2 ��ѧ���������Ի���̿������ֵ���Ǽ�������ֵ��Ӱ��
Fig. 2 Influence of chemical regeneration conditions on iodine adsorption value(a) and methylene blue adsorption value(b) of activated carbon
2.2 �����������Ի���̿����ָ���Ӱ��
����ǰ�����Ĺ��Ľ���ʵ����Ե�֪[1, 12]������̬����Ԫ�ع�������̬�������������ᣬ��ˣ��ϻ���̿�������Ĺ�������ͨ����ѧ��������ȫ�Ѹ��������ϻ���̿������ѧ����֮����δ�ﵽ��Ϊ�����Ч�������֮ǰ�Թ����������ȶ��Եķ���[13-16]��ͨ���ȴ�������ʹ��������ֽ⣬�����Ҫ�Ի�ѧ������Ļ���̿��Ʒ�����������������ڳ��������¶���������Ļ���̿��Ʒ�ĵ�����ֵ���Ǽ�������ֵ���вⶨ�������ͼ3��ʾ����ͼ3�п��Կ�����������ֵ���Ǽ�������ֵ�����ֳ������Ӻ��С�����ƣ����е�����ֵ�������¶�750 �桢����ʱ��2 hʱ��ߴﵽ1022.12 mg/g���Ǽ�������ֵҲ�ڴ��¶������´ﵽ���ֵ182.34 mg/g����˵��������ȡ�������õ�Ч����ͨ�������ȴ���ʹ����̿�����IJ�ͬ��̬�Ĺ������Ѹ�������ʹ����̿���ṹ�õ��ϺõĻָ����������¶ȳ���750 ʱ����������̿���������������½�������Ҫ�����ڹ��ߵ��¶Ȼ���ɻ���̿�ڲ������ṹ���ͣ��п��������Ӷ�Ӱ�����̿����������[17]�����⣬���ߵ��¶Ȼ�����ɻ���̿���ֹ����ŵķֽ⣬����������Ӱ�����̿��������ؼ�����[18]����ˣ����ߵ��¶Ȼ����������̿���������ܲ�������Ӱ�졣
����ʵ���������ʵ����������Ч��ʱ��ɱ���֪���Ի���̿������������¶�Ϊ750 �桢����ʱ��Ϊ2 h����ʱ�õ�����������̿������ֵ���Ǽ�������ֵ���š�
ͼ3 �����¶ȶԻ���̿������ֵ���Ǽ�������ֵ��Ӱ��
Fig. 3 Influence of regeneration temperature on iodine adsorption value(a) and methylene blue adsorption value(b) of activated carbon
2.3 ���ط���
Ϊ��һ��̽������̿�����Ĺ���̼����Լ������������ʵĽ��롢�Ѹ����ֽ���̣���������ԭʼ�ϻ���̿(WAC)����ѧ��������̿(SAC����������0.6 mol/L��0.5 h)���Ȼ�ѧ����������������̿(HSAC����������750 �桢2.0 h)������Ʒ���������ط���������ֱ���ͼ4(a)��(b)��(c)��ʾ�����Է��֣�������Ʒ����40~115 ���¶ȷ�Χ���ڷdz����Ե�ʧ�ط壬����Ҫ�����ڻ���̿��Ʒ������ˮ����ʧ���������̿�������������������������˿����ڵ����������Ѹ���������ͼ4(a)�л����Է��֣�ԭʼ�ϻ���̿��600~690 ���¶�����Ҳ����һ����Ϊ���Ե�ʧ�ط壬˵������һ������������ʧ���̣��ù���Ӧ���ǻ���̿������̼��Ƶķֽ���̣�����̼����ڸ��������·ֽ�Ϊ�������������̼���Ӷ�����������Ŀ�����ʧ����300~600 ���¶����䣬ͼ4(a)��ͼ4(b)�нԴ���һ��������ʧ�ع��̣����¶������Ӧ��������ķֽ��¶ȣ������Ӧ���ǻ���̿�����Ĺ�����Ҫ�Ƚ��[19]�����ǣ�����ڻ���̿�Ĺ����������˽�5%��������ʧ��Ȼ�Ǿ�ģ��ý�Ӧ��ͬʱҲ�����˻���̿����ʧ�Լ���ȼú�����������ļױ���֬�ࡢ�ؽ������������ʵ��Ƚ���̡�ͼ4(c)����̿��Ʒ��ˮ�Ѹ�֮��û�з��������仯�����һ��˵���˻�ѧ�������������������Ͽ��Գ���ѳ��ϻ���̿�ϵ����ʡ�

ͼ4 �ϻ���̿����������̿�����ط�������
Fig. 4 Thermogravimetric analysis curves of waste activated carbon and regenerated activated carbon
2.4 ����̿�ıȱ������������
����̿���������������̿�ȱ���������ֲ��зdz����еĹ�ϵ[20]��Ϊ�˱Ƚϻ���̿����ǰ����ۿ��ı仯����ԭʼ�ϻ���̿����ѧ��������̿���Ȼ�ѧ����������������̿������Ʒ���˱ȱ��������ֲ���������1��Ӧ������ǰ��Ļ���̿�ȱ�����Լ��ڲ����ṹ�����ı仯�����Կ����ϻ���̿�ıȱ����Ϊ320.7 m2/g���ױȱ����Ϊ109.3 m2/g���ױȱ������ռ������Ϊ34.07%���ܿ��ݻ�Ϊ0.1478 cm3/g�����ݻ�Ϊ0.0278 cm3/g�����ݻ���ռ����Ϊ18.84%������������ջ�ѧ�����Լ�����������̿�ıȱ�����ֱ����ӵ�510.4 m2/g��840.9 m2/g���ױȱ�������ӵ�150.4 m2/g��410.2 m2/g���ܿ��ݻ��ֱ����ӵ�0.2648 cm3/g��0.3894 cm3/g�����ݻ����ӵ�0.0553 cm3/g��0.1781 cm3/g�����Է�������ڷ�������̿��ָ����������Ե�����Ч�����������̿������ֵ���Ǽ�������ֵ�IJ��Խ������һ���ԡ��ӱ�1�л����Է����ڽ���������ջ�ѧ��������Ȼ����̿���ܱȱ�������ױȱ�������������ӣ������ױȱ����ȴ��34.07%�½�����29.47%����˵����ѧ����ʹ�пʹ�����ӵı������ߣ�����������������������̿���������ʽ��з�Ӧ��ͬʱ��Ҳ���������ʴ������ʹ�û���̿���ṹ����������ˣ��ܶ����������ͬʱҲ������һЩ�п��������ɡ���һ���棬Ҳ���Է��ֵ�����ѧ��ʹ�ܱȱ�������ر����ױȱ������Ӳ�������������Ҫ����Ϊ����̿�����Ĺ���û�б��Ѹ�������֮����������������Է����ױȱ������ռ���������ݻ���ռ�����ֱ�����������48.78%��45.75%����˵������̿�������Ĺ����仯�����Ѿ����ܺõ��Ѹ��������õ�������������֪���Ľṹ��ȱ�����Ի���̿��������������Ϊ��Ҫ������[21]����Ҳ�ǵ�����ֵ���Ǽ�������ֵ�ڽ��л���̿����������������ߵ�ԭ��
ͼ5��ʾΪ����ǰ�����̿��������-�Ѹ��������ߡ���ͼ5���Կ����������������Ǿ��������������̿�ĵ��������������������������ѹ��ϻ���̿��ȣ���������̿�����������õ������Իָ���ͬʱ���Կ�����������Ļ���̿Ϊ���͵�I�͵����ߣ���P/P0��0.2ʱ����Ҫ���������Ӳ���������������ݻ���䣬��ʱ����������������������P/P0��0.2ʱ����Ҫ�����ݻ��Ѿ�����䣬�����������ﵽ���ͣ���ʱ���������������ͱ�÷dz���������P/P0��0.8ʱ������̿����������δ�������Ե���β������˵��������Ļ���̿������Ϊ�����п�������ռ������С��
��1 ����̿�ȱ��������ṹ����
Table 1 Specific surface area and pore size structure parameters of activated carbon

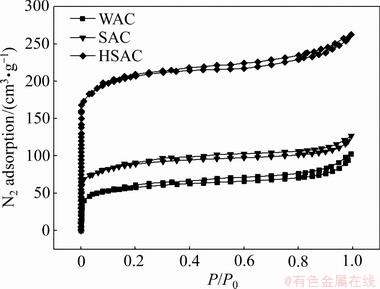
ͼ5 ����ǰ�����̿N2����-�Ѹ���������
Fig. 5 N2 absorption-desorption curves of activated carbon before and after regeneration
2.5 ��������̿�ѹ�Ч��
Ϊ�˼������������̿��ʵ���������ܣ���ʵ���ҹ̶�������ʵ��ϵͳ�϶����������̿�ĵ��ʹ�����Ч�������˲��ԣ�ʵ������ͼ6��ʾ����ͼ�п��Կ��������ԭʼ�ϻ���̿(WAC)��������Ļ���̿�Ե��ʹ�������Ч�����˷dz�����������������ԭʼ�ϻ���̿�������Ѿ������˴����Ĺ���̼��Ƶ����ʣ����ѹ������dz���������ʱ������ƣ�ԭʼ�ϻ���̿���ѹ����ܸ��Ǽ����½�����90 minʱ���Ĵ����Ѿ�������50%���ڽ�����180 min���ʹ��������Ĵ����Ѿ�������60%�����ڻ�ѧ�����Ļ���̿(SAC)���䵥�ʹ��������������ԭʼ�ϻ���̿�����������ڽ�����180 min�������Ĵ��ʵ���40%����ѧ�����Ļ���̿Ч������������Ϊ����̿�����Ĺ�û��ͨ����ѧ�����Ѹ����������Դ��ڱ�����״̬�������Ȼ�ѧ��������������Ļ���̿(HSAC)�����ѹ������Ѿ����������������������ʹ�180 min�����ѹ�Ч���Ը���80%(�����ʵ���20%)�����н�Ϊ����Ĺ��������ܣ�����������ʻ���̿�Ʊ��µĹ���ý���Ӷ�ʵ�ַϹ���ý��Դ��ѭ�����á�

ͼ6 ����ǰ�����̿�ѹ����ܶԱ�
Fig. 6 Comparison of mercury removal performance of activated carbon before and after regeneration
3 ����
1) ������ѧ����ʱ����Ũ��ֵΪ0.6 mol/L������ʱ��Ϊ0.5 hЧ���Ϻã��������������̿������������ǿ����һ���Ի�ѧ������Ļ���̿��������������������������¶�Ϊ750 �桢����ʱ��Ϊ2 hʱ��������ֵ�ߴﵽ1022.12 mg/g���Ǽ�������ֵҲ�ڴ������´ﵽ���ֵ182.34 mg/g��
2) ԭʼ�ϻ���̿���д�����̼��ƺ��������ѧ�������Զ�������̼��ƽ������õ��ѳ������Dz����ܽ������Ĺ����仯�����Ѹ���������һ�������������Ժܺõؽ������仯�����Ѹ��������Ӷ������������������̿�ıȱ�����Լ��ױ�������ѧ�����������������̿���ױȱ���������ݻ���ռ�����ɴ�48.78%��45.75%���������ʹ�180 min�����ѹ�Ч���Ը���80%�����н�Ϊ����Ĺ��������ܡ�
3) �����Ļ�ѧ��������������������������������Ч���ϲ���û�ѧ��������������ϵķ��������������˻���̿�Ĺ�������������ѧ�����������ѳ��ϻ���̿�дֵ�̼���Σ������˵���ʹ���������ܺĹ���̿��ʧ�������˷Ϲ���ý����̿�������ɱ���
REFERENCES
[1] л���, �����, �θ���, ��. �Ϲ���ý�й��Ľ���������������̿����������[J]. ��������ѧ��, 2019, 13(5): 1194-1201.
XIE Zi-nan, XU Ze-di, REN Fu-zhong, et al. Mercury leaching from waste mercury catalyst and the absorption property of regenerated activated carbon[J]. Journal of Environmental Engineering, 2019, 13(5):1194-1201.
[2] LIU C, PENG J H, MA A, et al. Study on non-isothermal kinetics of the thermal desorption of mercury from spent mercuric chloride catalyst[J]. Journal of Hazardous Materials, 2017, 322: 325-333.
[3] ��ս��, Ф��Ӫ, �ܺ���. �ҹ���ʯ��PVC��ҵ��ԡ����ڹ���ˮٶ��Լ��ʱ����ս���ȡ�Ļ�����ʩ������[J]. ������ϩ, 2018, 46(10): 1-11.
CAO Zhan-guo, XIAO Guo-ying, CAO He-ming. Positive measures and suggestions for China��s calcium carbide method PVC industry facing the time limit challenge of Minamata Convention on Mercury[J]. Polyvinyl Chloride, 2018, 46(10): 1-11.
[4] ����, ��ij�, �� ��, ��. �ҹ���ʯ������������ϩ��ҵ���ŷ��嵥[J]. ��������, 2016, 36(5): 572-576.
WANG Yu-jing, ZANG Wen-chao, ZHAO Jing, et al. Mercury emission inventory of PVC production by calcium carbide process in China[J]. Chemical Environmental Protection, 2016, 36(5): 572-576.
[5] BUSTO Y, TACK F M G, PERALTA L M, et al. An investigation on the modelling of kinetics of thermal decomposition of hazardous mercury wastes[J]. Journal of Hazardous Materials, 2013, 260: 358-367.
[6] ��С��, ��С��, �����, ��. �Ϲ���ý���ռ�����ʵ�����о�[J]. ������ϩ, 2017, 45(8): 33-35.
WANG Xiao-yan, WANG Xiao-chang, LI Guo-dong, et al. Laboratory study on recovery technology of waste mercury catalysts[J]. Polyvinyl Chloride, 2017, 45(8): 33-35.
[7] GB/T 36382��2018. �Ϲ���ý�������÷���[S].
GB/T 36382��2018. Treatment and disposal method for waste mercury catalyst[S].
[8] �� ��. ����̿���Ϲ���ý��ǿ���ѹ�����Դ�������о�[D]. ����: ����������ѧ, 2018: 1-157.
LIU Chao. Study on microwave enhanced mercury removal and resource utilization of waste mercury catalyst based on activated carbon[D]. Kunming: Kunming University of Science and Technology, 2018: 1-157.
[9] EL GAMAL M, MOUSA H A, EL-NAAS M H, et al. Bio-regeneration of activated carbon: A comprehensive review[J]. Separation and Purification Technology, 2018, 197: 345-359.
[10] ZHANG H P. Regeneration of exhausted activated carbon by electrochemical method[J]. Chemical Engineering Journal, 2002, 85(1): 81-85.
[11] LU P J, LIN H C, YU W T, et al. Chemical regeneration of activated carbon used for dye adsorption[J]. Journal of the Taiwan Institute of Chemical Engineers, 2011, 42(2): 305-311.
[12] ������, ���, ������, ��. ������п�������й����ȶ����о�[J]. ����������ѧ��, 2018, 39(7): 1630-1634.
ZHANG Ming-guang, LI Hai-long, ZHAO Yong-chun, et al. Study on the stability of mercury on Nano-ZnS adsorbents[J]. Journal of Engineering Thermophysics, 2018, 39(7): 1630-1634.
[13] YANG Z Q, LI H L, FENG S H, et al. Multiform sulfur adsorption centers and copper-terminated active sites of Nano-CuS for efficient elemental mercury capture from coal combustion flue gas[J]. Langmuir, 2018, 34(30): 8739-8749.
[14] LI H L, ZHU W B, YANG J P, et al. Sulfur abundant S/FeS2 for efficient removal of mercury from coal-fired power plants[J]. Fuel, 2018, 232: 476-484.
[15] LI H L, ZHANG W L, WANG J, et al. Coexistence of enhanced Hg0 oxidation and induced Hg2+ reduction on CuO/TiO2 catalyst in the presence of NO and NH3[J]. Chemical Engineering Journal, 2017, 330: 1248-1254.
[16] LI H L, ZHU L, WANG J, et al. Development of nano-sulfide sorbent for efficient removal of elemental mercury from coal combustion fuel gas[J]. Environmental Science & Technology, 2016, 50(17): 9551-9557.
[17] ������, �ſ�¡. ���´����Ի���̿��϶�ṹ��Ӱ��[J]. �ֲ���ѧ�빤ҵ, 1999, 19(3): 37-40.
LIU Jun-li, GU Ke-long. Effects of high temperature treatment on activated carbon pore structure[J]. Chemistry and Industry of Forest Products, 1999, 19(3): 37-40.
[18] �� ��. �Ʊ����̺ͱ�����Զ�ú�ʻ���̿������Ӱ������о�[D]. ����: �й���ҵ��ѧ, 2014: 1-81.
WANG Di. Study of preparation process and surface modification on coal based activated carbon functional groups[D]. Jiangsu: China University of Mining and Technology, 2014: 1-81.
[19] RUMAYOR M, DIAZ-SOMOANO M, LOPEZ-ANTON M A, et al. Temperature programmed desorption as a tool for the identification of mercury fate in wet-desulphurization systems[J]. Fuel, 2015, 148: 98-103.
[20] YALCIN N, SEVINC V. Studies of the surface area and porosity of activated carbons prepared from rice husks[J]. Carbon, 2000, 38(14): 1943-1945.
[21] PELEKANI C, SNOEYINK V L. Competitive adsorption between atrazine and methylene blue on activated carbon: the importance of pore size distribution[J]. Carbon, 2000, 38(10): 1423-1436.
Regeneration of activated carbon from waste mercury catalyst
WANG Sheng-cai1, YANG Qin2, ZHANG Ming-guang2, SONG Jian-fei1, LI Hai-long2, GUO Xue-yi1
(1. School of Metallurgy and Environment, Central South University, Changsha 410083, China;
2. School of Energy Science and Engineering, Central South University, Changsha 410083, China)
Abstract: After the recovery of mercury by heat treatment of waste mercury catalyst, a large amount of waste with activated carbon as the main component was formed. The new method combined hydrochloric acid chemical regeneration with thermal regeneration processes. The regeneration performances under different regeneration conditions were compared, the effects of hydrochloric acid concentration, impregnation time, thermal regeneration temperature and thermal regeneration time were analyzed. The characteristics of the regenerated activated carbon samples were analyzed, the adsorption indexes were tested and the mercury removal experiment was carried out in fixed bed. The results show that the mercury adsorption capacity of the regenerated activated carbon significantly is improved after the combination treatment of chemical regeneration and thermal regeneration. The optimal regeneration conditions are as follows: acid concentration of 0.6 mol/L, chemical regeneration time of 0.5 h, thermal regeneration temperature of 750 �� and thermal regeneration time of 2 h. After regeneration, the highest iodine adsorption value is 1022.12 mg/g activated carbon, methylene blue adsorption value is 182.34 mg/g activated carbon, and after continuous adsorption by fixed bed for 3 h, the mercury adsorption efficiency of regenerated activated carbon is above 80%. To realize the high value utilization of waste activated carbon from waste mercury catalyst after mercury recovery, a low cost, simple and efficient method to regenerate activated carbon from waste mercury catalyst is provided in this work.
Key words: waste mercury catalyst; activated carbon; chemical regeneration; thermal regeneration; mercury
Foundation item: Project(51776227) supported by the National Natural Science Foundation of China
Received date: 2019-11-02; Accepted date: 2020-12-24
Corresponding author: GUO Xue-yi; Tel: +86-0731-88876275; E-mail: xyguo@csu.edu.cn
LI Hai-long; Tel: +86-18670016725; E-mail: hailong_li@126.com
(�༭ �� ��)
������Ŀ��������Ȼ��ѧ����������Ŀ(51776227)
�ո����ڣ�2019-11-02�������ڣ�2020-12-24
ͨ�����ߣ���ѧ�棬���ڣ���ʿ���绰��0731-88876275��E-mail��xyguo@csu.edu.cn
��������ڣ���ʿ���绰��18670016725��E-mail��hailong_li@126.com
ժ Ҫ���Ϲ���ý�����������չ����γɴ����Ի���̿Ϊ��Ҫ��ֵķ���������������ữѧ���������������ϵķ������ԷϹ���ý����̿�����������Ƚϲ�ͬ���������µ��������ܣ���������Ũ�ȡ�����ʱ�䡢�������¶Ⱥ�������ʱ���Ӱ�졣��������Ļ���̿��Ʒ�����˱�������������ָ������Լ��̶����ѹ�ʵ�顣������������û�ѧ���������������ϵķ�������ʵ�ַϹ���ý����̿�ĸ�Ч�������Ż�����������Ϊ��Ũ��ֵ0.6 mol/L����ѧ����ʱ��0.5 h���������¶�750 �桢������ʱ��2 h����������̿������ֵ��߿ɴ�1022.12 mg/g���Ǽ�������ֵ��߿ɴ�182.34 mg/g�������ʻ���̿�൱����������̿�Ĺ�����Ч����3 h�ڿ���ά��80%���ϡ������ṩһ�ּ����á���Ч�ķϹ���ý����̿����������������ʵ�ַϹ���ý��ѭ�����á�
[4] ����, ��ij�, �� ��, ��. �ҹ���ʯ������������ϩ��ҵ���ŷ��嵥[J]. ��������, 2016, 36(5): 572-576.
[6] ��С��, ��С��, �����, ��. �Ϲ���ý���ռ�����ʵ�����о�[J]. ������ϩ, 2017, 45(8): 33-35.
[7] GB/T 36382��2018. �Ϲ���ý�������÷���[S].
GB/T 36382��2018. Treatment and disposal method for waste mercury catalyst[S].
[8] �� ��. ����̿���Ϲ���ý��ǿ���ѹ�����Դ�������о�[D]. ����: ����������ѧ, 2018: 1-157.
[12] ������, ���, ������, ��. ������п�������й����ȶ����о�[J]. ����������ѧ��, 2018, 39(7): 1630-1634.
[17] ������, �ſ�¡. ���´����Ի���̿��϶�ṹ��Ӱ��[J]. �ֲ���ѧ�빤ҵ, 1999, 19(3): 37-40.
[18] �� ��. �Ʊ����̺ͱ�����Զ�ú�ʻ���̿������Ӱ������о�[D]. ����: �й���ҵ��ѧ, 2014: 1-81.


